壯骨關節丸對腎虛型骨性關節炎大鼠臟器系數及總膽紅素的影響*
荊生龍,徐 彭,趙宏艷,何曉鵑,李 靜,孫舒玉,羅 丹,王敏智,肖 誠,呂 誠△
(1.江西中醫學院,南昌 330004;2.中國中醫科學院中醫基礎理論研究所,北京 100700;3.中國中醫科學院臨床所,北京 100700;4.中日友好醫院,北京 100029)
壯骨關節丸主要由狗脊、淫羊藿、獨活、骨碎補、續斷、補骨脂、桑寄生、雞血藤、熟地黃、木香、乳香、沒藥組成,功以補益肝腎,養血活血,舒筋活絡,理氣止痛為主,用于肝腎不足、血瘀氣滯、脈絡痹阻所致的骨性關節炎、腰肌勞損。自上市以來,臨床療效確切,得到市場認可,但2001年11月19日,國家藥品不良反應監測中心首次通報了壯骨關節丸引起肝損害等不良反應情況,通報后(2001年11月)至2008年5月27日,國家中心病例報告數據庫共收到相關病例報告158例,不良反應表現主要為皮疹、瘙癢、惡心、嘔吐、腹痛、腹瀉、胃痛、血壓升高、肝功能異常,其中表現為肝損害的47例占30.4%。來自13個省、自治區、直轄市的47例肝損害相關病例報告顯示,患者主要為骨性關節炎、風濕性關節炎、腰間盤突出、頸椎病、骨質增生、腰肌勞損等老年退行性骨關節病變。雖然癥狀明確,但未深入調查患者病因病機,因此推測由于臨床試驗中所選對象的局限性,不能完全反映藥物對于不同中醫證候人群的效應。為了探究壯骨關節丸對于不同類型骨性關節炎的影響,本研究通過壯骨關節丸連續灌胃腎虛型骨性關節炎及骨性關節炎模型大鼠4周后的臟器系數及血清中TBIL含量變化,評價其對大鼠不良反應的具體證況,為后續上市藥物安全性再評價中藥物毒理與證型研究提供實驗基礎。
1 材料與方法
1.1 動物
雌性SD大鼠72只,體重 160g~180g,由中國人民解放軍軍事醫學科學院實驗動物中心提供(合格證號SCXK-(軍)2007-004)。
1.2 藥物
注射用青霉素鈉由華北制藥股份有限公司生產(批號X1007206),壯骨關節丸由三九醫藥股份有限公司生產(批號1111020S),均由本實驗室人員粉碎后,實驗前以蒸餾水配成所需濃度。
1.3 儀器
HITACHI7180型全自動生化分析儀(日本Hitachi High-Tech Science SystemsCorporation),AE240型電子分析天平(日本 METTLER公司)。
1.4 方法
1.4.1 動物分組 動物適應性飼養1周后,隨機分為正常組、骨性關節炎組、腎虛型骨性關節炎組3大組,每組24只。每組大鼠按照不同的給藥劑量隨機分為正常對照組、治療量組、高倍量組3小組,每組8只。共分為骨性關節炎模型組、治療量組、高倍量組,腎虛型骨性關節炎模型組、治療量組和高倍量組。
1.4.2 建立模型 手術切除雌性大鼠卵巢,可造成NIM網絡平衡失調,從而反映臨床腎虛證的某些病理變化特征,因此被用作腎虛模型常用造模方法,其分為骨性關節炎模型組、治療量組、高倍量組;腎虛型骨性關節炎模型組、治療量組、高倍量組。當然也有其他方法,比如外源性糖皮質激素刺激[1]、腺嘌呤喂養等。此次研究主要采取無菌狀態下切除雌鼠雙側卵巢的方法進行腎虛模型的建立。將腎虛型骨性關節炎組大鼠麻醉后腹位固定,剪去鼠毛暴露手術視野,以75%酒精及碘酊消毒切開皮膚、背部肌肉和腹膜,用小鑷子分離脂肪團便可見卵巢,先將卵巢下端輸卵管用手術線結扎,然后摘除卵巢,切口縫合后敷以消炎粉。其他組全部大鼠手術入路同上,發現卵巢后僅切除與卵巢等量的脂肪后縫合皮膚。
腎虛模型建立 4周后,參考文獻方法[2~4]并加以調整,腎虛型骨性關節炎組及骨性關節炎組大鼠用戊巴比妥鈉麻醉,在無菌狀態下切斷右側膝關節內前交叉韌帶和內側部分半月板,制成骨性關節炎模型,縫合皮膚后連續3d腹腔注射4萬單位PG0.2ml/只。正常組將右側膝關節部位皮膚切開,然后縫合進行假手術處理。
1.4.3 給藥劑量及方法 骨性關節炎模型建立后第2天,各組大鼠按照如下方式給藥:所有高倍量組給予壯骨關節丸5.55g/(kg·d)(成人等效劑量的5倍)灌胃;治療量組按照壯骨關節丸1.11g/(kg·d)劑量(成人等效劑量)灌胃;模型組及對照組大鼠則給予同等體積的蒸餾水灌胃。所有給藥,持續4周,實驗過程中動物正常供給飼料和飲水。
1.4.4 取材 給藥結束后,麻醉處死大鼠,立即取臟器心、肝、脾、肺、腎、腎上腺、胸腺,稱濕重計算臟器系數并收集血清進行TBIL含量檢測。
2 結果
2.1 動物臟器系數
表1顯示,各組動物給藥4周后大鼠臟器系數(臟器重量/體重)變化情況:胸腺指數與正常對照組比較,正常治療量組及高倍量組卻顯著降低(P<0.05),而腎虛型骨性關節炎模型組顯著偏高(P<0.05),即藥物對于正常大鼠可能具有一定影響,而對于病理狀態下的大鼠胸腺無明顯影響;肝臟指數與正常對照組相比較,正常高倍量組顯著增加(P<0.05),而腎虛型骨性關節炎模型組卻顯著降低(P<0.05);腎臟指數與正常對照組相比較,腎虛型骨性關節炎模型組和治療量組顯著降低(P<0.01),而骨性關節炎模型組卻顯著偏高(P<0.01);腎上腺指數與正常對照組相比較,僅正常高倍量組顯著偏高(P<0.05),其他組別無統計學差異。心臟、脾臟以及肺臟指數與正常對照組相比,均無明顯差異(P>0.05)。
2.2 總膽紅素檢測結果
血液生化指標也為藥物毒性評價提供依據[5],血清中的膽紅素大部分來源于衰老紅細胞被破壞后產生出來的血紅蛋白衍化而成,在肝內經過葡萄糖醛酸化的叫做直接膽紅素,未在肝內經過葡萄糖醛酸化的叫做間接膽紅素,二者之和就是總膽紅素,是膽色素的1種,肝細胞具有攝取、結合、排泄膽紅素的功能。血清膽紅素數值的高低可以反映出肝臟病變或膽管阻塞等異常信息。報道顯示[6],急性肝炎中血清TBIL濃度水平異常,因此其在實際臨床肝病檢測中意義重大。
圖1顯示,大鼠血清總膽紅素(Total bilirubin,TBIL)結果顯示,與正常對照組相比,正常高倍量組和OA高倍量組具有顯著差異。
表1 不同骨性關節炎大鼠灌胃壯骨關節丸后臟器系數結果(±s)
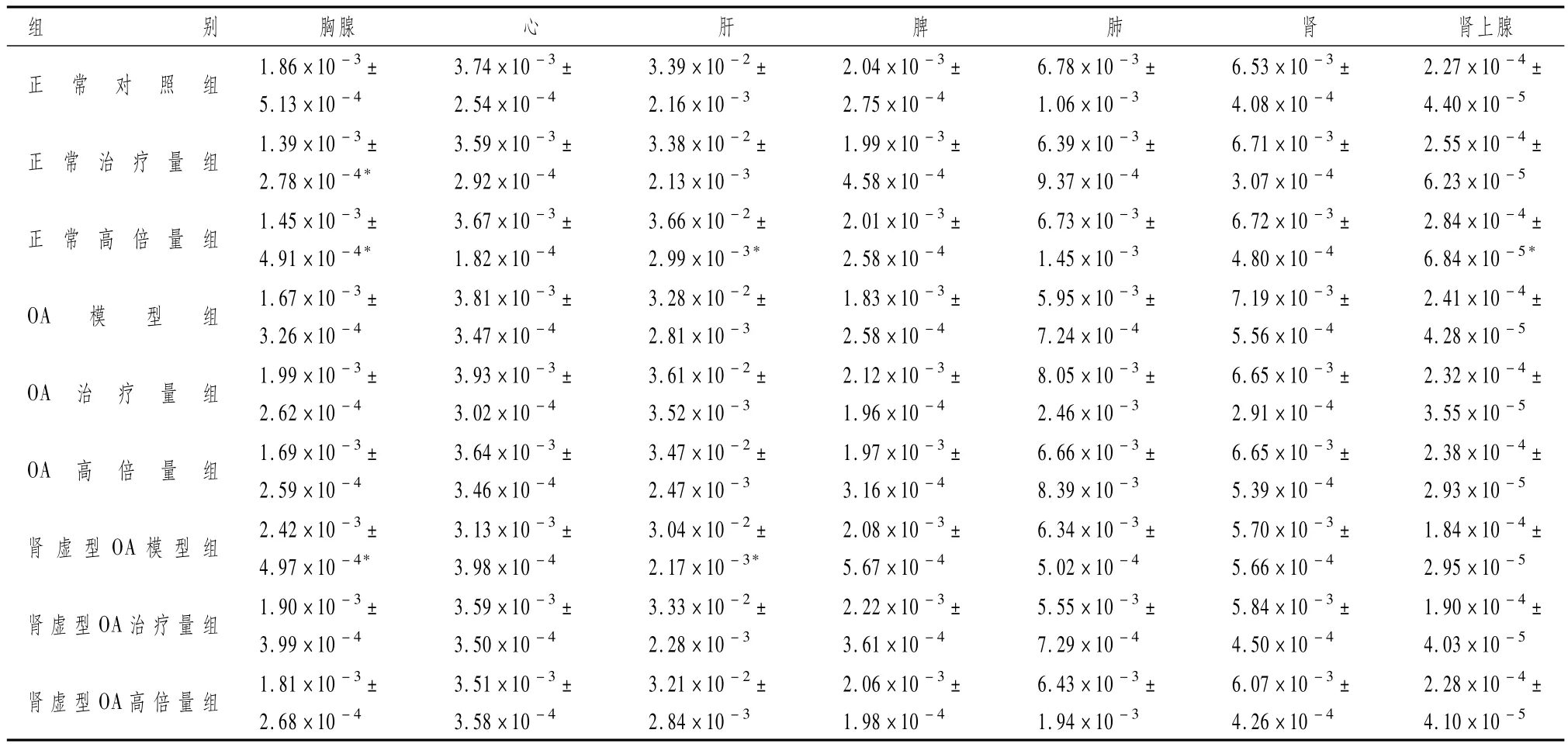
表1 不同骨性關節炎大鼠灌胃壯骨關節丸后臟器系數結果(±s)
注:各給藥組及模型組指標數值分別與正常對照組比較:*P<0.05,△P<0.01
組別胸腺 心 肝 脾 肺 腎 腎上腺正常對照組1.86 ×10 -3±5.13 ×10 -4 3.74×10-3±2.54×10-4 3.39×10-2±2.16×10-3 2.04 ×10 -3±2.75 ×10 -4 6.78×10-3±1.06×10-3 6.53×10-3±4.08×10-4 2.27×10-4±4.40 ×10-5正常治療量組正常高倍量組OA模型組OA治療量組OA高倍量組腎虛型OA模型組腎虛型OA治療量組1.39 ×10 -3±2.78 ×10 -4*1.45 ×10 -3±4.91 ×10 -4*1.67 ×10 -3±3.26 ×10 -4 1.99 ×10 -3±2.62 ×10 -4 1.69 ×10 -3±2.59 ×10 -4 2.42 ×10 -3±4.97 ×10 -4*1.90 ×10 -3±3.99 ×10 -4 3.59×10-3±2.92×10-4 3.67×10-3±1.82×10-4 3.81×10-3±3.47×10-4 3.93×10-3±3.02×10-4 3.64×10-3±3.46×10-4 3.13×10-3±3.98×10-4 3.59×10-3±3.50×10-4 3.38×10-2±2.13×10-3 3.66×10-2±2.99×10-3*3.28×10-2±2.81×10-3 3.61×10-2±3.52×10-3 3.47×10-2±2.47×10-3 3.04×10-2±2.17×10-3*3.33×10-2±2.28×10-3 1.99 ×10 -3±4.58 ×10 -4 2.01 ×10 -3±2.58 ×10 -4 1.83 ×10 -3±2.58 ×10 -4 2.12 ×10 -3±1.96 ×10 -4 1.97 ×10 -3±3.16 ×10 -4 2.08 ×10 -3±5.67 ×10 -4 2.22 ×10 -3±3.61 ×10 -4 6.39×10-3±9.37×10-4 6.73×10-3±1.45×10-3 5.95×10-3±7.24×10-4 8.05×10-3±2.46×10-3 6.66×10-3±8.39×10-3 6.34×10-3±5.02×10-4 5.55×10-3±7.29×10-4 6.71×10-3±3.07×10-4 6.72×10-3±4.80×10-4 7.19×10-3±5.56×10-4 6.65×10-3±2.91×10-4 6.65×10-3±5.39×10-4 5.70×10-3±5.66×10-4 5.84×10-3±4.50×10-4 2.55×10-4±6.23 ×10 -5 2.84×10-4±6.84 ×10 -5*2.41×10-4±4.28 ×10 -5 2.32×10-4±3.55 ×10 -5 2.38×10-4±2.93 ×10 -5 1.84×10-4±2.95 ×10 -5 1.90×10-4±4.03 ×10 -5腎虛型OA高倍量組1.81 ×10 -3±2.68 ×10 -4 3.51×10-3±3.58×10-4 3.21×10-2±2.84×10-3 2.06 ×10 -3±1.98 ×10 -4 6.43×10-3±1.94×10-3 6.07×10-3±4.26×10-4 2.28×10-4±4.10 ×10-5
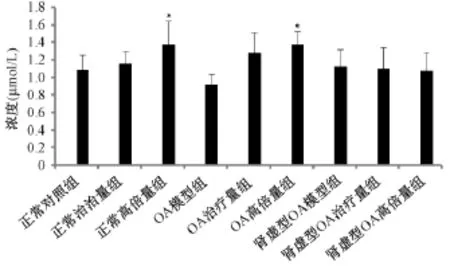
圖1 不同骨性關節炎大鼠灌胃壯骨關節丸后血清TBIL結果(μmol/L)
3 討論
骨性關節炎(osteoarthritis,OA)常被稱為退行性關節病、骨質增生、骨關節病,其主要病變是關節軟骨退行性變和繼發性骨質增生,是中老年人群多發的風濕性疾病,而其中又以女性更為常見,具體受累關節多發于負重較大的膝關節、髖關節、脊柱以及手指關節等。中醫認為,骨性關節炎首先是由于肝腎虧損,肝虛則血不養筋,筋不能維持骨節之張弛,關節失滑利,腎虛而髓減,致使筋骨失其所養;其次過度勞累,日積月累,筋骨受損,營衛失調,氣血受阻,經脈凝滯,筋骨失養,致生本病,故肝腎虧虛和慢性勞損是本病發病基礎[7]。
壯骨關節丸是治療退行性骨關節病的常用口服中藥復方制劑。據現代中藥藥理學毒理研究提示,該方劑12味中藥中至少已發現2種成分可造成實驗動物(大鼠和豚鼠)的肝損害,如獨活含有佛手柑內酯、歐芹酚甲醚、歐芹屬乙素、異補骨脂素和花椒毒素等,可引起實驗動物的肝毒損害。另1味中藥淫羊藿給藥3d,小鼠即出現嘔吐、納少、活動減少,給藥15d處死,可見肝臟脂肪變性[8~10]。臨床報道也是在肝損害方面最為突出,而且患者以老年人為主要人群。當然,單一成分的藥理研究結果不能等同于方劑的作用,對于其引起肝損害不良反應的機制還有待于進一步研究。
病證結合動物模型既有西醫疾病的特點,又有中醫證候特征,它將有助于中藥藥理學研究和中藥藥效的評價,有利于更全面、客觀地認識中藥的科學內涵,對于探討中藥毒性與中醫證候特征之間的關系,更是顯示出較大的優勢。由于中醫存在著同病異治和異病同治的理論,岳美中指出“病者本也,體也;證者標也,象也;有病始有證,辨證方能識病,識病后可以施治”,因此臨床中藥使用過程中必須依據患者病因病機朔本求源、辨證施治,否則可能會因為藥物應用不當而產生不良影響。本研究所采用的動物模型為病證結合模型,一定程度上能反映疾病的證候屬性,減少了中醫臨床的隨意性,使得中醫臨床辨病施治和辨證施治有證可循,這也將成為中醫理論與現代科技結合的一個突破口,為中藥臨床研究提供了廣闊的前景,所以采用對應病證結合動物模型評價中藥藥效和毒性更具有說服力。
臟器系數在藥物的毒性反應中,作為1項常規檢測指標,可為藥物的評價提供參考。本次實驗研究發現,臟器系數與正常對照組相比正常高倍量組胸腺、肝及腎上腺具有顯著變化,而腎虛型骨性關節炎模型組胸腺、肝、腎變化明顯,給藥后卻無顯著差異,提示本藥口服不會影響腎虛型骨性關節炎模型大鼠的飲食、體重及各主要器官的生長發育及組織形態,對這些方面無明顯毒副作用。但是對于正常大鼠影響較大,且血清中 TBIL的含量對比說明,高倍量藥物對于正常及骨性關節炎大鼠肝臟影響較為顯著,由此說明對證施藥在臨床中的重要性。
《內經》云:“……有故無殞,亦無殞也。”中醫傳統理論強調中藥藥性毒性和“證”的密切關系,而目前中藥毒理學研究采用正常動物研究中藥毒性的方法恰恰忽略了這些方面。所謂“有病則病受之”,反之無病則體受之[11,12]。在沒有病邪存在的情況下,中藥的藥性作用于正常機體就表現為毒性。而當我們采用證候動物模型時,其藥性作用于病邪,可能表現的就是治療作用,后者才能準確反映中藥應用于臨床的情況。但這種研究方法目前存在的最大問題,就在于中醫證候動物模型的建設尚未形成一個完善的體系。有毒中藥對不同狀態、不同層次證候模型所產生的藥物效應是有差異的,在評價中通過比較這些差異,可以為深入揭示其毒-效關系和發生機制提供科學依據[13]。因此,通過加強證候動物模型的建設來促進中藥毒理學研究是必要的。
[1]譚勇,李健,呂誠,等.白附片對健康及腎陽虛模型大鼠心電圖及心肌組織病理形態的影響[J].中國中醫基礎醫學雜志,2011,(17)10:1080-1083.
[2]趙京濤,方斌,楊俊興,等.補腎健骨中藥對骨關節炎腎虛模型大鼠的PGE2及 E2的影響[J].臨床和實驗醫學雜志,2006,5(7):912-913.
[3]Ashraf S,Mapp PI,Walsh DA.Contributions of angiogenesis to inflammation, jointdamage, and pain in a ratmodelof osteoarthritis[J].Arthritis Rheum,2011,63(9):2700-2710.
[4]Wen ZH,Tang CC,Chang YC,et al.Glucosamine sulfate reduces experimentalosteoarthritis and nociception in rats:association with changes of mitogen-activated protein kinase in chondrocytes[J].Osteoarthritis Cartilage,2010,18(9):1192-1202.
[5]譚勇,呂誠,趙宏艷,等.白附片對正常和腎陽虛大鼠血液生化指標的影響[J].中國中醫藥信息雜志,2010,17(1):31-33.
[6]劉亞萍,陳新軍.前白蛋白、總膽汁酸、總膽紅素測定在肝臟疾病中的應用[J].中國民族民間醫藥,2010,19(5):82,85.
[7]Wang Bin.Understanding and treating about pathogenesis of osteoarthritis in TCM[J].Clinical Journal of Chinese Medicine,2011,3(4):118.
[8]鄧培媛,蔡皓東,程經華,等.壯骨關節丸致肝損害30例報告[J].中國新藥雜志,1996,5(3):212-214.
[9]冉先德.中華藥海[M].哈爾濱:哈爾濱出版社,1993:76.78.654.
[10]李廣勛.中藥藥理毒理與臨床[M].天津:天津科技翻譯出版公司,1992:94.391.
[11]周宜,陳鋼,夏麗娜,等.從《內經》“有故無隕”思想看中藥毒性研究[J].中國中醫基礎醫學雜志,2007,13(5):342:343.
[12]譚勇,李健,陳杲,等.白附子對正常和腎陽虛證大鼠毒性作用的差異[J].中醫雜志,2011,52(14):1229-1232.
[13]譚勇,古潔乃特,呂誠,等.有毒中藥安全性評價中的問題與對策[J].中國中醫基礎醫學雜志,2009,15(9):696-697,699.

