具有平面手性和中心手性的二茂鐵基亞砜膦配體的合成及其催化活性
李高偉, 唐 貝, 王敏燦, 孔培培, 趙文獻
(1. 商丘師范學院 化學系 有機新材料合成重點實驗室,河南 商丘 476000; 2. 河南省醫藥學校,河南 開封 475000; 3. 鄭州大學 化學系 河南省化學生物與有機化學重點實驗室,河南 鄭州 450052)
在不對稱催化研究中,手性配體的設計與合成一直是研究的熱點之一,而合適的手性配體是不對稱催化反應成功的關鍵。在眾多結構各異的手性配體中,手性二茂鐵配體具有其特殊而重要的地位[1]。通過硫醚化合物的不對稱氧化是獲得手性亞砜化合物的一種重要途徑。由于手性亞砜本身具有體積大的硫原子,空間障礙小的孤對電子和極性較強的亞磺酰基,可以同多種金屬絡合形成手性絡合物進行不對稱誘導。
Fernández等[2]報道了具有二茂鐵基的手性亞砜配體Ⅰ(Chart 1)在用量為3 eq時催化對苯腙的不對稱烯丙基胺化反應取得了較好的對映選擇性(82%ee); Carretero等[3]合成了一類新型的氨基取代二茂鐵叔丁基亞砜Ⅱ(Chart 1),在其催化的二乙基鋅對芳香醛的加成反應中催化效果表現較好(26%ee~96%ee); Enders小組[4]合成了具有平面手性和中心手性的二茂鐵硫醚膦配體Ⅲ(Chart 1),將其應用于烯丙基取代反應的模板反應中,取得了97%的ee值。最近,Liao小組[5~7]發展了系列烷氧基取代的苯環骨架的手性膦亞砜配體Ⅳ(Chart 1),在其催化的二乙基鋅對亞胺不對稱加成反應,Pd-Ⅳ催化的不對稱烯丙基取代反應和Rh-Ⅳ催化的芳基硼酸對烯酮的1,4-加成反應中都取得了很好的ee值。

Chart1


Scheme1

Scheme2
本課題組[8~10]近年來在手性二茂鐵膦配體和硫醚配體的不對稱催化應用方面也取得了一些進展,開發了脯氨酸衍生的二茂鐵基胺膦配體,在銅絡合物存在下,二乙基鋅對N-磺酰基芳醛亞胺的加成取得了79%ee~86%ee。首次研究了手性二茂鐵基氮膦配體的銅絡合物對N-二苯基磷酰芳醛亞胺的不對稱加成,產物手性胺的ee值最高達到90%。開發的手性二茂鐵氮雜環丙烷硫醚配體在Pd-催化的烯丙基取代反應中取得高達91%ee。最近,Zhao等[7]報道了一種含硫的二茂鐵基氨基醇手性配體的合成,該手性配體在不對稱催化反應中的應用正在進一步考察之中。
本文在文獻[5~7,10]的基礎[10]上,借助二茂鐵側鏈上含有手性中心的雜原子(手性亞砜中的氧原子)的鄰位導向作用,在高活性鋰試劑丁基鋰的作用下,二茂鐵的鄰位被高度立體專一性的鋰化,然后在親電試劑二苯基氯化膦的作用下合成了手性二茂鐵亞砜膦配體3(Scheme 1),其結構經1H NMR,13C NMR, IR, MS和元素分析表征。以1,3-二苯基-2-丙烯基乙酸酯與丙二酸二甲酯/氫化鈉的模板反應為例,初步研究了絡合物Pd-3在烯丙基取代反應中的催化活性(Scheme 2),收率92%, 20%ee。
1 實驗部分
1.1 儀器與試劑
YRT-3型熔點儀(溫度計未經校正);Perkin Elmer 341型旋光儀(20 ℃, CHCl3為溶劑);Bruker DPX-400型超導核磁共振儀(CDCl3為溶劑,TMS為內標);Thermo Nicolet IR 200型紅外光譜儀(KBr壓片);Bruker Esquire 3000型質譜儀;Carlo Erba 1160型元素分析儀;高效液相色譜儀[HPLC, JASCO PU-1580智能型HPLC泵,JASCO UV-1575智能型紫外-可見檢測儀(254 nm),手性柱Chiralcel OD Column(250 nm×4.6 mm, Daicel Chemical Ind., LTD, Japan];柱層析和薄層色譜用硅膠GF254,青島海洋化工廠。
THF經金屬鈉(二苯甲酮)無水處理后壓入鈉絲保存;二氯甲烷經五氧化二磷無水處理后加入4 ?分子篩密封保存;其余所用試劑均為分析純。
1.2 合成
(1) 二茂鐵基叔丁基硫醚(1)的合成[12]
在反應瓶中加入二茂鐵2.8 g(15 mmol)的THF(15 mL)溶液,于室溫攪拌30 min。冰水浴冷卻至0 ℃,慢慢滴加叔丁基鋰10 mL(14.8 mmol, 1.5 mol·L-1in pentane),滴畢,反應2 h得二茂鐵鋰。升至室溫,加入過硫化二叔丁基3.5 mL(18 mmol),反應2 h(TLC跟蹤)。用2 mol·L-1氫氧化鈉溶液12 mL終止反應,用乙醚(3×30 mL)萃取,合并有機相,用飽和食鹽水(2×30 mL)洗至中性,無水硫酸鈉干燥,濃縮后經TLC[展開劑:A=V(正己烷) ∶V(乙酸乙酯)=125 ∶1]純化得紅色固體1 1.85 g,產率45%, m.p.62.6 ℃~63.8 ℃(61 ℃~62 ℃[13]);1H NMRδ: 1.20(s, 9H, CH3in Bu), 4.19~4.30(m, 9H, FcH); IRν: 3 415, 3 129, 1 721, 1 400, 1 170, 812, 496 cm-1; ESI-MSm/z: 185.2(Fc+), 274.3(M+)。
(2) 手性二茂鐵基叔丁基亞砜(2)的合成[14,15]
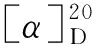
(3) 3合成[15,18]

1.3 Pd-3的催化活性
氮氣保護下將[Pd(η3-C3H5)Cl]23.7 mg(0.01 mmol)和3 4.9 mg(0.01 mmol)溶于THF(2 mL)中,絡合反應30 min得絡合物Pd-3。加入1,3-二苯基-2-丙烯基乙酸酯126 mg(0.5 mmol),反應10 min;加入新配制的NaCH(CO2Me)2-THF溶液[NaH(36 mg, 1.5 mmol)+丙二酸二甲酯(198 mg, 1.5 mmol)+THF(3 mL)],反應至終點(TLC跟蹤)。加入飽和氯化銨水溶液,用乙醚(3×10 mL)萃取,合并有機層,用無水硫酸鈉干燥, 減壓濃縮后經硅膠柱層析[洗脫劑:V(石油醚) ∶V(乙酸乙酯)=10 ∶1]純化得無色液體4,產率92%, 20%ee;1H NMRδ: 3.52(s, 3H, CO2CH3), 3.70(s, 3H, CO2CH3), 3.95(d,J=10.8 Hz, 1H, 1-H), 4.27(dd,J=8.8 Hz, 10.8 Hz, 1H, 2-H), 6.30(dd,J=8.8 Hz, 15.8 Hz, 1H, 3-H), 6.44(d,J=15.8 Hz, 1H, 4-H), 7.19~7.34(m, ArH, 10H)。
2 結果與討論
2.1 1的合成
經Kagan試劑的不對稱氧化合成1,其反應試劑要求(R,R)-DET/Ti(O-iPr)4都要經過減壓蒸餾精制,尤其是(R,R)-DET,必須是光學純品,CHP用4 ?分子篩儲藏過夜。在室溫下以無水二氯甲烷為溶劑,依次加入Ti(O-iPr)4, (R,R)-DET, H2O和CHP(1 ∶2 ∶1 ∶1),關鍵是在加入(R,R)-DET后才能再加入水,否則改變加入次序將產生沉淀物(TiO2),進而影響1的合成。
2.2 3的應用
用烯丙基取代反應考察了Pd-3的催化活性,結果表明,Pd-3的催化效果不佳(20%ee)。
[1] Arrayás R G, Adrio J, Carretero J C. Recent applicationsof chiral ferrocene ligands in asymmetric catalysis[J].Angew Chem Int Ed,2006,45:7674-7715.
[2] Fernández I, Valdivia V, Gori B,etal. The isopropylsulfinyl group:A useful chiral controller for the asymmetric aziridination of sulfinylimines and the organocatalytic allylation of hydrazones[J].Org Lett,2005,7:1307-1310.
[3] Priego J, Mancheńo O G, Cabrera S,etal. Aminosubstituted tert-butylsulfinylferrocenes as a new family of chiral ligands: asymmetric addition of diethylzinc to aldehydes[J].Chem Commun,2001:2026-2027.
[4] Enders D, Peters R, Lochtman R,etal. Asymmetric synthesis of novel ferrocenyl ligands with planar and central chirality and their application to Pd-catalyzed allylic substitutions[J].Eur J Org Chem,2000,20:3399-3426.
[5] Chen J M, Li D, Ma H F,etal. Catalytic asymmetric diethylzinc addition to diphenylphosphionyl imines using chiraltert-butanesulfinylphosphine ligands[J].Tetrahedron Lett,2008,49:6921-6923.
[6] Chen J M, Lang F, Li D,etal. Palladium-catalyzed asymmetric allylic nucleophilic substitution reactions using chiraltert-butanesulfinyl-phosphine ligands[J].Tetrahedron:Asymmetry,2009,20:1953-1956.
[7] Lang F, Li D, Chen J M,etal. tert-Butanesulfinylphosphines: simple chiral ligands in rhodium-catalyzed asymmetric addition of arylboronic acids to electron-deficient olefins[J].Adv Synth Catal,2010,(352):843-846.
[8] Wang M C, Xu C L, Zou Y X,etal. New chiral ferrocenyl amidophosphine ligand for remarkable improvement of enantioselectivities in copper-catalyzed addition of diethylzinc toN-sulfonylimines[J].Tetrahedron Lett,2005,46:5413-5416.
[9] Wang M C, Liu L T, Hua Y Z,etal. Novel chiral copper complexes of N,P-ferrocenylligands with central and planar chirality as effecient catalyst for asymmetric addition of diethylzinc to imines[J].Tetrahedron:Asymmetry,2005,16:2531-2534.
[10] Niu J L, Wang M C, Kong P P,etal. Origin of enantioselectivity with heterobidentates sufide-tertiary amine(sp3) ligands in palladium-catalyzed allylic substitution[J].Tetrahedron,2009,65:8869-8878.
[11] 趙文獻,鄭昕,李高偉,等. 一種新的含硫手性β-氨基醇配體的合成與表征[J].有機化學,2010,30:760-763.
[12] Rebiere F, Samuel O, Kagan, H B. A convenient method for the preparation of monolithioferrocene[J].Tetrahedron Lett,1990,31:3121-3124.
[13] Diter P, Samuel O, Taudien S,etal. Highly enantioselective oxidation of ferrocenyl sulfides[J].Tetrahedron: Asymmetry,1994,5:549-552.
[14] Rebiere F, Riant O, Ricard L,etal. Asymmetric synthesis and highly diastereoselective ortho-lithiation of ferrocenyl sulfoxides:Application to the synthesis of ferrocenyl derivatives with planar chirality[J].Angew Chem Int Ed Engl,1993,32:568-570.
[15] Minière S, Reboul V, Arrayás R G,etal. First epoxidation reaction of carbonyl compounds via ferrocenyl sulfur ylides[J].Synthesis,2003:2249-2254.
[16] Pichon C, Odell B, Brown J M. A direct meta-lithiation route to 1,3-disubstituted ferrocenes[J].Chem Commun,2004:598-599.
[17] Sato M, Sekino M. Synthesis and some properties of Pd(BF4)2and Pt(BF4)2complexes of 1,1′-bis[(alkyl- or phenyl-)chalcogeno]ferrocenes[J].J Organomet Chem,1989,(371):327-331.
[18] Lagneau N M, Chen Y, Robben P M,etal. Chiral sulfur-containing 1,2-disubstituted ferrocenes[J].Tetrahedron,1998,54:7301-7334.

