新型苦味酸銅(Ⅱ)配合物的合成、晶體結(jié)構(gòu)及其熱性能
馮建華
(滁州學(xué)院 材料與化學(xué)工程學(xué)院,安徽 滁州 239000)
目前,含有四齒配位席夫堿配體的過(guò)渡金屬配合物因具有催化性能而被人們所研究,其作為催化劑可以用于有機(jī)氧化還原反應(yīng)以及電化學(xué)降解工藝過(guò)程等[1]。近來(lái),金屬有機(jī)Salen型化合物已被作為催化活性物質(zhì)而用于開發(fā)表面改性電極材料,主要用于傳感器[2]、非線性光學(xué)材料[3]、磁性質(zhì)[4]、生物學(xué)[5]以及作為超分子體系單元結(jié)構(gòu)等領(lǐng)域和過(guò)程[6]。盡管大部分該類化合物在液體和固體狀態(tài)都是穩(wěn)定的,但是其中的碳氮雙鍵單元時(shí)常會(huì)遇到交換反應(yīng)以及水解作用。金屬有機(jī)Salen型化合物中肟類化合物的反應(yīng)速率常數(shù)小于該類化合物中亞胺類化合物的反應(yīng)速率常數(shù),但是前者的反應(yīng)平衡常數(shù)要比后者大幾個(gè)數(shù)量級(jí)[7]。因此,肟類Salen型化合物在阻止碳氮雙鍵單元的交換反應(yīng)方面是具有足夠的穩(wěn)定性的[8, 9]。
為了研究雙肟型Salen類化合物與苦味酸銅(Ⅱ)之間的配位性能,本文參考文獻(xiàn)[11]方法合成了新的雙肟型Salen衍生物H2L{H2L=6,6′-二甲氧基-2,2′-[(1,3-亞丙基)二氧雙(氮次甲基)]二酚), Scheme 1};室溫下,H2L與四水合苦味酸銅[Cu(pic)·4H2O]在丙酮中反應(yīng)合成了一種新型的苦味酸銅(Ⅱ)配合物——[Cu4L2(pic)4(H2O)2]·2(CH3COCH3)·2H2O(1),其結(jié)構(gòu)和熱性能經(jīng)IR,元素分析,X-射線單晶衍射及TG-DTA表征。
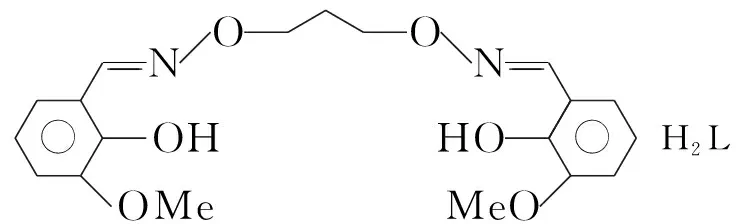
Scheme1
1 實(shí)驗(yàn)部分
1.1 儀器與試劑
X-4型數(shù)字顯微熔點(diǎn)儀(溫度計(jì)未校正);Avance DRX-400型核磁共振波儀(CDCl3為溶劑,TMS為內(nèi)標(biāo));Nicolet 6700型傅里葉變換紅外光譜儀(KBr壓片);GC-MS 2010 Plus型氣質(zhì)聯(lián)用儀;Elementar Vario EL型元素分析儀;Bruker Apex-2 CCD型單晶衍射儀;ZRY-1P型綜合熱分析儀(空氣氣氛,升溫速率2 ℃·min-1)。
1,3-二胺氧丙烷參照文獻(xiàn)[10]方法合成;其余所用試劑均為分析純。
1.2 合成
(1) H2L的合成[11]
在反應(yīng)瓶中加入3-甲氧基-2-羥基苯甲醛608.6 mg(4.0 mmol)的無(wú)水乙醇(8 mL)溶液,氮?dú)獗Wo(hù),攪拌下于55 ℃(浴溫)滴加1,3-二胺氧丙烷212.2 mg(2.0 mmol)的無(wú)水乙醇(6 mL)溶液,滴畢,于55 ℃(浴溫)反應(yīng)6 h。冷卻至室溫,過(guò)濾,濾餅用混合溶劑[V(乙醇)∶V(正己烷)=1 ∶4]洗滌,無(wú)水乙醇重結(jié)晶,真空干燥得無(wú)色粒色晶體H2L 608.8 mg,收率81.3%, m.p.164 ℃~165 ℃;1H NMRδ: 2.14(t,J=6.0 Hz, 2H, CH2), 3.89(s, 6H, OCH3), 4.30(t,J=6.0 Hz, 4H, CH2O), 6.83(dd,J=7.0 Hz, 6H, ArH), 8.18(s, 2H, NCH), 9.87(s, 2H, OH); GC-MSm/z(%): 282(M+, 46), 162(11), 148(100), 135(72), 118(14), 107(23), 81(25); Anal.calcd for C19H22N2O6: C 60.95, H 5.92, N 7.48; found C 60.44, H 6.07, N 7.12。
(2) 1的合成
在反應(yīng)瓶中加入H2L 18.7 mg(0.05 mmol)的丙酮(5 mL)溶液,攪拌下于室溫滴加四水合苦味酸銅(Ⅱ)29.6 mg(0.05 mmol)的丙酮(5 mL)溶液,滴畢,制得棕色透明溶液。置正己烷氣氛中,通過(guò)氣相擴(kuò)散法,經(jīng)數(shù)天得棕褐色六棱柱狀晶體1。 Anal.calcd for C68H68N16O46Cu4: C 38.90, H 3.26, N 10.67, Cu 12.11; found C 38.64, H 3.39, N 10.21, Cu 12.28。
1.3 1的晶體結(jié)構(gòu)測(cè)定
將單晶1置衍射儀上,采用Mo Kα射線(λ=0.0710 73 nm),于298(2) K下在1.75° ≤θ≤ 25.01°內(nèi)共收集21 765個(gè)衍射點(diǎn),其中7 485個(gè)獨(dú)立衍射點(diǎn),I>2σ(I)的4 867個(gè)可觀測(cè)衍射點(diǎn)用于結(jié)構(gòu)測(cè)定和修正。全部數(shù)據(jù)經(jīng)Lp因子和經(jīng)驗(yàn)吸收校正,晶體結(jié)構(gòu)由直接法解出,根據(jù)E-圖確定金屬原子位置,用直接法得到全部非氫原子坐標(biāo),氫原子坐標(biāo)由差值Fourier合成法得到,采用各向異性參數(shù)修正,所有計(jì)算均使用SHEXTL-97程序完成。
2 結(jié)果與討論
2.1 表征
H2L和1的IR譜圖見(jiàn)圖1。從圖1可見(jiàn),H2L中ν(C=N)和ν(Ar-O)的伸縮振動(dòng)峰分別出現(xiàn)在1 607 cm-1和1 254 cm-1,形成配合物后,二者分別藍(lán)移了2 cm-1和23 cm-1,這是H2L中的N原子和酚氧原子與Cu原子配位的結(jié)果。從圖1還可以看出,1的IR譜圖中未出現(xiàn)自由苦味酸根在1 169 cm-1處OH的面外彎曲振動(dòng),表明其中的H原子被參與配位的Cu(Ⅱ)所取代。自由苦味酸根中,νas(NO2)和νs(NO2)的特征峰分別在1 576 cm-1和1 344 cm-1處;而在1的IR譜中觀察到了它們均分裂為兩特征峰,分別位于1 578 cm-1, 1 539 cm-1和1 362 cm-1, 1 335 cm-1,說(shuō)明苦味酸根中的部分氧原子參與了配位[12]。在1的IR譜中,3 452 cm-1處的寬峰屬于水分子中OH的伸縮振動(dòng),1 632 cm-1處的吸收帶為水分子的彎曲振動(dòng)帶,858 cm-1和567 cm-1處吸收峰可分別歸屬于水分子的面內(nèi)、面外搖擺振動(dòng),證明水分子參與了配位[13]。
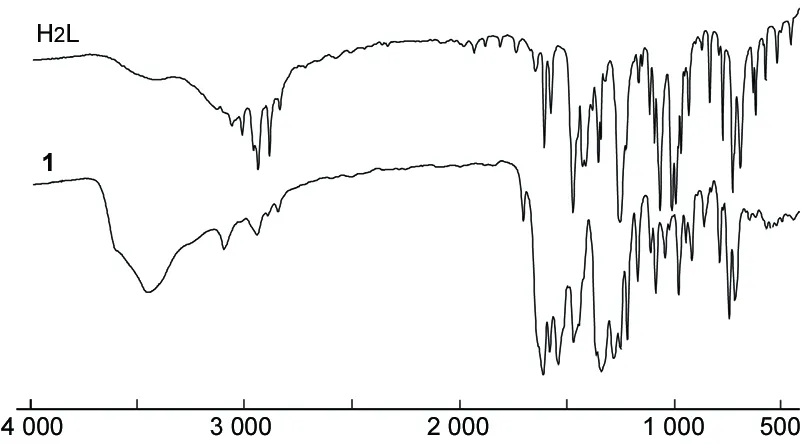
ν/cm-1圖1 H2L和1的IR譜圖Figure 1 IR spectra of H2L and 1
1的晶體學(xué)數(shù)據(jù)見(jiàn)表1,主要鍵長(zhǎng)和鍵角分別見(jiàn)表2和表3,分子結(jié)構(gòu)見(jiàn)圖1,晶胞中分子堆積分別見(jiàn)圖2和圖3。
晶體結(jié)構(gòu)解析表明,1為四核結(jié)構(gòu),其分子結(jié)構(gòu)單元含有4個(gè)Cu(Ⅱ)離子,2個(gè)L單元(提供N2O2給予體),4個(gè)苦味酸根離子,2個(gè)配位水分子,2個(gè)結(jié)晶丙酮分子和2個(gè)結(jié)晶水分子。1中參與配位的L并不是平面結(jié)構(gòu),而是形成了一個(gè)扭曲的幾何構(gòu)型。該對(duì)稱分子結(jié)構(gòu)中最顯著的特點(diǎn)是4個(gè)參與配位的苦味酸根離子中僅有2個(gè)采取了雙齒螯合配位方式,而另外2個(gè)則采取了三齒螯合橋聯(lián)配位模式。Cu(1)離子分別與來(lái)自同一個(gè)L的O(3)和N(1),一個(gè)雙齒螯合配位苦味酸根離子的O(14)和O(15)以及同一個(gè)三齒螯合配位苦味酸根離子的O(7)和O(8)進(jìn)行配位;而與Cu(Ⅱ)離子形成配位的原子分別是一個(gè)L的O(3)和O(4),另一個(gè)L的O(5)和N(2),三齒螯合配位苦味酸根離子的O(7)以及其中一個(gè)配位水分子上的O(21);另外2個(gè)Cu(Ⅱ)離子也分別采用了類似的配位模式。因此1中的4個(gè)Cu(Ⅱ)離子的配位數(shù)均為6,而以每個(gè)Cu(Ⅱ)離子為中心均形成了八面體幾何構(gòu)型。在1中同一個(gè)L的5個(gè)雜環(huán)原子[N(1), N(2), O(3), O(4), O(5)]分別與3個(gè)Cu(Ⅱ)離子[Cu(1), Cu(2), Cu(2#)]發(fā)生了配位作用,而O(3)則是起到橋聯(lián)作用的L的酚氧原子。在配位中心離子中,Cu(1)和Cu(2)雙雙被L的O(3)和三齒螯合苦味酸根離子的O(7)所橋聯(lián),二者之間的距離為0.323 5(8) nm。 Cu(1)-O(3)和Cu(1)-O(7)的鍵長(zhǎng)分別為0.193 8(3) nm和0.194 1(3) nm,而二者則分別短于Cu(2)-O(3)和Cu(2)-O(7)的鍵長(zhǎng)[0.206 1(3) nm, 0.239 3(3) nm]。兩個(gè)配位平面[O(3)-Cu(1)-O(7)和O(3)-Cu(2)-O(7)]之間的二面角為9.06°。

表1 1的晶體學(xué)數(shù)據(jù)Table 1 Crystal data of 1

表2 1的主要鍵長(zhǎng)Table 2 Selected bond lengths of 1
2.2 1的熱穩(wěn)定性
1的熱分析結(jié)果表明,1 在25 ℃~600 ℃有兩個(gè)失重階段:第一階段在43 ℃~96 ℃,質(zhì)量損失7.1%(理論值7.2 %),對(duì)應(yīng)失去2個(gè)結(jié)晶丙酮分子和2個(gè)結(jié)晶水分子,伴隨此過(guò)程有一個(gè)較強(qiáng)吸熱峰出現(xiàn),峰溫64 ℃;第二階段在121 ℃~430 ℃,失重緩慢,質(zhì)量損失77.4%(理論值77.6%),對(duì)應(yīng)失去配位水分子及部分有機(jī)質(zhì),此過(guò)程先出現(xiàn)一個(gè)較弱吸熱峰后緩慢放熱,該過(guò)程為1的分步氧化分解過(guò)程。總質(zhì)量損失為84.5%(理論值84.8%),余下15.5%的殘余物與CuO相當(dāng)(理論值15.2%)。
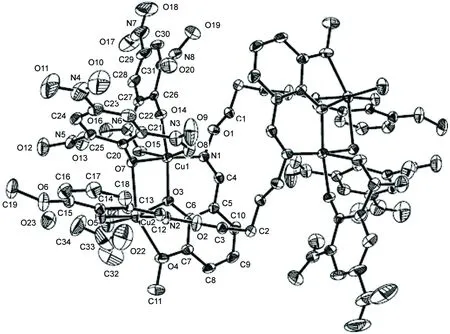
圖2 1的分子結(jié)構(gòu)圖Figure 2 Molecular structure of 1
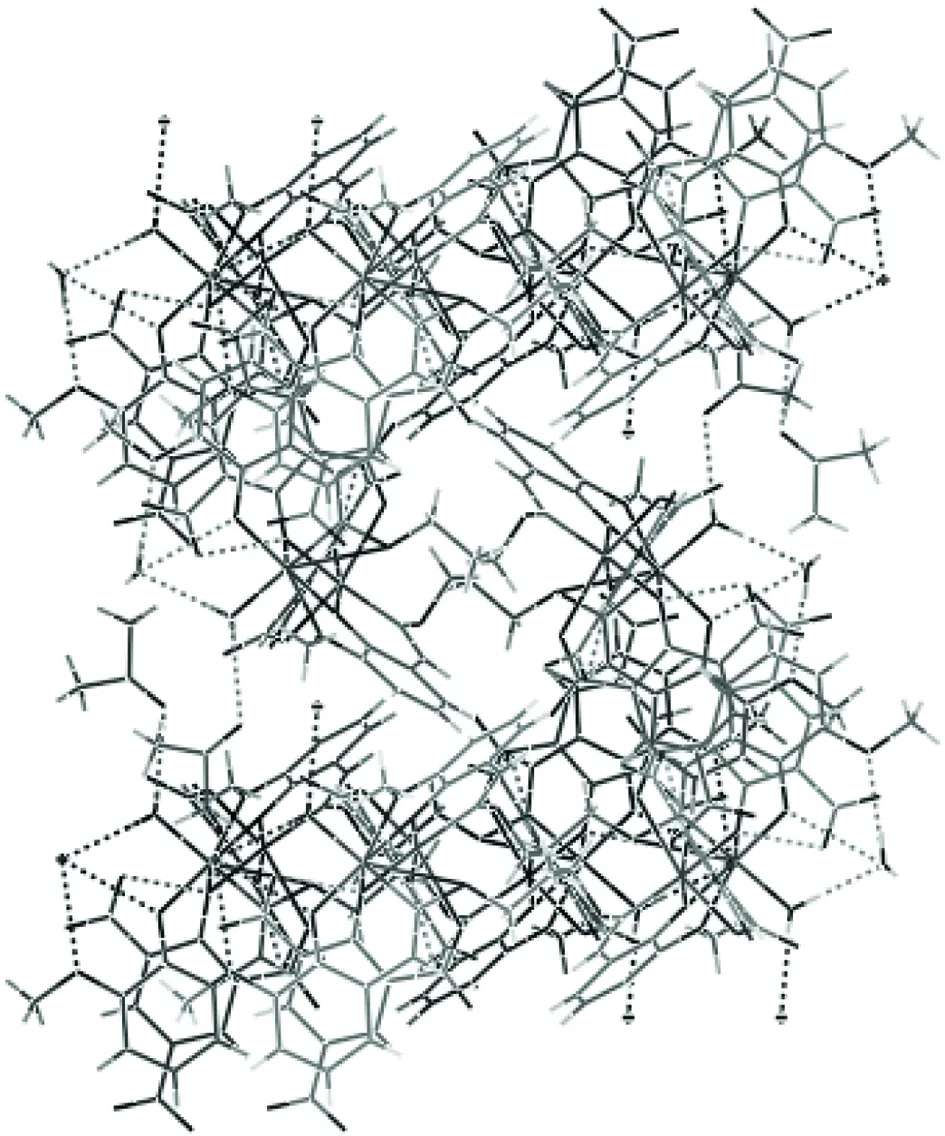
圖3 1的c軸晶胞堆積圖Figure 3 Packing structure of 1 viewed along the c-axis
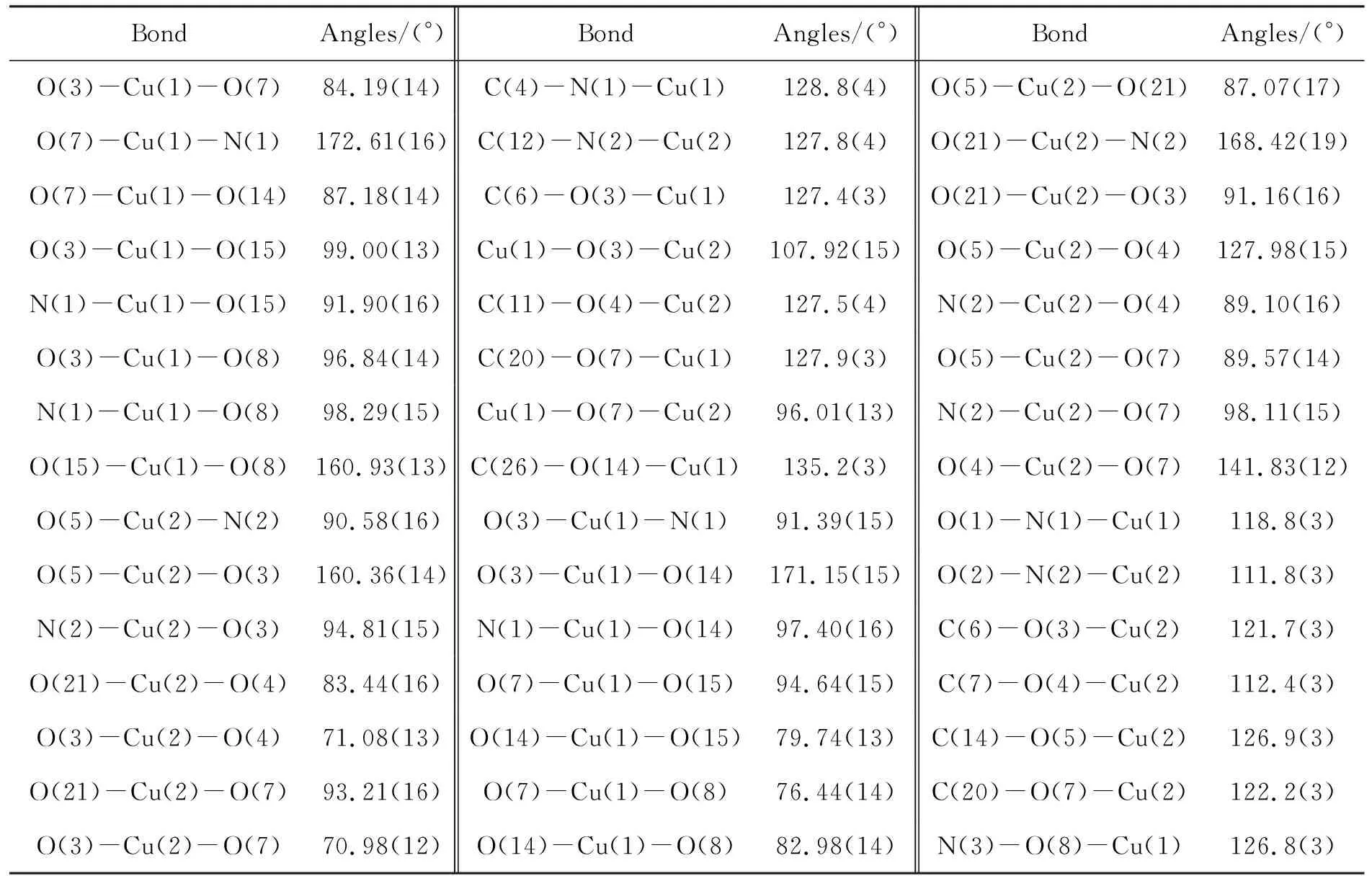
表3 1的主要鍵角Table 3 Selected bond angles of 1
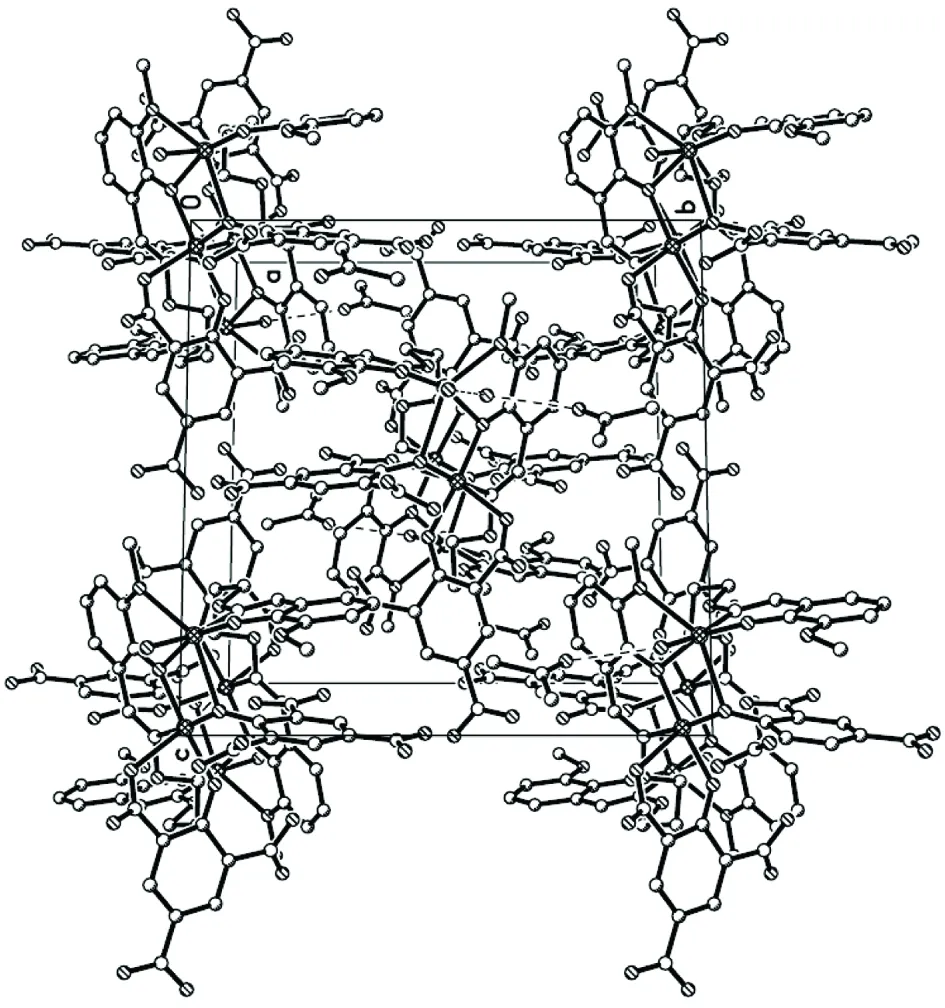
圖4 1的a軸晶胞堆積圖Figure 4 Packing structure of 1 viewed along the a-axis
3 結(jié)論
合成了一種新型的苦味酸銅(Ⅱ)配合物,其在DMF和DMSO中的摩爾電導(dǎo)值分別為25.6 Ω-1·cm2·mol-1和37.2 Ω-1·cm2·mol-1。 配合物為四核配合物,由4個(gè)Cu(Ⅱ)離子,2個(gè)配體單元L(提供N2O2給予體),4個(gè)苦味酸根離子,2個(gè)配位水分子,2個(gè)結(jié)晶丙酮分子和2個(gè)結(jié)晶水分子組成。以每個(gè)銅原子為中心均形成了六配位的稍微扭曲的八面體幾何構(gòu)型,參與配位的苦味酸根在該配合物中采用了一種新的三齒配位模式。
[1] Lacroix P G. Second-order optical nonlinearities in coordination chemistry:The case of bis(salicylaldiminato)metal Schiff base complexes[J].Eur J Inorg Chem,2001,14(1):339-348.
[2] Houjou H, Nagawa Y, Hiratani K. Spontaneous macrocyclization via recombination of a Schiff-base linkage[J].Tetrahedron Lett,2001,42:3861-3863.
[3] Baseer M A, Jadhav V D, Phule R M. Synthesis and antibacterial activity of some new Schiff bases[J].Oriental Journal of Chemistry,2000,16(3):553-556.
[4] Costes J P, Dahan F, Dupuis A. Influence of anionic ligands(X) on the nature and magnetic properties of dinuclear LCuGdX3·nH2O complexes(LH2standing for tetradentate Schiff base ligands deriving from 2-hydroxy-3-methoxybenzaldehyde and X being Cl,N3C2,and CF3CO2)[J].Inorg Chem,2000,39(2):165-168.
[5] Akine S, Taniguchi T, Nabeshima T. Novel synthetic approach to trinuclear3d~4fcomplexes:Specific exchange of the central metal of a trinuclear zinc(Ⅱ) complex of a tetraoxime ligand with a lanthanide(Ⅲ)[J].Angew Chem Int Ed,2002,41:4670-4673.
[6] Sun S S, Stern C L, Nguyen S T,etal. Directed assembly of transition-metal-coordinated molecular loops and square from Salen-type components.Examples of metalation-controlled structural conversion[J].J Am Chem Soc,2004,126:6314-6326.
[7] Akine S, Dong Wen-kui, Nabeshima T. Octanuclear zinc(Ⅱ) and cobalt(Ⅱ) clusters produced by cooperation tetrameric assembling of oxime chelate ligands[J].Inorg Chem,2006,45:4677-4684.
[8] Reglinski J, Morris S, Stevenson D E. Supporting conformational change at metal centres.Part 1:octahedral systems[J].Polyhedron,2002,21:2175-2182.
[9] Venkataramanan N S, Kuppuraj G, Rajagopal S. Metal-salen complexes as efficient catalysts for the oxygenation of heteroatom containing organic compounds-synthetic and mechanistic aspects[J].Coord Chem Rev,2005,249(11-12):1249-1268.
[10] Dong W K, Feng J H, Yang X Q. Crystal structure of 4,4′-dibromo-2,2′-[(1,3-propylene)dioxybis(nitrilomethylidyne)]diphenol,C17H16N2O4Br2[J].Z Kristallogr NCS,2006,221:447-448.
[11] Wen-kui Dong, Jian-hua Feng, Li Wang,etal. Synthesis and structural characterization of a novel tetranuclear Cu(Ⅱ) complex:[Cu4L2(pic)4(H2O)2]·2H2O[J].Trans Met Chem,2007,32:1101-1105.
[12] Akine S, Takanori T, Dong Wen-kui,etal. Oxime-based Salen-type tetradentate ligands with high stability against imine metathesis reaction[J].J Org Chem,2005,70:1704-1711.
[13] Wenkui Dong, Jianhua Feng, Li Xu,etal. Synthesis,crystal structure and thermal behavior of {4,4′,6,6′-tetra(tert-butyl)-2,2′-[ethylenedioxybis(nitrilomethylidyne)]diphenolato}Cu(Ⅱ)[J].Indian Journal of Chemistry,2008,47A:1343-1347.

