頂空固相微萃取-氣質聯用分析不同儲藏條件下小麥粉揮發性成分變化
袁 建 付 強 高瑀瓏 鞠興榮 沈崇鈺
(南京財經大學食品科學與工程學院1,南京 210003)
(江蘇進出口檢驗檢疫局2,南京 210004)
頂空固相微萃取-氣質聯用分析不同儲藏條件下小麥粉揮發性成分變化
袁 建1付 強1高瑀瓏1鞠興榮1沈崇鈺2
(南京財經大學食品科學與工程學院1,南京 210003)
(江蘇進出口檢驗檢疫局2,南京 210004)
利用頂空固相微萃取和氣相色譜-質譜(HS-SPME-GC/MS)對不同儲藏條件下的小麥粉揮發性成分進行研究。對固相微萃取頭、萃取溫度、萃取時間和解析時間進行條件優化。實驗結果表明:小麥粉揮發性成分的最佳分析條件為,萃取頭DVB/CAR/PDMS;萃取溫度80℃;萃取時間60 min;解析時間3 min。經鑒定分析小麥粉中揮發性成分主要有烴類、醛類、酮類、醇類、有機酸及雜環類等多種成分。原樣和儲后2個月樣中最高的是烴類和醛類,其次為醇類、酮類。儲藏2個月后,變化較明顯的揮發性物質有己醛、苯甲醛、辛醛、2-壬醛、己醇、十二烷、十六烷和十八烷。
小麥粉 儲藏 揮發性成分 頂空固相微萃取 氣質聯用
小麥粉在儲藏期間由于完全喪失了保護組織,其品質會因儲藏環境以及有害生物等的變化而不斷變化。因而,小麥粉會逐漸失去原有的香味、食味而產生各種異味、霉味、酸味和哈味,以及小麥粉顏色變灰暗,酸度增高等現象。
目前國內外關于利用頂空固相微萃取技術分析小麥[1]、稻谷[2]、大米[3]、玉米[4]等揮發性成分的研究較多,且已把揮發物作為谷物儲藏品質檢測的重要指標之一。Lorenz等[5]通過對冬麥和春麥粉比較發現,兩種小麥粉揮發物無本質區別,只有量的差別。Lorenz等[5]和 Youngs等[6]研究發現小麥粉中主要含有低分子醛類,烴類化合物在小麥粉中含量很少,n-正構烷在C9和C33之間,且C11含量最少。
目前有關小麥粉儲藏過程中揮發物變化研究尚未見報道。因此若能找到一種或幾種揮發性物質來反映小麥粉的儲藏品質,對指導小麥粉安全儲藏,減少糧食損失具有重要意義。
1 材料與方法
1.1 儀器與材料
7890A/5975C GC/MS氣質聯用儀和20 mL頂空微萃取瓶:美國 Agilent公司;30 m ×0.25 mm ×0.25 μm DB-5MS色譜柱:美國Agilent公司;固相微萃取頭:美國Supelco公司;CH-9230恒溫水浴鍋:瑞士步琪公司;PQX-300D型多段可編程人工氣候箱:寧波東南儀器有限公司。
含水量為14%的新加工中筋小麥粉(產自江蘇,儲藏期為1年):南京金陵面粉有限公司。取小麥粉樣品600 g裝入自封袋,密封后置于人工氣候箱中,分別在20、25、30和35℃條件下進行儲藏試驗。
1.2 樣品制備
稱取5.00 g小麥粉加入頂空樣品瓶中,密封后置于預先設好的恒溫水浴鍋中平衡10 min,再將萃取頭插入頂空瓶吸附60 min,于 GC/MS進樣口250℃解析3 min。
1.3 GC/MS 分析條件
采用DB-5MS毛細管柱;MSD檢測器;升溫程序:起始溫度40℃,保持4 min;以5℃/min上升至200℃,保持2 min;再以20℃/min上升至280℃,保持4 min;進樣口溫度250℃;載氣:He;氦氣流速1.0 mL/min;不分流方式。
質譜條件:離子源EI源,離子源溫度230℃,接口溫度280℃,電子能量為70 eV,掃描范圍m/z為50.0~500.0,采集方式 Scan。
1.4 數據處理
樣品中各未知揮發性成分的定性由計算機檢索與NIST08標準質譜庫匹配求得,統計匹配度均大于800左右的揮發性成分;揮發性成分定量分析采用峰面積歸一化法。
2 結果與討論
2.1 固相微萃取頭的選擇
合適的萃取纖維頭對提取待測物質具有重要影響。本試驗選用了4種萃取頭:100 μm PDMS(聚二甲基硅氧烷)、65 μm PDMS/DVB(聚二甲基硅氧烷/聚二乙烯基苯)、85 μm PA(聚甲基丙烯酸甲酯)和30/50 μm DVB/CAR/PDMS(聚二甲基硅氧烷/碳分子篩/聚二乙烯基苯),在相同的吸附時間(60 min)、萃取溫度(80℃)和解析(250℃ 3 min)條件下比較。
如圖1所示,中等極性DVB/CAR/PDMS萃取總峰面積明顯最大,而極性PA涂層的吸附能力最差,因此,本研究選擇30/50 μm DVB/CAR/PDMS萃取頭。
2.2 萃取溫度及時間的選擇
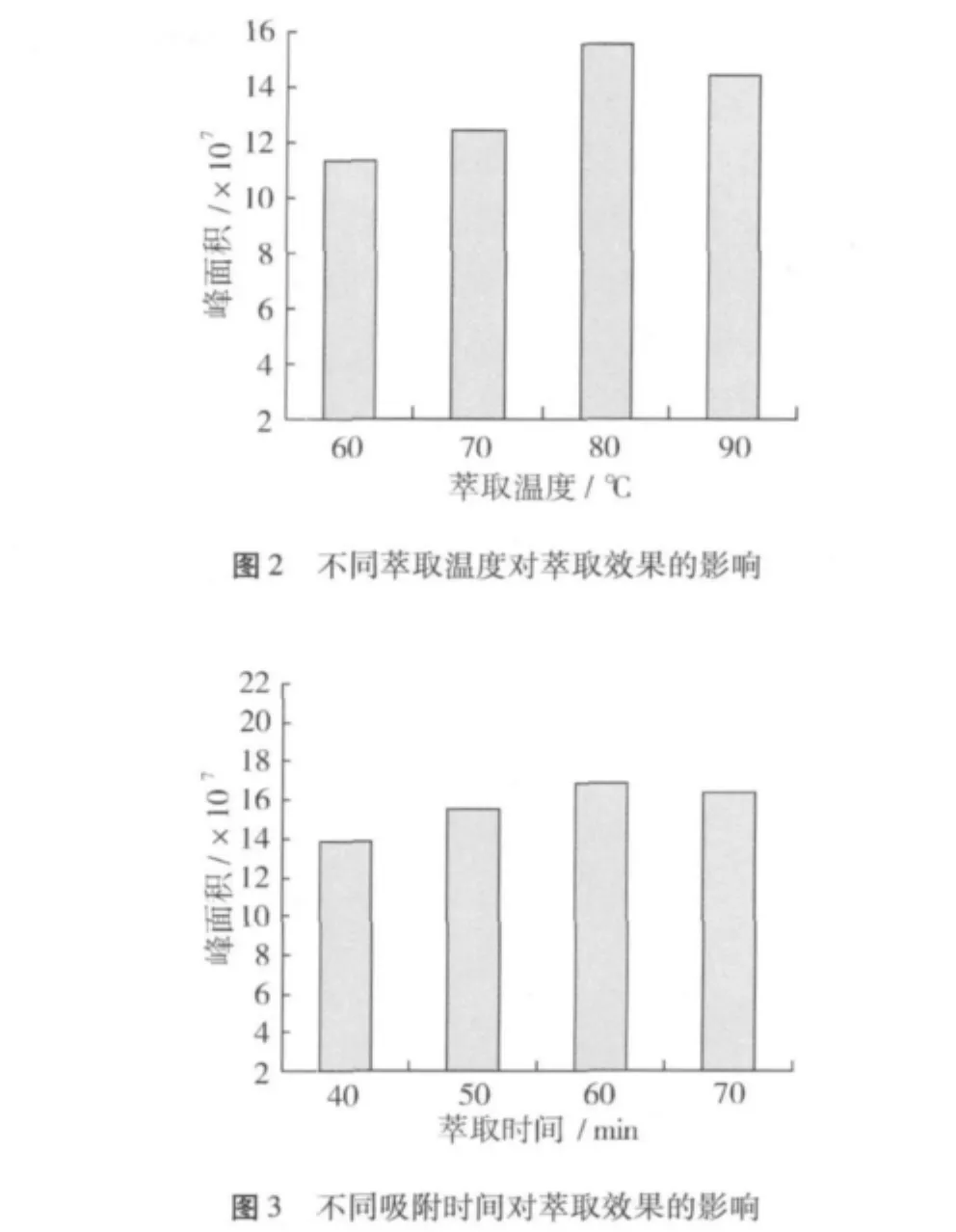
萃取溫度對吸附樣品的影響具有兩面性[7],一方面,升高溫度有利于頂空萃取;另一方面,升高溫度同時會降低萃取頭萃取分析組分的能力。本試驗選取30/50 μm DVB/CAR/PDMS萃取頭,分別在60、70、80、90℃4種溫度下考察萃取溫度對萃取效果的影響。結果表明,隨著萃取溫度的升高,峰面積呈遞增趨勢,在80℃時峰面積達到最大1.5×108,后又下降。因此,以80℃作為萃取溫度,見圖2所示。
萃取時間過長和過短都不利于樣品的收集。本實驗比較了在萃取溫度80℃下40、50、60和70 min 4個不同萃取時間。隨著萃取時間的延長,峰面積遞增幅度不大,特別在60和70 min處,見圖3所示,峰面積相接近,本研究萃取時間為60 min。
2.3 解析時間的選擇
解析時間不完全時將會影響下一次測定,本研究采用250℃下分別解析1、3、5 min。圖4結果表明,樣品解析量隨解析時間的延長呈現先上升后下降趨勢,在3 min時達到最大,可能由于解析時間過長而導致不同的峰相疊加造成峰面積下降。

圖4 不同解析時間對萃取效果的影響
2.4 精密度
在最佳頂空固相微萃取條件下,同一樣品進行5次重復性試驗,計算總峰面積和總峰高的相對標準偏差,總峰面積0.31%和總峰高4.04%。
2.5 SPME提取的小麥粉揮發性物質及鑒定
使用優化的SPME提取條件對小麥粉揮發性物質進行GC/MS鑒定,如圖5所示。共檢出43種化合物,其中醛類12種,醇類8種,酮類最少5種,烷烴類最多18種,各成分及相對含量見表2。小麥粉大部分成分出峰位置相似,僅在含量上有所區別。與原始樣品相比,不同儲藏溫度下小麥粉種類差別主要在8~22 min之間,且色譜峰圖形有所不同,說明揮發性成分組成存在差別。說明在上述氣相色譜條件和萃取方法下,可將原始樣品以及儲藏后2個月樣品中的各個揮發性成分達到最好的分離效果。

圖5 不同儲藏時間、溫度下小麥粉揮發性成分總離子流色譜圖
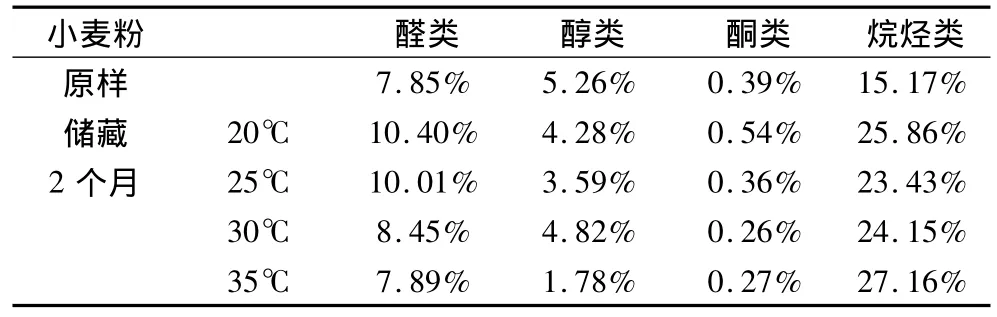
表1 小麥粉各類揮發性成分質量分數隨儲藏溫度的變化
由表1知,儲藏后與原樣相比,醛類質量分數最大增加了2.19%,35℃時烴類含量比原樣增加了79.04%,醇類下降幅度最大比原樣少了3.48%,酮類隨溫度的升高而下降,20℃時最高為0.54%,35℃時最小為0.27%。在揮發性成分中,烷烴類所占面積百分比含量最大,可能一方面是因為烷烴類種類較多,主要含有大量支鏈烷烴類;另一方面因為在儲藏過程中,小麥粉未發生明顯變質現象,即沒有產生大量的醛、酮類物質。因此,烷烴類物質在4類揮發物中的相對含量最高。
其次,各溫度間總揮發物含量差別不大,20℃時含量最高,總揮發物含量比原樣增加了43.29%。35℃總揮發物含量增加的最小,增加值為37.1%。除烴類隨儲藏溫度增高略有增加外,醛、酮和醇類隨溫度的升高呈明顯下降趨勢。
2.6 儲藏過程小麥粉揮發性物質變化
小麥粉揮發性成分中烴類、醛類、醇類主要是由脂類的氧化或分解而形成的;酮類主要是糖類或蛋白質的降解,也可能是微生物引起上述揮發性成分的變化。
除少量硅氧烷類化合物以及柱流失外,在匹配度大于800的43種揮發物中,變化較為顯著的主要成份見表2。
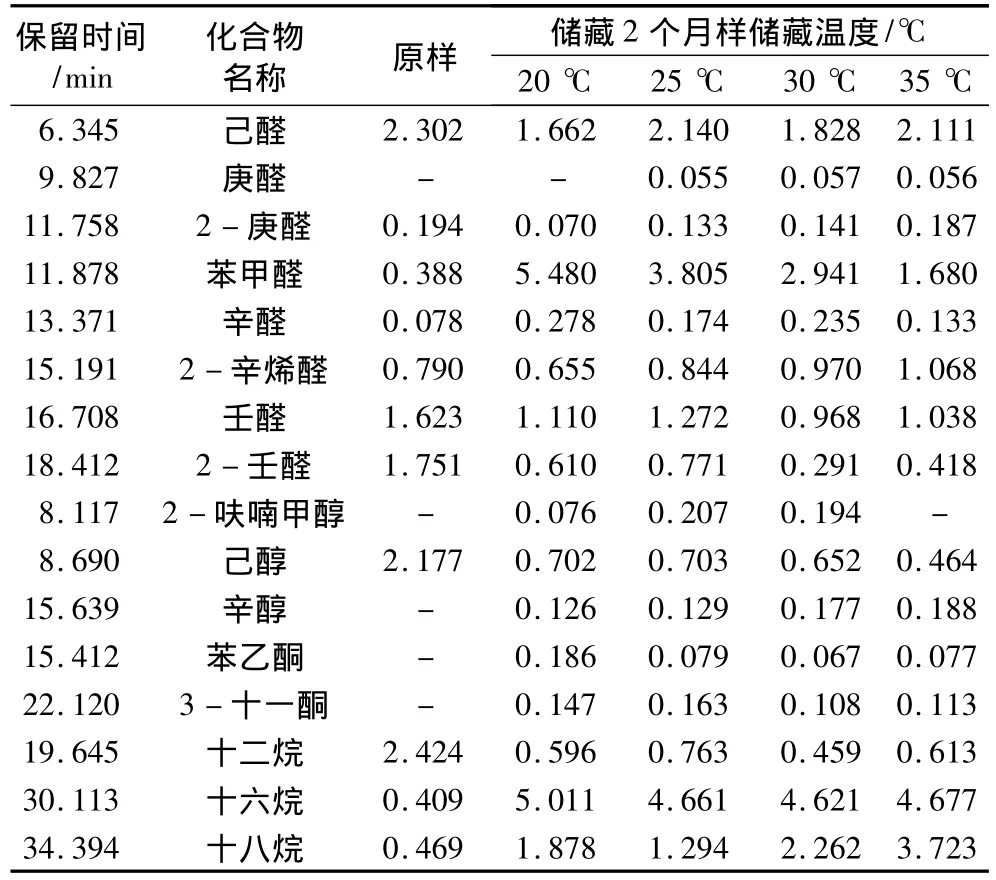
表2 小麥粉各類揮發性成分及質量分數/%
由表2可知,對于醛類,庚醛在原樣中未檢出,己醛、2-庚醛、壬醛、2-壬醛下降較為明顯,儲藏2個月后小麥粉中苯甲醛、辛醛要比原樣高,其他揮發物含量變化不明顯。己醛、2-庚醛、2-辛烯醛隨儲藏溫度升高而明顯增高;苯甲醛和辛醛隨儲藏溫度的升高呈下降趨勢,其余各物質無明顯變化規律。對于醇類,2-呋喃甲醇、2-乙基-己醇、辛醇、2-己基-癸醇在原樣中未檢出,己醇下降最為明顯,從2.177%下降到最低的0.464%,而其他物質變化無明顯趨勢,除辛醇隨儲藏溫度升高而明顯增高外,其余所有醇類物質隨儲藏溫度的升高呈下降趨勢。苯乙酮、3-十一酮在原樣檢出,且隨儲藏溫度升高而下降。烷烴類,下降較明顯的有十二烷、十四烷、壬基-環戊烷。上升較明顯的有十六烷、十七烷、十八烷,其中3-甲基-十八烷在原樣中無檢出,其余無明顯變化規律。除十七烷、十八烷和二十烷等隨儲藏溫度的升高而升高外,大部分烷烴類隨儲藏溫度的升高呈下降趨勢。
3 結論
利用頂空固相微萃取和氣相色譜-質譜技術對不同儲藏條件下小麥粉的揮發性成分進行研究,優化了試驗條件,包括固相微萃取頭、萃取溫度、萃取時間和解析時間。小麥粉揮發性成分的最佳分析條件為:萃取頭DVB/CAR/PDMS,萃取溫度80℃,萃取時間60 min,解析時間3 min,經鑒定分析小麥粉中揮發性成分主要有烴類、醛類、酮類、醇類、有機酸及雜環類等多種成分。
原樣和儲后2個月樣中各揮發性成分總含量順序沒什么變化,最高的是烴類和醛類,其次為醇類、酮類。醛類質量分數比原樣最大增加了2.19%,35℃時烴類含量比原樣增加了79.04%,醇類和酮類隨儲藏溫度的升高而下降,而各溫度間總揮發物含量差別不大。儲藏2個月后,變化較明顯的揮發性物質有庚醛、苯甲醛、辛醛、2-壬醛、己醇、十二烷、十六烷和十八烷。
[1]張玉榮,高艷娜,林家永,等.頂空固相微萃取-氣質聯用分析小麥儲藏過程中揮發性成分變化[J].分析化學,2010,38(7):953 -957
[2]林家永,高艷娜,吳勝芳,等.頂空固相微萃取-氣質聯用法分析稻谷揮發性成分[J].食品科學,2009,30(20):277-282
[3]周顯青,張玉榮,張勇.儲藏玉米陳化機理及揮發物與品質變化的關系[J].農業工程學報,2008,24(7):242-246
[4]Riana W,John D C,Michael W.Changes in volatile components of paddy,brown and white fragrant rice during storage[J].Journal of the Science of Food and Agriculture,1996,71:218-224
[5]Lorenz K,Maga J A.Triticale and wheat flour studies:composition of fatty acid,carbonyls,and hydrocarbons[J].Journal of the Agriculture of Food Chemistry,1972,26(1):769 -772
[6]Youngs V L,Gilles K A.Wheat hydrocarbons[J].Cereal Chemistry,1970,47(4),317 -323
[7]田懷香.金華火腿風味物質研究及其風味基料的研制[D].江蘇:江南大學,2005:23.
Analysis of Volatile Compounds Changes in Wheat Flour during Storage by Headspace Solid Phase Micro-Extraction and Gas Chromatography-Mass Spectrometry
Yuan Jian1Fu Qiang1Gao Yulong1Ju Xingrong1Shen Chongyu2
(College of Food Science and Engineering,Nanjing University of Finance and Economics1,Nanjing 210003)
(Import and export inspection and Quarantine Bureau of Jiangsu2,Nanjing 210004)
The volatile compounds of wheat flour sample were analyzed by using headspace solid-phase micro- extraction,together with gas chromatography and mass spectrometry.The HS - SPME conditions such as extraction fiber,extraction temperature,extraction time,and desorption time have been optimized.The results showed that the optimized pretreatment conditions were DVB/CAR/PDMS,80 ℃,60 min,and 3 min,respectively.The main volatile compounds in wheat flour by this identification method were hydrocarbons,aldehydes,alcohols,ketones,organic acid and heterocyclic material.The wheat flour volatile compounds with more significant changing after two months storage were hexanal,benzaldehyde,octanal,2 - nonenal,hexanol,dodecane,hexadecane and octadecane.
wheat flour,storage,volatile compounds,head space solid phase micro - extraction,gas chromatography-mass spectrometry
TS211.7
A
1003-0174(2012)04-0106-04
國家科技支撐計劃(2006BAD08B04),國家科技支撐計劃重點項目(2009BAD A0B005)
2011-06-15
袁建,男,1965年出生,教授,食品質量與安全

