獸藥GMP 復驗準備之淺見
馮小花,洪厚成,張長弓,王 璐
(1.湖南省畜牧獸醫研究所,湖南長沙 410131;2.湖南省平江縣三陽鄉畜牧獸醫水產站,湖南平江 414500;3.湖南廣大畜牧獸醫研發有限公司,湖南長沙 410131)
獸藥GMP 即獸藥生產質量管理規范(Good ManufacturingPractice for Animal Drugs)的簡稱。近兩年來,獸藥企業已進入第二輪GMP 復驗高峰期,筆者結合自身的獸藥GMP 復驗工作經驗,對獸藥GMP 復驗準備工作中主要問題進行了總結和分析。
1 復驗工作計劃表的制定
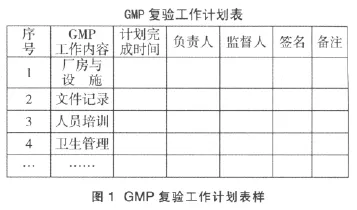
從準備復驗工作到GMP 正式檢查,大概需要半年到一年的時間。獸藥GMP 工作主要分為硬件、軟件和濕件三大類。硬件包括獸藥生產企業的生產環境、廠房設施、設備等,是實施獸藥GMP 的“舞臺”;軟件包括:制度、組織、記錄、教育培訓等管理規定;濕件是指人,是實施獸藥GMP 的主體。針對如何能有效的開展GMP 復驗工作,企業最好制定一個切實可行的GMP 復驗工作計劃表,如圖1 所示。
由表樣可看出總工作計劃表具體落實到人,落實到工作完成期限,增強了員工個人的責任感。同時總工作計劃還可以具體到周計劃,每周末及時開工作例會,進行周工作總結,隨時發現問題,及時改正。這樣可以隨時掌握GMP 工作進度。
2 存在的主要問題及整改
2.1 廠房與設施方面
一些中小企業,由于考慮成本問題,中央空調或空調未定時開放,故車間溫濕度很難達到生產所需要求,不僅造成工人生產時對環境的不適,更重要影響了一些原料藥的質量。如制備粉散制劑,一些糖類物質(含中藥提取物)在高溫潮濕環境就很容易吸潮溶解變質;未定期進行車間十萬級及萬級潔凈區塵埃粒子計數檢測,或檢測數據不合格;除塵效果達不到要求;生產設備銹蝕、老化;水磨石地面污染變色嚴重,欠平整;車間外墻破損、開縫;廠區草坪雜草叢生。損壞較嚴重的應請專業施工隊伍進行維修,有必要時生產車間需停產整修。
2.2 倉庫方面
倉庫是GMP 檢驗項目的重點之一。倉庫面積、物料管理及物料的種類數量能反映出該公司的發展規模及經營管理狀況,倉庫應由原輔料庫、包材庫、成品庫構成,每個庫又分為待驗區、合格區和不合格區。倉庫的每一種物料必須要有貨位卡,有出入庫記錄。一些企業原先建設的倉庫面積已不能滿足現有庫存產品的擺放,物料管理混亂,有的產品甚至堆放到生產車間、辦公生活區域。各企業需根據其生產的劑型、物料種類及儲存要求,擴建倉庫或進行布局調整,增加必要的特殊管理倉庫,如危險品庫,陰涼庫等。倉庫需改擴建時,應按獸藥GMP 管理要求進行,同時應報獸藥主管部門備案。
2.3 實驗室檢測儀器設備及試劑方面
質檢實驗室包括高溫室、精密儀器室、天平室、中藥檢驗室、無菌室、生化室、理化室、澄明度儀室、水分測定室、小型儀器室、標定室等。一些中小企業缺乏必需的儀器設備,如無抗生素檢測、無菌檢測設施設備,可想而知,平時就沒有做抗生素制劑的效價測定、注射液無菌檢測等相關項目。遇到GMP 檢查,就臨時借用,這種情況在GMP 復驗中是嚴格禁止的。試驗室的每臺儀器都必須具備儀器設備卡、經當地市計量監督局審查合格簽發的合格證,同時也要具備儀器操作規程、使用及清潔記錄;試驗室需配備相應的溫濕度表及做好溫濕度記錄;無菌室應定期做好塵埃粒子計數檢測并做好記錄。
試劑應有專門的試劑存放室。一些劇毒試劑如醋酸汞、三氧化二砷等必須雙鎖雙柜保存,嚴格控制好每次使用量并記錄完整;試驗室滴定液應有相關的配制與標定記錄;實驗室對照品一般需到中國藥品監察所購買,也可到省市藥檢所購買;生產中所用的原料尤其是中草藥原料都必須采用標本留樣的方式,置于中藥檢驗室;實驗室菌種的購買,最好固定一個采購點,以免影響菌種的純度,減少實驗誤差。
2.4 員工培訓工作方面
人員培訓工作一般包括車間工人培訓、質保部培訓及全員培訓,此外員工入職前均應有上崗前培訓。當前獸藥生產企業人員流動性比較大,不少企業現在職的人員與前次驗收相比有了很大改變,但企業對新的生產、質量等關鍵崗位負責人沒有及時任命和授權,質檢負責人變更后也沒有到省所備案;新補充的質量檢驗人員未經過足夠的培訓,無上崗證;車間制劑配料工人不是相關藥學專業畢業或學歷偏低;國內大部分獸藥企業生產第一線的工人文化水平偏低,遠遠達不到GMP 的學歷要求(車間工人必須具備高中或高中以上學歷)。質保部檢驗人員須經省級藥檢所培訓并頒發檢驗合格證書方可上崗開展檢測工作,如果需增加中藥提取生產線的,則需增加一名具有中藥檢驗證書的專職中藥師。企業應立足于培養內部管理人才,檢驗管理人員和生產管理人員都必須專職,不允許兼職或臨時“租借”外來人員。
2.5 狀態標識在獸藥GMP 中要引起足夠重視
狀態標識包括質檢實驗室、生產車間儀器設備狀態標識、衛生狀態標識、房間狀態標識、消防安全狀態標識等。其中儀器設備狀態標識卡使用的范圍比較廣,一般包括設備完好、運行中、已清潔、待清潔、待修等;車間房間狀態標識包括易清潔、待清潔、生產中等,狀態標識應根據實際生產情況隨時更換;廠區內應有禁煙標識、人流、物流標識;目前,獸藥生產企業在圖形標志管理方面存在的問題:有狀態標識卡卻未使用,圖形標志種類不足,標識與現場管理脫節,卡物不符、標識卡殘缺不全等等;在實施GMP 的過程中,應對標識引起足夠的重視,加強對標識卡的設計、分類及設置進行標準化規范,進一步加強對狀態標識的現場管理。
2.6 GMP 文件方面
文件是對實施GMP 的一種制度與考核,所謂有制度就應執行,有執行就應有記錄作為考核憑證。文件包括廠房與設施、人員管理、設備管理、記錄表格、衛生管理、驗證管理、生產管理、質量管理、物料管理、銷售管理、文件管理、自檢等十二大塊內容。記錄主要包括批生產記錄和批檢驗記錄兩大塊,此外還包括驗證、物料、自檢、產品質量檔案、人員培訓檔案、供應商審計檔案等記錄。在批生產與批檢驗記錄中,缺乏原始數據和液相圖譜、紫外圖譜。在員工培訓檔案上,有的企業只有培訓考核試卷而沒有現場培訓人員的簽到表及培訓現場照片。有些企業通過驗收后忽略了對供應商的審計工作,對新增加的主要供應商只一味注重供貨產品價格的高低,忽略了供貨產品的質量,對供應商的資質、質量信譽等未進行認真審查,也沒有建立相應的供應商檔案。
在迎接獸藥GMP 復驗的工作上,不少企業花費了大量的人力物力,因為這關系到企業的生存問題,更關系到企業的生存質量。農業部實施GMP的最終目的是引導獸藥生產企業通過獸藥GMP認證,去參加高品質的獸藥市場競爭,盡早地去占領高品位的獸藥市場,而不僅僅只是一種行政行為。一些小型獸藥企業一旦通過獸藥GMP 驗收,就省去了相關的一些人員和設備,還有個別企業生產偽劣獸藥,依靠低價、回扣等不正當競爭手段的獸藥生產企業,最終不僅是被吊銷《獸藥生產許可證》,而是遲早會被市場淘汰。
筆者希望我國獸藥企業立足于長遠發展,只有做好藥,做良心藥,動物和人類的健康才能得以保障,才會不斷涌現出更多、更強的獸藥GMP 企業,參與國際獸藥市場的競爭,為中國畜牧業發展做出貢獻。 □
[1] 鄭麗俠,鮑嘉銘,蒙英玲.實施獸藥GMP 需要把握的關鍵[J].甘肅畜牧獸醫,2007,197(6):47~48.
[2] 平 星,畢昊容,時 勇,等.獸藥GMP 復驗準備要點解析[J].中國獸藥雜志,2009,43(2):50~54.
[3] 秦國棟.對推廣獸藥GMP 的幾點看法[J].山東畜牧獸醫,2010,(l0):88~89.
[4] 邵耀東,徐 峰,周衛斌,等.文件管理在獸藥GMP 復驗時的重要性[J].山東畜牧獸醫,2009,(9):56~57.

