心力衰竭患者循環內皮祖細胞水平的Meta分析
承燕,胡若愚,2,江時森,2
(1.南京大學醫學院 臨床學院,江蘇南京 210002;2.南京軍區南京總醫院心內科,江蘇南京 210002)
1997年Asahara等[1]在成人外周血單個核細胞分 選出的CD34+細胞中發現可在體外向內皮表型分化
心力衰竭(heart failure,HF)患者都有一定程度的內皮細胞功能紊亂。他們的內皮細胞凋亡會增加,一氧化氮的合成也下降,從而影響到冠狀動脈和全身的灌注[2-3]。可以說內皮細胞的狀態從根本上影響著HF的發病率和死亡率。而骨髓中的干細胞能在一定程度上修復內皮的損傷,改善HF患者的心功能[4]。
于是一些人開始研究外周血中循環EPC(circulating EPC,cEPC)的數量與HF的關系,但因為這些多是小規模研究,而且結果并不完全一致,因此本研究采用Meta分析方法綜合評價cEPC與HF間的關系。
1 材料與方法
1. 1 資料來源
檢索PubMed、Embase和Cochrane library等數據庫尋找2000年10月至2011年10月公開發表的比較正常人和HF患者cEPC數量的文獻,其中包括期刊論文和會議文獻等。檢索方法:(endothelial progenitor cells or circulating angiogenic cells or circulating progenitor cells or endothelial outgrowth cells or endothelial progenitor outgrowth cells or outgrowth endothelial cells or((progenitor cells or stem cells)and(angiogenesis or neovascularization)))and heart failure,語種不限。同時至南京大學圖書館手工檢索相關文獻。
1. 2 納入標準
2000年10月至2011年10月發表的關于HF患者cEPC數量的研究;研究對象為HF患者,并有正常人作為對照;文獻提供平均值和標準差,或根據文獻提供數據可以轉化出平均值和標準差。
1. 3 排除標準
無對照組的文獻;同批研究對象重復報道的文獻;無目標結果、質量差或信息太少的文獻;非原始數據的文獻,如綜述。
1. 4 文獻選擇
由2位作者分別按照納入、排除標準獨立收集文獻,選出符合要求的研究。用Kappa值計算兩人對相關研究提取的一致性,如有異議,討論決定是否納入。
1. 5 統計學處理
采用RevMan 5.1軟件分析數據。用Q檢驗判斷各研究間的統計學異質性。若為同質研究則采用固定效應模型,若為異質研究則采用隨機效應模型進行Meta分析。
2 結 果
2. 1 文獻納入
兩位作者分別對初選文獻進行評價后進行一致性評測:Kappa值為0.87,表明本評價可靠性很好。計算機及手工共檢索到475篇文獻,閱讀文題和摘要排除重復或無關文獻后共收集到15篇文獻。閱讀全文后,發現15篇文獻中6篇信息較少或無目標結果,1篇病例組與對照組均小于10例,最后有8篇文獻[5-12]納入本Meta分析 。納入的8項研究共包括HF患者453例,對照166例。
2. 2 信息和數據抽提
抽提研究中對照組和HF組的基本信息(年齡、性別、基礎疾病、心臟功能等)和基本數據(人數、平均值、標準差或標準誤等)。由于各研究間cEPC水平的表達方式并不完全一致,有的用1 ml外周血內所含cEPC的數量表示,有的則用每106個細胞中所含cEPC的數量表示,所以本研究統一將各研究中HF患者的cEPC水平轉換成與正常對照相比的百分比,同時將部分原始數據中的標準誤統一轉換成標準差。
2. 3 發表偏倚
由于納入研究較少(n<10),漏斗圖沒有呈現典型的倒V型,但也未見明顯的發表偏倚(圖1)。
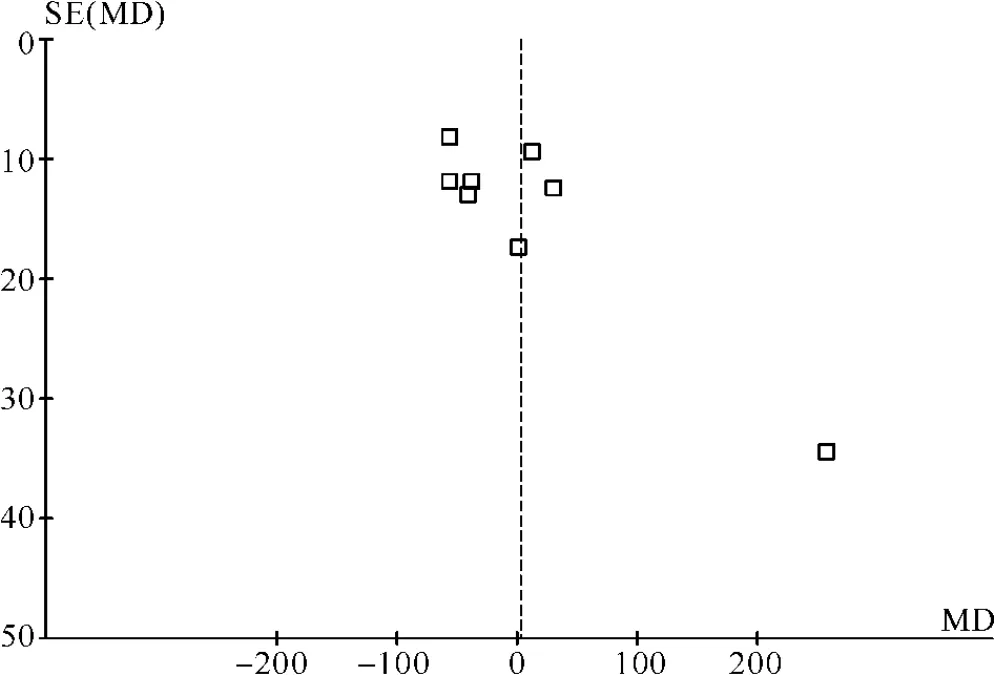
圖1 8項關于心力衰竭患者循環內皮祖細胞數量研究的Meta分析漏斗圖Fig 1 Funnel plot of eight studies about the level of circulating endothelial progenitor cells in patients with heart failure
2. 4 Meta 分析
2.4.1 cEPC在HF患者組和正常對照組的狀況 如圖2所示,8項研究間的異質性檢驗P<0.001,表明存在異質性,采用隨機效應模型分析數據。Z檢驗顯示P=0.88,表明兩組間 cEPC水平的差異無統計學意義。
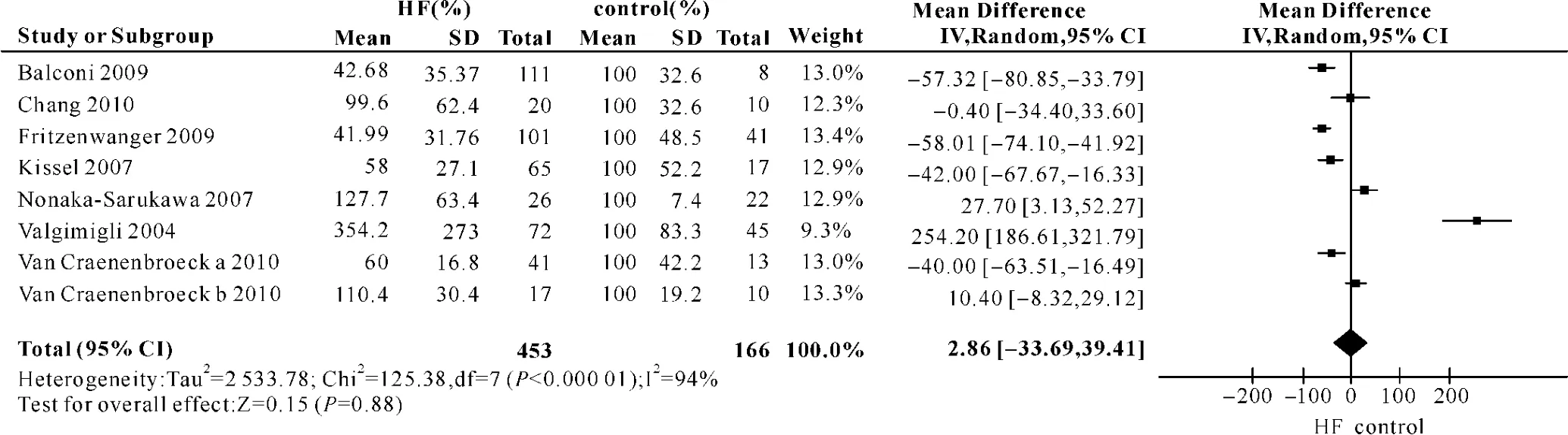
圖2 心力衰竭組(HF)與正常對照組(control)循環內皮祖細胞水平的比較Fig 2 Comparison of levels of circulating endothelial progenitor cells between patients with heart failure and healthy people
2.4.2 分層分析 根據心力衰竭的程度進行分層分析,分為輕度HF組(NYHA分級Ⅰ、Ⅱ級,Killip分級Ⅰ級)和中重度HF組(NYHA分級Ⅲ、Ⅳ級,Killip分級Ⅱ、Ⅲ、Ⅳ級)。Meta分析顯示:mean(95%CI)為69.24[12.09,126.39],Z檢驗P<0.05,表明輕度HF組和中重度HF組cEPC水平的差異有統計學意義(圖3)。
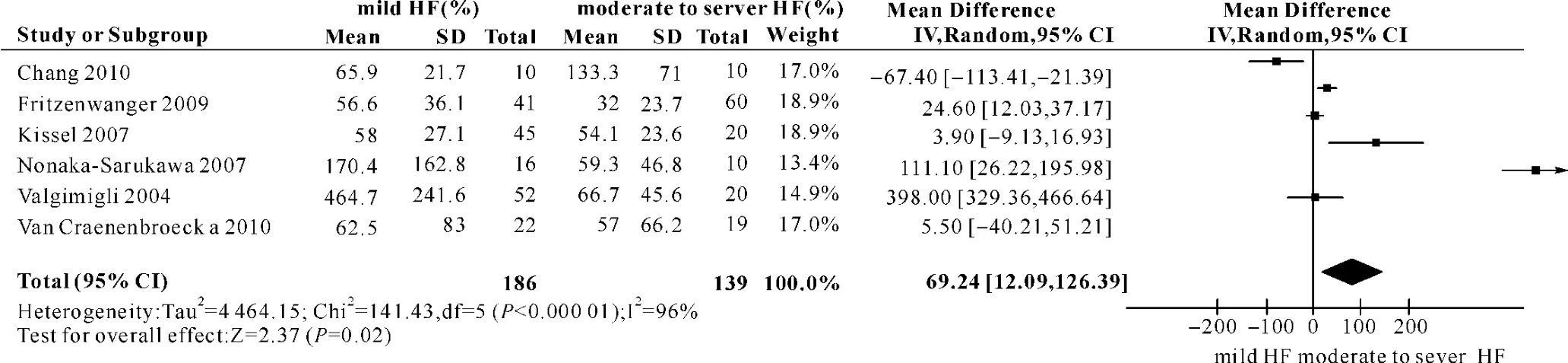
圖3 輕度心力衰竭組(mild HF)與中重度心力衰竭組(moderate to sever HF)循環內皮祖細胞水平的比較Fig 3 Comparison of levels of circulating endothelial progenitor cells between patients with mild heart failure and those with moderate to sever heart failure
2.4.3 cEPC在中重度HF患者組和正常對照組的狀況 如圖4所示,中重度HF組的cEPC數量較正常對照組平均下降37.19%,Z檢驗P=0.004,表明兩者間差異具有統計學意義。
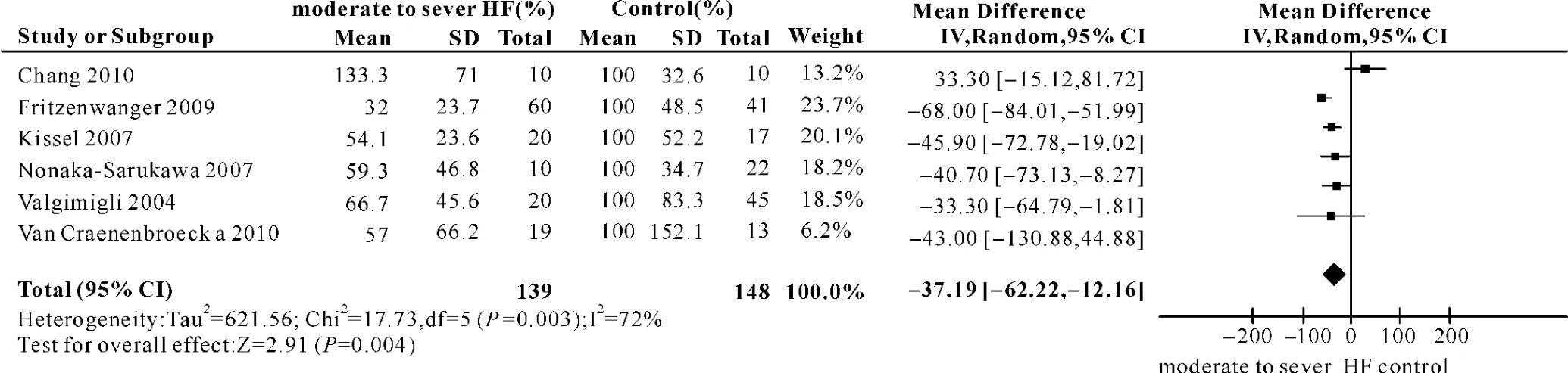
圖4 中重度心力衰竭組(moderate to sever HF)與正常對照組(control)循環內皮祖細胞水平的比較Fig 4 Comparison of levels of circulating endothelial progenitor cells between patients with moderate to sever heart failure and healthy people
3 討 論
十多年的研究顯示,EPC能改善心血管的功能,但是其具體機制還沒有被完全破解。目前認為骨髓中的EPC主要通過直接的增殖、遷移、分化和間接的分泌相關細胞因子來促進血管的新生與修復[13-15]。有研究[16]提示,cEPC的水平與心血管事件的風險密切相關,可以作為一個獨立的預后因素。現在臨床上有很多與心血管危險因素相關的指標,比如年齡、性別、血壓、血脂、血糖等等,每一個指標只能反映一個方面,卻無法體現總體效應。cEPC作為一個細胞層面的指標,有可能綜合多種不利因素復雜的相互作用,更好地反映體內真實的情況。
HF與cEPC有著怎樣的聯系,目前的研究結果并不完全一致。在納入的8項研究中,3項認為輕度HF患者的cEPC水平升高,而另外5項不支持此觀點;5項認為中重度HF患者的cEPCs水平下降,而還有1項不支持。我們進行正式的Meta分析可能有助于理清其中的關系。籠統地將所有HF患者的cEPC水平與正常人進行比較,發現兩者的差異沒有統計學意義,這提示需要進行亞組分析。將HF患者分為輕度組和中重度組后發現,兩組的cEPC水平存在明顯的差別。利用隨機效應模型進行Meta分析后顯示,中重度HF患者的cEPC水平較正常人下降,且下降程度具有統計學意義。
事實上很多因素都影響著cEPC的水平,比如年齡、雌激素、高血壓、高血脂、糖尿病、運動、吸煙、他汀類藥物等等[17]。雖然這8項研究在患者年齡、性別方面相似,但在Q檢驗中顯示具有異質性,可能與其他影響cEPC水平的因素存在差異有關,但這并不影響cEPC作為一個獨立的預后指標。
需要說明的是本Meta分析存在不可避免的局限性。首先納入的8項研究僅包括453例患者,可導致統計檢驗效能不足。不能排除日后大樣本研究結果加入后結論與此相背。其次對于EPC的鑒定存在差異:納入的8項研究中,6項選擇流式細胞儀鑒定細胞表面標志,1項研究選擇吞噬乙酰化低密度脂蛋白并結合荊豆凝集素這種功能上的鑒定,還有1項綜合了上述2類鑒定方法。雖然近十幾年來有很多EPC相關研究的發表,但是至今還沒有發現EPC特異性的細胞表面標志,在其鑒定上還存在著一定的爭議。這也不可避免地造成了多年來關于EPC研究結果的差異,但是Meta分析過程中(敏感性分析)未發現鑒定方法的差異對統計學結論的影響。
越來越多的證據提示,cEPC的水平很可能是HF預后的獨立影響因素[7,18]。本Meta分析結果表明,中重度HF患者較正常人的cEPC水平有顯著下降,與輕度HF患者相比也有明顯差異,體現出cEPC水平在HF患者預后中的重要性。實際上,除了簡單的cEPC計數外,cEPC的功能情況也是十分值得關注的。在今后的研究中,有必要采用統一的EPC鑒定指標,設計良好的隨機對照試驗,進行大規模的多中心臨床試驗來探索cEPC與HF的關系。
[1]ASAHARA T,MUROHARA T,SULLIVAN A,et al.Isolation of putative progenitor endothelial cells for angiogenesis[J].Science,1997,275(5302):964-967.
[2]NIESSNER A,HOHENSINNER P J,RYCHLI K,et al.Prognostic value of apoptosis markers in advanced heart failure patients[J].Eur Heart J,2009,30(7):789-796.
[3] BAUERSACHS J,WIDDER J D.Endothelial dysfunction in heart failure[J].Pharmacol Rep,2008,60(1):119-126.
[4]黎葉飛,盛祖龍,姚玉宇,等.兩種骨髓間充質干細胞移植途徑治療急性心肌梗死的比較研究[J].東南大學學報:醫學版,2011,30(5):687-691.
[5]CRAENBROECK E M,HOYMANS V Y,BECKERS P J,et al.Exercise training improves function of circulating angiogenic cells in patients with chronic heart failure[J].Basic Res Cardiol,2010,105(5):665-676.
[6]CRAENBROECK E M,BECKERS P J,POSSEMIERS N M,et al.Exercise acutely reverses dysfunction of circulating angiogenic cells in chronic heart failure[J].Eur Heart J,2010,31(15):1924-1934.
[7]SCHWARTZENBERG S,AFEK A,CHARACH G,et al.Comparative analysis of the predictive power of different endothelial progenitor cell phenotypes on cardiovascular outcome[J].World J Cardiol,2010,2(9):299-304.
[8]CHANG H W,LEU S,SUN C K,et al.Level and value of circulating endothelial progenitor cells in patients with acute myocardial infarction undergoing primary coronary angioplasty:in vivo and in vitro studies[J].Transl Res,2010,156(4):251-263.
[9]FRITZENWANGER M,LORENZ F,JUNG C,et al.Differential number of CD34+,CD133+and CD34+/CD133+cells in peripheral blood of patients with congestive heart failure[J].Eur J Med Res,2009,14(3):113-117.
[10]BALCONI G,LEHMANN R,FIORDALISO F,et al.Levels of circulating pro-angiogenic cells predict cardiovascular outcomes in patients with chronic heart failure[J].J Card Fail,2009,15(9):747-755.
[11] KISSEL C K,LEHMANN R,ASSMUS B,et al.Selective functional exhaustion of hematopoietic progenitor cells in the bone marrow of patients with postinfarction heart failure[J].J Am Coll Cardiol,2007,49(24):2341-2349.
[12]VALGIMIGLI M,RIGOLIN G M,FUCILI A,et al.CD34+and endothelial progenitor cells in patients with various de-grees of congestive heart failure[J].Circulation,2004,110(10):1209-1212.
[13]KRENNING G,LUYN M J,HARMSEN M C.Endothelial progenitor cell-based neovascularization:implications for therapy[J].Trends Mol Med,2009,15(4):180-189.
[14]SEN S,MCDONALD S P,COARES P T,et al.Endothelial progenitor cells:novel biomarker and promising cell therapy for cardiovascular disease[J].Clin Sci(Lond),2011,120(7):263-283.
[15]吳雪暉,羅飛,何清義,等.血管內皮祖細胞研究進展[J].醫學研究生學報,2008,21:981-985.
[16]WEMER N,KOSIOL S,SCHIEGL T,et al.Circulating endothelial progenitor cells and cardiovascular outcomes[J].N Engl J Med,2005,353(10):999-1007.
[17]LEONE A M,VALGIMIGLI M,GIANNICO M B,et al.From bone marrow to the arterial wall:the ongoing tale of endothelial progenitor cells[J].Eur Heart J,2009,30(8):890-899.
[18]MICHOWITZ Y,GOLDSTEIN E,WEXLER D,et al.Circulating endothelial progenitor cells and clinical outcome in patients with congestive heart failure[J].Heart,2007,93(9):1046-1050.

