1,3-丙二醇發酵液后提取技術研究進展
吳如春,許赟珍,劉德華
1 清華大學化工系應用化學研究所,北京 100084
2 廣西民族大學化學與生態工程學院 化學與生物轉化過程新技術廣西高校重點實驗室,南寧 530006
1,3-丙二醇發酵液后提取技術研究進展
吳如春1,2,許赟珍1,劉德華1
1 清華大學化工系應用化學研究所,北京 100084
2 廣西民族大學化學與生態工程學院 化學與生物轉化過程新技術廣西高校重點實驗室,南寧 530006
1,3-丙二醇是一種重要的化工原料,以甘油或葡萄糖為原料發酵法制備1,3-丙二醇具有原料可再生、反應條件溫和等優點,是近年來國內外的研究熱點。由微生物發酵獲得的 1,3-丙二醇發酵液是含多種強極性的醇及鹽類的稀溶液,這使得采用傳統的分離方法難以經濟、有效地的將 1,3-丙二醇從發酵液中純化出來,后提取過程成為發酵法工業化生產1,3-丙二醇的瓶頸。1,3-丙二醇后提取過程主要包括微生物菌體等高分子物質的去除,鹽的去除、回收,有機物的純化和水的去除。以下對應用于以上分離過程的技術的研究進展進行討論,提出在該領域應該重視的發展方向。
1,3-丙二醇,發酵液,后提取,研究進展
Abstract:1,3-propanediol is an important raw material in chemical industry. Microbial conversion of glycerol or glucose into 1,3-propanediol has been given much attention due to its renewable resource, mild reaction conditions, and other advantages. It is a challenge to efficiently separate 1,3-propanediol from a mixture of multiple components, such as 1,3-propanediol, 2,3-butanediol, water, residual glycerol, ethanol, macromolecules and salts, for the reason that 1,3-propanediol, glycerol and 2,3-butanediol are all very hydrophilic and have intense polarity. The conventional evaporation and distillation techniques used in the purification of 1,3-propanediol suffer from the problem of high energy consumption and low recovery. It makes the recovery of 1,3-propanediol from a fermentation broth become a bottleneck in industrial production. The down-stream processing of biologically produced 1,3-propanediol mainly includes the removal of protein,salts, water and other impurities. This paper analyze the research progress of these separation technologies and point out the developing direction worth further investigation.
Keywords:1,3-propanediol, fermentation broth, down-stream processing, research progress
1,3-丙二醇 (PDO) 是一種重要的化工原料,其最主要的一個用途是與對苯二甲酸生成聚對苯二甲酸丙二醇酯 (PTT)[1-2]。目前 1,3-丙二醇的生產方法有化學合成法和微生物發酵法[3-5]。相對于化學合成法,微生物發酵生產1,3-丙二醇具有原料可再生、操作簡便、反應條件溫和、副產物較少、環境污染小等優點。隨著石油資源的日益匱乏,利用可再生資源發酵生產1,3-丙二醇的路線越來越受到關注[6-7],其中以甘油為底物發酵制備 1,3-丙二醇的路線更是研究的熱點,這是由于甘油不僅是一種可再生資源,并且隨著生物柴油生產規模的不斷擴大,其副產物甘油的產量不斷增加,價格不斷下降,使得以甘油為底物發酵制備 1,3-丙二醇的工藝路線越來越具競爭力。在利用微生物發酵生產 1,3-丙二醇時,由于發酵液體系的復雜性使得產品的分離純化成本占生產總成本的50%以上,成為大規模生產1,3-丙二醇的瓶頸問題。
在微生物發酵生產 1,3-丙二醇的過程中,菌體在產生目標產物 1,3-丙二醇的同時還會產生 2,3-丁二醇及丁二酸、乙酸、乳酸等有機酸,使得發酵過程中發酵液的pH值不斷下降,影響菌體的生長,所以需要加入堿液 (如氫氧化鈉溶液) 來中和這些有機酸以保持發酵液中pH值的穩定,同時發酵培養基中含有硫酸銨等無機鹽類,因此發酵結束時發酵液是一種含目標產物 1,3-丙二醇的稀溶液,發酵液中的雜質包括大分子物質 (菌體、可溶性蛋白質、核酸和多糖等)、有機物 (甘油、2,3-丁二醇等)、鹽 (堿液與丁二酸、乙酸和乳酸等作用形成的鹽及培養基中未耗完的鹽) 和水。由于目標產物1,3-丙二醇在發酵液中的含量通常為80~110 g/L,同時1,3-丙二醇、2,3-丁二醇和甘油都是高沸點 (三者在常壓下的沸點分別為 214 ℃、184 ℃和 290 ℃)、親水性強的物質,因此將 1,3-丙二醇從這樣的復雜體系中分離出來是一項艱巨的任務[8],特別是鹽和2,3-丁二醇的存在會降低 1,3-丙二醇的最終收率而使整個提取成本增加。如在采用反應萃取法提純 1,3-丙二醇時,鹽的存在會使得作為催化劑的強酸性陽離子樹脂的催化效率下降;而在采用蒸發、精餾法提純 1,3-丙二醇的時候,鹽的濃度會隨著蒸發過程的進行不斷增加,最終使料液呈漿狀,不僅降低 1,3-丙二醇的收率,甚至會堵塞管路使過程無法進行。副產物2,3-丁二醇則由于其物化性質與 1,3-丙二醇接近,會使得多種提純方法難以進行,如常用的有機物提純方法-溶劑萃取法就無法實現二者的分離,而對于傳統的精餾法,二者沸點的相近使得分離所需的回流比增加,大大增加了能耗。目前 1,3-丙二醇后提取過程迫切需要尋找一條高效、低耗、環保的工藝路線。一些研究者嘗試引入新的技術來解決以上問題[9-10],如采用反應萃取法降低 1,3-丙二醇的強極性和強親水性后實現 1,3-丙二醇的分離和采用電滲析法來實現脫鹽過程中污染的減少等。另一些研究者考慮改進傳統的分離技術來適用于這個體系[11-12],如采用多效蒸發以降低過程能耗和開發新的適用于該體系的絮凝劑來實現較完全地去除大分子物質的目的。這些研究都取得了很大進展。一般而言,分離純化1,3-丙二醇需要3個步驟 (圖1),第一步是通過膜過濾、高速離心和溶劑沉淀等方法去除菌體等高分子物質;第二步是通過離子交換、電滲析等方法去除鹽類,最后一步是通過雙水相萃取、精餾和離子交換層析等方法純化 1,3-丙二醇。本文綜述了這些研究在經濟、高效地分離1,3-丙二醇方面取得的進展,并展望了今后發展的重點和方向。
1 生物高分子物質的去除
發酵結束后發酵液中生物高分子物質主要包括菌體及其細胞碎片、可溶性雜蛋白、核酸和其他膠狀物,從發酵液中分離 1,3-丙二醇的第一步是這些生物高分子物質的去除,否則隨著后續減壓蒸餾除水過程的進行,發酵液中殘留的蛋白、核酸和多糖等大分子物質的濃度會隨著水分的減少而逐漸升高,使料液呈濃漿狀,阻礙蒸餾操作的順利進行,并降低最終產物的收率。可以采用的分離方法主要有高速離心法、超濾法、有機溶劑沉淀法和絮凝法。
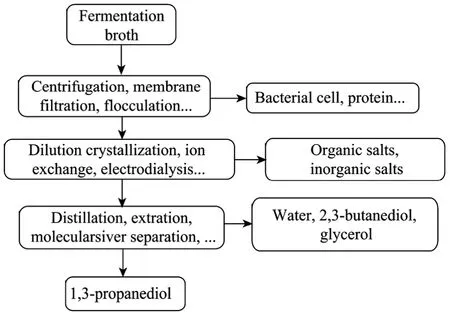
圖1 從1,3-丙二醇發酵液中回收、提純1,3-丙二醇的步驟及主要使用的分離方法Fig. 1 General scheme and major methods studied for the recovery and purification of 1,3-propanediol from fermentation broth.
1.1 高速離心法
該法屬于機械法,當離心機轉速到達一定后能將菌體等大分子物質沉降下來,實驗室采用這種方法可以實現1,3-丙二醇發酵液中大分子物質的去除,但該方法應用于工業規模時存在設備投入成本高、運行能耗大的缺點,經濟性差。
1.2 絮凝
絮凝法是通過加入絮凝劑后產生的電中和或橋連等作用促進液體中不易沉降的固體懸浮微粒結合成團、沉降后再經過過濾或離心來達到去除固體懸浮微粒的目的。Hao等[13]采用殼聚糖和聚丙烯酰胺兩種絮凝劑耦合對 1,3-丙二醇發酵液進行了絮凝處理,實驗結果表明發酵液中蛋白質的去除率大于99.0%。李凡鋒等[14]用天然絮凝劑Ⅱ型 B組分處理1,3-丙二醇發酵液時發現絮凝處理后可以加快后續電滲析脫鹽時的速度。魯詩峰等[15]對12種絮凝劑進行了篩選和工藝優化,其中分子量 4萬的殼聚糖絮凝效果較好,發酵液中菌體和蛋白質去除率分別為99.97%和 91.56%。該方法工業應用存在的問題是難以獲得便宜且高效的絮凝劑。
1.3 有機溶劑沉淀法
有機溶劑沉淀法是在含蛋白質、糖等物質的水溶液中加入乙醇、丙酮等能與水互溶的有機物,使高分子物質的溶解度顯著降低并從溶液中沉淀出來而達到分離目的的方法。修志龍等[16]利用乙醇來沉降生物大分子和回收有機酸鹽,實驗表明乙醇可以在去除 1,3-丙二醇濃縮液中的蛋白和核酸等大分子物質的同時使濃縮液中的有機酸鹽出現溶析現象,從而將大部分的鹽也分離出去。有機溶劑沉淀法具有分辨率高,溶劑易實現循環使用的優點,但該方法工業應用存在的問題是溶劑用量大,部分溶劑的殘留會影響最終1,3-丙二醇產品的質量。
1.4 超濾
超濾是根據物質相對分子質量的不同來進行分離的膜技術,其傳質推動力為靜壓差,其截留物質的分子量范圍為5 000~500 000 Da,是一種應用最廣泛的膜分離技術。我國研究開發的膜品種有以醋酸纖維素 (CA)、聚砜 (PS)、聚砜酰胺 (PSA)、磺化聚砜 (SPSF)、聚丙烯腈 (PAN)、聚氯乙烯 (PVC)、聚偏氟乙烯 (PVDF)、聚醚砜 (PES) 和聚醚酮(PEK)等為材料的有機膜和以陶瓷、多孔玻璃、氧化鋁等為材料的無機膜。
發酵液體系中存在大量的蛋白質、糖、色素和菌體等雜質,對所用膜的孔隙大小,耐酸性及膜通量方面都有較高的要求。魯詩峰等[17]使用三醋酸中空纖維透析膜對 1,3-丙二醇發酵液進行超濾處理,菌體和蛋白質的去除率分別為 100%和 92.1%。我們應用截留分子量為5 000 Da的陶瓷膜對實際發酵液進行了超濾處理,蛋白質的去除率大于95%,滲透液平均通量大于30 L/(m2·h),有工業應用的價值。
因此相比較而言,超濾法是目前較經濟可行的去除生物高分子的方法,具有操作時間短、膜通量高、高分子雜質去除效果好等優點,如果能進一步減少操作過程中膜的污染,提高膜的耐溶劑能力和使用壽命,該方法有望大規模應用于 1,3-丙二醇發酵液中高分子雜質的去除。
2 鹽的去除
微生物發酵時鹽的來源有兩種,一種是為中和發酵過程產生的副產物如乙酸、乳酸、丁二酸等產生的有機鹽,一種是在發酵過程添加的培養基中所包含的無機鹽。這些鹽分在后續的濃縮和精餾操作過程中含量會不斷增加,使發酵液呈漿糊狀,阻止蒸餾操作的進行,并且還會使有機物的沸點增加,增加精餾過程的能耗和降低產物的最終收率。通常采用的除鹽方法有溶析結晶法、離子交換法和電滲析法。
2.1 溶析結晶
溶析結晶是利用被分離物質與溶劑分子間相互作用力的差異,通過改變溶劑的性質來選擇性地溶解其中一種組分,從而使另一組分最大限度地從溶劑中結晶析出的過程。如加入甲醇或乙醇能顯著降低鉻酸鉀在水中的溶解度[18]。應用溶析結晶法可以有效地分離出生物大分子,其典型的工業應用是蛋白質及多糖的分離提取。我們用溶析結晶法對 1,3-丙二醇發酵液進行了脫鹽實驗,實驗結果表明分離效果不理想,需要加入大量的溶劑但鹽析出不完全,且有部分1,3-丙二醇、2,3-丁二醇和甘油一并析出。該方法存在的主要問題是溶劑加入量大,回收困難且分離效率低。
2.2 離子交換法
據我們實驗結果可知,采用離子交換法處理1,3-丙二醇發酵液也可以取得較好的效果,同時還可以去除部分色素,改善最終產品的色度。該方法工業化應用存在的問題是由于發酵液中鹽含量高使得樹脂容易達到飽和,需要頻繁再生,而樹脂的再生需消耗3~5倍的酸、堿和大量的水,這不僅增加了過程能耗,還產生大量的酸、堿廢液導致環境污染問題。
2.3 電滲析
電滲析是利用離子交換膜和直流電場的作用,從水溶液和其他不帶電組分中分離帶電組分的一種電化學分離過程,已廣泛應用于各種天然水淡化,海水濃縮制鹽,有機溶液中電解質離子的去除等領域。實驗證明[19-20],用電滲析法可以有效脫除 1,3-丙二醇發酵液中90%以上的有機酸鹽和無機鹽,具有能耗低、操作簡便、環境污染小等優點,同時采用結晶的方法可以部分回收高附加值的鹽類[21],是去除1,3-丙二醇發酵液中鹽分的有效方法。
目前,電滲析法除鹽存在的最大問題是過程能耗相對較高,膜的價格較貴,但隨著膜技術的不斷發展,膜的性能不斷地提高而價格在不斷地下降,目前國產異相離子交換膜的價格就有一定的吸引力(如上海產異相離子交換膜yk04價格為187元/m2,使用壽命2~4年)。另一方面,隨著國家對生產過程環保要求的提高,該方法由于不形成二次污染,不需要添加化學品,能部分回收發酵液中的鹽,具有較高的生態和環境效益,因此是目前較可能大規模應用于1,3-丙二醇發酵液脫鹽的方法。
3 醇的分離
去除了菌體、蛋白質等高分子物質和鹽分后,1,3-丙二醇發酵液中目標產物 1,3-丙二醇、甘油和2,3-丁二醇的含量分別為10%、2%和2% (質量) 左右。這時需要將大量的水去除,回收 2,3-丁二醇和甘油,但由于這三種醇極性較強,彼此的物化性質比較接近,在發酵液中的濃度都比較低,這給分離提純帶來了很大的困難。傳統的精餾技術與反應萃取等新技術相比各有優缺點。
3.1 多效蒸發+精餾
精餾是最傳統的分離醇、水混合物的方法。發酵液中1,3-丙二醇、2,3-丁二醇和甘油在常壓下沸點分別為214 ℃、184 ℃和290 ℃,所以傳統的精餾法可以實現三者的分離,但傳統的蒸發和精餾存在著能耗高、產物收率低等問題。因此許多研究者對蒸餾技術進行改進以降低能耗[22-23],如采用四效蒸發將質量分數為5%~15%的1,3-丙二醇水溶液濃縮到80%以上,甚至達到90%后再通過精餾獲得合格的1,3-丙二醇產品[24]。總的來說,由于發酵液中1,3-丙二醇的濃度較低,需處理的發酵液量比較大,因此該方法存在的問題是過程能耗比較高,并且需要脫鹽、脫蛋白質等預處理過程。
3.2 萃取
3.2.1 有機溶劑萃取
溶劑萃取法具有效率高、生產能力大、能耗低等優點,是 1,3-丙二醇提純技術研究的一個熱點,許多研究者都試圖找到一種適合工業化需要的萃取劑。但由于 1,3-丙二醇的極性較強,使其在普通疏水溶劑中的溶解度較小,用物理萃取法難以達到滿意的結果[25]。如 Janusz等[26]采用 ESP(Extractant screening program) 程序選擇萃取劑,該程序利用UNIQUAC基團分配法來計算多組分液液平衡,主要考察醇的同分異構體和含有功能基團的醇類的萃取能力,實驗結果表明對于直鏈醇分配系數隨著碳個數增加減小,同碳的異構物分配系數較大,但與少一個碳的直鏈醇差不多,二元醇的分配系數比一元醇的高。但體系中存在的 2,3-丁二醇、甘油與溶劑的親和力較大而使得 1,3-丙二醇的選擇性降低。Baniel等[27]研究使用戊醇、丙醇、己醇、蓖麻油等萃取分離1,3-丙二醇,該方法很難大規模應用,其原因在于該過程需加入大量的溶劑且分配系數很低。
3.2.2 絡合萃取
具有Lewis酸性或Lewis堿性的物質可以與醇發生絡合作用實現醇溶液的分離。向波濤等[28]選取磷酸三丁酯、己酸、辛酸為絡合劑,對 1,3-丙二醇的稀溶液進行絡合萃取。實驗結果表明隨著磷酸三丁酯體積分數的增加,分配系數增大,但最大也僅僅為 0.07;使用純的己酸和辛酸進行萃取時,分配系數也僅為0.07和0.03,遠遠小于這三種萃取劑對乙醇稀溶液進行萃取時的分配系數,可見由于 1,3-丙二醇的強親水性,絡合萃取的方法對該體系不適用。
3.2.3 反應萃取
由上可知,只有降低 1,3-丙二醇的強極性和強親水性后萃取法才可能應用于 1,3-丙二醇體系,其中一種降低 1,3-丙二醇親水性的方法是將其羥基屏蔽,如用醛類物質與 1,3-丙二醇的伯羥基進行可逆縮醛反應以屏蔽羥基,得到親水性大大降低的化合物后再采用萃取法將其分離,再生后可得到純的1,3-丙二醇。這就是目前的另一個研究熱點—反應萃取分離法[29-30]。Janusz等[31]以強酸性樹脂為催化劑,加入乙醛與 1,3-丙二醇發生可逆縮醛反應,生成 2-甲基-1,3-二 烷 (2MD),脫去有機相中水后,用鄰二甲苯、甲苯或乙苯萃取2MD,最后2MD水解得到 1,3-丙二醇。實驗結果表明使用甲苯進行同步萃取可以改變反應的平衡位置,促使平衡向生成2MD的方向移動,使得最終的1,3-丙二醇轉化率和2MD收率 (分別為98%和91%) 都高于不加萃取劑時。反應萃取工藝較為經濟合理,但其所得到的 1,3-丙二醇產品中會殘留一定濃度的乙醛,該產品用來生產 PTT時會對其纖維產品的多項質量指標產生影響,其中對纖維染色的上染效果以及染色穩定性的影響尤為顯著,因此該方法得到的 1,3-丙二醇需要采用其他方法處理后才可用于PTT的聚合過程。如徐澤輝等[32]使用顆粒白土來處理含有殘余醛基物質的 1,3-丙二醇。該方法除了乙醛殘留問題以外,還存在2MD水解較為困難,1,3-丙二醇收率低和強酸性樹脂催化效果受鹽影響較大等問題,也難以應用于工業實際。
3.2.4 雙水相萃取
雙水相萃取具有萃取條件溫和、容量高等優點,常用于高附加值產品的小規模生產。已經有研究者開發出新的雙水相體系如使用短鏈醇等來降低萃取劑的價格和避開反萃取操作[33],實驗結果表明由強極性溶劑和含高價態陰離子的鹽組成的雙水相體系能有效地從1,3-丙二醇發酵液中萃取1,3-丙二醇,如在乙醇/硫酸銨組成的雙水相體系中,1,3-丙二醇的分配系數可達到 4.08,回收率為 93.7%,并且可直接應用于未去除高分子物質的發酵液。該方法可以實現微生物菌體與 1,3-丙二醇的同時分離,簡化分離過程,具有一定的經濟價值,有工業放大的可能性,但其存在的問題是萃取后目標產物 1,3-丙二醇的回收研究尚未進行,分離所得鹽的回收也未考慮,這些鹽直接排放將造成經濟損失和環境污染,因此需進一步研究得到較完整的工藝后再重新評估該方法大規模應用的可行性。
3.3 分子篩分離
原位分離是目前分離研究的另一個熱點,在1,3-丙二醇生產期間如能將 1,3-丙二醇及時分離出來可以避免產物對細胞生長的抑制和促進 1,3-丙二醇總產量的增加。Gunzel 等[34]用脫鋁 NaY和硅沸石處理1,3-丙二醇水溶液,可以實現每克沸石負荷0.112 g 1,3-丙二醇,但該實驗沒有研究甘油的選擇性。Schlieker 等[35]使用活性炭分離1,3-丙二醇,發現由于甘油顯著的非特異性吸附使得活性炭在吸附 1,3-丙二醇的同時也部分吸附甘油,導致最終甘油發酵產率大大降低。Schoellner等[36]檢驗了幾種沸石的吸附性能,沸石吸附存在的問題是鹽也可能會被瀝濾到沸石中,此外還需考慮如何將 1,3-丙二醇從沸石中回收。Li等[37-38]使用ZSM-5型沸石膜分離1,3-丙二醇,根據動力學半徑與擴散速率的不同,可以實現絕大部分 1,3-丙二醇 (0.61 nm) 分子被吸收到ZSM-5通道中 (0.62 nm),而甘油、水和葡萄糖大部分不經過沸石通道而達到分離 1,3-丙二醇的目的,但該實驗只考察了模擬液,沒有對實際發酵液進行研究。總的來說,分子篩法存在單程產率低,沸石的機械強度和熱穩定性較差,耗時較長等問題。
3.4 陽離子交換樹脂吸附
利用磺化聚苯乙烯陽離子樹脂中磺酸基(SO3H)的離子交換功能,可以吸附醇類。Ahmad等[39]采用模擬移動床使發酵液與磺化聚苯乙烯陽離子樹脂接觸,進行吸附后加入溶劑洗脫被樹脂吸收的組分,最后在洗脫液中回收 1,3-丙二醇。實驗結果表明使用三種不同類型的樹脂 (Na型UB K555 型,Ca型UB K555 型和Ca 型CS11GC350 型) 1,3-丙二醇的回收率都達到95%以上。但磺酸基對極性水分子的吸附作用也很強,這使得該方法的單程轉化率較低,為得到高收率的產品,必須循環操作,循環操作不僅增加動力消耗,也增加樹脂損失,使得整個過程的經濟性下降。因此,只有在獲得對 1,3-丙二醇具有高選擇性的樹脂并且提高其抗磨損性能后該方法才有望實現工業化。
由上可知,許多新技術被應用于 1,3-丙二醇的提純研究中,但許多技術僅僅在小規模操作時有效,涉及大規模生產時存在各種問題,比較而言傳統的蒸發+精餾法具有工藝成熟、產品回收率高等優點而備受矚目,特別是通過采用多效蒸發和真空精餾技術后該方法的能耗大大降低,經濟可行性大大提高。
綜上所述,鑒于實際發酵液成分的復雜性和工業化生產所需要的經濟性,使得經濟、高效地實現1,3?丙二醇的分離提純難度很大,迄今為止,還沒有一條經濟可行的提取工藝路線被報道,結合我們的研究工作和上述分析,提出圖 2所示的后提取工藝路線,該工藝過程中無化學品加入,實現了發酵液中1,3-丙二醇、2,3-丁二醇、甘油和副產物丁二酸鈉的分離和回收。相對于其他工藝路線,該路線考慮了副產物鹽的回收,目前報道的鹽去除方法大部分只考慮到將鹽從發酵液中分離出來,沒有考慮鹽的回用,這部分分離出來的鹽如果直接排放會造成環境污染,因此在 1,3-丙二醇真正工業化生產的時候必須考慮這部分鹽的處理,所以從盡可能的實現零排放,更好的實現生產過程的綠色化角度來說,研究該部分鹽的回收勢在必行。這些鹽中丁二酸鈉是含量較高,價格也較高的一種 (每生產1 t 1,3-丙二醇會產生大約 0.1 t丁二酸鈉,其市場價格為1.1萬元/t左右),回收其有較大的經濟和環境利益。在圖 2所示的后提取工藝路線中丁二酸鈉的回收采用濃縮結晶法,可以得到工業級丁二酸鈉晶體,有一定經濟價值,而且減少了鹽污染[21]。但還存在回收過程能耗較高,經濟性不明顯的問題,需要嘗試更佳的回收方法。綜合考慮到經濟和生態效益,圖2所示的 1,3-丙二醇后提取工藝路線具有一定的可行性,但其在能耗和 1,3-丙二醇收率上還存在著局限性,需要進一步研究改進。

圖2 具有工業應用前景的1,3-丙二醇后提取工藝路線圖Fig. 2 Flow scheme of downstream processing of 1,3-propanediol with potential industrial application prospect.
4 展望
1,3-丙二醇作為一種重要的化學品和生物柴油副產物甘油的關聯產物,其生物發酵法制備已成為國內外的研究熱點。當前該方法迫切需要解決的問題是如何獲得一條經濟、高效的后提取工藝路線,以提高其對石化合成路線的競爭力。
根據目前有關 1,3-丙二醇后提取的研究現狀來看,許多研究工作是對模擬發酵液進行的,而實際發酵液的成分更為復雜,這就使得工業化規模提取分離 1,3-丙二醇的難度很大。綜合而言,采用超濾法去除生物高分子物質,電滲析法除鹽和多效蒸發加精餾的工藝路線在經濟性和環保性上都具有一定優勢 (圖2)。考慮到環境污染和增加產品的經濟性,回收 1,3-丙二醇發酵液中高附加值的副產物如丁二酸鈉等及減少目標產物 1,3-丙二醇在后提取過程中的損失已成為今后研究的方向。
為增加甘油發酵生產1,3-丙二醇的經濟競爭力,除了采用更高效的純化工藝外,通過基因工程和代謝工程等近代分子生物學技術來培育和構建新的生產菌株也至關重要,新菌株的構建不僅應考慮提高發酵時 1,3-丙二醇的濃度,增加底物的轉化效率和生產強度,還應該考慮到后續提純工藝的簡化。
REFERENCES
[1] Witt U, Müller RJ, Widdecke H, et al. Synthesis, properties and biodegradability of polyesters based on 1,3-propanediol.Macromol Chem Phy, 1994, 195(2): 793?802.
[2] Smith JG, Kibler CJ, Sublett BJ. Preparation and properties of poly (methylene terephthalates). J Polym Sci,Part A, 1966, 14(7): 1851?1859.
[3] Feng JW, Zhang HL, Jiang LS, et al. The study on the synthesis of 1,3-propanediol. Sci Technol Chem, 2002,10(6): 43?47.
馮婧微, 張洪林, 蔣林時, 等. 1,3-丙二醇合成方法研究.化工科技, 2002, 10(6): 43?47.
[4] Liu YJ, Zhao QG, Jiang W, et al. The productive and technical analysis of 1,3-Propandiol. Chem Eng, 2002,88(1): 45?52.
劉艷杰, 趙慶國, 蔣巍, 等. 1,3-丙二醇的生產技術分析.化學工程師, 2002, 88(1): 45?52.
[5] Xu YZ, Ou XJ, Guo NN, et al. Utilization of high value-added products based on crude glycerol from biodiesel process. Process Eng, 2008, 8(4): 695?702.
許赟珍, 歐先金, 郭妮妮, 等. 生物柴油副產物甘油的高附加值利用. 過程工程學報, 2008, 8(4): 695?702.
[6] Summerfield FW, Tappel AL. Cross-linking of DNA in liver and testes of rats fed 1,3-propanediol. Chem Biol Inter, 1984, 50(1): 87?96.
[7] Kurian JV. A new polymer platform for the future-sorona?from corn derived 1,3-propanediol. J Polym Environ,2005, 13(2): 159?167.
[8] Huang H, Gong CS, Tsao GT. Production of 1,3-propanediol by Klebsiella pneumoniae. Appl Biochem Biotech, 2002, 98: 687?698.
[9] Hari Babu S, Robert John U, John RB. Proeess for the purification of l,3-propanediol: US, 6235948. 2001-05-22.
[10] Malinowski JJ. Reactive extraction for downstream separation of 1,3-propanediol. Biotechnol Progr, 2000,16(1): 76?79.
[11] Homann T, Tag C, Biebl H, et al. Fermentation of glycerol to 1,3-propanediol by Klebsiella and Citrobacter strains.Appl Microbiol Biotechnol, 1990, 33(2): 121?126.
[12] Li SG, Tuan VA, Falconer JL, et al. Separation of 1,3-propanediol from aqueous solutions using pervaporation through an X-type zeolite membrane. Ind Eng Chem Res, 2001, 40(8): 1952?1959.
[13] Hao J, Xu F, Liu DH, et al. Downstream processing of 1,3-propanediol fermentation broth. Chem Technol Biotechnol, 2006, 81(1): 102?108.http://dx.doi.org/10.10 02/jctb.1369.
[14] Li FF, Zhou YJ, Liu DH. Flocculation of fermented broth with 1,3?propanediol. Microbiol China, 2004, 31(3): 30?35.
李凡鋒, 周玉杰, 劉德華. 1,3-丙二醇發酵液的絮凝預處理研究. 微生物學通報, 2004, 31(3): 30?35.
[15] Lu SF, Zhang DJ, Xiu ZL. Flocculation of 1,3-PD fermentation broth and reuse of cell in flocs. Food Fermentation Industries, 2006, 32(9): 10?13.
魯詩鋒, 張代佳, 修志龍. 1,3-丙二醇發酵液的絮凝處理及絮凝細胞的再利用. 食品與發酵工業, 2006, 32(9):10?13.
[16] Xiu ZL, Zhang DJ, Gao SJ, et al. Extraction and separation of downstream of 1,3-propanedid from fermentation broths: CN, 3133584. 2003-12-10.
修志龍, 張代佳, 高素軍, 等. 微生物發酵液中提取分離1,3-丙二醇的方法: 中國專利, 03133584. 2003-12-10.
[17] Lu SF. Downstream processing of 1,3-propanediol from fermentation broths[D]. Dalian: Dalian University of Technology, 2006.
魯詩鋒. 發酵液中 1,3-丙二醇的分離提取工藝的研究[D]. 大連: 大連理工大學, 2006.
[18] Wang J, Xu HB, Zhang SP, et al. Experimental investigation on separation of potassium chromate from its aqueous solution by solventing-out crystallization. Process Eng, 2007, 7(2): 246?251.王烔, 徐紅彬, 張頌培, 等. 溶析結晶法分離鉻酸鉀.過程工程學報, 2007, 7(2): 246?251.
[19] Gong Y, Tong Y, Wang XL, et al. The possibility of the desalination of actual 1,3-propanediol fermentation broth by electrodialysis. Desalination, 2004, 161(2): 169?178.
[20] Hao J, Liu DH. Desalination of fermented broth containing 1,3-propanediol by electrodialysis. J Process Eng, 2005, 5(1): 36?39.
郝健, 劉德華. 1,3-丙二醇發酵液電滲析法脫鹽. 過程工程學報, 2005, 5(1): 36?39.
[21] Wu RC, Ren HJ, Xu YZ, et al. The final recover of salt from 1,3-propanadiol fermentation broth. Sep Purif Technol, 2010, 73(2): 122?125.
[22] Hermann BG, Patel M. Today’s and tomorrow’s bio-based bulk chemicals from white biotechnology: a techno-econ omic analysis. Appl Biochem Biotechnol, 2007, 136(3):361?388.http://dx.doi.org/10.1007/s120 10-007-9031-9.
[23] Zhou P, Fang YJ. Progress of purifying 1,3-propanediol from dilute fermentation broth. J Chem Bioeng, 2005, 22(2): 4?6.
周鵬, 方云進. 發酵液中低濃度 1,3-丙二醇濃縮提純工藝研究進展. 化學與生物工程, 2005, 22(2): 4?6.
[24] Norbert B, Georg D, Hanswilhelm B. Process for purifying 1,3-propanediol: US, 5008473. 1991-04-16.
[25] Cho MH, Joen SI, Pyo SH, et al. A novel separation and purification process for 1,3-propanediol. Process Biochem, 2006, 41(3): 739?744.
[26] Malinowski JJ. Evaluation of liquid extraction potentials for downstream separation of 1,3-propanediol. Biotechnol Tech, 1999, 13(2): 127?130.
[27] Baniel AM, Jansen RP, Vitner A, et al. Process for producing 1, 3-propanediol: US, 0222153. 2004-11-11.
[28] Xiang BT, Chen SF, Liu DH. Extraction of 1,3-propanediol in dilute fermentation broth. J TsinghuaUniversity: Sci Technol, 2001, 41(12): 53?55.
向波濤, 陳書鋒, 劉德華. 發酵液中 1,3-丙二醇的萃取分離. 清華大學學報: 自然科學版, 2001, 41(12): 53?55.
[29] Broekhuis RR, Lynn S, King CJ. Recovery of propylene glycol from dilute aqueous solutions via reversible reaction with aldehydes. Ind Eng Chem Res, 1994, 33(12):3230?3237.
[30] Broekhuis RR, Lynn S, King CJ. Recovery of propylene glycol from dilute aqueous solutions by complexation with organoboronates in ion-pair extractants. Ind Eng Chem Res, 1996, 35(4): 1206?1214.
[31] Malinowski JJ. Reactive extraction for downstream separation of 1,3-propanediol. Biotechol Prog, 2000, 16(1):76?79.
[32] Xu ZH, Xia RH, Cao Q, et al. A new method of eliminating trace aldehyde group in 1,3-propanediol: CN,1345710. 2003-10-22.
徐澤輝, 夏蓉暉, 曹強, 等. 一種去除 1,3-丙二醇中微量殘余醛基物質的方法: 中國專利, 1345710. 2003-10-22.
[33] Li ZG, Jiang B, Zhang DJ, et al. Aqueous two-phase extraction of 1,3-propanediol from glycerol-based fermentation broths.Sep Purif Technol, 2009, 66(3): 472?478.
[34] Gunzel B, Berke CH, Ernst S. Adsorption von diolenaus fermentation smedien an hydrophobe zeolithe. Chem Ing Tech, 1990, 62(9): 748?750.
[35] Schlieker H, Gunzel B, Deckwer WD. Einsatz der adsorption zur produrt tabt rennung beider glycerinvergarung zu 1,3-propanediol. Chem Ing Tech,1992, 64(8): 727?728.
[36] Schoellner R, Elnicke WD, Unverricht S. Investigation of adsorptive separation of glycerol/1,3-propanediol in aqueous solution on zeolites by liquid phase adsorption. J Prakt Chem, 1994, 33(5): 404?407.
[37] Li SG, Tuan VA, Falconer JL, et al. Separation of 1,3-propanediol form glycerol and glucose using a ZSM-5 zeolite membrane. Membrane Sci, 2001, 191: 53?59.
[38] Li SG, Tuan VA, Falconer JL, et al. X-type zeolite membranes: preparation, characterization, pervaporation performance. Micropor Mesopor Mat, 2002, 53(1/3):59?70.
[39] Ahmad KH, Thomas PB. Method of recovering 1,3-propanediol from fermentation broth: US, 6479716.2002-11-12.
Progress in down-stream processing of biologically produced 1,3-propanediol
Ruchun Wu1,2, Yunzhen Xu1, and Dehua Liu1
1 Institute of Applied Chemistry, Department of Chemical Engineering, Tsinghua University, Beijing 100084, China
2 Key Laboratory of Chemical and Biological Transforming Process, College of Chemistry and Ecological Engineering, Guangxi University for Nationalities, Nanning 530006, China
Received: November 21, 2010; Accepted: January 12, 2011
Supported by: National High Technology Research and Development Program of China (863 Program) (No. 2006AA020103).Corresponding author: Dehua Liu. Tel: +86-10-62782654; E-mail: dhliu@tsinghua.edu.cn
國家高技術研究發展計劃 (863計劃) (No. 2008AA05Z302) 資助。

