α-淀粉酶在D201GF樹脂上的吸附性能研究
李 湘,郭海福,李 妍,陳新鵬
(肇慶學院 化學化工學院,廣東 肇慶 526061)
α-淀粉酶在D201GF樹脂上的吸附性能研究
李 湘,郭海福,李 妍,陳新鵬
(肇慶學院 化學化工學院,廣東 肇慶 526061)
應用D201GF陰離子交換樹脂吸附固載α-淀粉酶.研究了D201GF陰離子交換樹脂對水溶液中α-淀粉酶的吸附熱力學和吸附動力學特性.分析了體系溫度、pH值和離子強度對α-淀粉酶吸附的影響.熱力學研究表明,α-淀粉酶在D201GF陰離子交換樹脂上的吸附平衡數據遵循Langmuir吸附等溫方程,過程吸熱.較高的溫度、較低的pH值和離子強度均有利于α-淀粉酶的吸附.動力學研究顯示,D201GF陰離子交換樹脂對α-淀粉酶的吸附過程主要受內擴散控制.
D201GF樹脂;α-淀粉酶;吸附動力學;吸附熱力學
α-淀粉酶主要用作淀粉的液化劑,廣泛應用于葡萄糖、酒精、發酵和紡織褪漿的生產上[1-2].由于游離酶對環境十分敏感,各種物理及化學因素均有可能使酶喪失生物活力,因此較難回收,使用成本高.有研究者將酶吸附或者鍵合在高分子材料上[3-4],賦予酶以下優點:對熱及pH值等變化的穩定性提高;反應完成后經簡單的過濾就可回收,便于重復使用,大大降低了生產成本;能實現連續自動化生產;體系中較少代入甚至不帶入酶蛋白,簡化了后續分離純化工藝.目前,有關α-淀粉酶在高分子吸附材料上固化的吸附熱力學和吸附動力學研究報道還比較少見.
本文中,筆者擬用靜態吸附的方法考察α-淀粉酶在D201GF陰離子交換樹脂上的吸附熱力學性質,研究體系pH值、離子強度以及反應溫度對該相平衡的影響.同時,采用邊界模型考察α-淀粉酶在D201GF陰離子交換樹脂上的交換動力學,確定速度控制步驟.此外,擬從熱力學和動力學的角度揭示α-淀粉酶在D201GF陰離子交換樹脂上的吸附行為,為α-淀粉酶的固定化提供理論依據.
1 材料與方法
1.1 實驗材料
α-淀粉酶購自廣東環凱微生物科技有限公司.D201GF購自南開大學化工廠,為強堿性苯乙烯系陰離子交換樹脂,功能基團為-N+(CH3)3,篩取平均粒徑為1.1 mm的樹脂,依次用體積分數為95%的乙醇、1 mol/L NaOH和1 mol/L HCl處理后,洗滌至中性,烘干備用.其他無機鹽試劑均為國產分析純產品.
實驗所用儀器如下:UV/VIS916紫外-可見分光光度計(澳大利亞GBC公司);PHS-25酸度計(上海雷磁儀器廠);恒溫震蕩器(億通SHA-B型)等.
1.2 平衡吸附和動力學實驗
準確稱取適量經過預處理的D201GF陰離子交換樹脂,置于250 mL的錐形瓶中,分別加入適量體積的系列濃度α-淀粉酶水溶液.在恒溫震蕩器中恒速振動超過24 h,確保達到吸附平衡.采用紫外分光光度法測定溶液中α-淀粉酶的初始濃度和平衡濃度,根據式(1)計算平衡吸附量q(mmol/g).分別變化溫度、pH值和離子強度重復上述實驗.

式中:Qe為樹脂的平衡交換容量,mg/g;C0為α-淀粉酶溶液的初始濃度,mg/L;C為平衡時α-淀粉酶的濃度,mg/L;V為溶液的體積,L;ms為樹脂質量,g.
動力學實驗采用有限浴法,將一定量的D201GF陰離子交換樹脂和α-淀粉酶溶液同時放入錐形瓶中,置于恒溫震蕩器上振蕩,使吸附質與吸附劑之間充分接觸并定時取樣,測定溶液中的α-淀粉酶濃度,可計算得出各時刻的吸附量.某一時刻的吸附分數可由式(2)計算得到.

式中:Ci為第i次取樣測得的α-淀粉酶的濃度,mg/L;V0為α-淀粉酶溶液的初始體積,L;Vi為第i次取樣時α-淀粉酶溶液的體積,L;vj為第j次取樣的溶液體積,L;Q為樹脂的交換容量,mg/g.
2 結果與討論
2.1 靜態吸附熱力學研究
2.1.1 溫度對吸附相平衡的影響
圖1是D201GF樹脂對α-淀粉酶在溫度為293.0 K、303.5 K和313.2 K下的吸附等溫線.從圖1可以看出,在本文考察濃度范圍內,D201GF樹脂對α-淀粉酶的吸附等溫線屬于優惠型的I類等溫線.溫度越高,α-淀粉酶在D201GF樹脂上的吸附量就越大.這表明α-淀粉酶在D201GF樹脂上的吸附過程為吸熱反應.
2.1.2 溶液pH值對吸附相平衡的影響
D201GF陰離子交換樹脂是強堿性樹脂,溶液pH值是影響樹脂交換容量的一個重要因素.pH值對吸附劑吸附性能的影響見圖2.由圖2可見,在本研究的pH值范圍內,隨著pH值增大,D201GF陰離子交換樹脂對α-淀粉酶的吸附能力由大變小,總體上變化不超過7%.溶液pH值對離子交換樹脂α-淀粉酶的吸附能力的影響是多方面的[6].首先,溶液pH值增大,α-淀粉酶作為一種兩性蛋白質分子,堿性增強有利于α-淀粉酶陰離子化,帶負電荷陰離子化的α-淀粉酶濃度增大,使得其在D201GF陰離子交換樹脂上的吸附容量上升.這一點對α-淀粉酶在D201GF陰離子交換樹脂上吸附的影響占主導地位.其次,溶液pH值對蛋白質分子的立體結構有較大影響,隨著溶液pH值增大,會使得蛋白質分子呈現膨脹擴展的趨勢,導致蛋白質分子的幾何尺寸變大[7],從而使得吸附容量下降.另外,隨著溶液pH值的增加,陰離子交換劑中配基的離子化程度減弱,這也會導致吸附容量降低[8],但對于強堿性樹脂D201GF,pH值對配基離子化程度的影響可以忽略.正是這3方面的協同作用,決定了α-淀粉酶在D201GF陰離子交換樹脂上吸附容量的變化.最后還必須考慮的是,對于生物活性分子而言,過強的吸附作用力以及劇烈的負載條件都會增加蛋白變性失活的機會,所以吸附時α-淀粉酶溶液的pH值不宜過低或過高.為此,在考察pH值對樹脂吸附α-淀粉酶的影響時,選擇pH值在5.0~7.0之間為宜,在此pH值范圍內α-淀粉酶主要顯現負離子特性.
2.1.3 離子強度對吸附相平衡的影響
離子強度對吸附劑吸附性能的影響見圖3.由圖3可見,在本研究的離子強度值范圍內,隨著離子強度的增高,α-淀粉酶在D201GF陰離子交換樹脂上的吸附容量有較大幅度的降低.這主要有2方面原因:一是溶液離子強度的提高掩蔽蛋白質自身所帶的電荷,使之與陰離子吸附劑中配基的相互作用力減弱,導致吸附容量下降;二是溶液離子可能與α-淀粉酶的吸附點位競爭性結合,從而吸附容量下降.該實驗結果也表明,采用離子濃度梯度洗脫的方法,可以將α-淀粉酶從D201GF陰離子交換樹脂上解吸.
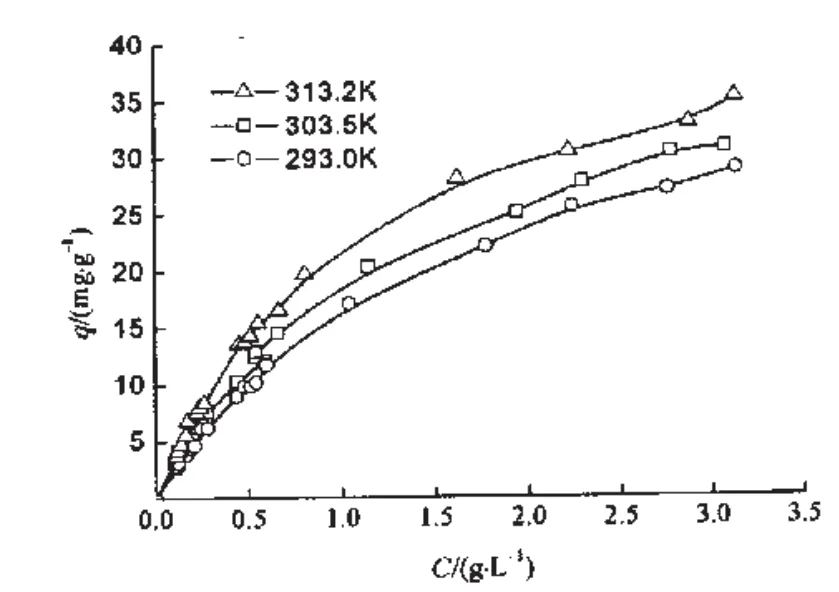
圖1 溫度對α-淀粉酶在D201GF樹脂上的吸附等溫線的影響(pH值為6.8,離子強度為0.6)
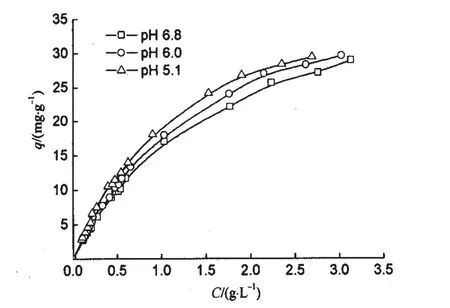
圖2 pH值對α-淀粉酶在D201GF樹脂上吸附等溫線的影響 (體系溫度為293.0 K,離子強度為0.6)
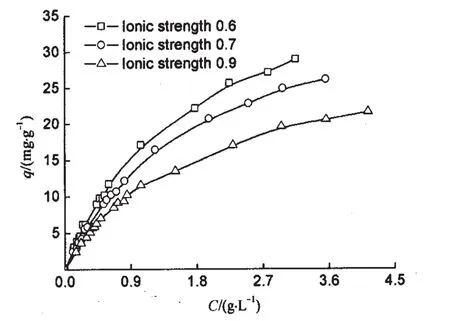
圖3 離子強度對α-淀粉酶在D201GF樹脂上吸附等溫線的影響(體系溫度為293.0 K,pH值為6.8)
2.1.4 吸附等溫線模型
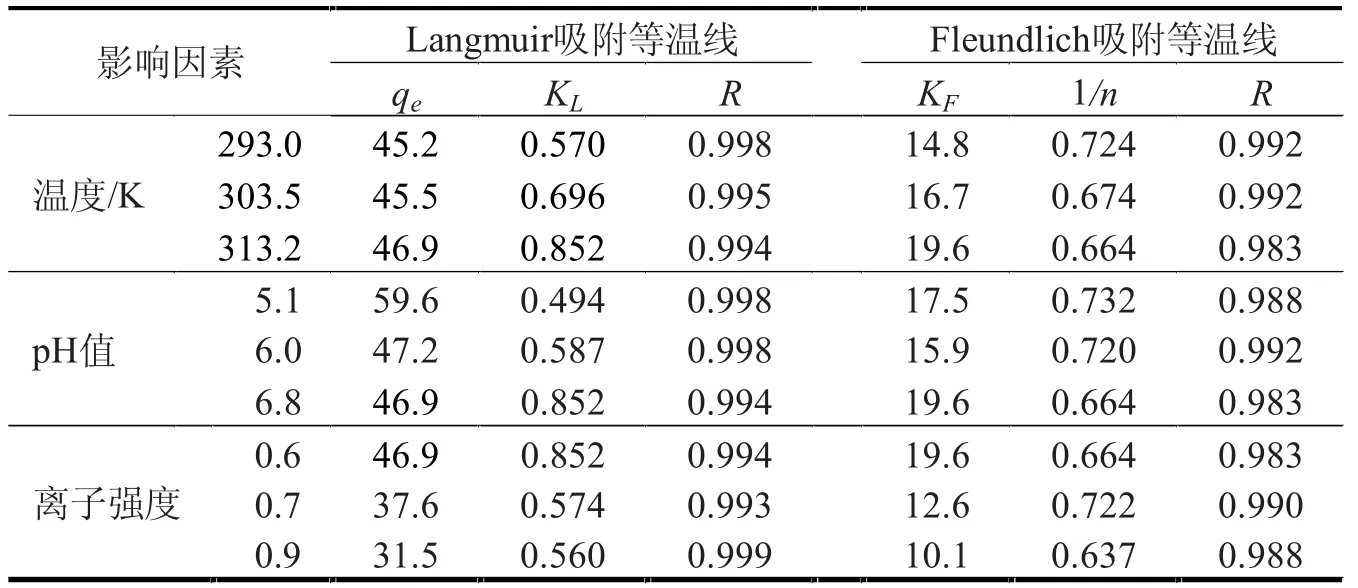
表1 α-淀粉酶在D201GF樹脂上吸附的相平衡常數
2.1.5 α-淀粉酶在D201GF樹脂上吸附的熱力學性質
α-淀粉酶在D201GF樹脂上吸附的焓變ΔH可采用Van’t Hoff方程進行計算,如式(3)所示:

吸附熵變ΔS按式(4)的方程計算:

吸附自由能變ΔG按式(5)計算:

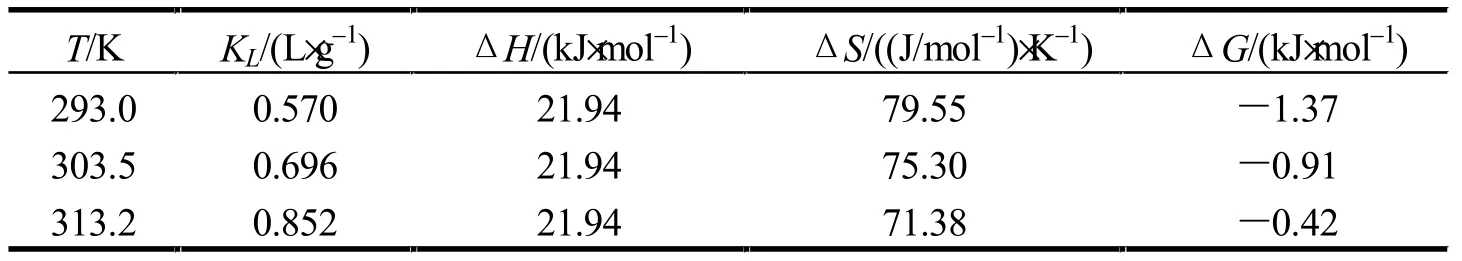
表2 α-淀粉酶在D201GF樹脂上吸附的熱力學參數
吸附過程的焓變ΔH、熵變ΔS及自由能變ΔG結果如表2所示.由表2可見,吸附過程的焓變ΔH為正值,說明α-淀粉酶在D201GF樹脂上的吸附過程為吸熱反應.ΔS為正,說明α-淀粉酶在D201GF樹脂上的吸附是熵推動過程.根據吸附交換理論,對于固-液吸附,溶質分子由液相吸附交換到固體表面時,其自由度降低,該過程屬于熵減少過程;但在液相中,溶質的交換吸附往往使樹脂發生收縮,樹脂相中的交換基團和反離子的部分水化水釋放到溶液相中,而水分子的脫附進入液相是熵增大的過程,交換吸附過程的熵變是兩者的總和[5].對于以水為溶劑的體系,由于大多數有機物的分子體積遠大于水,故而它們的吸附過程ΔS常常大于零;因此,盡管吸附使α-淀粉酶分子的自由度減少,但由于存在表面的化學吸附,吸附質在D201GF樹脂表面以化學鍵結合,最終導致ΔS>0.自由能變 ΔG<0,說明α-淀粉酶在D201GF樹脂上的吸附過程能夠自發進行.
2.2 靜態吸附動力學研究
2.2.1 吸附動力學模型
采用Hellfrich的理論分析方法,運用邊界模型研究α-淀粉酶在D201GF樹脂上吸附的傳質控速步驟,以此為基礎計算相應的擴散系數.根據該動邊界模型理論,離子交換反應控速步驟有3種可能性,即液膜擴散控制、顆粒擴散控制和化學反應控制.
當離子交換過程為液膜擴散控制時,

當離子交換過程為顆粒擴散控制時,

當離子交換過程為化學反應控制時,

在式(3)~(5)中:r0為樹脂粒徑,m;a 是化學計量常數 8.315,kc是化學反應速率常數,m4/(mo1·s-1);D 為顆粒擴散系數,m2/s;kf為液膜傳質系數,m/s.
根據動力學實驗結果,以 t為橫軸,分別對函數 F、[1-3(1-F)2/3+2(1-F)]和[1-(1-F)2/3]作圖并進行線性回歸,結果如圖 4 所示.圖 4 回歸結果顯示,t與[1-3(1-F)2/3+2(1-F)]線性相關性最佳(R2=0.992),可初步認定α-淀粉酶在D201GF樹脂上的吸附過程主要受顆粒擴散控制[5,9].
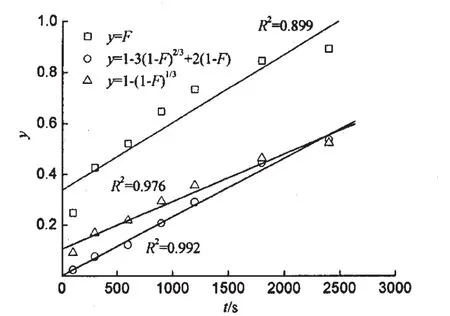
圖4 α-淀粉酶在D201GF樹脂上吸附動力學模型線性擬合結果(pH值為 6.8,離子強度為0.59)

圖5 不同溫度下α-淀粉酶在D201GF樹脂上吸附動力學模型擬合結果(pH 值為6.8,離子強度為0.59)
2.2.2 溫度對擴散系數的影響
維持其他條件不變,分別測定了D201GF樹脂在不同溫度下吸附α-淀粉酶的吸附動力學曲線,實驗結果如圖 5所示.在不同溫度下,t均與[1-3(1-F)2/3+2(1-F)]呈良好的線性關系,這進一步表明顆粒擴散控制是該反應過程的控速步驟.由圖5各直線斜率計算可知,隨著體系溫度升高,內擴散系數也增大,分別為 5.82×10-12m2/s,7.63×10-12m2/s和 8.52×10-12m2/s.
3 結論
本文應用D201GF陰離子交換樹脂吸附固載α-淀粉酶,研究了α-淀粉酶在D201GF陰離子交換樹脂上的吸附熱力學和吸附動力學特性.分析了體系溫度、pH值和離子強度對α-淀粉酶吸附的影響.研究表明,α-淀粉酶在D201GF陰離子交換樹脂上的吸附平衡數據遵循Langmuir吸附等溫方程.吸附過程ΔH>0,ΔS>0,表明此吸附過程吸熱,升高溫度有利于吸附反應的發生;較低的溶液pH值及較低的離子強度都有利于α-淀粉酶的吸附.采用動邊界模型理論研究結果顯示,D201GF陰離子交換樹脂對α-淀粉酶的吸附過程主要受內擴散控制,擴散系數數量級為10-12.
[1] SWETHA S,DHANYA G,KESAVAN M,et al.α-amylases from microbial sources[J].Food Technol Biotechnol,2006,44(2):173-184.
[2]SCHALLMEY M,SINGH A,WARD O P.Developments in the use of Bacillus species for industrial production[J].Can J Microbiol,2004,50(1):1-17.
[3] 玄光善,聶紅艷,吳效楠.α-淀粉酶的固定化及其在鄰硝基對甲基苯酚還原反應中的應用[J].化學與生物工程,2008,25(10):31-34.
[4] SZCZESNA-ANTEZAK M,ANTCZAK T,RZYSKA M,et a1.Catalytic properties Of membrane-bound Mucor lipase immobilized in a hydrophilic carrier[J].J Mol Catalysis B:Enzymatic,2002,19/20:261-268.
[5] WENMING W,VASILIS F.Kinetics study on separation of cadmium from tellurium in acidic solution media using ion-exchange resins[J].Journal of Hazardous Materials,2005,125(1/3):80-88.
[6] 陳衛東,董曉燕,孫彥.陰離子交換劑DEAE-Spherodex M的蛋白質吸附性能[J].化學工程,2004,32(6):57-61.
[7] TANFORD C,BUZZELL J G,RANDS D G,et a1.The reversible expansion of bovine serum albumin in acid solutions[J].J Am Chem Soc,1955,77:6 421-6 428.
[8] BAUTLSTA L F,MARTINEZ M,ARACIL J.Adsorption equilibrium of a-amylase in aqueous solutions[J].AIChE Journal,1999,45:761-768.
[9] 陶大峻,張磊,吳偉杰,等.陰離子樹脂D02吸附2-酮基-L-古龍酸的熱力學和動力學研究[J].離子交換與吸附,2007,23(6):498-505.
Study on Adsorption Thermodynamics and Kinetics of α-Amylase on D201GF Resin
LI Xiang,GUO Haifu,LI Yan,CHEN Xinpeng
(College of Chemistry and Chemical Engineering,Zhaoqing University,Zhaoqing,Guangdong 526061,China)
The aqueous adsorption thermodynamics and kinetics ofα-amylase on D201GF resin have been investigated by batch experiments.The influence of pH,ionic strength and temperature on the equilibrium of a-amylase adsorption was studied.The adsorption isotherms were fit well by the Langmuir equation within the concentration range studied.The results showed that the process of adsorption of α-amylase on D201GF resin was endothermic.A moderate higher temperature,lower pH or lower ionic strength is in favor of the adsorption of a-amylase on D201GF resin.The kinetics experiments showed that the particle diffusion was the rate-controlling step.
D201GF resin;a-amylase;adsorption thermodynamics;adsorption kinetics
O647.3
A
1009-8445(2011)02-0037-05
(責任編輯:陳 靜)
2010-11-22
廣東省科學技術攻關項目(2006B20330006)
梁廣堅(1949-),男,廣東郁南人,肇慶學院生命科學學院教授,碩士.

