吉西他濱治療RRM1陰性晚期難治非小細胞肺癌患者1例
趙美玲 楊海虹 何建行
目前吉西他濱/鉑類方案是晚期非小細胞肺癌(nonsmall cell lung cancer, NSCLC)的標準治療方法之一。Anderson等[1]報告吉西他濱單藥治療NSCLC客觀緩解率(objective response rate, ORR)為20%;國內(nèi)管忠震等[2]報道吉西他濱聯(lián)合順鉑方案的疾病控制率為56.1%,部分緩解率為43.9 %,中位緩解時間(174 ±18.5)天。核糖核苷酸還原酶1(ribonucleotide reductase M1, RRM1)是腫瘤抑制基因,也是吉西他濱的分子靶點。RRM1 mRNA高表達導致腫瘤細胞DNA損傷修復能力增強,從而對吉西他濱/鉑類方案產(chǎn)生耐藥,RRM1 mRNA低表達提示對吉西他濱敏感[3]。基因mRNA表達和蛋白表達有一定的相關(guān)性,因此我們采用半定量免疫組化技術(shù)檢測腫瘤組織RRM1的蛋白表達,現(xiàn)將1例吉西他濱(健擇)反復治療的難治性晚期NSCLC患者的治療情況及對初診獲得的腫瘤組織進行RRM1等蛋白的免疫組化檢測報告如下。
1 資料與方法
1.1 病例資料 患者,女性,74歲,2006年3月因“反復咳嗽、咳痰1月”入院。胸部CT示右下肺中央型肺癌,并右上肺轉(zhuǎn)移,癌性淋巴管炎。腹部CT、頭顱MRI和骨ECT檢查無異常。纖支鏡病理活檢示低分化鱗癌。診斷:“右下肺低分化鱗癌T4N2M0(IIIb期)”。隨后進行吉西他濱、紫杉醇、長春瑞賓和培美曲塞等鉑類聯(lián)合方案化療多次(表1)。治療反應率根據(jù)RECIST標準評估,治療前后以胸片或胸部CT的影像學資料進行評價。
1.2 免疫組化檢測 對患者2006年初診時的石蠟病理活檢組織進行相關(guān)藥敏蛋白免疫組化檢測。采用SP法檢測病理切片中的ERCC1、RRM1、Beta-Tubulin、TS和BRCA1表達。ERCC1、RRM1和Beta-Tubulin一抗購自北京中杉金橋公司;TS和BRCA1一抗購自DAKO公司。免疫組化染色根據(jù)試劑說明書操作。結(jié)果評估:RRM1、ERCC1以腫瘤細胞核出現(xiàn)棕黃色顆粒著色為陽性,Beta-Tubulin、TS、BRCA1以腫瘤細胞漿出現(xiàn)棕黃色顆粒著色為陽性。免疫組化標準:每例標本在400倍視野下隨機選取500個-1,500個腫瘤細胞,觀察陽性細胞染色強度,并計數(shù)陽性細胞百分數(shù)。按細胞染色強度記為0分-3分:無著色為0分,淡黃色為1分,棕黃色為2分,深棕色或棕褐色為3分。按陽性細胞百分數(shù)的構(gòu)成比記為0分-3分:<10%為0分,10%-25%為1分,26%-50%為2分,>50%為3分。以染色強度記分和陽性細胞百分數(shù)記分相加所得總分進行判斷,總分0-1分為陰性(-),2-3分為弱陽性(+),4-5分為中陽性(++),6分為強陽性(+++)。
2 結(jié)果
2.1 化療療效及不良反應 化療療效及不良反應見表1和圖1。患者前后9次的化療中吉西他濱聯(lián)合順鉑 (gemcitabi-ne plus cisplatin, GP)方案化療4次,療效有3次為部分緩解(partial response, PR),1次為疾病穩(wěn)定(stable disease,SD)。患者GP方案化療前地塞米松做預處理,化療中常規(guī)應用5-HT3受體拮抗劑止吐,惡心、嘔吐等胃腸反應不明顯。化療后骨髓抑制多為1-2度,經(jīng)休息后2周內(nèi)能恢復正常,其它不良反應主要為輕度皮疹。
2.2 免疫組化檢測 RRM1(-)(圖2),ERCC1(+),BRCA1(-),Beta Tubulin(+++),TS(++)。
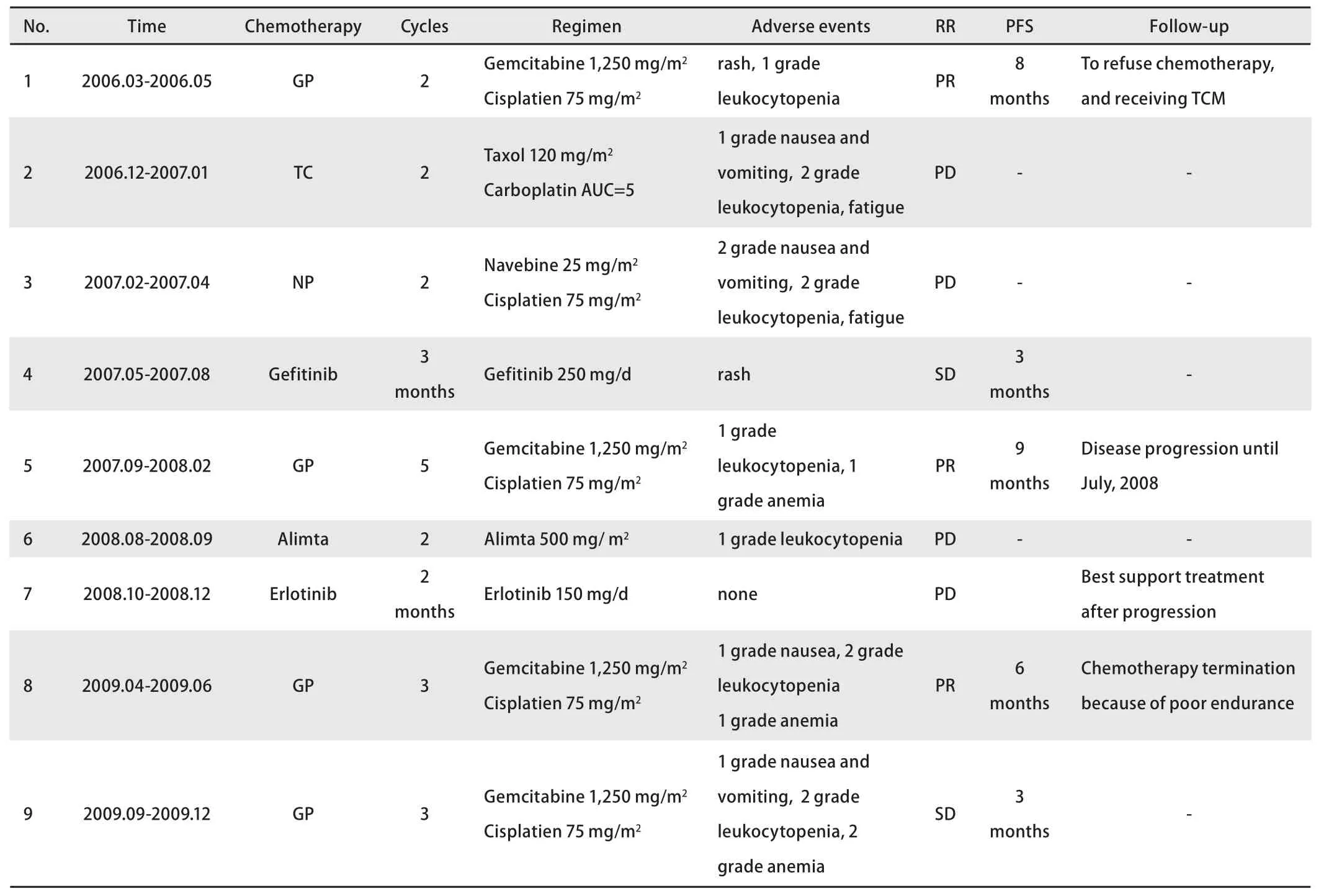
表 1 化療方案及療效總結(jié)表Tab 1 Chemotherapy and ORR
3 討論
RRM1 mRNA在肺鱗癌中高于肺腺癌,但在不同分期中表達無差異[4]。對于晚期不可手術(shù)的RRM1 mRNA低表達的NSCLC患者,應用吉西他濱治療預示著較好的生存期和療效[5,6]。本研究應用免疫組化技術(shù)回顧性檢測患者腫瘤組織RRM1等蛋白表達,其中腫瘤組織RRM1表達陰性,4次使用吉西他濱,3次療效達到PR,1次為SD;無疾病生存(progression-free survival, PFS)時間為3個月-9個月,平均為6.3個月。因此,我們將擴大樣本量研究吉西他濱治療RRM1蛋白免疫組化低表達的NSCLC患者的有效率。研究[7,8]已顯示在晚期NSCLC患者中Beta-Tubulin蛋白高表達者對紫杉類藥物耐藥,TS mRNA高表達者與培美曲塞耐藥相關(guān)。免疫組化檢測患者腫瘤組織Beta-Tubulin和TS蛋白均為高表達,并且患者應用抗微管類藥物(長春瑞賓、紫杉醇)及培美曲賽治療療效不佳,與上述研究結(jié)果相符。
本次報道病例在病情進展后多次使用原來的吉西他濱聯(lián)合鉑類方案治療,仍獲得較好的療效,提示患者腫瘤進展以后可以考慮重復使用原先有效的化療方案。吉西他濱聯(lián)合順鉑化療方案治療晚期NSCLC患者毒副反應較輕,患者耐受性較好[9]。患者雖為74歲高齡,但對多次的GP方案化療耐受性較好,并且最佳的療效是原發(fā)病灶消失,轉(zhuǎn)移灶較前明顯縮小。由于該患者GP方案化療療效佳,吉西他濱的毒副反應輕,耐受性好,是否適宜進行吉西他濱單藥維持治療有待進一步探討。
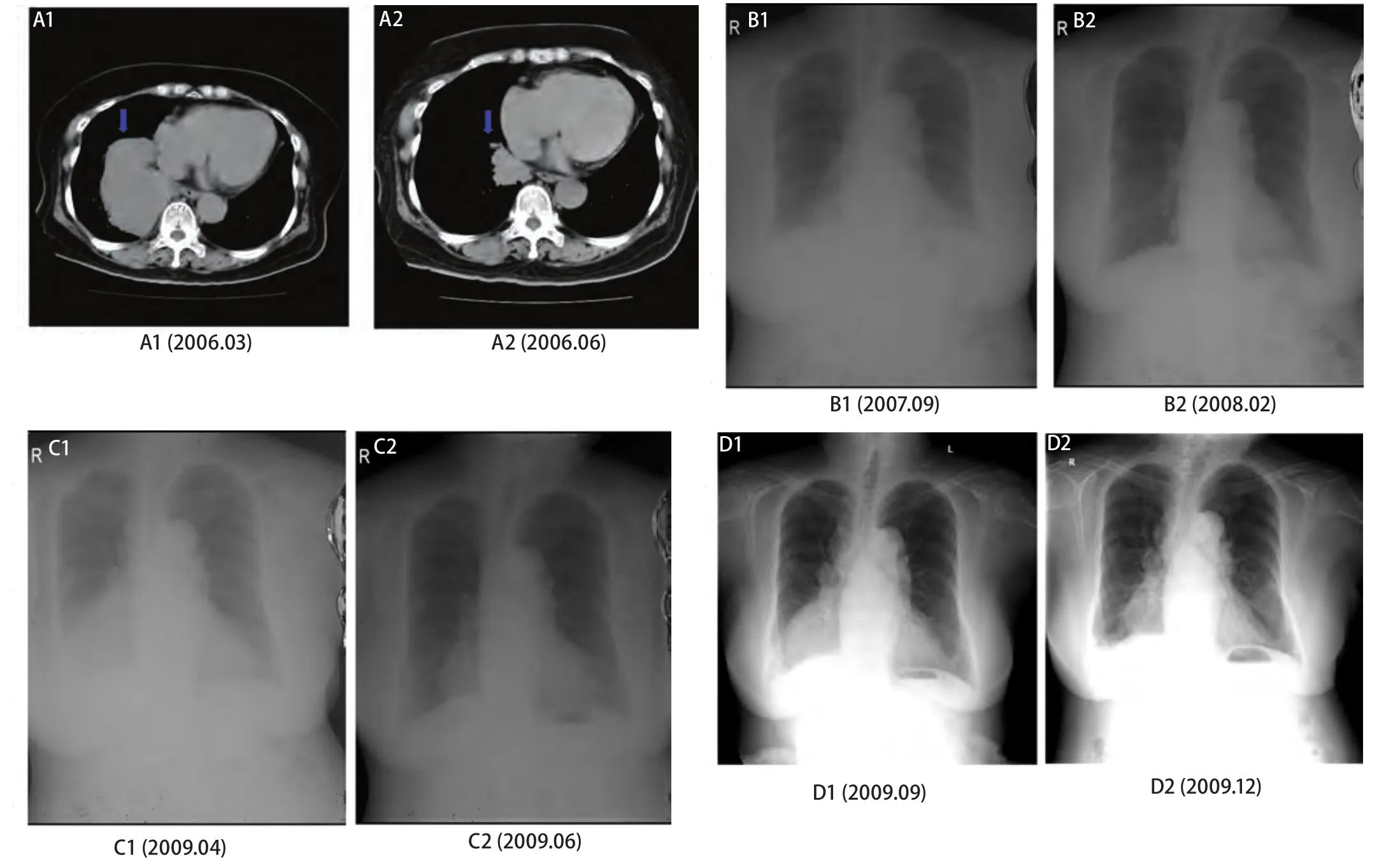
圖 1 治療前后CT及X光影像。A1:GP方案治療前右肺腫瘤(9.6 cm×5.3 cm);A2:GP方案治療后右肺腫瘤(4.2 cm×2.2 cm);B1:GP方案治療前右肺腫瘤(3.0 cm×2.5 cm);B2:GP方案治療后右肺腫瘤幾乎消失;C1:GP方案治療前右肺腫瘤(7.0 cm×8.5 cm);C2:GP方案治療后右肺腫瘤(4.2 cm×5.7 cm);D1:GP方案治療后右肺腫瘤(6.7 cm×6.5 cm);D2:GP方案治療后右肺腫瘤(4.9 cm×6.1 cm)。Fig 1 CT image and X-ray image before or after chemotherapy. A1: Tumor in right lung (9.6 cm×5.3 cm) before GP treatment; A2: Tumor in right lung (4.2 cm×2.2 cm) after GP treatment; B1: Tumor in right lung (3.0 cm×2.5 cm) before GP treatment; B2: Tumor in right lung (almost disappeared) after GP treatment; C1: Tumor in right lung (7.0 cm×8.5 cm) before GP treatment; C2: Tumor in right lung (4.2 cm×5.7 cm) after GP treatment; D1: Tumor in right lung (6.7 cm×6.5 cm) before GP treatment; D2: Tumor in right lung (4.9 cm×6.1 cm) after GP treatment.
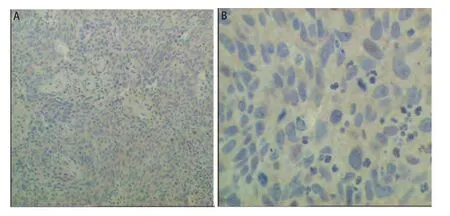
圖 2 RRM1蛋白免疫組化結(jié)果圖像。A(SP, ×100)與B(SP, ×400)免疫組化RRM1蛋白低表達。Fig 2 RRM1 protein e xpression by immunohistochemistry. A (SP, ×100) and B (SP, ×400) showed RRM1 protein expression negative by IHC.
目前,關(guān)于晚期NSCLC患者接受吉西他濱維持治療仍有爭議。Brodowicz等[10]報道接受GP方案化療,治療達到緩解后進行吉西他濱維持治療疾病進展時間(time to progress, TTP)及總生存期(overall survival, OS)明顯延長。但是2010年ASCO會議有學者[11]報道吉西他濱聯(lián)合卡鉑(gemcitabine plus carboplatin, GC)方案化療,治療達到緩解后吉西他濱(1,000 mg/m2, d1, d8)維持治療并無獲益。上述兩項研究結(jié)果存在差異,可能的原因包括:①維持治療前化療方案的鉑類不同;②維持治療的吉西他濱用量不同;③入組進行維持治療的PR及SD患者構(gòu)成比不同。上述原因都可能會對結(jié)果產(chǎn)生一定影響。此外ASCO會議也有報道[11]顯示,接受GP方案化療緩解后進行吉西他濱維持治療或者厄洛替尼維持治療對比最佳支持治療均有獲益,并且吉西他濱維持治療效果更佳。因此,吉西他濱單藥維持治療仍需進一步探討,關(guān)鍵可能在適宜人群的選擇。
綜上所述,對晚期NSCLC患者進行RRM1等相關(guān)藥敏基因的免疫組化檢測可能對化療方案的選擇有一定的臨床指導意義。

