普通離子液體和功能化離子液體的合成研究進展
唐 婧,馮 利,高尚芬
(1.四川文理學院化學與化學工程系,四川 達州 635000;2.成都市青白江區環境保護局,四川 成都 610300)
1 引言
傳統的化學反應和分離過程由于使用大量易揮發的有機溶劑,對環境污染較嚴重。隨著科技進步和環保意識的日益增強,化學反應必然向清潔、低耗、高效的趨勢發展,尋找綠色替代化合物與原料、高效催化劑及有利于反應控制的介質和溶劑已成為化學工業需要解決的緊迫問題。
針對有機溶劑產生的污染,一種新型綠色溶劑——離子液體(Ionic liquids,ILs)正在快速發展,離子液體用作有機合成中環境友好型溶劑已經得到公認,受到學術界和工業界越來越多的關注。20世紀90年代以來,此領域的研究更是方興未艾,許多新的功能化離子液體得以開發和應用[1~3],功能化的酸性離子液體[4,5]、手性離子液體[6,7]、高分子離子液體的研究不斷被報道。離子液體在電化學[8,9]、分離分析[10,11]、化學反應[12,13]和無機納米材料[14,15]以及食品工業[16]等領域已得到廣泛應用。
目前,對離子液體[17~19]的研究主要集中在新型離子液體的合成、物理化學特性的表征及其作為溶劑和電解質的應用等方面。作者在此就普通離子液體和功能化離子液體的合成研究進展等進行綜述,并對其前景進行了展望。
2 離子液體簡介

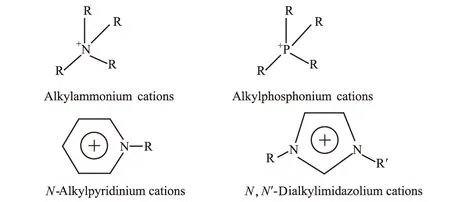
圖1 離子液體的陽離子結構
與傳統的分子溶劑不同,離子液體具有設計最優化的特點,這歸功于其組成可以從100多種陰陽離子中選擇,可以進行范圍較廣的陰陽離子組合。離子液體的物理化學特性(如極性、與其它溶劑的互溶和鹽的溶解度等)在一定程度上都能進行有規律的調節,這是其它傳統溶劑幾乎無法實現的。離子液體還具有低疏水性[25]、低粘度[26]、寬的液態范圍(-50~400 ℃)、良好的熱穩定性(400 ℃)、寬的電化學窗口(-4~4 eV)[27]、生物可降解性以及能夠加快反應速率獲得高的產率[20]等特性。此外,也可以將離子液體設計成腐蝕性和毒性較低、不易燃的結構。離子液體具有很強的Br?nsted、Lewis和Franklin酸性以及超酸性質,酸堿性可進行調節;能溶解大多數無機物、金屬配合物、有機物和高分子材料(但不能溶解聚乙烯、PTFE或玻璃),還能溶解一些氣體,如H2、CO和O2等;價格相對便宜,且容易制備。這些獨特的性能使離子液體成為有害有毒揮發性溶劑的潛在的替代品[28]。
3 離子液體的合成
3.1 普通離子液體的合成
3.1.1 傳統合成方法
3.1.1.1 直接合成法
直接合成法是將有機酸堿進行中和反應或季銨化反應一步合成離子液體[28,29]。此方法操作簡便、無副產物、產品易提純。具體制備過程如下:中和反應后真空除去多余的水,再將其溶解在乙腈或四氫呋喃等有機溶劑中,用活性炭處理,最后真空除去有機溶劑得到離子液體。如[emim]Cl+HPF6(aq)→[emim] PF6↓+HCl;也可通過含氮雜環化合物與鹵代烴發生季銨化反應得到,如[bmim]++C4H9Br→[bmim]Br([bmim]+為1-丁基-3-甲基咪唑陽離子)。
3.1.1.2 兩步合成法
兩步合成法主要包括陰離子和陽離子的合成以及陰陽離子的反應結合[30]。具體制備過程如下:首先通過季銨化反應制備目標陽離子的鹵鹽([陽離子]X);然后用目標陰離子(Y-)置換出X-或加入Lewis酸MXY來得到目標離子液體。其中,使用金屬鹽MY(常用的是AgY或NH4Y)時,產生AgY沉淀或NH3、HX氣體而容易除去;加入強質子酸HY,反應要求在低溫攪拌條件下進行,然后多次水洗至中性,用有機溶劑提取離子液體,最后真空除去有機溶劑得到純凈的離子液體。
以咪唑類離子液體為例,其合成過程如圖2所示。
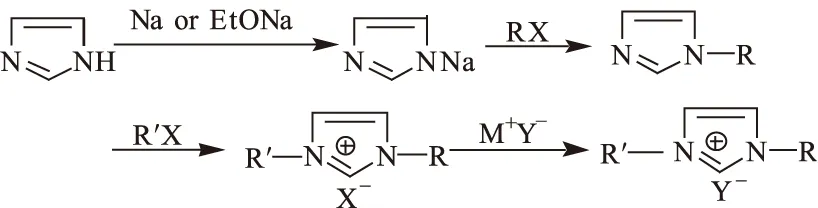
X-=Cl-、Br-、、、
采用兩步合成法合成離子液體時,對于需加熱的反應,合成第一步加熱耗時較長,且為了得到較高的產率,通常需要鹵化物過量,這使得離子液體合成的第一步既不環保且成本較高;與此同時,合成第二步會產生大量的鹵化副產物(MX或HX)。
從綠色化學的角度來看,傳統的離子液體合成方法并不是環境友好型的,這就促使研究者去開發清潔、高效的離子液體新型合成方法。
3.1.2 新型合成方法
3.1.2.1 微波輔助合成離子液體
微波是一種強電磁波,在微波照射下能產生熱力學方法得不到的高能態原子、分子和離子,可以迅速升高反應體系中自由基或碳陽離子的濃度,使體系中活化分子增加,加快反應速率、縮短反應時間。
微波加熱是以均相和選擇性的方式對材料中心進行瞬時加熱[33,34]。相對傳統加熱方式由于弱的熱傳導性能而導致的低加熱效率而言,局部過熱成為微波加熱的主要問題。微波加熱可以使由于加熱密封容器產生的壓力過大而帶來的安全問題最小化,進而被證明是優越的。就離子液體的合成而言,微波能與反應混合物直接作用,在非常短的時間內發生化學反應,不僅降低了反應能耗,也縮短了反應時間,從而提高反應效率。
Varma等[35]最先報道了在家用微波爐中不用溶劑合成離子液體的方法。離子液體能有效地吸收微波的能量,如20 g [bmim]BF4在300 W的微波照射下,55 s即可升溫至100 ℃,400 W照射只需35 s。在制備過程中,微波提供了反應分子所需的活化能,但隨著離子液體的生成,吸收能量增多,反應體系很容易過熱和失控,造成鹵代烴的氣化和產物的分解。為解決這一問題,Varma等采用微波間歇輻射、間歇混合反應物的操作,快速地合成了離子液體。
Law等[36]在微波爐中用升溫慢的水浴轉移反應體系吸收的過多熱量,有效地控制了離子液體的合成反應。Khadilkar等[37]通過控制微波照射時間,進行了密閉體系中離子液體的微波輔助合成,在防止反應過熱的同時,避免了開放體系中反應物與產物的氣化和腐蝕。這兩種改進方法雖然操作復雜,但提高了反應的安全性與穩定性,更為重要的是實現了大量離子液體的一次性合成。
為了將微波和離子液體的優勢結合起來,有學者對微波輻射條件下諸如乙酰化、低聚、二聚、高聚和共聚等類型的有機反應進行了研究[38,39]。
微波輻射通過微波與起始原料的分子偶極矩分子之間相互作用,對分子直接加熱[40],從而實現快速容積加熱、高效節能熱合成;但微波輻射或多或少存在一些缺陷,如反應不易控制、有副反應發生、反應器價格昂貴等,因此,僅限于實驗室小規模合成。
3.1.2.2 超聲波輔助合成離子液體
超聲波能夠加快化學反應速率、減小液體中懸浮粒子的尺寸、加快異相反應速率[41]。與傳統方法相比,超聲波輔助合成縮短了反應時間、提高了產品收率,并可在常溫條件下進行有機反應(若用常規方法,則需要較高溫度和較大壓力,有時甚至無法反應[42])。
Namboodiri等[43]在密閉體系非溶劑條件下采用超聲波輔助合成離子液體時發現,鹵化物與甲基咪唑的反應活性大小依次為:I>Br>Cl。溴化物和碘化物在室溫下0.5~2 h即可完成反應,收率均高于90%;氯化物則需要加熱和較長時間的超聲波作用。Leveque等[44]研究[bmim]Cl與NH4BF4、NH4CF3SO3、NH4PF6等鹽的離子交換反應時發現,磁力攪拌一般需要5~8 h,而超聲波作用只需1 h,大大縮短了反應時間。
總之,微波和超聲波輔助合成離子液體能在獲得高產率的同時加快反應速度、避免長時間加熱、降低能耗、減少有機溶劑的使用,具有普遍的實用性。
3.2 功能化離子液體的合成
近來,功能化離子液體(Task-specific ionic liquids,TSILs)的合成愈來愈受到人們的重視,其功能化是通過在離子液體的陽離子或陰離子上引入官能團來實現的[45]。引入官能團能夠賦予離子液體特殊的性能。胺、酰胺、腈、乙醚、酒精、酸、尿素或硫脲、咪唑和吡啶陽離子、含氟陰離子等都能夠作為官能團引入到離子液體中[46~49],合成的離子液體不僅可以作為可替代的綠色溶劑,也可作為有機反應中的試劑和催化劑,具有較高的應用價值。由于功能化離子液體具有可控的物理化學特性,許多學者對其合成進行了廣泛的研究[50]。
3.2.1 功能化手性離子液體的合成
功能化手性離子液體(Chiral ionic liquids,CILs)由于在不對稱合成、立體選擇性聚合和手性色譜等方面具有潛在的應用價值,越來越受到重視。其合成方法主要有以下幾種:直接在普通離子液體中引入帶有手性中心的陰離子;用手性烷基化試劑對胺、咪唑或吡啶進行烷基化;用帶有手性中心的天然產物合成氮雜環;利用手性池制備含有手性陽離子的手性離子液體。自1999年,通過引入乳酸鹽陰離子合成了第一個具有手性的CILs[50]以來,相繼成功制備了較多具有中心、軸向和平面手性的CILs[51~53]。但是,由于受到發展和應用范圍的限制,CILs的研究現在還處在初步階段。
引入手性胺官能團從而將有效的不對稱誘導模式賦予離子液體,所得到的CILs在不對稱合成中用于手性轉移比傳統手性試劑更有效。Ishikawa等采用離子交換法制備了以手性樟腦磺酸根離子為陰離子的CILs[54],在Diels-Alder反應中取得了endo∶exo高達10.3的選擇性,但遺憾的是該研究未涉及對映選擇性。Kim等[18]利用Mitsunobu烷基化反應制備基于咪唑陽離子的CILs,但需要昂貴的手性烷基化試劑,限制了該類CILs在合成反應中的應用。
由于手性烷基化試劑的昂貴,人們將目光轉向價廉的天然手性物質,希望能以其為原料直接合成所預想的CILs。有效、便捷地合成離子液體的方法之一就是使用來源于手性庫,特別是生物可再生資源的基質,如麻黃堿[55,56]、尼古丁、薄荷[57~59]、松香芹酮[60]和氨基酸[55]等。
研究表明,只有少數CILs可用于有非手性基質參與反應的手性誘導,因此尋找新的CILs迫在眉睫。Matos等[61]報道了基于薄荷[62,63]、龍腦[64]的一系列CILs的合成和表征,與已經報道的一些含有醚官能團的薄荷基[62,63]CILs的合成不同,Matos在合成中引入酯基,除了可以得到所需的CILs,還可改善其與聚合物穩定性相關的某些性能。
其合成路線如圖3所示。
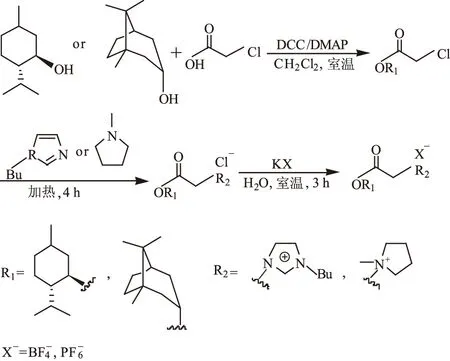
圖3 基于薄荷、龍腦的CILs的合成
CILs不僅可以用作有效的反應介質,也可用于手性催化。由于其合成初始原料易得、反應條件適宜、方法簡單實用,可預見CILs的合成和應用研究將得到更快的發展。
3.2.2 功能化酸性離子液體的合成
功能化酸性離子液體(Functionalized acidic ionic liquids,FAILs)是指具有明顯的Lewis酸性或Br?nsted酸性的離子液體。一般具有Lewis酸性的FAILs是由金屬鹵化物與季銨化的胺或咪唑、吡啶等雜環或四級磷鹽混合制備的,最為常見的是以鋁氯酸根為陰離子,在室溫下大多呈液態,可以作為反應介質和Lewis酸催化劑[65~67]。與傳統溶劑和催化劑相比,FAILs更易于循環利用,用作催化劑時可重復和循環使用多次,其活性沒有明顯的降低。
由于合成化學工業中酸性催化劑的廣泛使用,使得基于離子液體的酸性催化劑日益受到重視[68,69]。在過去的十幾年里,鋁酸鹽離子液體,由于其幾乎可以忽略的蒸汽壓、可調的溶解度等被用來替代礦物質和固體酸性催化劑,受到更多的關注。然而,鋁酸鹽離子液體易水解,痕量的水便可改變鹽的組成和質子的濃度,很難準確地控制其酸度。因此,迫切需要開發對水和空氣穩定且更高效的酸性離子液體。通過研究,現已成功制備出非鋁酸鹽酸性離子液體如磺酸基FAILs[70]、磺酰氯FAILs[71]。通過[bmim]Cl(1-Butyl-3-methylimidazolium)和H2SO4(或NaHSO4)間的離子交換,也可制備磺酸氫鹽FAILs,可用作酯化和烷基化反應的催化劑。此外,一些無機或有機酸,如HCl、HBF4和CF3COOH也可與N-烷基咪唑反應形成一類新的質子型離子液體。
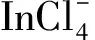

圖4 三辛基甲銨離子液體的合成
4 結語
作為環境友好型綠色溶劑的離子液體,在不同的領域都有潛在的應用價值,近年來受到世界各國的廣泛關注。人們已經開發出多種手性離子液體,它們的應用研究也已經起步。除了拓展特殊的功能和應用,降低成本也是手性離子液體發展的關鍵。合成時需要優先考慮的是手性源的選擇,使用天然手性源作為起始原料將是獲得手性離子液體的發展方向。Lewis酸性離子液體尤其是AlCl3類離子液體的發展較早,應用也較廣;相比之下,Br?nsted酸性離子液體的合成才剛剛起步,還需要進一步提高Br?nsted酸性離子液體的酸度;從已有研究可以看到,要開發適于工業應用的酸性離子液體,應充分發揮酸性離子液體類似固體酸和液體酸的優勢,并發展兼具Lewis酸性和Br?nsted酸性的離子液體的合成方法,設計出具有獨特物理化學性質的功能化離子液體來適應各種特殊需要將是功能化離子液體未來發展的方向。
以離子液體作為反應溶劑,為化學反應提供了不同于傳統分子溶劑的環境,可能改變反應機理,使催化劑的活性、穩定性更好,轉化率、選擇性更高。將催化劑溶于液體中,可以與離子液體一起循環使用,催化劑兼具均相催化效率高及多相催化易分離的特點。
目前,離子液體的研究面臨的主要問題是:如何降低離子液體的合成成本、如何進行離子液體的回收利用、如何減輕離子液體對環境和生物的影響。相信隨著科技的不斷進步和研究的不斷深入,離子液體的研究和開發必將為“綠色化學”和“綠色工藝”開辟新的道路。
[1] Gao Y,Arritt S W,Twamley B,et al.Guanidinium-based ionic liquids[J].Inorg Chem,2005,44(6):1704-1712.
[2] Genisson Y,Lauth-de Viguerie N,Andre C,et al.New chiral imidazolinic derivatives[J].Tetrahedron:Asymmetry,2005,16(5):1017-1023.
[3] Zhao D S,Duan E H,Liu R,et al.Efficient synthesis of 1,4-diazabicyclo(2.2.2)octane in ionic liquids[J].Catal Commun,2008,9(8):1725-1727.
[4] Wang L,Li H J,Li P H.Task-specific ionic liquid as base,ligand and reaction medium for the palladium-catalyzed Heck reaction[J].Tetrahedron,2009,65(1):364-368.
[5] Yue C B,Mao A Q,Wei Y Y,et al.Knoevenagel condensation reaction catalyzed by task-specific ionic liquid under solvent-free conditions[J].Catal Commun,2008,9(7):1571-1574.
[6] Fukumoto K,Yoshizawa M,Ohno H.Room temperature ionic liquids from 20 natural amino acids[J].J Am Chem Soc,2005,127(8):2398-2399.
[7] Baudoux J,Judeinstein P,Cahard D,et al.Design and synthesis of novel ionic liquid/liquid crystals (IL2Cs) with axial chirality[J].Tetrahedron Lett,2005,46(7):1137-1140.
[8] Xia J,Masaki N,Jiang J,et al.Deposition of a thin film of TiOxfrom a titanium metal target as novel blocking layers at conducting glass/TiO2interfaces in ionic liquid mesoscopic TiO2dye-sensitized solar cells[J].J Phys Chem B,2006,110(50):25222-25228.
[9] Yang J Z,Jin Y,Xu W G,et al.Studies on mixture of ionic liquid EMIGaCl4and EMIC[J].Fluid Phase Equilibria,2005,227(1):41-46.
[10] Mank M,Stahl B,Boehm G.2,5-Dihydroxybenzoic acid butylamine and other ionic liquid matrixes for enhanced MALDI-MS analysis of biomolecules[J].Anal Chem,2004,76(10):2938-2950.
[11] Tian K,Qi S D,Cheng Y Q,et al.Separation and determination of lignans from seeds ofSchisandraspecies by micellar electrokinetic capillary chromatography using ionic liquid as modifier[J].J Chromatogr A,2005,1078(1-2):181-187.
[12] Martin R,Teruel L,Aprile C,et al.Imidazolium ionic liquids in OLEDs:Synthesis and improved electroluminescence of an ′ionophilic′ diphenylanthracene[J].Tetrahedron,2008,64(27):6270-6274.
[13] Venkatesan K,Pujari S S,Lahoti R J,et al.An efficient synthesis of 1,8-dioxo-octahydro-xanthene derivatives promoted by a room temperature ionic liquid at ambient conditions under ultrasound irradiation[J].Ultrason Sonochem,2008,15(4):548-553.
[14] Fonseca G S,Machado G,Teixeira S R,et al.Synthesis and characterization of catalytic iridium nanoparticles in imidazolium ionic liquids[J].J Colloid Interface Sci,2006,301(1):193-204.
[15] Hou X M,Zhou F,Sun Y B,et al.Ultrasound-assisted synthesis of dentritic ZnO nanostructure in ionic liquid[J].Mater Lett,2007,61(8-9):1789-1792.
[16] 劉曉庚,鞠興榮,陳梅梅,等.幾種離子液體對生物活性物的溶解行為[A].中國化學會第四屆有機化學學術會議論文集[C].2005:145.
[17] Ranu B C,Banerjee S.Ionic liquid as catalyst and reaction medium.The dramatic influence of a task-specific ionic liquid,[bmim]OH,in Michael addition of active methylene compounds to conjugated ketones,carboxylic esters,and nitriles[J].Org Lett,2005,7(14):3049-3052.
[18] Kim E J,Koa S Y,Dziadulewiczb E K.Mitsunobu alkylation of imidazole:A convenient route to chiral ionic liquids[J].Tetrahedron Lett,2005,46(4):631-633.
[19] Zou D B,Xu C,Luo H,et al.Synthesis of Co3O4nanoparticles via an ionic liquid-assisted methodology at room temperature[J].Mater Lett,2008,62(12-13):1976-1978.
[20] Welton T.Room-temperature ionic liquids:Solvents for synthesis and catalysis[J].Chem Rev,1999,99(8):2071-2084.
[21] 李汝雄.綠色溶劑——離子液體的合成與應用[M].北京:化學工業出版社,2004:10,16.
[22] Mallakpour S,Taghavi M.Microwave heating coupled with ionic liquids:Synthesis and properties of novel optically active polyamides,thermal degradation and electrochemical stability on multi-walled carbon nanotubes electrode[J].Polym,2008,49(15):3239-3249.
[23] Przybysz K,Drzewinska E,Stanislawska A,et al.Ionic liquids and paper[J].Ind Eng Chem Res,2005,44(13):4599-4604.
[24] Cho C,Pham T P,Jeon Y C,et al.Toxicity of imidazolium salt with anion bromide to a phytoplanktonSelenastrumcapricornutum:Effect of alkyl-chain length[J].Chemosphere,2007,69(6):1003-1007.
[25] Swatloski R P,Visser A E,Reichert W M,et al.Solvation of 1-butyl-3-methylimidazolium hexafluorophosphate in aqueous ethanol——A green solution for dissolving ′hydrophobic′ ionic liquids[J].Chem Commun,2001,(20):2070-2071.
[26] MacFarlane D R,Golding J,Forsyth S,et al.Low viscosity ionic liquids based on organic salts of the dicyanamide anion[J].Chem Commun,2001,(16):1430-1431.
[27] Bühler G,Zharkouskaya A,Feldmann C.Ionic liquid based approach to nanoscale functional materials[J].Solid State Sci,2008,10(4):461-465.
[28] Bradaric C J,Downard A,Kennedy C,et al.Industrial preparation of phosphonium ionic liquids[J].Green Chem,2003,5(2):143-152.
[29] Holbrey J D,Reichert W M,Swatloski R P,et al.Efficient,halide free synthesis of new,low cost ionic liquids:1,3-Dialkylimidazolium salts containing methyl-and ethyl-sulfate anions[J].Green Chem,2002,4(5):407-413.
[30] Zhao S H,Zhao E L,Shen P,et al.An atom-efficient and practical synthesis of new pyridinium ionic liquids and application in Morita-Baylis-Hillman reaction[J].Ultrason Sonochem,2008,15(6):955-959.
[31] Xue H,Verma R,Shreeve J M.Review of ionic liquids with fluorine-containing anions[J].J Fluorine Chem,2006,127(2):159-176.
[32] Quek S K,Lyapkalo I M,Huynh H V.Synthesis and properties ofN,N′-dialkylimidazolium bis(nonafluorobutane-1-sulfonyl)imides:A new subfamily of ionic liquids[J].Tetrahedron,2006,62(13):3137-3145.
[33] Mallakpour S,Rafiemanzelat F.New optically active poly(amide-imide-urethane) thermoplastic elastomers derived from poly(ethylene glycol diols),4,4′-methylene-bis(4-phenylisocyanate),and a diacid based on an amino acid by a two-step method under microwave irradiation[J].J Appl Polym Sci,2005,98(4):1781-1792.
[34] Kretschmann O,Schmitz S,Ritter H.Microwave-assisted synt-hesis of associative hydrogels[J].Macromol Rapid Commun,2007,28(11):1265-1269.
[35] Varma R S,Namboodiri V V.An expeditious solvent-free route to ionic liquids using microwaves[J].Chem Commun,2001,(7):643-644.
[36] Law M C,Wong K Y,Chan T H.Solvent-free route to ionic liquid precursors using a water-moderated microwave process[J].Green Chem,2002,4(4):328-330.
[37] Khadilkar B M,Rebeito G L.Microwave-assisted synthesis of room-temperature ionic liquid precursor in closed vessel[J].Org Proc Res Dev,2002,6(6):826-828.
[38] Hakala U,W?h?l? K.Expedient deuterolabeling of polyphenols in ionic liquidssDCl/D2O under microwave irradiation[J].J Org Chem,2007,72(15):5817-5819.
[39] Borriello A,Nicolais L,Fang X,et al.Synthesis of poly(amide-ester)s by microwave methods[J].J Appl Polym Sci,2007,103(3):1952-1958.
[40] Mallakpour S,Rafiee Z.Use of ionic liquid and microwave irradiation as a convenient,rapid and eco-friendly method for synthesis of novel optically active and thermally stable aromatic polyamides containingN-phthaloyl-L-alanine pendent group[J].Polym Degrad Stab,2008,93(4):753-759.
[41] Rajagopal R,Jarikote V,Srinivasan K V.Ultrasound promoted Suzuki cross-coupling reactions in ionic liquid at ambient conditions[J].Chem Commun,2002,(6):616-617.
[42] Ambulgekar G V,Bhanage B M,Samant S D.Low temperature recyclable catalyst for Heck reactions using ultrasound[J].Tetrahedron Lett,2005,46(14):2483-2485.
[43] Namboodiri V V,Varma R S.Solvent-free sonochemical preparation of ionic liquids[J].Org Lett,2002,4(18):3161-3163.
[44] Leveque J M,Luehe J L,Rouxa C P R,et al.An improved preparation of ionic liquids by ultrasound[J].Green Chem,2002,4(4):357-360.
[45] Germani R,Mancini M V,Savelli G,et al.Mercury extraction by ionic liquids:Temperature and alkyl chain length effect[J].Tetrahedron Lett,2007,48(10):1767-1769.
[46] Visser A E,Swatloski R P,Reichert W M,et al.Task-specific ionic liquids incorporating novel cations for the coordination and extraction of Hg2+and Cd2+:Synthesis,characterization,and extraction studies[J].Environ Sci Technol,2002,36(11):2523-2529.
[47] Holbrey J D,Visser A E,Spear S K,et al.Mercury(Ⅱ) partitioning from aqueous solutions with a new,hydrophobic ethylene-glycol functionalized bis-imidazolium ionic liquid[J].Green Chem,2003,5:129-135.
[48] Zhao D B,Fei Z F,Ohlin C A,et al.Dual-functionalised ionic liquids:Synthesis and characterisation of imidazolium salts with a nitrile-functionalised anion[J].Chem Commun,2004,(21):2500-2501.
[49] Ouadi A,Gadenne B,Hesemann P,et al.Task-specific ionic liquids bearing 2-hydroxybenzylamine units:Synthesis and americium-extraction studies[J].Chem,2006,12(11):3074-3081.
[50] Earle M J,McCormac P B,Seddon K R.Diels-Alder reactions in ionic liquids[J].Green Chem,1999,1(1):23-25.
[51] Baudequin C,Bregeon D,Levillain J,et al.Chiral ionic liquids,a renewal for the chemistry of chiral solvents Design,synthesis and applications for chiral recognition and asymmetric synthesis[J].Tetrahedron:Asymmetry,2005,16(24):3921-3945.
[52] Branco L C,Gois P M P,Lourenco N M T,et al.Simple transformation of crystalline chiral natural anions to liquid medium and their use to induce chirality[J].Chem Commun,2006,(22):2371-2372.
[53] Patil M L,La Rao C V,Yonezawa K,et al.Design and synthesis of novel chiral spiro ionic liquids[J].Org Lett,2006,8(2):227-230.
[54] Nobuoka K,Kitaoka S,Kunimitsu K,et al.Camphor ionic liquid:Correlation between stereoselectivity and cation-anion interaction[J].J Org Chem,2005,70(24):10106-10108.
[55] Clavier H,Boulanger L,Audic N,et al.Design and synthesis of imidazolinium salts derived from (L)-valine.Investigation of their potential in chiral molecular recognition[J].Chem Commun,2004,(10):1224-1225.
[56] Vo-Thanh G,Pegot B,Loupy A.Solvent-free microwave-assisted preparation of chiral ionic liquids from (-)-N-methylephedrine[J].Eur J Org Chem,2004,2004(5):1112-1116.
[57] Biedron T,Kubisa P.Radical polymerization in a chiral ionic liquid:Atom transfer radical polymerization of acrylates[J].J Polym Sci Part A:Polym Chem,2005,43(15):3454-3459.
[58] Pernak J,Feder-Kubis J.Synthesis and properties of chiral ammonium-based ionic liquids[J].Chem Eur J,2005,11(15):4441-4449.
[59] Malhotra S V,Wang Y.Application of chiral ionic liquids in the copper catalyzed enantioselective 1,4-addition of diethylzinc to enones[J].Tetrahedron:Asymmetry,2006,17(7):1032-1035.
[60] Bao W L,Wang Z M,Li Y X.Synthesis of chiral ionic liquids from natural amino acids[J].J Org Chem,2003,68(2):591-593.
[61] Matos R A F,Andrade C K Z.Synthesis of new chiral ionic liquids based on (-)-menthol and (-)-borneol[J].Tetrahedron Lett,2008,49(10):1652-1655.
[62] Ding J,Desikan V,Han X,et al.Use of chiral ionic liquids as solvents for the enantioselective photoisomerization of dibenzobicyclo[2.2.2]octatrienes[J].Org Lett,2005,7(2):335-337.
[63] Pernak J,Feder-Kubis J.Synthesis and properties of chiral ammonium-based ionic liquids[J].Chem Eur J,2005,11(15):4441-4449.
[64] Gadenne B,Hesemann P,Moreau J J E.Ionic liquids incorporating camphorsulfonamide units for the Ti-promoted asymmetric diethylzinc addition to benzaldehyde[J].Tetrahedron Lett,2004,45(44):8157-8160.
[65] Fang D,Luo J,Zhou X L,et al.Mannich reaction in water using acidic ionic liquid as recoverable and reusable catalyst[J].Catal Lett,2007,116(1-2):76-80.
[66] Fang D,Gong K,Fei Z H,et al.A practical and efficient synthesis of quinoxaline derivatives catalyzed by task-specific ionic liquid[J].Catal Commun,2008,9(2):317-320.
[67] Gong K,Fang D,Wang H L,et al.The one-pot synthesis of 14-alkyl-or aryl-14H-dibenzo[a,j]xanthenes catalyzed by task-specific ionic liquid[J].Dyes and Pigments,2009,80(1):30-33.
[68] Fang D,Luo J,Zhou X L,et al.One-pot green procedure for Biginelli reaction catalyzed by novel task-specific room-temperature ionic liquids[J].J Mol Catal A:Chem,2007,274(1-2):208-211.
[69] Wang W J,Shao L L,Cheng W P,et al.Br?nsted acidic ionic liquids as novel catalysts for Prins reaction[J].Catal Commun,2008,9(3):337-341.
[70] Cole A C,Jensen J L,Ntai I.Novel Br?nsted acidic ionic liquids and their use as dual solvent-catalysts[J].J Am Chem Soc,2002,124(21):5962-5963.
[71] Gui J Z,Deng Y Q,Hu Z D,et al.A novel task-specific ionic liquid for Beckmann rearrangement:A simple and effective way for product separation[J].Tetrahedron Lett,2004,45(12):2681-2683.
[72] Du Z Y,Li Z,Deng Y.Synthesis and characterization of sulfonyl-functionalized ionic liquids[J].Synth Commun,2005,35(10):1343-1349.
[73] Kim Y J,Varma R S.Microwave-assisted preparation of imidazolium-based tetrachloroindate(Ⅲ) and their application in the tetrahydropyranylation of alcohols[J].Tetrahedron Lett,2005,46(9):1467-1469.
[74] Duan Z Y,Gu Y L,Zhang J,et al.Protic pyridinium ionic liquids:Synthesis,acidity determination and their performances for acid catalysis[J].J Mol Catal A:Chem,2006,250(1-2):163-168.
[75] Kogelnig D,Stojanovic A,Galanski M,et al.Greener synthesis of new ammonium ionic liquids and their potential as extracting agents[J].Tetrahedron Lett,2008,49(17):2782-2785.

