對氨基苯甲酸修飾玻碳電極方波伏安檢測銅離子
王嘉博, 楊國程, 王 璐, 趙振波, 李東風
(長春工業大學化學與生命科學學院,吉林長春 130012)
0 引 言
化學修飾電極是當前電化學、電分析化學方面十分活躍的研究領域。通過化學、物理化學或者電化學的方法對電極表面進行分子剪裁、修飾,可以按意圖給電極預定結構和功能。目前,常用電化學氧化或者電化學還原的方法進行化學修飾,修飾分子與電極表面多以共價鍵形式相連,所制得的共價化學修飾電極結構穩定、長效[1]。由于重金屬離子對環境生態及人類健康都有著至關重要的影響,因此,尋找簡便、快捷、高效的重金屬離子檢測方法具有十分重要的意義,而具有預定功能的化學修飾電極在這方面顯示出了強大的吸引力[2-4]。
文中將對氨基苯甲酸(4-aminobenzoic acid,4-ABA)通過電化學氧化方法共價修飾到玻碳電極(G lassy Carbon Electrode,GCE)上,考查了該修飾電極對銅離子的傳感效應。
1 實驗部分
1.1 試劑與儀器
K3Fe(CN)6,KCl,4-ABA,Cu(NO3)2均為分析純;
電化學工作站(CS 350),武漢科斯特儀器有限公司;
單道固定量程移液器(Genex),Finland Genex;
超聲波清洗器(KQ-100E),昆山市超聲波儀器有限公司;
超純水機(WP-UP-II-20),四川沃特爾水處理設備有限公司。
1.2 方法
1.2.1 共價化學修飾電極的制備
在使用GCE做實驗之前,需要先清潔其表面:取適量α-A l2O3(1μm)拋光粉鋪在拋光絨布上,用超純水調成糊狀,研磨GCE,然后用超聲波清洗器清洗,再在 5 mmol/L Fe(CN)3-6(0.1 mol/L KCl作為支持電解質)溶液中進行循環伏安測試,磨到Fe(CN)3-6在GCE上氧化還原峰電位差值小于75mV方可使用。電極表面活性達到要求后,將GCE用超純水沖洗,再超聲清洗10 s,放入1 mmol/L 4-ABA溶液中(0.1 mo l/L KC l作為支持電解質)進行共價化學修飾,所得到的衍生結構如圖1所示[5]。
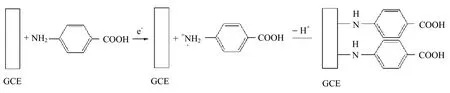
圖1 4-ABA在GCE上的修飾過程及衍生結構
1.2.2 方波溶出伏安檢測Cu2+
將工作電極(GCE或4-ABA/GCE)、輔助電極(旋轉鉑絲電極)和參比電極(KCl飽和的Ag/AgCl電極)插入2m L 0.1m ol/L KCl溶液中(pH值接近7),首先測量空白溶液方波溶出伏安曲線,然后每次加4μL 50mmol/LCu(NO3)2水溶液,采用方波溶出伏安法進行檢測Cu2+,具體的實驗參數如下:清洗電位:0.4 V;清洗時間: 15 s;富集電位:-0.5 V;富集時間:15 s;靜置時間:15 s;電位增量:0.004 V;初始電位:-0.5 V;終止電位:0.5 V;振幅:0.025 V。
2 結果與討論
2.1 GCE修飾過程
4-ABA在GCE上的共價化學修飾過程及探針行為如圖2所示。
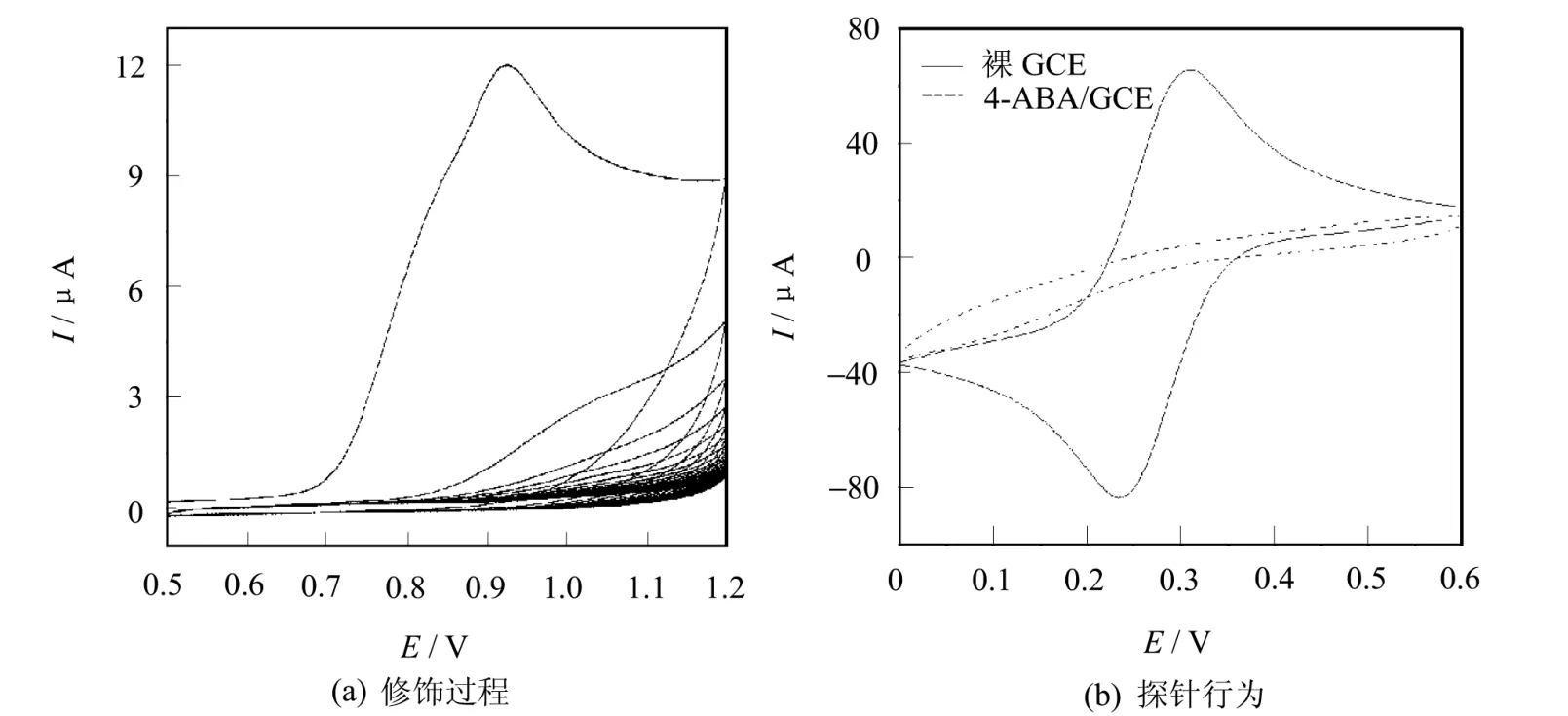
圖2 4-ABA在GCE上的共價化學修飾過程及探針行為
GCE在4-ABA溶液中電氧化過程的循環伏安行為(見圖2(a))。從圖中可以看出,第一圈電位掃描時在~0.9 V處出現了一個不可逆的氧化峰,在隨后的掃描中該氧化峰逐漸消失,這說明4-ABA共價鍵合到了GCE上。
考查了修飾前后電極在Fe(CN)3-6探針溶液中的循環伏安行為(見圖2(b))。結果發現,在修飾前Fe(CN)3-6的氧化峰和還原峰出現,但修飾后卻無峰出現,這也確定4-ABA鍵合到GCE上了,因為修飾后GCE表面的4-ABA外端為-COO-,使 GCE表面帶負電荷,完全阻礙Fe(CN)3-6在GCE表面的氧化還原反應[5]。
2.2 溶出伏安檢測Cu2+
GCE在 4-ABA修飾前后都被考查其對Cu2+的方波溶出伏安檢測效果,結果如圖3所示。

圖3 Cu2+在裸GCE表面的溶出伏安曲線及校正曲線
從結果可以看出,裸GCE在溶出伏安檢測Cu2+時,出現了兩個溶出峰,分別在-0.012 V和0.188 V,底物濃度與溶出峰電流都成直線關系:

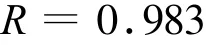
但是低電位的峰電流在Cu2+濃度相同時比高電位的要大。
Cu2+在4-ABA/GCE表面的溶出伏安曲線及校正曲線如圖4所示。

圖4 Cu2+在4-ABA/GCE表面的溶出伏安曲線及校正曲線
用修飾后得到的4-ABA/GCE在同樣的條件下方波溶出伏安檢測Cu2+,方波溶出伏安曲線見圖4(a)。可以看出,曲線也由兩個溶出峰組成,底物濃度與溶出峰電流關系也成直線關系,見圖4 (b)。
底物濃度與溶出峰電流直線關系的方程如下:
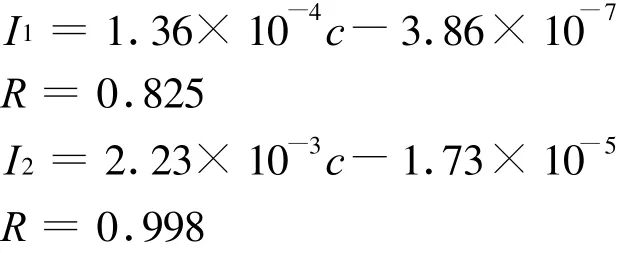
但是低電位的峰電流在Cu2+濃度相同時比高電位的要小很多,這一點與在裸GCE上的結果相反。
裸GCE和4-ABA/GCE對于Cu2+的溶出峰都有兩個,說明在電沉積過程中都存在欠電位沉積和本體電沉積,分別對應于-0.012 V和0.188 V,但是濃度與峰電流關系不同,說明在兩電位下沉積Cu2+的量不同。對于裸GCE來說,電極表面活性高,易于電沉積Cu2+,因而裸GCE對Cu2+的靈敏度也高,這一點從校正曲線的斜率就可以清楚地看出,而棱面碳的活性位點更多,欠電位沉積的量將會比本體電沉積的量要大。對于4-ABA/GCE,由于電極界面外端為-COO-,電極表面原有的活性被阻擋,活性位點降低,因而靈敏度變差,而羧基對Cu2+具有非常強的絡合作用,特別容易形成多層膜,也就是特別容易發生本體電沉積[6-8]。
3 結 語
通過電化學氧化的方法將4-ABA共價修飾到GCE上,利用方波溶出伏安法研究了電極修飾前后對中性溶液中Cu2+的檢測效果,結果顯示,Cu2+在裸GCE和4-ABA/GCE表面上的溶出峰都有兩個,即都存在欠電位沉積和本體電沉積行為,但是程度不同,GCE的欠電位沉積能力較本體電沉積要強,4-ABA/GCE則相反,這是由于裸GCE具有比4-ABA/GCE更好的表面活性引起的。
[1] 董紹俊,車廣禮,謝遠武.化學修飾電極[M].2版.北京:科學出版社,2003.
[2] Liu L X,Liu E.N itrogenated diamond-like carbon films for metal tracing[J].Surf.Coat.Technol.,2005,198(1/3):189-193.
[3] 劉穎,柳翱.電化學測定化學反應熱力學函數變化值[J].長春工業大學學報:自然科學版,2009,30 (3):258-261.
[4] 林海波,伍振毅,黃衛民,等.工業廢水電化學處理技術的進展及其發展方向[J].化工進展,2008,27 (2):223-230.
[5] Yang G C,Shen Y,W ang M K,et al.Copper hexacyanoferrate multilayer films on g lassy carbon electrode modified with 4-am inobenzoic acid in aqueous solution[J].Talanta,2006,68(3):741-747.
[6] A llen J B,Larry R F.Electrochem ical methods fundamentals and applications[M].2th ed.New York:John W iley&Sons,Inc.,2001.
[7] 張祖訓,汪爾康.電化學原理與方法[M].北京:科學出版社,2000.
[8] 吳輝煌.電化學[M].北京:化學工業出版社,2004.

