珍珠冰硼散微生物限度檢查方法學驗證
王德啟
(安徽孟仁壽制藥有限公司質檢中心,安徽 宿州234300)
在2005年以前的《中國藥典》版本中未規定對供試品的微生物限度檢驗方法進行驗證,造成在實際檢驗工作中,由于某些藥品成分具有抗菌活性,抑制了藥品中部分微生物的生長,按常規法檢驗得到的結果不準確[1]。為確保微生物限度檢查方法的科學性和檢驗結果的準確性,2005年版《中國藥典》開始規定藥品的微生物限度檢查應進行方法學驗證,以確保藥品微生物限度檢查結果準確可信。珍珠冰硼散是由珍珠、朱砂、冰片、硼砂(煅)、玄明粉等5味藥物組成的散劑,具有去腐、解毒、消炎止痛功效,臨床用于口舌生瘡、齒齦腐爛、腫痛、急慢性咽喉炎等癥[2]。本文就分別采用平皿法、培養基稀釋法、直接接種法[3]對其微生物限度檢查進行了方法學驗證。
1 材料
1.1 樣品
珍珠冰硼散(安徽孟仁壽制藥有限公司,規格:1.5 g/瓶,批號:20070415、20070416、20070417)。
1.2 菌種
大腸埃希菌[CMCC(B)44102]、金黃色葡萄球菌[CMCC(B)26003]、枯草芽孢桿菌[CMCC(B)63501]、白色念珠菌[CMCC(F)98001]、黑曲霉菌[CMCC(F)98003]、銅綠假單胞菌[CMCC(B)10104](中國藥品生物制品檢所)。
1.3 培養基
膽鹽乳糖增菌液、玫瑰紅鈉瓊脂培養基、營養瓊脂培養基、營養肉湯培養基、改良馬丁培養基、改良馬丁瓊脂培養基、溴化十六烷基三甲銨瓊脂培養基、甘露醇氯化鈉瓊脂培養基、硫乙醇酸鹽流體培養基(中國藥品生物制品檢定所)。
1.4 稀釋劑
pH7.0無菌氯化鈉-蛋白胨緩沖液(自制)。
2 方法
參照2005年版《中國藥典》(一部)微生物限度檢查法[4]進行試驗。
2.1 菌液制備
接種大腸埃希菌、金黃色葡萄球菌、枯草芽孢桿菌、銅綠假單胞菌的新鮮培養物至營養肉湯培養基中,于30~35℃培養18~24 h;各肉湯培養物分取1m L,加9m L生理鹽水,10倍稀釋至約含50~100 cfu/mL的菌懸液,備用。
接種白色念珠菌的新鮮培養物至改良馬丁培養基中,于23~28℃培養24~48 h,取經培養好的白色念珠菌真菌斜面培養物,加入生理鹽水4m L,洗下孢子,吸出轉移至無菌試管內,取1m L,加9m L生理鹽水,10倍稀釋至約含50~100 cfu/m L的菌懸液,備用。接種黑曲霉菌斜面的新鮮培養物至改良馬丁瓊脂斜面培養基中,于23~28℃培養5~7 d,使大量的孢子成熟。取黑曲霉菌斜面培養物,加入生理鹽水4m L,洗下孢子,吸出,轉移至無菌試管內,取1m L,加9m L生理鹽水,10倍稀釋至約含50~100 cfu/m L的孢子懸液,備用。
2.2 供試液的制備
取供試品10 g,加pH 7.0無菌氯化鈉-蛋白胨緩沖液至100m L,混勻,作為供試液。
2.3 回收率試驗
2.3.1 平皿法
2.3.1.1 試驗組 取供試液1m L和50~100個/m L試驗菌,分別注入平皿中,立即傾注瓊脂培養基,待凝固后,置規定溫度培養24~72 h,逐日觀察結果。每株試驗菌平行制備2個平皿,按平皿法測定其菌數。
2.3.1.2 菌液組 取上述試驗菌液,測定每一菌株所加的試驗菌菌數。
2.3.1.3 供試液對照組 取供試液1m L加入平皿中,立即傾注瓊脂培養基,待凝固后,置規定溫度培養24~72 h,逐日觀察結果,測定供試品本底菌數。
2.3.1.4 稀釋劑對照組 以稀釋劑替代供試液,加入上述試驗菌菌液,置規定溫度下培養24~72 h,逐日觀察結果,按試驗組的供試液制備方法和菌落計數方法測定其菌數。
2.3.2 培養基稀釋法
2.3.2.1 試驗組 取供試液分別按0.5m L/皿、0.2m L/皿加入平皿后,加入上述50~100 cfu/m L的試驗菌,立即傾注2005版藥典規定的瓊脂培基,置規定溫度培養24~72 h,逐日觀察結果。
2.3.2.2 菌液組 同平皿法。
2.3.2.3 供試品對照組 除不加菌液外,同試驗組測定方法,置規定溫度培養24~72 h,逐日觀察結果,測定供試品本底菌數。
2.4 結果判斷
在3次獨立的平行試驗中,試驗組的菌回收率均應不低于70%。若試驗組的菌回收率均不低于70%,照該供試液制備方法和計數法測定供試品的細菌、霉菌和酵母菌數。
2.5 控制菌檢查方法的驗證
2.5.1 直接接種法
2.5.1.1 試驗組 取供試液各10m L,分別加入100m L營養肉湯和膽鹽乳糖(BL)培養基中,加入上述金黃色葡萄球菌、銅綠假單胞菌、大腸埃希菌菌液各1m L,按相應的金黃色葡萄球菌、銅綠假單胞菌、大腸埃希菌檢查法進行檢查。
2.5.1.2 陰性菌對照組 金黃色葡萄球菌、銅綠假單胞菌檢查,取上述大腸埃希菌菌液各1m L,分別加入100m L BL增菌液和營養肉湯培養基中;大腸埃希菌檢查,取上述金黃色葡萄球菌菌液1m L加入至100m L BL增菌液中,方法同試驗組。
2.5.2 培養基稀釋法
2.5.2.1 試驗組 取供試液10m L加入400m L營養肉湯培養基中,加入上述50~100cfu/m L的金黃色葡萄球菌1m L,置35℃培養24 h,按金黃色葡萄球菌檢查法檢查。
2.5.2.2 陰性菌對照組 取上述大腸埃希菌菌液1m L,加入400m L營養肉湯培養基中,方法同試驗組。
3 結果
結果見表1,表2。
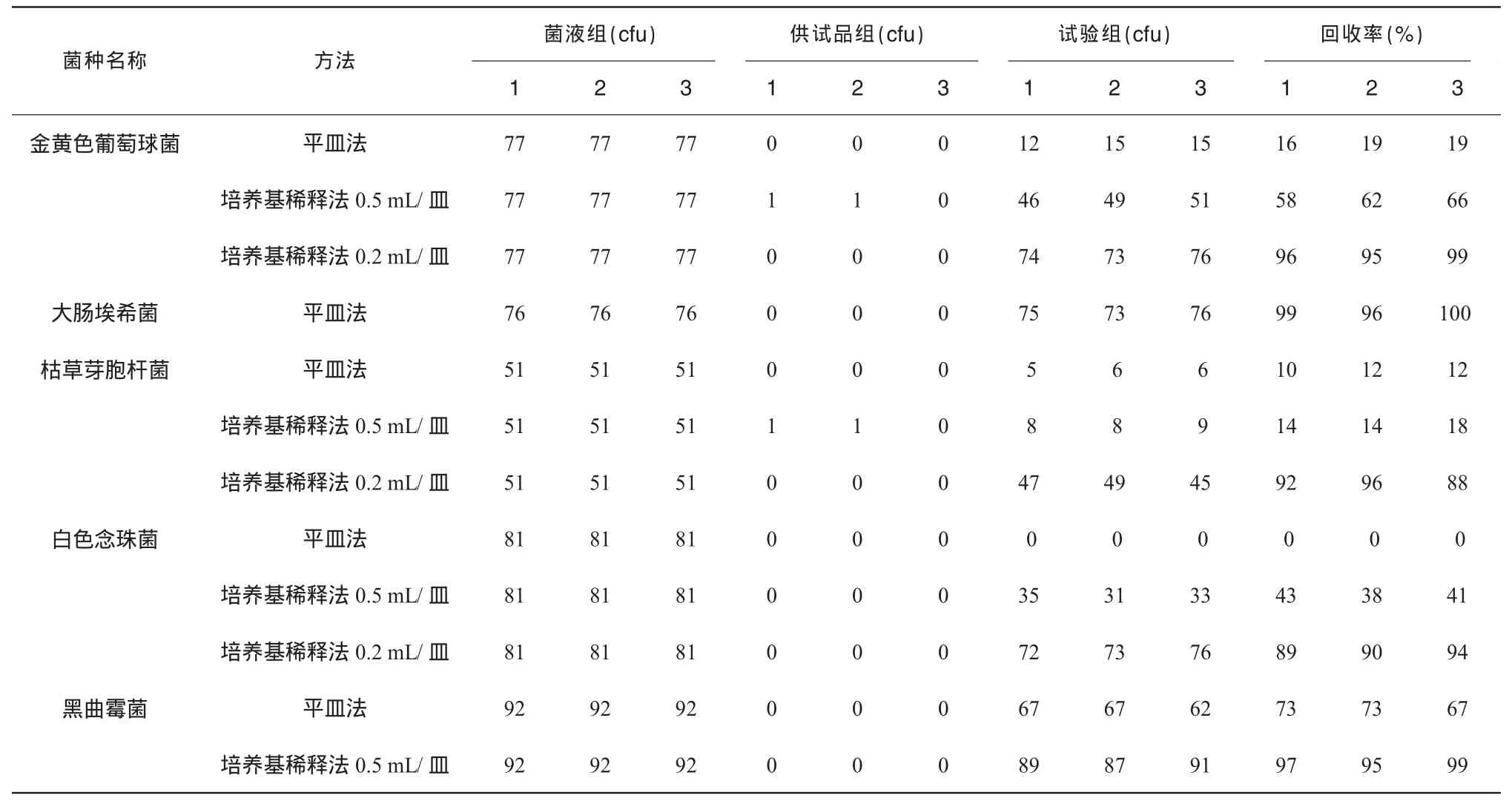
表1 回收率試驗結果
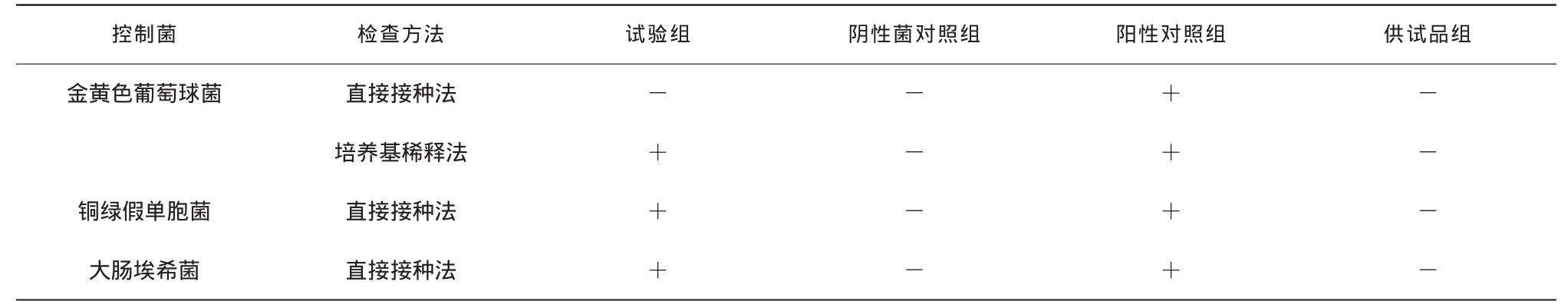
表2 控制菌試驗結果
4 討論
從驗證結果分析,本品具有一定的抑菌性,只是在相同的濃度下對不同細菌的抑制能力不同。從表1可以看出:細菌、霉菌和酵母菌數檢查方法采用平皿法時,對大腸埃希菌的回收率高于70%;采用培養基稀釋法(0.5 m L/皿)時,對黑曲霉的回收率能達到70%;采用培養基稀釋法(0.2 mL/皿)時,對白色念珠菌、金黃色葡萄球菌、桔草芽孢桿菌的回收率均能達到70%。從表2可以看出對控制菌金黃色葡萄球菌的檢查可采用培養基稀釋法,對銅綠假單胞菌、大腸埃希菌的檢查均可采用直接接種法。
驗證結果表明,本品細菌數、霉菌和酵母菌數均可采用培養基稀釋法(0.2 m L/皿)測定,對金黃色葡萄球菌的檢查可采用培養基稀釋法,對銅綠假單胞菌、大腸埃希菌的檢查均可采用直接接種法。
[1] 吳曉玲,李春蓉,陳引秀.清熱解毒藥微生物限度檢查方法學驗證的研究[J].中國藥事,2006,20(8):496-498.
[2] 國家藥典委員會.衛生部藥品標準(第7冊)[M].北京:人民衛生出版社,1993:111.
[3] 馬緒榮,蘇德模.藥品微生物學檢驗手冊[M].北京:科學出版社,2000:62.
[4] 國家藥典委員會.中華人民共和國藥典2005年版[M].北京:化學工業出版社,一部附錄:70.

