高效價凍干人用狂犬病疫苗暴露后免疫程序的研究
汝東宇,雷連成
(吉林大學畜牧獸醫學院微生物與免疫學實驗室,吉林長春130000)
狂犬病是由狂犬病病毒引起的人獸共患疾病。根據世界衛生組織的報告,全世界每年死于狂犬病的患者約55 000例,99%的病例發生在發展中國家,其中亞洲約占全球狂犬病發病總數的56%,非洲約占發病總數的44%。其中印度發病人數最多,位居第一,我國次之[1-2]。人用狂犬病疫苗的免疫分為暴露前免疫及暴露后免疫,各國推薦使用的人用狂犬病疫苗免疫程序也不相同[3-4]。世界衛生組織推薦的狂犬病毒暴露前免疫方案為0、7、21或28 d各免疫1劑量的疫苗,疫苗效力不低于2.5 IU/劑。暴露后免疫則有多種方案:埃森法(Essen regimen),第0、3、7、14和28天各肌肉注射1個劑量的疫苗(2.5 IU)。薩格勒布法(Zagreb regimen,2-1-1),第0天,分別在左和右上臂肌肉各注射1個劑量的疫苗,此后于第7和21天,各將1個劑量的疫苗注射至上臂,此種程序可免去2次就診和1劑疫苗。泰國紅十字會皮內注射法(Thai Red Cross Schedule“2-2-2-1-1”法),第0、3、7天,在2個不同的淋巴引流區(通常為左、右上臂)皮內注射1個劑量(0.1 mL)的疫苗,在第30和90天各注射0.1 mL疫苗。8部位皮內注射法(8-0-4-0-1-1),第0天,在8個不同部位皮內注射1個劑量疫苗(0.1 mL)。第7天,在每側上臂和每側大腿的外側皮內注射4個0.1 mL的疫苗,此后,第28和90天各注射0.1 mL劑量的疫苗。上述各國應用的人用狂犬病疫苗免疫方案均需接種4針次以上疫苗,全程免疫時間為21~90 d。在薩格勒布方案中,雖只接種4針,但在暴露后第3天沒有接種疫苗,而第3天對暴露后傷口的檢查是非常重要的。本文制備了一種高效價的凍干人用狂犬病疫苗,在高效價的基礎上,以減少狂犬病疫苗的免疫針次并縮短全程接種時間,對暴露后免疫程序進行了初步研究。
1 材料與方法
1.1 材料
1.1.1 實驗動物BALB/c小鼠,雌性,11~13 g;比格犬,5~6 kg(上海交通大學實驗動物中心,經狂犬病毒抗體檢測為陰性)。
1.1.2 病毒和細胞狂犬病街毒株CNX8601(由中國疾病預防控制中心病毒病預防控制所提供,1986年分離自中國寧夏病人腦組織);狂犬病街毒株BD06(由軍事醫學科學院軍事獸醫研究所流行病學研究室提供);狂犬病病毒株CVS11;BSR細胞(由武漢生物制品研究所基因工程室提供)。
1.1.3 試劑和標準品人用狂犬病毒免疫球蛋白(21.4 IU/mL),購自中國藥品生物制品檢定所;FITC標記的抗狂犬病毒核蛋白熒光抗體(Chemico);胎牛血清、胰蛋白酶、牛血清白蛋白、谷氨酰胺、DMEM培養基(GIBCO);丙酮(北京化工廠);依文思藍(Sigma)。
1.1.4 實驗樣品高效價凍干人用狂犬病疫苗(HPRabV),效價6.0 IU/劑,凍干人用狂犬病疫苗(RabV),效價3.1 IU/劑。
1.2 方法
1.2.1 以小鼠為試驗動物HPRabV暴露后保護效果評價BALB/c小鼠,11~13 g,隨機分成3組,每組32只;狂犬病街毒株CNX8601,毒力為4.2 LgLD50,病毒采用30 LD50劑量接種于小鼠咬肌,接種病毒后2 h,腹腔免疫0.5 mL實驗用疫苗。HPRabV(6.0 IU/劑)按0、3、14免疫程序免疫,RabV按0、3、7、14、28免疫程序免疫,設病毒對照組。于第5、7、10、14、18、22、26、33、37、44天于眼眶后靜脈采血,分離血清,采用RFFIT法測定血清中的中和抗體效價[5]。對HPRabV和RabV產生的中和抗體進行統計分析。每天觀察小鼠死亡情況,于第4天開始記錄死亡的小鼠,根據病毒對照組死亡率及疫苗組的生存率計算HPRabV和RabV的保護率,并對兩者進行評價。
1.2.2 以比格犬為實驗動物HPRabV暴露后保護效果評價實驗動物為比格犬,體重5~6 kg,隨機分成4組,每組10只,每只均咬肌接種200 000 LD50狂犬病街毒BD06株,前腿肌肉注射HPRabV(效價6.0 IU/劑)或RabV(效價3.1 IU/劑),并設病毒對照組。免疫程序:①HPRabV于0、3、10 d各接種1劑量的疫苗;②HPRabV于0、3、14 d各接種1劑量的疫苗;③RabV于0、3、7、14、28 d各接種1劑量的疫苗;④病毒對照組。各組分別在5、7、10、14、18、22、26、33、37、44 d用注射器頸部靜脈取血1.0 mL,37℃放置1 h,4℃12 h,5 000 r/min離心10 min,吸取上層血清,56℃滅活30 min,利用RFFIT法檢測血清中的中和抗體效價。觀察并記錄實驗動物死亡情況,計算疫苗保護率。
2 結果與分析
2.1 小鼠暴露狂犬病街毒后接種HPRabV和RabV產生的中和抗體比較
以小鼠為實驗動物的暴露后免疫保護實驗中和抗體測定結果顯示,HPRabV 0/3/14同RabV 0/3/7/14/28比較,經統計分析,P<0.05,2組之間相比有顯著性差異,HPRabV 0/3/14產生的中和抗體高于RabV 0/3/7/14/28組。

圖1 小鼠暴露街毒后接種HPRabV和RabV產生的中和抗體檢測結果Fig.1 RVNA responses induced by HPRabV(6.0 IU/dose)and RabV(3.1 IU/dose)in BALB/c post exposure
2.2 小鼠暴露狂犬病街毒后接種HPRabV及RabV的保護率
小鼠咬肌接種狂犬病街毒CNX8601,劑量為30LD50,結果病毒對照組死亡率為93.8%,HPRabV組疫苗保護率為56.2%,RabV組的保護率為40.6%,結果見圖2。
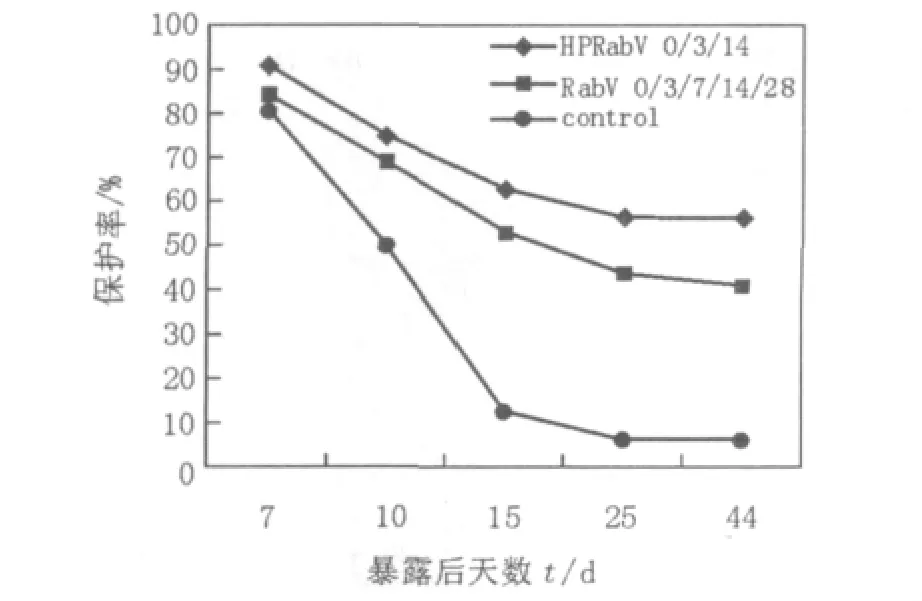
圖2 小鼠暴露狂犬病街毒后接種HPRabV及RabV的保護率Fig.2 Survival rate of BALB/c mice after post-exposure prophylaxis
2.3 以比格犬為實驗動物暴露后免疫中和抗體檢測結果
利用RFFIT法檢測血清中的中和抗體效價,計算各組中和抗體幾何平均效價(IU/mL),結果見圖3。經統計學分析,HPRabV 0/3/10組、HPRabV 0/3/14組與RabV 0/3/7/14/28組之間分別進行中和抗體水平比較,經t檢驗,P>0.05,不同免疫程序產生的中和抗體效價均無顯著性差異。免疫后10 d前HPRabV組中和抗體水平明顯高于RabV組。第10天抗體檢測,RabV組為23.8 IU/mL,HPRabV組為29.5 IU/mL和29.0 IU/mL,HPRabV組與RabV組分別進行t檢驗,P<0.001,有極顯著性差異。同時第5、7天HPRabV組中和抗體水平均高于RabV組。HPRabV能夠更早的刺激機體產生高效價的中和抗體。HPRabV 0/3/10組與HPRabV 0/3/14組間比較,兩者前期(0~18 d)中和抗體幾何平均效價基本持平,而后者在后期(22~56 d)中和抗體幾何平均效價均高于前者。

圖3 比格犬暴露后2種疫苗不同免疫程序產生的抗體效價比較Fig.3 RVNA responses induced by HPRabV and RabV in beagles post exposure prophy laxis
2.4 比格犬暴露狂犬病街毒后疫苗保護率結果
比格犬經200 000 LD50狂犬病毒街毒株BD06攻擊后,2種不同效價疫苗的保護率結果見圖4。由圖4可見,病毒對照組死亡率為100%,表明比格犬街毒暴露后保護率試驗結果成立。街毒攻擊后HPRabV 0/3/10免疫程序死亡3只實驗動物,疫苗保護率為70%;HPRabV 0/3/14免疫程序死亡2只實驗動物,疫苗保護率為80%;RabV 0/3/7/14/28免疫程序死亡3只實驗動物,疫苗保護率為70%。保護率試驗結果表明HPRabV 0/3/10組、HPRabV 0/3/14組與RabV 0/3/7/14/28組街毒攻擊均具有保護作用,HPRabV 0/3/14組疫苗保護率高于其他2組。

圖4 街毒攻擊后2種疫苗不同免疫程序免疫比格犬保護率結果Fig.4 Survival rate of beagles after post-exposure prophylaxis
3 討論
狂犬病疫苗主要應用于暴露后免疫,WHO推薦使用的是埃森法,在0、3、7、14、28 d各免疫1個劑量的人用狂犬病疫苗,疫苗的效力不低于2.5 IU/劑,本研究制備的高效價凍干人用狂犬病疫苗(6.0 IU/劑)目標是使暴露后免疫針次減少到3針,達到和現有疫苗同樣的保護效果。
以小鼠為實驗動物的暴露后免疫保護實驗中和抗體測定結果顯示,HPRabV 0/3/14同RabV 0/3/7/14/28比較,經統計分析,P<0.05,2組之間相比有顯著性差異,HPRabV 0/3/14產生的中和抗體高于RabV 0/3/7/14/28組。并且2組的最高值均出現在18~22 d,2組產生的中和抗體水平消長情況比較相似,是高效價凍干人用狂犬病疫苗比較理想的免疫程序。
在以比格犬為實驗動物的暴露后免疫程序研究中,以BD06株作為攻擊用毒株,病毒對照組死亡率為100%,表明本次比格犬街毒暴露后保護率試驗結果成立。HPRabV 0/3/10免疫程序疫苗保護率為70%;HPRabV 0/3/14免疫程序疫苗保護率為80%;RabV 0/3/7/14/28免疫程序疫苗保護率為70%。保護率試驗結果表明HPRabV 0/3/10組、HPRabV 0/3/14組與RabV 0/3/7/14/28組街毒攻擊均具有保護作用,HPRabV 0/3/14組疫苗保護率高于其他2組。
[1] 俞永新.狂犬病和狂犬病疫苗(第2版)[M].北京:中國醫藥科技出版社,2009.
[2] WHO Weekly Epidemiological Record[M].2007,49/50:425-435.
[3] Manning SE,Rupprecht CE,Fishbein D,et al.Human rabies prevention-United States,2008:recommendations of the Advisory Committee on Immunization Practices[J].MMWR Recomm Rep,2008,57(RR03):1-26,28.
[4] LeGuerrier P,Pilon PA,Deshaies D,et al.Pre-exposure rabies prophylaxis for the international traveler:a decision analysis[J].Vaccine,1996,14(2):167-176.
[5] F-X Meslin,MM Kaplan,H Koprowski.Laboratory techniques in rabies.4th Edn[M].World Health Organization publications,1996.

