電沉積金屬Ni涂層的高溫腐蝕性能
馬 莉,周科朝,李志友
電沉積金屬Ni涂層的高溫腐蝕性能
馬 莉,周科朝,李志友
(中南大學 粉末冶金國家重點實驗室,長沙 410083)
通過調控電沉積過程中的陰極電流密度制備具有不同晶粒尺寸和擇優取向的 Ni鍍層。采用透射電鏡(TEM)、掃描電鏡(SEM)、能譜儀(EDS)和X射線衍射儀(XRD)對高溫腐蝕前、后不同Ni鍍層進行檢測分析,對比研究不同Ni鍍層經過960 ℃的78.07%Na3AlF6-9.5%AlF3-5%CaF2(質量分數)熔鹽氣氛腐蝕后的結構、成分和形貌。結果表明:在高電流密度下易獲得晶粒細小,平均晶粒尺寸為120 nm,具有較強〈100〉擇優取向的Ni鍍層;而在低電流密度下所得的Ni鍍層晶粒較粗大,平均晶粒尺寸為925 nm,具有較弱的〈111〉擇優取向。在腐蝕氣氛下,低電流密度下所得的Ni鍍層在高溫腐蝕后有利于生成晶粒粗大、且具有完整“八面體”結構的NiAl2O4尖晶石相;而高電流密度下所得Ni鍍層表層腐蝕層的晶粒細小,且主要為NiO相。
電沉積;高溫腐蝕性能;鎳;晶粒尺寸;電流密度;擇優取向
金屬或合金的耐蝕性不僅取決于它的化學組成,還取決于其微觀結構。例如,Ni基高溫合金晶粒納米化后可以有效地促進氧化膜中連續、致密的 Al2O3和Cr2O3膜的快速生成[1?4]。此外,晶粒細化還可以改善材料在室溫下的耐點腐蝕性能[5]。除晶粒尺寸外,擇優取向對單質金屬材料及單晶材料耐氧化和耐腐蝕性能的影響也是不容忽略的。已有研究表明,在973 K空氣中氧化時,在Ni(111)晶面上氧化物的生長速率要比Ni(100)上氧化物的生長速率低一個數量級[6]。這是由于基體取向影響NiO生長過程中晶界特征分布,因此,基體取向控制高溫氧化或腐蝕過程中金屬離子、氧離子或其他離子的擴散速率和路徑[6]。
金屬Ni作為一種重要的金屬材料和合金元素,它的氧化和腐蝕性能一直頗受關注[6?12]。同時,為適應不同環境的需求,通過改變工藝參數來探索和了解Ni的氧化/腐蝕機理也備受重視。但在Ni的氧化研究中,多數研究集中在 Ni的純度[7]、氧化溫度[8]、爐內氣氛[9]和表面粗糙度[10]等方面,且對納米金屬Ni涂層耐蝕性的研究也多集中在室溫溶液環境[11?12]。而關于金屬 Ni涂層的晶粒大小和晶體擇優取向對其耐高溫氣氛腐蝕性能的影響的報道較少。
直流電沉積是制備金屬或合金涂層的常用方法之一。眾多研究表明,電沉積工藝參數與沉積層的結構和性能密切相關[13?14]。通過調節陰極電流密度和 pH值等工藝參數可以改變金屬或合金鍍層的晶粒大小和擇優取向等,進而改變材料性能[13?14]。
在鋁電解過程中,惰性陽極的金屬導桿的氣氛腐蝕行為也一直備受重視。本文作者通過調控電流密度來制備具有不同晶粒尺寸和擇優取向的Ni涂層,并將該涂層置于 960 ℃鋁電解的熔鹽介質氣氛(78.07%Na3AlF6- 9.5%AlF3-5%CaF2,質量分數)中進行12 h的腐蝕實驗,通過研究腐蝕層的結構、成分和形貌來討論分析上述因素對抗高溫腐蝕性能的影響。
1 實驗
本實驗采用直流電沉積方法制備Ni涂層,電解液組成為 NiSO4·6H2O(250 g/L)、NiCl2·6H2O(45 g/L)、H3BO3(35 g/L),鍍液pH值為4.5,沉積溫度為45 ℃,電流密度分別為1 A/dm2和15 A/dm2。所用試劑均為分析純,溶液用蒸餾水配制。陽極為加拿大INCO公司生產的電解鎳,其化學組分見表 1。在鎳基體上進行電沉積,工作面積為3 cm×3 cm。電沉積前基體依次經過除油,稀硫酸腐蝕,水和蒸餾水清洗。在電沉積過程中,鍍液采用磁力器攪拌,攪拌速度恒定。調整電鍍時間,使鍍層厚度控制在為40 μm左右。腐蝕實驗在大氣和熔鹽氣氛的雙重作用下進行,溫度為960 ℃,熔鹽介質為78.07%Na3AlF6-9.5%AlF3-5%CaF2(質量分數),腐蝕時間為12 h,加熱爐為普通馬弗爐。
采用線切割設備將沉積層切成小塊,經過磨制、離子減薄制成薄膜樣品,在H?800型透射電鏡(TEM)下觀察其微觀結構,并通過統計500個晶粒的粒徑繪制沉積層的晶粒尺寸分布圖;采用JSM?5600LV型掃描電子顯微鏡(SEM/EDS)分析鍍層腐蝕前、后腐蝕層的截面形貌和元素分布;采用 RIGAKU/MAX?3A型X射線衍射分析儀(XRD)考察鍍層的晶體結構和腐蝕后腐蝕層的物相組成,實驗所用的X射線為CuKα輻射(λCu-K=0.154 nm,步長為0.02°)。根據XRD檢測數據計算沉積層的織構,以晶面(hkl)的織構系數TC來表征晶面擇優程度[15],如式(1)所示。
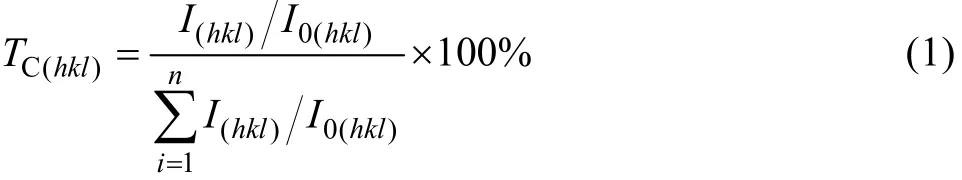
式中:I(hkl)和 I0(hkl)分別表示沉積層試樣和標準鎳粉末的(hkl)晶面的衍射線強度;n為衍射峰個數,為避免平行面的影響,本研究中n取值為3,即取(111)、(200)和(220)晶面進行計算。當各衍射面的 TC值相同時,晶面取向是無序的。如果某個(hkl)面的TC值大于平均值(33.3%)時,則該晶面呈擇優取向。TC值越大,說明擇優取向程度越高。
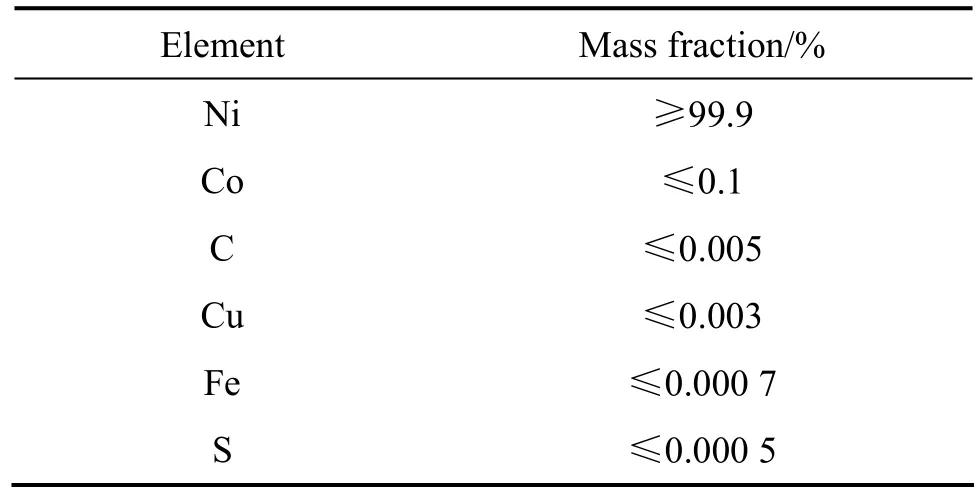
表1 陽極用IncoNi板的化學組分Table 1 Chemical composition of Inco Ni plate used as anode
2 結果與分析
2.1 不同電流密度下制備的Ni鍍層的XRD和TEM分析
圖1所示為不同電流密度下電沉積所得的厚度約為50 μm Ni鍍層的XRD譜。從圖1可以看出,在低電流密度(J=1 A/dm2)下沉積的鍍層的晶粒具有〈111〉擇優取向;而在高電流密度(J=15 A/dm2)下沉積的鍍層的晶粒具有〈100〉擇優取向。
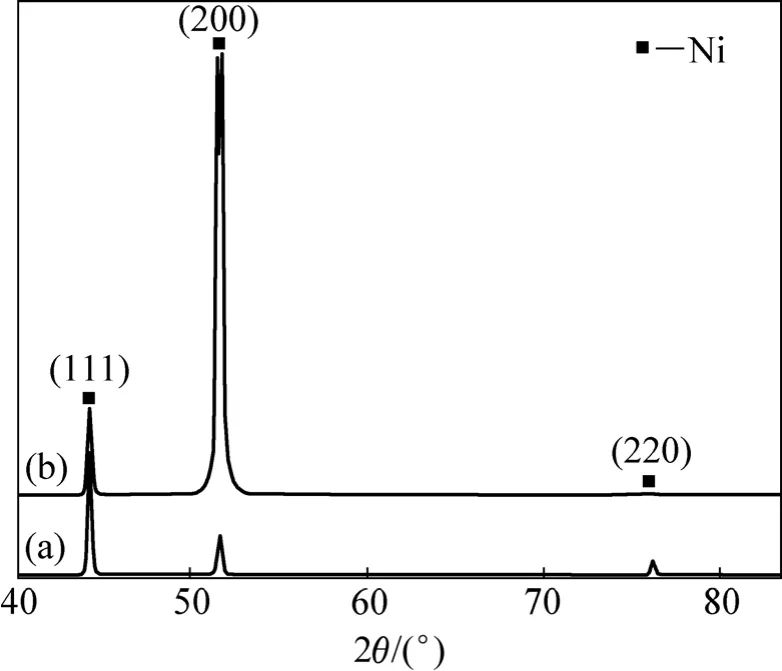
圖1 Ni鍍層的XRD譜Fig.1 XRD patterns of Ni coatings: (a) J=1 A/dm2; (b) J=15 A/dm2
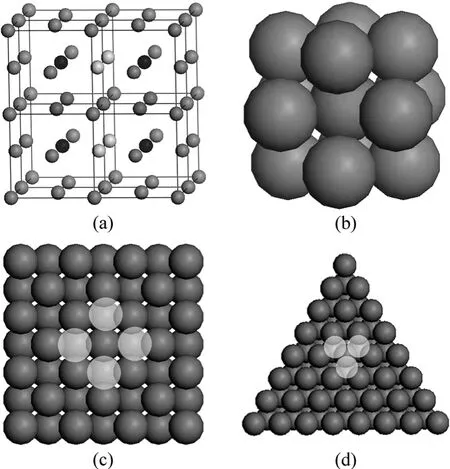
圖2 Ni的原子結構Fig.2 Atomic structure of Ni: (a) Eight Ni single-cells (100);(b) Nearest neighbor atomic structure of Ni; (c) Ni(100); (d)Ni(111)
Ni是典型的具有面心立方結構的金屬(見圖2(a)),Ni原子的排列具有高度的對稱性,每個Ni原子由12個最近鄰Ni包圍(見圖2(b)),且中心原子與最近鄰原子之間距離相等,均為2a / 2,a為布拉菲點陣常數。在此,假定每個Ni原子和周圍12個Ni原子之間的相互作用遠強于與其他原子之間的相互作用。從圖 2(c)和(d)可以看出,Ni(100) 表面每個Ni原子被最近鄰8個 Ni原子“固定”,有 4個最近鄰原子位“懸掛”;而Ni(111) 表面每個Ni原子被最近鄰的9個Ni原子“固定”,只有3個最近鄰原子位“懸掛”。因此,Ni(111) 面Ni原子具有更高的穩定性。
此外,亦可根據fcc的表面自由能公式(2)[16],計算的Ni(100)、Ni(110)與Ni(111)的表面自由能之比為γ100:γ110:γ111=1:1/2:1/3,說明Ni(111)的能量最低,為最穩定晶面。

式中:Εb表示相鄰兩個原子之間的鍵能;d0表示鍵長;h、k、l 表示晶面指數。
當電流密度比較小時,晶體生長以平衡或近似平衡生長,晶體生長比較緩慢、有序。從熱力學觀點來看,當晶粒的每個表面均為{111}時,可以最大限度地滿足晶體生長的Gibbs條件,即滿足總表面自由能最小。由式(2)可知,Ni的{111}面具有最低表面能,由8個{111}面圍成的正八面體結構為 Ni晶體的平衡形狀,當晶粒以平衡或近似平衡生長時,晶體趨向于向正八面體結構生長。
當增大電流密度時,晶體生長速度加快,晶體生長不再遵循能量最低原則,將可能以最快堆垛形式生長[17?18]。由于Ni的{100}晶面的原子密度較小、面間距較小、面與面之間的吸引力較強,〈100〉成為另一個晶體優先生長的方向。
圖3所示為兩種不同結構和晶粒尺寸的純Ni鍍層的 TEM 明場像和選區電子衍射花樣(SAED)譜。圖4所示為其相對應的晶粒尺寸分布圖。從圖3可以明顯地看到,當J=1 A/dm2時,所得鍍層晶粒尺寸粗大,晶粒尺寸分布范圍為0.2~2.0 μm,其中尺寸在0.6~1.2μm的晶粒占55%以上(見圖3(a));當J=15 A/dm2時,所得鍍層的晶粒尺寸相對細小,晶粒尺寸分布范圍為10~300 nm,其中尺寸在40~200 nm的晶粒占70%以上。通過分別對500個晶粒進行統計并計算出它們的平均晶粒尺寸分別為975 nm和120 nm。這主要是由于低電流密度下晶體生長比較緩慢,故晶粒粗大;而高電流密度下晶粒生長迅速,故晶粒細小。
另外,由于圖3(c)和(d)的SAED譜是由相同直徑的選區光闌得到的,其中,圖3(c)中的SAED譜為單晶Ni的衍射斑,而圖3(d)中的SAED譜為多晶Ni的近同心圓環。這一實驗結果也同樣證明低電流密度下所得鍍層的晶粒較粗大,而高電流密度下所得鍍層的晶粒較細小。
此外,由于具有織構樣品的倒易點陣可以用單晶的點陣繞織構軸旋轉而得,其中的SAED是一層同心圓。當織構軸與電子束入射方向成一傾角時,原來衍射圖中的圓環被分割成一些孤段。圖3(d)樣品的衍射環被分割成一些孤段,亦可說明圖3(b)樣品的晶粒具有一定的擇優取向,這一點也與 XRD分析結果一致。

圖3 Ni鍍層的TEM明場像和其相應的選取電子衍射圖譜(SAED)Fig.3 TEM bright-field images of Ni coatings (a, b) and corresponding SEAD patterns (c, d): (a), (c) 1 A/dm2; (b), (d) 15 A/dm2

圖4 Ni鍍層的晶粒尺寸分布Fig.4 Grain size distribution of Ni coatings: (a) 1 A/dm2; (b) 15 A/dm2
表2所列為不同電流密度下所得Ni鍍層的XRD譜和TEM數據分析。從表2中可以明顯地看出,在低電流密度下制備的 Ni鍍層,平均晶粒尺寸為 975 nm,具有較弱的〈111〉擇優取向,擇優取向度為38.7%;而在高電流密度下制備的 Ni鍍層的平均晶粒尺寸為120 nm,具有較強的〈100〉擇優取向,擇優取向度為91.5%。
2.2 960 ℃氣氛腐蝕12 h后Ni鍍層的結構
圖5所示為不同電流密度下電沉積所得Ni鍍層在960 ℃的 78.07%Na3AlF6-9.5%AlF3-5%CaF2熔鹽氣氛下腐蝕12 h后的XRD譜。從圖5可以看出,兩種Ni鍍層經腐蝕后表面除有NiO外,均有NiAl2O4生成。但NiO與NiAl2O4峰的峰強和峰數存在明顯差異。高電流密度所得樣品的 NiAl2O4的特征峰的數量和強度少于低電流密度所得樣品的。這可能是由于不同電流密度所得鍍層在高溫氣氛腐蝕后腐蝕層中 NiO、NiAl2O4的含量及其擇優取向不同所致。在標準 PDF卡片中,NiO(111)峰的2θ角為37.248°,NiAl2O4(311)峰所對應的 2θ角為 37.009°,二者只相差 0.239°。A峰所對應的 2θ值均位于 36.6°~37.9°,因此,A 峰是NiO(111)峰與 NiAl2O4(311)峰共同作用的體現,故這里無法通過峰強度的方法計算NiO與NiAl2O4各個晶面的擇優取向度。但除 A峰以外,圖 5(a)中I NiAl2O4(220) IA , I NiAl2O4(400) IA , I NiAl2O4(422) IA ,I NiAl2O4(511) IA 和 I NiAl2O4(440) IA等峰強相對值均高于圖 5(b)的,說明低電流密度下獲得的 Ni鍍層在腐蝕后 NiAl2O4含量相對較高。此外,圖 5(a)中INiO(200)IA的強度相對值明顯大于圖 5(b)中INiO(200)IA的相對強度值,所以低電流密度下獲得的Ni鍍層經腐蝕后,腐蝕產物中 NiO存在明顯的〈100〉擇優取向。
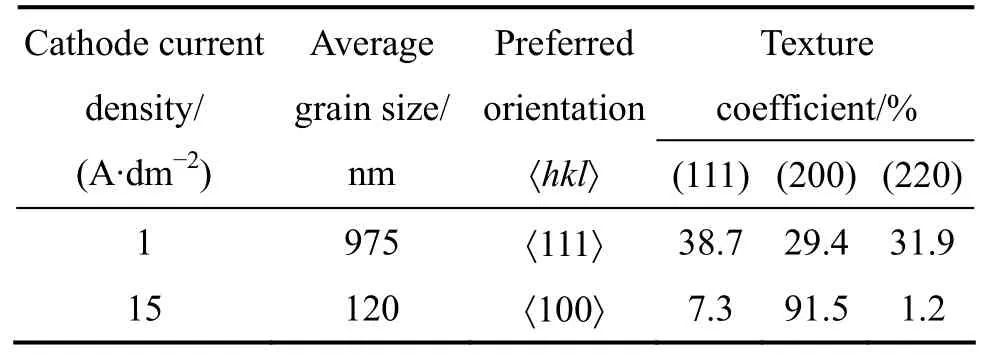
表2 不同電流密度下制備的Ni鍍層的XRD和TEM數據分析Table 2 XRD and TEM data analysis of Ni coatings prepared under different current densities
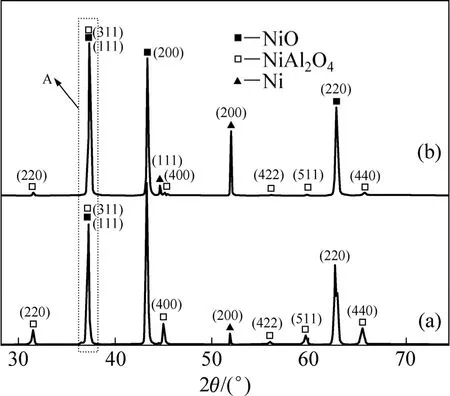
圖5 Ni鍍層在960 ℃的78.07%Na3AlF6-9.5%AlF3-5%CaF2氣氛中腐蝕12 h后的XRD譜Fig.5 XRD patterns of Ni coatings electrodeposited with different current densities and then subjected to hot corrosion in environment of 78.07%Na3AlF6-9.5%AlF3-5%CaF2 at 960 ℃for 12 h: (a) 1 A/dm2; (b) 15 A/dm2
2.3 960 ℃腐蝕12 h后鍍層的表面形貌
圖6所示為不同電流密度下電沉積所得Ni鍍層經大氣與熔鹽氣氛混合氣氛腐蝕后的表面形貌。從圖 6可以看出,在低電流密度下制得的Ni鍍層經腐蝕后,表層腐蝕層局部破裂(見圖6(a)),呈現“包狀”結構,且晶粒較粗大,晶粒尺寸為1~4 μm,晶形完整,每個晶粒具有明顯的“正八面體”結構(見圖6(b));而內腐蝕層晶粒相對較小(見圖6(c)),這可能是腐蝕過程中內層的腐蝕氣氛需要通過晶界和缺陷由表面擴散遷移到內層,故內層的腐蝕氣體濃度要小于表面的濃度。而在高電流密度下制得的Ni鍍層經腐蝕后,表層腐蝕層完整,無剝落,且表面氧化膜較平整、晶粒非常細小,晶界豐富(見圖 6(d)和(e))。由于低電流密度下所得的Ni鍍層晶粒粗大,晶界較少,腐蝕產物形核密度較小,腐蝕物晶粒可自由生長,導致腐蝕層晶粒粗大。而高電流密度下所得Ni鍍層本身晶粒細小,且均為納米尺度,晶界豐富,而晶界是易氧化和腐蝕的區域,氧化腐蝕速度快,單位面積腐蝕產物形核數量多,故腐蝕產物晶粒細小。
同時,根據表3的EDS分析可知,大氣腐蝕后的鍍層表面均沒有發現 F元素及其化合物。其中 B區Al元素含量較多,C區Al元素含量相對B區有所減少;Ε區Al元素含量最少,Ni和O元素含量較多。
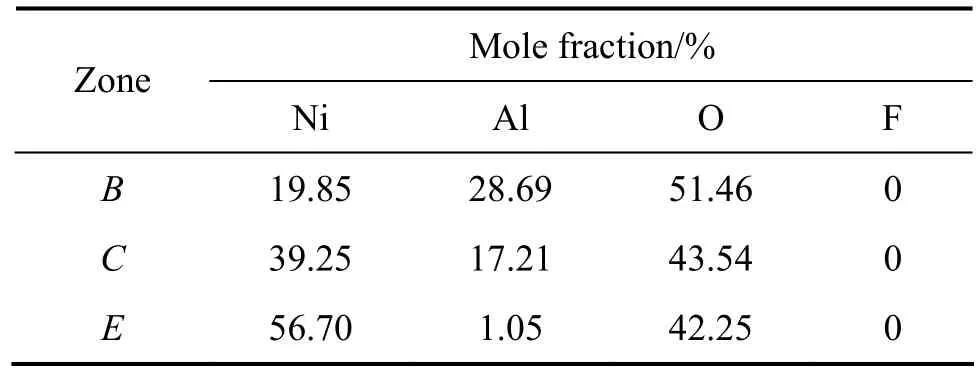
表3 圖6中各微區的元素分析Table 3 Micro-area element analysis in Fig.6
2.4 960 ℃腐蝕12 h后樣品的截面形貌
圖7所示為不同電流密度下電沉積所得Ni鍍層經熔鹽氣氛腐蝕后的SEM像。由圖7可看出,不同電流密度下電沉積所得 Ni經熔鹽氣氛腐蝕后所得腐蝕層的厚度相差不大。在低電流密度下所得Ni鍍層經腐蝕后,在腐蝕層/氣體界面以及腐蝕層/金屬界面出現了兩條顏色較深的帶(見圖 7(a)和(b))。在高電流密度下所得Ni鍍層經腐蝕后,其在腐蝕層/金屬界面出現了一條顏色較深的帶(見圖7(c)和(d))。

圖6 Ni鍍層在 960 ℃的 78.07%Na3AlF6-9.5%AlF3-5%CaF2氣氛中腐蝕12 h后的表面形貌Fig.6 Surface photographs of Ni coatings subjected to hot corrosion in environment of 78.07%Na3AlF6-9.5%AlF3-5%CaF2 at 960 ℃for 12 h: (a) 1 A/dm2; (b) Enlarged graphs of zone B; (c) Enlarged graphs of zone C; (d) 15 A/dm2; (e) Enlarge graph of zone Ε
圖8 所示為不同電流密度下所制備的Ni鍍層在960 ℃熔鹽氣氛下腐蝕 12 h后所得腐蝕層的截面的EDS分布。從圖8(a)可以清楚地看出,在腐蝕層/氣體界面以及腐蝕層/金屬界面出現的兩條顏色較深的帶為Al元素的富集區域,腐蝕層/氣體界面處富集Al元素在圖8(a)的EDS表面能譜分析結果中進一步得到證實(見表 3)。而由圖 8(b)可以看出,在腐蝕層/金屬界面只出現了一條較深的帶,該帶為Al的富集區域。從圖 8(c)的 EDS表面能譜分析中可知,該樣品表面的Al含量較少(見表3),然而根據圖5的XRD分析結果有表面腐蝕產物含有有NiO和NiAl2O4兩相,故結合圖5,表3和圖8的檢測結果可推測該Al元素的富集區域主要為NiAl2O4相。

圖7 Ni鍍層在960 ℃的78.07%Na3AlF6-9.5%AlF3-5%CaF2氣氛下腐蝕12 h后氧化膜截面的SEM背散射像Fig.7 SEM back scattered images of oxides formed on Ni coatings subjected to hot corrosion in atmosphere of 78.07%Na3AlF6-9.5%AlF3-5%CaF2 at 960 ℃ for 12 h: (a) 1 A/dm2; (b) Enlarged graph of Fig.7(a); (c) 15 A/dm2 ; (d) Enlarged graph of Fig.7(c)
此外,從圖7和8還可以看出,在不同電流密度下電沉積所得 Ni經熔鹽氣氛腐蝕后所得腐蝕層的平均厚度在40 μm左右,可能均為Ni涂層本身的厚度(40μm左右)。導致腐蝕層厚度相差不大的原因可能是:在涂層/金屬基體界面由于應力產生裂紋,使得腐蝕介質、O2通過裂紋等區域擴散進入,并與暴露在腐蝕氣氛和大氣中的金屬Ni基體發生反應。根據表4中1 200 K時的反應標準自由能可以看出,金屬Ni與O2和AlF3同時作用生成 Al2O3的吉布斯自由能為?106.09 kJ/mol,且金屬Ni或NiO形成NiAl2O4的吉布斯自由能分別為?150.05 kJ/mol和?16.18 kJ/mol,3個反應的吉布斯自由能均為負值,說明反應趨勢較大,即易在基體/涂層界面處生成一層 NiAl2O4膜。由于 NiAl2O4尖晶石本身結構致密,對Ni2+和O原子的進一步擴散起到了阻礙作用。因此,經腐蝕后兩組樣品的腐蝕層厚度相差不大。
在進行高溫氣氛腐蝕實驗時,在升溫過程中,在溫度未達到熔鹽的熔融溫度時,沒有腐蝕介質揮發,Ni鍍層表面暴露在富含氧氣的大氣環境中,隨著溫度的不斷升高,表面Ni原子將被氧化生成NiO。由于不同電流密度下所得鍍層晶粒尺寸存在明顯差異,在溫度由室溫升至熔鹽熔融溫度的這段時間內,Ni鍍層表面生成的NiO的氧化速率也存在很大差異。通常情況下,在氧化初期,氧化膜生長主要是沿晶界進行的短路擴散。在高電流密度下所得Ni鍍層的晶粒細小,平均晶粒尺寸近納米級,比表面能較大,活性較高,且富含大量晶界,在氧化初期,成膜離子或原子可通過大量的晶界迅速擴散遷移,故氧化速率較快,在較短的時間內金屬Ni外層就會被一層較致密的NiO膜包裹;而在低電流密度下所得Ni鍍層,晶粒較粗大,平均晶粒尺寸近微米級,晶界相對較少,成膜離子或原子通過晶界擴散的路徑有所減少,氧化速率較慢,故在短時間內只有極少量的NiO生成。
為了進一步說明晶粒尺寸對氧化速率的影響,這里引用Hart模型[19]說明:

式中:Db和Dgb分別為體擴散系數和晶界擴散系數;f為通過晶界擴散系數所占的分數。假定Ni鍍層的晶粒為柱狀晶,對于柱狀晶粒,f=2δ/d,其中 δ是晶界寬度,通常為10?7cm[20];d為柱狀晶直徑。當晶粒尺寸由微米級降到納米級時,沿晶界擴散所占的比例將大幅度增加,而晶界擴散系數遠大于體擴散系數(通常Dgb/Db=104~106)[20],高電流密度下所得Ni鍍層的平均晶粒尺寸為120 nm,因此,在氧化初期,成膜離子或原子的有效擴散系數將會大幅度增大。此外,對于純金屬Ni來說,在973 K空氣氧化中,(111)晶面的氧化速率比(100)晶面低一個數量級[6]。故可能上述兩個原因的同時作用使得在腐蝕介質揮發前的升溫過程中,在空氣的作用下,低電流密度下制得的Ni鍍層氧化速率較慢,而在高電流密度下制得的鍍層氧化速率較快。

圖8 Ni鍍層在960 ℃的78.07%Na3AlF6-9.5%AlF3-5%CaF2氣氛下腐蝕12 h后氧化膜的截面背散射圖和EDS面分布圖Fig.8 BSE images (a, b) and EDS mappings (b~h) along cross-section of oxides formed on Ni coatings subjected to hot corrosion in environment of 78.07%Na3AlF6-9.5%AlF3-5%CaF2 at 960 ℃ for 12 h: (a), (c), (e), (g) 1 A/dm2; (b), (d), (f), (h) 15 A/dm2
在腐蝕介質揮發前,由于低電流密度下所獲得Ni鍍層氧化速率較慢,在短時間內外層均主要是晶界處存在少量氧化,晶內幾乎未被氧化。根據表4中式(3)的標準吉布斯自由能ΔGΘ<0可知,低電流密度下所獲得Ni鍍層在高溫下與O2和腐蝕介質AlF3共同作用后,外表面有Al2O3生成。同時,根據表4中式(5)可知,Ni氧化形成NiO和NiAl2O4的標準吉布斯自由能分別為?133.19 kJ/mol和?150.05 kJ/mol,二者均為負值,說明反應的趨勢較大,即該表層易于生成NiAl2O4相。
而在高電流密度下所獲得的 Ni鍍層經腐蝕后表面幾乎沒有 NiAl2O4的生成。可能的原因是:腐蝕初期,在大氣的作用下,具有近納米晶粒尺度、且具有〈100〉高擇優取向的 Ni鍍層的表面氧化速率較快,在很短的時間內便會被一層生成的NiO膜包裹。由表4中式(2)可知,在1 200 K時,NiO與AlF3相互作用生成 Al2O3的標準吉布斯自由能為 27.10 kJ/mol,即ΔGΘ>0,說明表層 NiO 與 AlF3相互作用無法生成NiAl2O4,故在大氣氣氛和腐蝕氣氛的共同作用下,在腐蝕層/氣體界面幾乎沒有NiAl2O4的生成。
但關于 Ni晶粒尺寸和晶粒擇優取向對氧化膜中NiO和NiAl2O4各晶面擇優生長的影響目前還未能給出具體分析和解釋,這一部分工作還有待進一步研究。
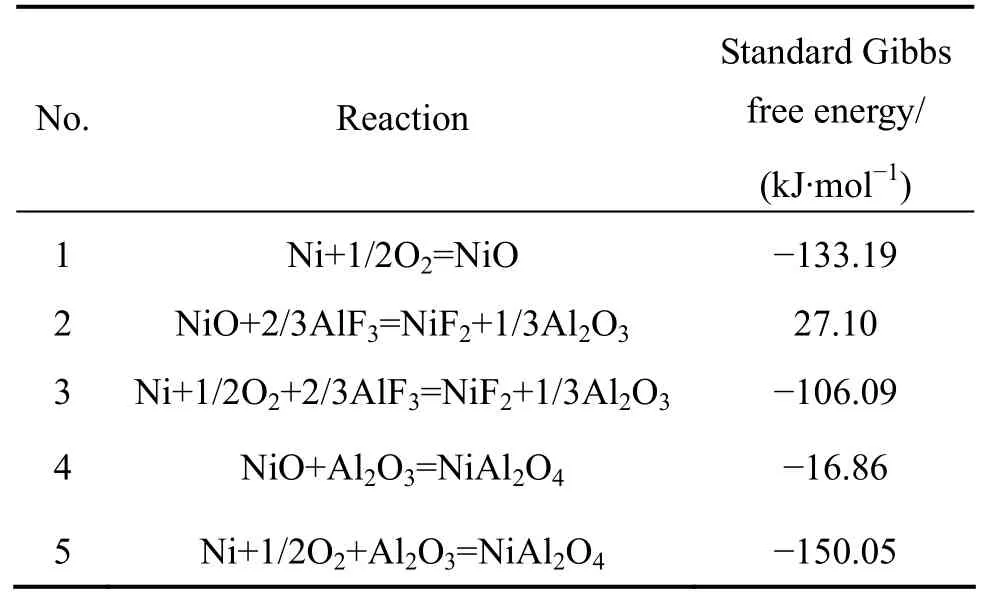
表4 1 200 K時的反應標準吉布斯自由能Table 4 Standard Gibbs free energy of reactions at 1 200 K
3 結論
1) 采用直流電沉積法,在低電流密度下制備的Ni鍍層晶粒尺寸粗大,平均晶粒尺寸為945 nm,晶粒具有輕微的〈111〉擇優取向,取向度為 38.7%;而在高電流密度下制備的Ni鍍層晶粒尺寸細小,平均晶粒尺寸為120 nm,晶粒具有強烈的〈100〉擇優取向,取向度為91.5%。
2) 在960 ℃時,低電流密度制備的Ni鍍層在大氣氣氛和腐蝕氣氛的雙重作用下表層更有利于生成結構致密的 NiAl2O4尖晶石相,且腐蝕層的晶粒粗大;而在高電流密度制備的Ni鍍層表層有大量的NiO和極少量 NiAl2O4尖晶石的生成,且其腐蝕層的晶粒細小。
REFERENCES
[1] YANG X, PENG X, WANG F. Hot corrosion of a novel electrodeposited Ni-6Cr-7Al nanocomposite under molten(0.9Na, 0.1K)2SO4at 900 ℃[J]. Scripta Materialia, 2007, 56:891?894.
[2] RAHMAN A, JAYAGANTHAN R, PRAKASH S, CHAWLA V, CHANDRA R. High temperature oxidation behavior of nanostructured Ni-Al coatings on superalloy[J]. Journal of Alloys and Compounds, 2009, 472: 478?483.
[3] MAHESH R A, JAYAGANTHAN R, PRAKASH S, CHAWLA V, CHANDRA R. High temperature cyclic oxidation behavior of magnetron sputtered Ni-Al thin films on Ni- and Fe-based superalloys[J]. Materials Chemistry and Physics, 2009, 114:629?635.
[4] SINGH R R K, GUPTA R K. Oxidation resistance of nanocrystalline vis-à-vis microcrystalline Fe-Cr alloys[J].Corrosion Science, 2009, 51: 316?321.
[5] YE W, LI Y, WANG F H. Effects of nanocrystallization on the corrosion behavior of 309 stainless steel[J]. Electrochim Acta,2006, 51: 4426?4432.
[6] CZERWINSKI F, SMELTZER W W. Microscopy of Oxidation-2[M]. 2nd ed. NEWCOMB S B, BENNETT M J.London: The Institute of Materials, 1993: 128.
[7] HUNTZ A M, ANDRIEUX M, MOLINS R. Relation between the oxidation mechanism of nickel, the microstructure and mechanical resistance of NiO films and the nickel purity Ⅰ.Oxidation mechanism and microstructure of NiO films[J].Materials Science and Engineering A, 2006, 415: 21?32.
[8] PERALDI R, MONCEAU D, PIERAGGI B. Correlations between growth kinetics and microstructure for scales formed by high-temperature oxidation of pure nickel I. Morphologies and microstructures[J]. Oxidation of Metals, 2002, 58: 249?273.
[9] AHN J H, KIM B J, KIM J G, KIM H J,HONG G W, LEE H G,YOO J M, RRADEEP H. Effects of oxidation conditions on the microstructure and texture of NiO in a cube-textured polycrystalline nickel substrate[J]. Physica C, 2006, 445/448:620?624.
[10] HUNTZ A M, LEFEVRE B, CASSINO F. Roughness and oxidation: application to NiO growth on Ni at 800 ℃[J].Materials Science and Engineering A, 2000, 290: 190?197.
[11] RAFAGHA R, LANGER R, EL-SHERIK A M, ERB U,PALUMBO G, AUST K T. The corrosion behaviour of nanocrystalline nickel[J]. Scripta Metall, 1991, 25: 2867?2872.
[12] MISHRA R, BALASUBRAMANIAM R. Effect of nanocrystalline grain size on the electrochemical and corrosion behavior of nickel[J]. Corrosion Science, 2004, 46: 3019?3029.
[13] THIEMIG D, LANGE R, BUND A. Influence of pulse plating parameters on the electrocodeposition of matrix metal nanocomposites[J]. Electrochimica Acta, 2007, 52: 7362?7371.
[14] BUND A, THIEMIG D. Influence of bath composition and pH on the electrocodeposition of alumina nanoparticles and nickel[J].Surface & Coatings Technology, 2007, 201: 7092?7099.
[15] YU Z, FLODSTROM A. Orientation of (1×1)-surface free energies of crystals[J]. Surface Science, 1998, 401: 236?247.
[16] CHEN L, WANG L P, ZENG Z X, XU T. Influence of pulse frequency on the microstructure and wear resistance of electrodeposited Ni-Al2O3composite coatings[J]. Surface &Coatings Technology, 2006, 201: 599?605.
[17] 余志明, 魏秋平, 葉 浚, FLODRSTR?M A. 正二十面體金剛石的形成及其計算機模擬[J]. 新型炭材料, 2009, 23(6/7):1676?1682.YU Zhi-ming, WEI Qiu-ping, YE Jun, FLODRSTR?M A.Formation of an icosahedral diamond crystal and its computer simulation[J]. New Carbon Materials, 2009, 23(6/7):1676?1682.
[18] HIBBARD G D, PALUMBO G, AUST K T, ERB U. Nanoscale combined reactions: non-equilibrium α-Co formation in nanocrystalline e-Co by abnormal grain growth[J]. Philosophical Magazine, 2006, 86(2): 125?139.
[19] HART E W. On the role of dislocations in bulk diffusion[J].Acta Metall, 1957, 5: 597.
[20] ATKINSON A. Diffusion along grain boundaries and dislocations in oxides, alkali halides and carbides[J]. Solid State Ionics, 1984, 12: 309?320.
Hot corrosion performance of Ni electrodeposited coatings
MA Li, ZHOU Ke-chao, LI Zhi-you
(State Key Laboratory of Powder Metallurgy, Central South University, Changsha 410083, China)
Ni coatings with different grain sizes, preferred orientation and impurity element contents can be electrodeposited by regulating cathode current density. Using transmission electron microscopy(TEM), scanning electron microscopy (SEM), energy dispersive spectroscopy (EDS) and X-ray diffractometry(XRD), the oxide film structures,composition and morphology of Ni coatings before and after being corroded in corrosive atmosphere of 78.07%Na3AlF6-9.5%AlF3-5%CaF2(mass fraction, %) were investigated comparatively at 960 ℃. The results show that Ni coatings with smaller grains and a strong 〈100〉 preferred orientation are easily obtained under higher current density.While Ni coatings deposited under lower current density have coarser grains and a weak 〈111〉 preferred orientation. In the corrosive atmosphere, Ni coating prepared with a lower current density is benefit to the formation of dense NiAl2O4spinel phase on the surface layer, while NiO is the major phase on the surface of oxide film after the corroding Ni coating prepared with a high current density.
electrodeposition; hot corrosive performance; nickel; grain size; current density; preferred orientation
TG133.4;TG174.2
A
1004-0609(2010)12-2377-10
國家重點基礎研究發展計劃資助項目(2005CB623703);國家高技術研究發展計劃資助項目(2008AA030501);國家自然科學基金創新團隊資助項目(50721003);湖南省博士研究生創新基金資助項目(CX2009B032);中南大學貴重儀器開放共享基金資助項目(ZKJ2009024);中南大學優秀博士論文扶持基金資助項目(2009ybfz02)
2009-12-28;
2010-03-05
周科朝,教授,博士;電話:0731-88836264;E-mail:marycsupm@gmail.com
(編輯 李艷紅)

