p H沖擊對同步厭氧生物脫氮除硫反應器性能的影響
蔡靖, 鄭平
(浙江大學環境與資源學院,浙江杭州 310029)
p H沖擊對同步厭氧生物脫氮除硫反應器性能的影響
蔡靖, 鄭平*
(浙江大學環境與資源學院,浙江杭州 310029)
研究了p H沖擊對同步厭氧生物脫氮除硫反應器性能的影響。同步厭氧生物脫氮除硫體系的酸堿緩沖容量不大,反應液p H值對進水p H沖擊的響應較為靈敏。實際響應曲線不同于單純水力停留時間分布所致的理論響應曲線,反應液p H值變化是水力傳遞等物理作用、基質解離等化學作用以及細菌代謝等生物作用的綜合效應。p H值沖擊對硫化物氧化過程有一定的影響,但可恢復。反應液p H值較高時,出水硫酸鹽質量濃度較低,高p H值可抑制硫化物向硫酸鹽的完全氧化。硝酸鹽還原對p H沖擊較為敏感,但出水硝酸鹽質量濃度對p H沖擊的響應曲線具有滯后性,可能與硝酸鹽運輸至細胞體內的運輸方式有關。
厭氧脫氮除硫;p H沖擊;工藝性能
農業與食品加工等諸多行業,所排放的廢水不僅含有高濃度的有機污染物,而且含有高質量濃度的硫酸鹽和氨氮[1-2]。以發酵行業的味精廢水為例,其生產過程中產生的離交尾液COD質量濃度高達30 000~70 000 mg/L,N H+4-N質量濃度高達5 000~7 000 mg/L,SO42-質量濃度高達8 000~9 000 mg/L。全國每年排放這類廢水1 500萬t以上[3]。受高質量濃度硫酸鹽和氨氮的影響,味精廢水至今沒有經濟有效的治理技術,對環境的污染極為嚴重[4]。
經過厭氧處理后,硫酸鹽被還原為硫化物。它不僅會損害環境,如腐蝕金屬材料、建筑物和藝術品,也會損害人體呼吸系統、循環系統、消化系統及神經系統[5]。氨氮是水體富營養化的重要致因,通常采用硝化反硝化工藝脫除。在硝化過程中氨氮轉化成硝氮和亞硝氮。研究證明,一些微生物能夠以硝酸鹽為電子受體將硫化物氧化成單質硫[6]。若將硫化物作為電子供體來還原硝化段產生的硝酸鹽(簡稱為同步脫氮除硫),則可實現以廢制廢,達到對氮硫兩種污染物的同時去除[7]。
作者利用微生物的脫氮除硫反應研發了同步厭氧生物脫氮除硫工藝。在工程應用中,經常會遇到水量、水質波動所致的負荷沖擊,影響反應器功效的穩定性。研究反應器的抗負荷沖擊能力對于反應器的穩定運行具有重要的理論指導意義。對于同步脫氮除硫反應器穩定性的研究,迄今少見文獻報道。作者考察了p H沖擊對同步厭氧脫氮除硫反應器穩定性的影響。
1 材料與方法
1.1 接種污泥
接種污泥取自杭州某養殖場厭氧污泥床反應器,部分污泥性狀為:TS 145.03 g/L,VS 68.68 g/L,VS/TS 0.474。
1.2 試驗廢水
試驗廢水采用模擬廢水,其組成為MgCl21 g/L,KH2PO41 g/L,(NH4)2SO40.24 g/L,NaHCO31 g/L,微量元素液1 ml/L。其中Na2S·9H2O模擬硫化氫經堿液吸收后的硫化物溶液,KNO3模擬厭氧消化液中的硝態氮,微量元素溶液組成見表1。
1.3 試驗裝置
供試上流式厭氧污泥床(UASB)反應器由有機玻璃制成,總容積為1.7 L,有效容積為1.6 L。反應器置于28~30℃恒溫室中運行,工藝流程見圖1。進水由蠕動泵泵入反應器底部,流經污泥床后,由上部溢出。為了加強進水與污泥的混合,并消除可能的基質抑制效應,采用回流泵回流,回流比約為2.5。
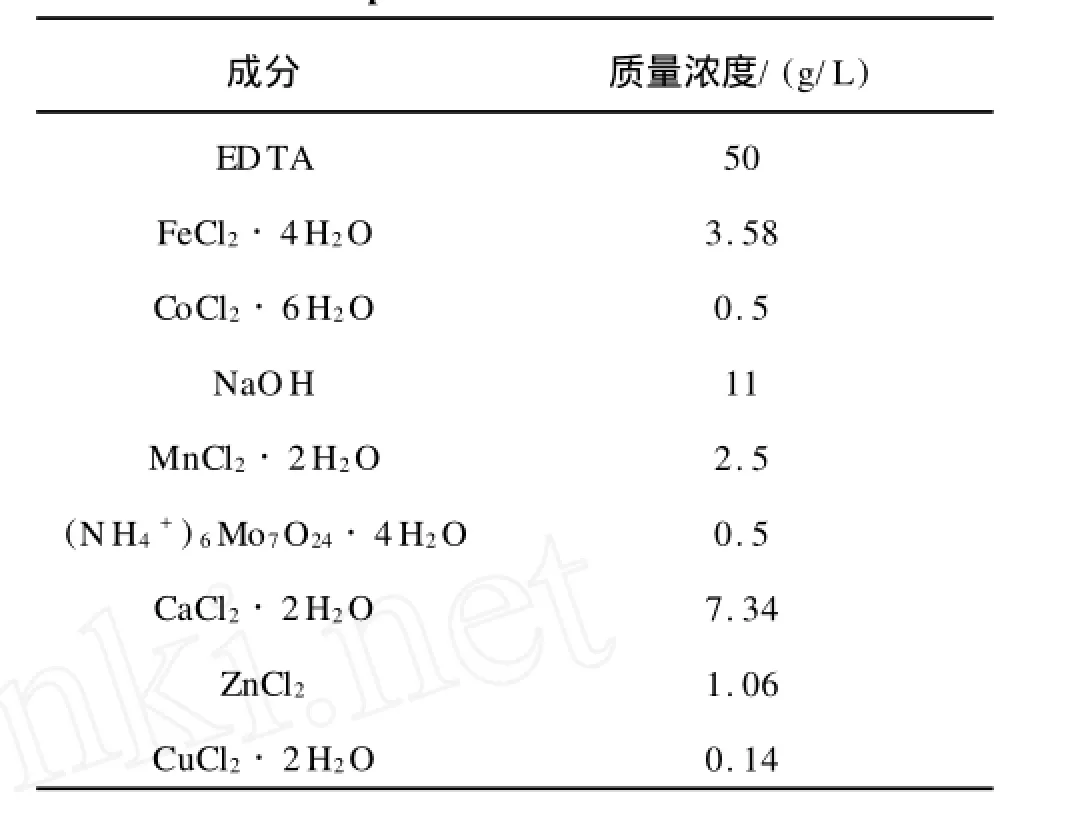
表1 微量元素溶液組成Tab.1 Components of trace element solution
1.4 試驗方法
在進行p H沖擊試驗前,該厭氧生物脫氮除硫反應器已穩定運行4個多月。其運行狀態為:進水p H約為7.0,水力停留時間(HRT)為4 h時,進水硫化物質量濃度和硝酸鹽質量濃度分別為520 mg/L和95.5 mg/L(平均值,分別以硫元素、氮元素計算),反應器容積硫化物去除速率和反應器容積硝酸鹽去除速率分別為6.23 kg/(m3·d)和1.04 kg/(m3·d),出水硫化物和硝酸鹽質量濃度分別為0.51 mg/L和8.92 mg/L(平均值),幾乎沒有亞硝酸鹽產生。
由于同步厭氧生物脫氮除硫工藝是一個產堿過程,過高的p H值將不利于該工藝的穩定運行。在本試驗中,保持其他運行參數不變,對穩態運行的反應器,采用突然提高進水p H值的方法,模擬機械故障或人為操作失誤所致的p H沖擊(沖擊p H值分別為8.0、9.0、10.0),沖擊持續時間為HRT的0.5倍(即2 h)。跟蹤監測出水基質質量濃度、p H值的變化。一旦沖擊持續時間達到設定值,即恢復原來的操作參數,繼續跟蹤監測出水基質質量濃度和p H值的變化,直至其性能完全恢復。到恢復穩態的持續時間超過HRT的100倍后,再進行下一組沖擊試驗。沖擊試驗的操作方式見圖2。
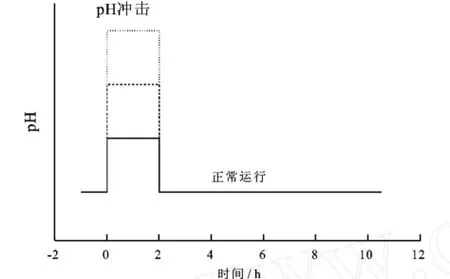
圖2 沖擊試驗的操作方式Fig.2 Operation of shock tests
1.5 測定方法
硝氮(NO3--N):紫外分光光度法[8];亞硝氮(NO2--N):N-(1-萘基)-乙二胺光度法[8];硫化物(S2--S):亞甲基蘭分光光度法[8];硫酸鹽(SO42--S):鉻酸鋇分光光度法[8];p H值:PHS-9V型酸度計。
2 結果與討論
2.1 pH沖擊對出水pH值的影響
由于回流有助于整個反應器內的基質質量濃度基本均勻一致,因此可將同步脫氮除硫反應器簡化為連續流全混合反應器。若是不考慮生物反應及緩沖作用,僅僅考慮由于進水氫離子濃度改變所引起的反應液p H值變化,結果見圖3。當p H沖擊開始后,反應液p H值應迅速直線上升,并在沖擊結束時達到最大值。當p H沖擊結束后,反應液p H值慢慢下降,最后恢復到初始狀態。
反應器的實際p H值響應曲線見圖4。實際p H沖擊對反應液p H的影響不如理論計算顯著。遭受p H沖擊時,反應液p H值在0.5 h內躍升到8.0左右,爾后幾乎呈直線上升。p H沖擊結束1 h后,反應液p H值達到最大值,p H沖擊強度越大,上升幅度越大。反應液p H值越過最大值后開始緩慢回落,最后恢復到穩定狀態。

圖3 pH沖擊的理論響應曲線Fig.3 Theoretical responsive curve to pHshock
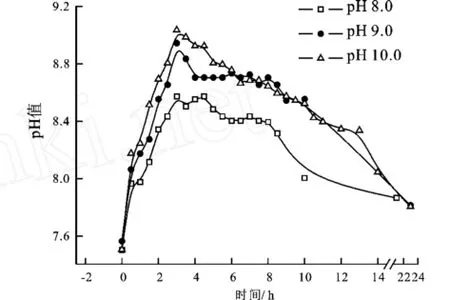
圖4 pH沖擊的實際響應曲線Fig.4 Practical responsive curve to pH shock
盡管反應液中存在酸堿緩沖體系,但其容量不大,因此反應液p H值對p H沖擊的響應仍十分靈敏。根據理論計算,p H升至8.0的沖擊強度可使反應液p H值由7.60升到7.67,升幅為0.07。p H沖擊結束后(即第2小時時),反應液p H值達到最大值;至p H沖擊結束8 h后(即第10小時時),基本恢復到平衡狀態。在實際測定中,p H升至8.0的沖擊強度就可使反應液p H值由7.50升到8.57,升幅為1.07。p H沖擊結束后,反應液p H值繼續上升,1 h后才達到最大值;至p H沖擊結束20 h后(即第22小時時),才基本恢復到平衡狀態;響應曲線類似零級反應動力學曲線。上述現象表明,反應液p H值變化不僅僅是進水p H值升高的直接結果,更可能是p H值沖擊引起同步脫氮除硫性能惡化的間接結果。一般認為,微生物的生長和代謝與p H值密切相關[9]。p H值變化會引起多種效應:影響微生物體表面的電荷變化,進而影響微生物對營養物的吸收;影響微生物體內的酶活性,進而影響微生物細胞內的生物化學反應;影響硫化物的存在形式,進而影響基質的有效性和毒性。
2.2 pH沖擊對硫化物氧化的影響
由圖5可知,遭遇p H沖擊時,出水硫化物質量濃度幾乎呈線性上升;沖擊結束1 h后,出水硫化物質量濃度達到最大值,p H沖擊強度越大,上升幅度越大;爾后出水硫化物質量濃度快速下降,至沖擊結束4 h后(即第6小時時)恢復到穩定狀態。在所試條件下,p H沖擊對硫化物的氧化有一定的影響,但影響不大。
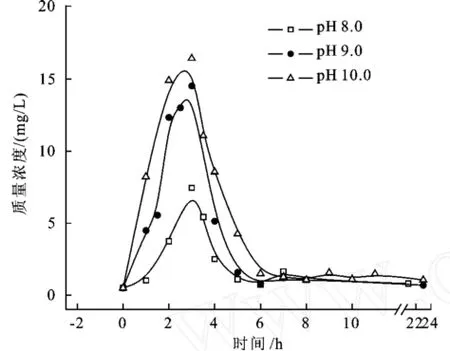
圖5 pH沖擊對硫化物氧化的影響Fig.5 Effect of pHshock on sulfide-oxidation
據文獻報道,生物脫硫反應器一般在中性略偏堿性條件(p H 7~8)下運行。筆者發現,當反應液p H值過高時(9.11±0.38),會導致反應器運行失穩[10]。在所試條件下,遭受p H升至9.0的沖擊時,反應液p H值升至8.94,已超過高適宜p H范圍,出水硫化物質量濃度也相應升至14.93 mg/L。但經過3 h后,反應液p H緩慢降至8.70,出水硫化物質量濃度回落到0.8 mg/L。這表明高p H沖擊對硫化物氧化的影響具有可恢復性。
Krishnakumar等人[6]認為,高p H值會導致硫化物氧化不徹底,造成終產物以單質硫為主。Mahmood等人[11]也發現,p H值升高時,硫酸鹽產量急劇減少。另有文獻[12-14]報道,在硫化物氧化過程中,高p H值會引起中間產物(如硫代硫酸鹽、聚多硫酸鹽等)積累。然而,上述報道的現象都發現于反應液長期處于高p H值的狀態下。在本試驗中,高p H值持續時間較短,但也發現了類似現象,見圖6。p H值沖擊開始時,出水硫酸鹽質量濃度直線下降;沖擊結束1 h后,出水硫酸鹽質量濃度達到最小值;越過最小值,出水硫酸鹽質量濃度慢慢回升,最后恢復到穩定狀態。出水硫酸鹽質量濃度對p H沖擊的響應曲線,與反應液p H值對p H沖擊的響應曲線具有良好的負相關性。反應液p H值較高時,出水硫酸鹽質量濃度較低;隨著反應液p H值慢慢回落,出水硫酸鹽質量濃度慢慢回升。
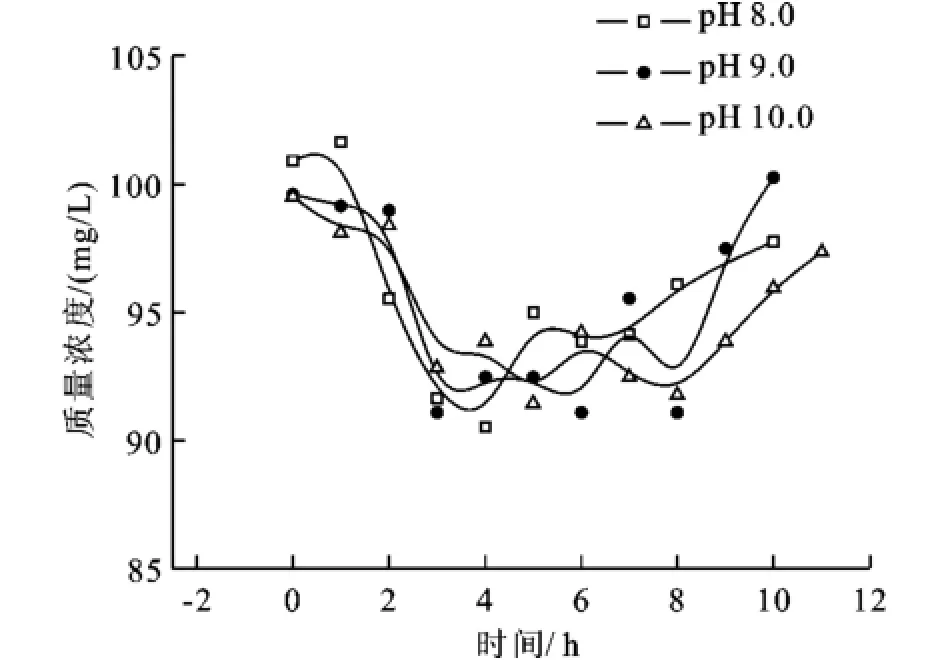
圖6 pH沖擊對硫酸鹽產量的影響Fig.6 Effect of pHshock on sulfate-production
通常認為硫化物先氧化為單質硫,再進一步被氧化為硫酸鹽[15]。根據Suzuki提出的硫氧化模型,硫氧化反應式為:

其中Sn為聚合態硫;GSH為還原型谷胱甘肽; GSSnH為谷胱甘肽多硫化物中間體;GSSG為氧化型谷胱甘肽。
在單質硫氧化為亞硫酸鹽的過程中,通過谷胱甘肽多硫化物作為中間體,硫原子逐個從聚合態Sn上解離下來,被氧化成亞硫酸鹽。當硫原子全部被氧化后,生成的氧化型谷胱甘肽可在谷胱甘肽還原酶作用下,再生成還原型谷胱甘肽[16-18]。若p H值過高,[H+]質量濃度較低,式(3)不易向右進行,從而影響單質硫向亞硫酸鹽的氧化過程,最后導致硫酸鹽產生量的減少。
2.3 pH沖擊對硝酸鹽還原的影響
由圖7可知,遭受p H沖擊時,出水硝酸鹽質量濃度幾乎呈線性上升,但不同于出水p H值和硫化物質量濃度的響應曲線;出水硝酸鹽質量濃度沒有在沖擊結束1 h后達到最大值,而是繼續上升,在沖擊結束6 h后(第8小時時)才達到最大值,p H沖擊強度越大,上升幅度越大;越過最大值后,出水硝酸鹽質量濃度緩慢下降,至p H沖擊結束20 h后(即第22小時時)恢復到穩定狀態。
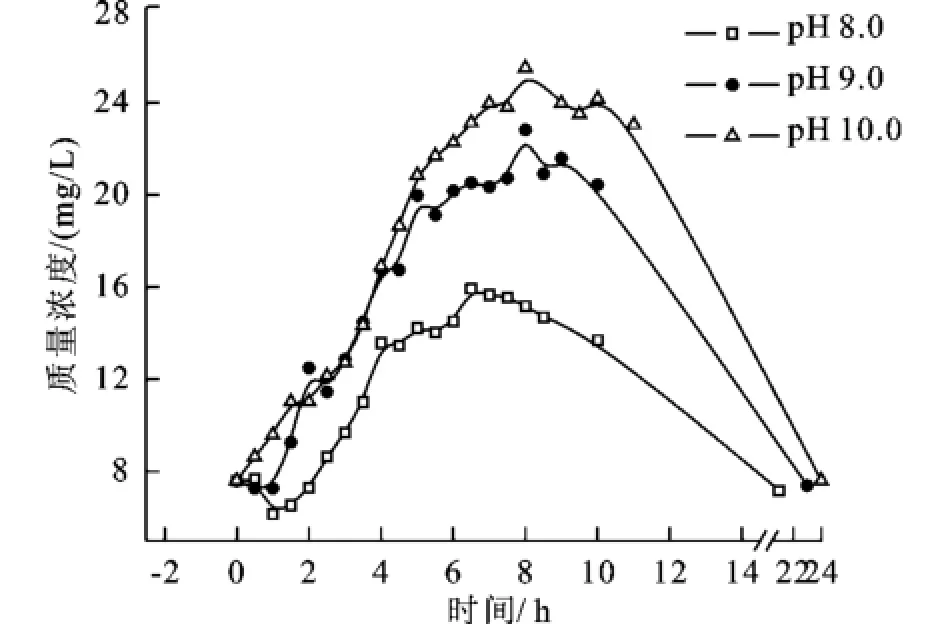
圖7 pH沖擊對硝酸鹽還原的影響Fig.7 Effect of pHshock on nitrate-reduction
據文獻[19]報道,硫化物質量濃度過高時,會抑制反硝化過程。一般認為,硫化物的抑制作用主要取決于水中硫化氫的質量濃度[20]。H2S可以通過形成硫鏈使輔酶A和輔酶M失活[21]。然而,硫化氫所占比例是受pH值左右。在所試條件下,反應器內殘留的硫化氫并沒有超過臨界抑制濃度(1 mmol/L),因此不會對反硝化過程產生顯著抑制。
從文獻[23]看,自養反硝化的最佳p H值為6.5~7.5;但當p H值偏離適宜范圍(即高于8或低于6)時,反硝化速率大幅度下降[23]。遭受p H沖擊時,反應液p H值在0.5 h內突躍到8.0左右,爾后直線上升。在p H沖擊結束6 h后(第8小時時),反應液p H值雖已慢慢回落,但仍處在8.70左右。直到反應液p H值低于8.70后,出水硝酸鹽質量濃度才開始慢慢降低。在p H沖擊過程中,所產生的亞硝酸鹽很少(<1 mg/L)。這表明硝酸鹽還原過程對p H值波動的敏感性高于硫化物氧化過程,可能與硝酸鹽進入細胞體內時需要通過NO3-/H+同向轉運載體有關[1],反應液中氫離子濃度過低,不利于硝酸鹽運輸到細胞體內。
3 結 語
1)同步厭氧生物脫氮除硫體系的酸堿緩沖容量不大,反應液p H值對p H沖擊的響應較為靈敏。反應器對p H沖擊的實際響應曲線不同于單純水力停留時間分布所致的理論響應曲線,反應液p H值變化是水力傳遞等物理作用、基質解離等化學作用以及細菌代謝等生物作用的綜合效應。
2)p H沖擊對硫化物氧化過程有一定的影響,但可恢復。反應液p H值較高時,出水硫酸鹽質量濃度較低,高p H值可抑制硫化物向硫酸鹽的徹底氧化。
3)硝酸鹽還原對p H沖擊較為敏感,但出水硝酸鹽質量濃度對p H沖擊的響應曲線具有滯后性。
[1]北京水環境技術與設備研究中心,北京市環境保護科學研究院,國家城市環境污染控制工程技術研究中心.三廢處理工程技術手冊[M].北京:化學工業出版社,2000.
[2]王偉,阮文權,鄒華,等.EGSB反應器處理高濃硫酸鹽廢水[J].食品與生物技術學報,2006,25(6):23-28.
WANG Wei,RUAN Wen-quan,ZOU Hua,et al.Treatment of sulfate-rich wastewater with EGSB reactor[J].Journal of Food Science and Biotechnology,2006,25(6):23-28.(in Chinese)
[3]王凱軍,秦人偉.發酵工業廢水處理[M].北京:化學工業出版社,2000.
[4]陶濤,詹德昊,盧秀青,等.味精廢水治理的現狀及進展[J].環境污染治理技術與設備,2002,3(1):68-73.
TAO Tao,ZHAN De-hao,LU Xiu-qing,et al.Present situation and advancement in monosodium glutamate wastewater treatment[J].Techniques and Equipment for Environmental Pollution Control,2002,3(1):68-73.(in Chinese)
[5]Mahmood Q,Zheng P,Cai J,et al.Sources of Sulfide in waste streams and current biotechnologies for its removal[J]. Journal of Zhejiang University Science A,2007,8(7):1126-1140.
[6]Krishnakumar B,Manilal V B.Bacterial oxidation of sulfide under denitrifying conditions[J].Biotechnological Letter, 1999,21:437-440.
[7]Kleerebezem R,Mendez R.Autotrophic denitrification for combined hydrogen sulfide removal from biogas and post-denitrification[J].Water Science and Technology,2002,45(10):349-356.
[8]國家環境保護總局.水和廢水監測分析方法(第四版)[M].北京:中國環境科學出版社,2005.
[9]Karline S,Andreas F H,Jack J M,et al.The effect of biogeochemical processes on p H[J].Marine Chemistry,2007, 105:30-51.
[10]蔡靖,鄭平,胡寶蘭,等.p H和堿度對同步厭氧生物脫氮除硫性能的影響[J].化工學報,2008,59(5):1264-1270.
CAIJing,ZHENG Ping,HU Bao-lan,et al.Influence of p H and alkalinity on process performance of simultaneous anaerobic sulfide and nitrate removal[J].Journal of Chemical Industry and Engineering,2008,59(5):1264-1270.(inChinese)
[11]Mahmood Q,Zheng P,Hayat Y,et al.Effect of p H on anoxic sulfide oxidizing reactor performance[J].Bioresource Technology,2008,99(8):3291-3296.
[12]Buisman C J N,Ijspeert P,Lettinga G.Kenetic parameters of a mixed culture oxidizing sulfide and sulfur with oxygen [J].Biotechnology and Bioengineering,1991,38:813.
[13]Jassen A J H,Ma S C,Lens P,et al.Performance of a sulfide oxidizing expended bed reactor supplied with dissolved oxygen[J].Biotechnology Bioengineering,1997,53:32-40.
[14]Krishnakumar B,Majumdar S,Manilal V B,et al.Treatment of sulfide containing wastewater with sulfur recovery in a novel reverse fluidized loop reactor(RFLR)[J].Water Research,2005,39:639-647.
[15]Tang K,Baskaran V,Nemati M.Bacteria of the sulphur cycle:an overview of microbiology,biokinetics and their role in petroleum and mining industries[J].Biochemical Engineering Journal,2009,44(1):73-94.
[16]Suzuki I.Oxidation of elemental sulfur by an enzyme system ofThiobacillus thiooxidans[J].Biochim Biophys Acta, 1965,104(2):359-371.
[17]Suzuki I.Incorporation of atmospheric oxygen-18 into thiosulfate by the sulfur-oxidizing enzyme ofThiobacillus thiooxidans[J].Biochim Biophys Acta,1965,110(1):97-101.
[18]Suzuki I,Siver M.The initial product and properties of the sulfur-oxidizing enzyme ofThiobacilli[J].Biochim Biophys Acta,1966,122(1):22-33.
[19]Aranda-Tamaura C,Estrada-Alvarado M I,Texier A C,et al.Effects of different quinoid redox mediators on the removal of sulphide and nitrate via denitrification[J].Chemosphere,2007,6(11):1722-1727.
[20]Cheny,Cheng J J,Creamer K S.Inhibition of anaerobic digestion process:A review[J].Bioresource Technology,2008, 99(10):4044-4064.
[21]涂保華,張潔,張雁秋.對厭氧消化中硫化氫毒性的控制[J].污染防治技術,2003,6(4):57-59.
TU Bao-hua,ZHANGJie,ZHANG Yan-qiu.Research on controlling toxicity of sulfureted hydrogen in anaerobic digestion[J].Pollution Control Technology,2003,6(4):57-59.(in Chinese)
[22]Sorensen J,Rasmussen L K,Koike I.Micromolar sulfide concentrations alleviate acetylene blockage of nitrous oxide reduction by denitrifyingPseudomonas jluorescens[J].Canadian Journal of Microbiology,1987,33:1001-1005.
[23]王白楊.廢水生物處理脫氮原理與新工藝[J].江西師范大學學報:自然科學版,2006,30(4):399-403.
WANG Bai-yang.Denitrification theory and novel processes of biological wastewater treatment[J].Journal of Jiangxi Normal University:Natural Science,2006,30(4):399-403.(in Chinese)
(責任編輯:李春麗)
Effect of pH Shock on Performance of Reactor for Simultaneous Anaerobic Sulfide and Nitrate Removal
CAI Jing, ZHEN G Ping*
(College of Environmental and Resource Sciences,Zhejiang University,Hangzhou 310029,China)
The effect of p H shock on the performance of reactor for simultaneous anaerobic sulfide and nitrate removal was investigated in this study.The response of p H in reaction system to the p H shock was very sensitive,even though there were phosphate and carbonate to buffer p H variations.The practical p H responsive curve was different from the theoretical one caused by hydraulic retention time distribution,which means that is the comprehensive results from physical,chemical and biological interaction.The sulfide-oxidation was infuenced in some way by p H shock,but recoverable.The higher p H in reaction system,the lower sulfate concentration in the effluent,which suggested that high p H inhibits the sulfur oxidation.The nitrate reduction was sensitive to p H shock,but the responsive curve of effluent nitrate concentration slightly lagged behind,which was possibly related with the mechaniam of nitrate uptake.
anaerobic sulfide and nitrate removal,p H shock,operation performance
X 703.1
:A
1673-1689(2010)01-0098-06
2008-12-22
國家863計劃項目(2006AA06Z332);國家自然科學基金項目(30770039);國家科技支撐計劃項目(2008BADC4B10)。
蔡靖(1984-),女,浙江溫州人,環境工程博士研究生。
*通訊作者:鄭平(1962-),男,浙江金華人,工學博士,教授,博士生導師,主要從事廢物生物處理與資源化方面的研究。Email:pzheng@zju.edu.cn。

