非水相脂肪酶催化合成L-抗壞血酸硬脂酸酯
晏日安, 姜新慧, 張廣文, 黃才歡, 段翰英
(暨南大學食品科學與工程系,廣東廣州 510632)
非水相脂肪酶催化合成L-抗壞血酸硬脂酸酯
晏日安, 姜新慧, 張廣文, 黃才歡, 段翰英
(暨南大學食品科學與工程系,廣東廣州 510632)
研究了非水介質中Novozym 435脂肪酶催化合成L-抗壞血酸硬脂酸酯(L-AS)。脂肪酶用量固定為L-抗壞血酸質量的20%,底物L-抗壞血酸與硬脂酸的摩爾比限定為1∶2,對影響脂肪酶催化的因素如溶劑、溫度、溶劑量、反應時間、分子篩用量和搖床轉速進行了研究。優化后的反應條件:在30 mL叔丁醇中加入6.82 mmolL-抗壞血酸,13.64mmol硬脂酸,0.24 g脂肪酶和3.0 g 4A分子篩,搖床轉速150 r/min,反應在55℃水浴中進行48 h。通過分離提純,產品采用紅外及質譜檢測后確定為L-抗壞血酸硬脂酸酯,產率最高時達64.7%。脂肪酶重復使用5次,最低產率為61%。
非水介質;脂肪酶催化;L-抗壞血酸硬脂酸酯;合成
L-抗壞血酸硬脂酸酯(INS 305;CAS(26395-66-8))是微有光澤的白色或黃白色結晶粉末,溶于酒精、乙醚和油脂,對熱及重金屬較抗壞血酸穩定,美國和日本均有批量生產,目前國內該產品生產企業極少。L-AS一般與L-抗壞血酸棕櫚酸酯合用,是一種安全、高效、易被人體消化吸收的脂溶性抗氧化劑,同時也是一種營養強化劑,適合添加在油脂類食品中。目前報道的化學法合成L-AS主要采用直接酯化法[1]、酰氯法[1]和酯交換法[2-3],其產率在50%至77%不等,化學法易產生副反應、腐蝕性強、對設備要求高、對環境污染大。脂肪酶催化法具有反應溫和、選擇性高、副反應少、對設備要求低和產物易于純化[4-5]等優點。酶法合成抗壞血酸棕櫚酸[6-9]和抗壞血酸月桂酸[10-11]均有大量文獻,目前酶法合成L-AS僅有一篇外文文獻[12]采用Amano PS脂肪酶催化乙烯基硬脂酸與L-抗壞血酸進行酯交換,國內還沒有酶法合成L-AS文獻報道。
鑒于酶法催化反應的優點和L-AS應用前景,本文擬采用脂肪酶在非水介質中催化L-抗壞血酸與硬脂酸合成L-AS,對反應條件進行優化,對產物進行提純并進行鑒定。
1 材料和方法
1.1 主要材料與儀器
Novozym 435脂肪酶:諾維信(中國)廣州分公司產品,L-抗壞血酸,硬脂酸,4A分子篩(以下簡稱分子篩),叔丁醇、叔戊醇、丙酮(經分子篩干燥),甲苯,正己烷:試劑均為分析純。
SHA-B型水浴恒溫振蕩器:金壇市宏華儀器廠生產;RE-52 AAB型旋轉蒸發器:上海嘉鵬科技有限公司生產;X-5顯微熔點測定儀:北京泰克儀器有限公司生產;傅里葉變換紅外吸收光譜儀:EQUINOX55;EI低分辨率質譜儀:DSQ,Thermo產品;高分辨率質譜儀:MA T 95XP,Thermo產品。
1.2 L-AS的合成
150 mL具塞錐形瓶中加入0.24 g酶、1.20 g (6.82mmol)L-抗壞血酸、3.88 g(13.64 mmol)硬脂酸、30 mL叔丁醇及3.0 g分子篩,放在55℃水浴恒溫振蕩器中,以150 r/min的轉速振蕩反應48 h。
1.3 L-AS的分離純化過程

1.4 L-AS波譜數據
紅外光譜特征峰(未經KBr壓片,直接檢測): 3 467cm-1,υ-OH;2 916 cm-1、2 849 cm-1,(-CH2, -CH3);1 731 cm-1,υC=O(酯);1 635/1 682 cm-1, υC=C;1 466 cm-1,δas(CH3);1 385 cm-1, δs(CH3);1 161cm-1,δC-O;721 cm-1,-(CH2)n-指紋區特征吸收峰。
EI-MS檢測數據(電子轟擊能量70 eV;離子源溫度250℃;檢測器電壓1 400 V):442:弱的分子離子峰;424:[M-H2O]信號峰;267為酯鍵α裂解后[R=CH3(CH2)16CO+]質譜信號;239為[R= CH3(CH2)16CO+]脫去羰基后的質譜信號(強峰)。
FAB-MS檢測數據(倍增器電壓:1.8KV;基質:3-硝基芐醇):465:[M+Na]+信號峰;443:[M +H]+峰強度加強;267:酯鍵α裂解后[R=CH3(CH2)16CO+]質譜信號峰;239:[R=CH3(CH2)16CO+]脫去羰基后的質譜信號(強度降低)。
綜合紅外和質譜數據可判斷產物為抗壞血酸硬脂酸酯。
2 結果與討論
2.1 溶劑對反應的影響
Laane[13]用有機溶劑的極性參數lgP(lgP是該有機溶劑在正辛醇/水體系中的分配系數的對數)來描述有機溶劑對酶催化反應的影響,隨著溶劑lgP值降低,酶的水化層會逐漸受到破壞,研究認為lgP<2的有機溶劑不適合作為反應介質,因有機溶劑將強烈破壞酶的必須水化層而使酶失活。150 mL具塞錐形瓶中加入0.24 g脂肪酶、1.20 g (6.82 mmol)L-抗壞血酸、3.88 g(13.64 mmol)硬脂酸、40 mL溶劑、2.0 g分子篩,55℃水浴中以200 r/min振蕩反應24 h。表1所示為溶劑對酶催化酯化的影響。正己烷的lgP>2,脂肪酶能較好的保持原有構象,但在正己烷中不能催化L-AS的合成。表1顯示脂肪酶在lgP<2的3種溶劑中都具有較強的催化能力。丙酮的lg P相對較低,其作為溶劑對酶的活性有一定破壞作用。以叔丁醇為反應溶劑時所得產率最高(見表1)。故下一輪選擇叔丁醇為反應介質。
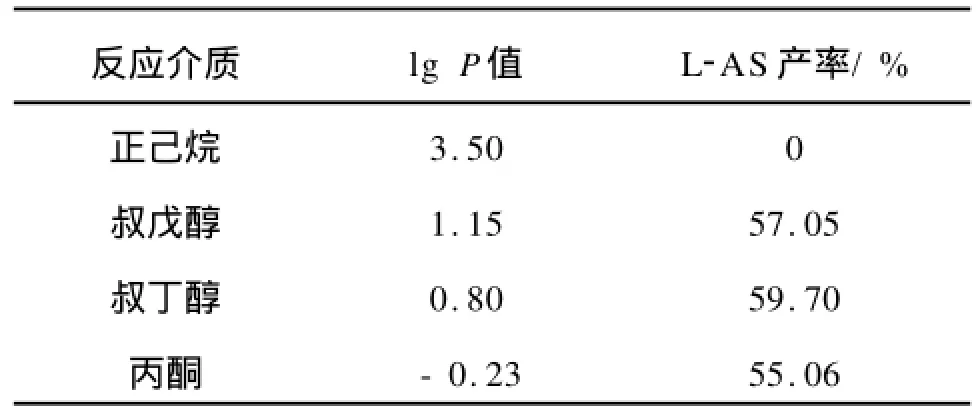
表1 溶劑對反應的影響Tab.1 Effect of solvents on the reaction
2.2 溫度對反應的影響
固定化的Novozym 435脂肪酶催化酯化反應的適宜溫度在40~70℃之間[14]。溫度對Novozym435脂肪酶催化抗壞血酸與硬脂酸酯化反應的影響如圖1所示。

圖1 溫度對反應的影響Fig.1 Effect of temperature on the reaction
由圖1可見,反應溫度為55℃時,反應所得產率最高,表明此時酶催化能力最強,在此溫度下脂肪酶有較好的溫度穩定性;溫度低于55℃時,產率隨溫度升高而增加,這是因為溫度的提高加快了底物分子的熱運動速度、激發了酶的活性中心催化能力,從而使酶與底物的結合以及酶與產物的分離速度大大提高。當溫度高于55℃,產率會隨溫度升高而下降,這與溫度過高酶的活性中心受到破壞以及抗壞血酸因高溫部分分解有關。故選擇55℃作為下一輪反應的溫度。
2.3 溶劑用量對反應的間接影響
0.24 g脂肪酶催化1.20 g L-抗壞血酸與3.88 g硬脂酸進行48 h的酯化反應。硬脂酸在叔丁醇中易溶,而L-抗壞血酸卻難溶于叔丁醇(55℃水浴、搖床轉速150 r/min下每10 mL叔丁醇約溶解0.04 g L-抗壞血酸)。隨著溶劑量從10 mL增加到50 mL,硬脂酸濃度從1.364 mol/L減少到0.273mol/L,抗壞血酸處于飽和狀態。固定物料投入量后,溶劑量的變化可改變底物濃度和酶濃度,還會影響反應體系的傳質,所以底物濃度、酶濃度以及傳質對酯化反應影響可通過溶劑量與產率的間接關系反映出來見圖2。
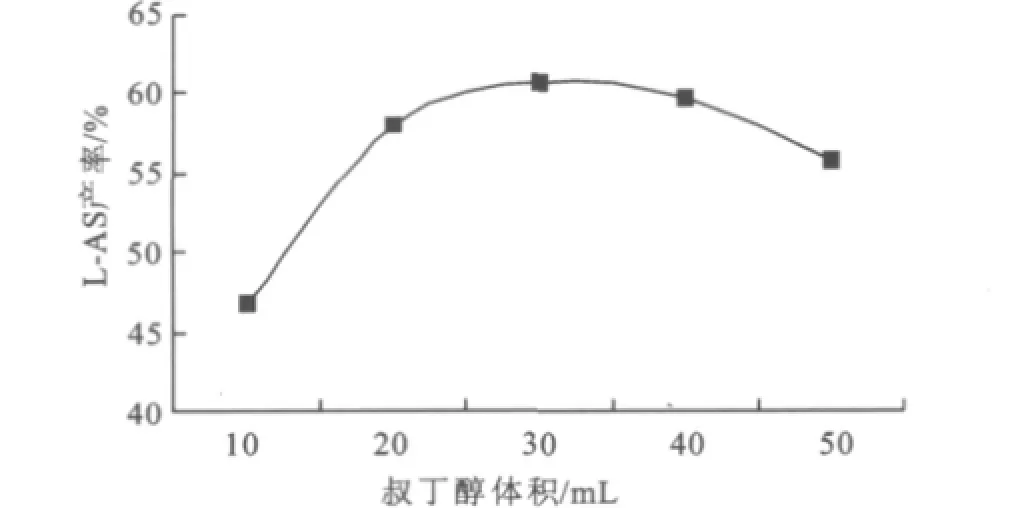
圖2 叔丁醇用量對反應的間接影響Fig.2 Indirectly effect of t-butanol alcohol consumption on the reaction
圖2所示,叔丁醇用量30 mL時,產率最高。溶劑少于30 mL時,產率隨溶劑用量增加而上升,這與溶劑中抗壞血酸的溶解量增加、產物得到較好的分散、分子篩對傳質的影響降低有關。溶劑用量大于30 mL時,產率降低,原因是溶劑的增加降低硬脂酸濃度和酶濃度,反應體系攪拌不均使酶在反應液中分布不均,上述原因降低了底物和酶的有效碰撞率。所以下一輪反應中溶劑用量以30 mL為宜,即硬脂酸濃度為0.455 mol/L。
2.4 時間對酯化反應的影響
酶促L-AS合成是一個可逆的平衡反應,反應時間短產率低,時間過長又不能明顯提高產率,副反應還會隨之增多(見圖3)。
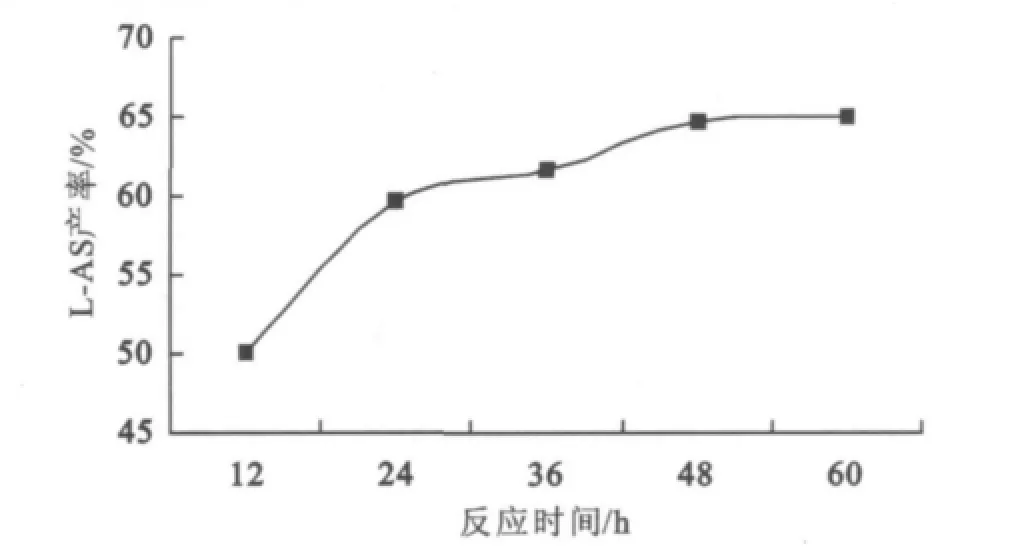
圖3 時間對酯化反應的影響Fig.3 Effect of reaction time on the esterification reaction
圖3顯在48 h前,產率隨時間延長而上升,這與反應逐步接近平衡有關;反應48 h后,產率無明顯增加,表明反應已達到平衡,延長反應時間不會提高反應產率反而增加了合成成本。因此下一輪反應時間限定在48 h。
2.5 分子篩用量對反應的影響
4A型分子篩可吸收水、氧氣、甲醇、乙醇等物質,是一種大容量的高效吸水劑。直接酯化法合成L-AS,水是反應副產物,向反應體系中投入分子篩吸水可使反應平衡右移有利于提高酯化產率。30 mL反應液中分子篩用量與產率關系如圖4所示。
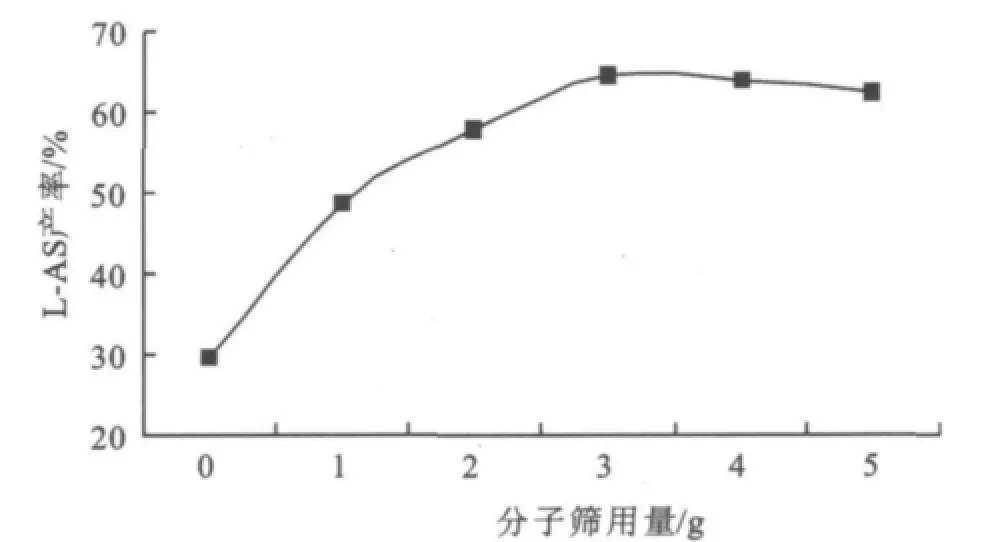
圖4 分子篩用量對反應的影響Fig.4 Effect of molecular sieves amount on the reaction
圖4顯示當體系中不加分子篩時,產率非常低,這是副產物水使平衡向左移的緣故;增加分子篩投入量,產率隨之上升,原因是分子篩吸收水后,打破原有反應的平衡,使酯化反應平衡右移。當分子篩用量為3.0 g時,產率達到最高。分子篩用量超過3.0 g時,產率開始下降,分子篩加入過多的吸水效應導致酶自身的微環境破壞,也會阻礙體系中傳質以及造成固定化酶的脫落。因此選擇在下一輪反應中每30 mL的反應液加入3.0 g分子篩。
2.6搖床轉速對反應的影響
酶催化效率受到反應體系擴散速度的影響,搖床轉速的不同可以帶來反應體系外擴散速度的變化。轉速對反應影響如圖5所示。
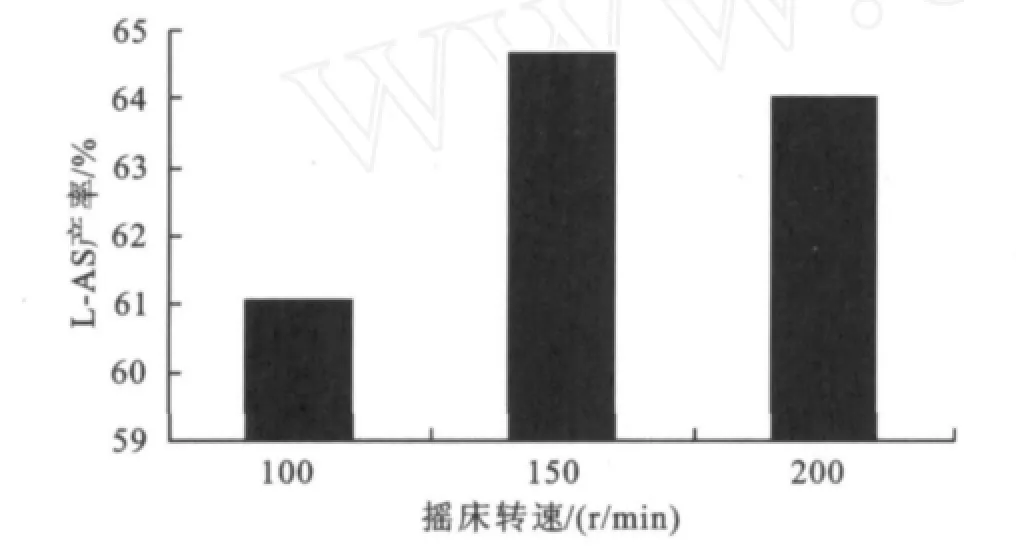
圖5 搖床轉速對反應的影響Fig.5 Effect of shaker speed on the reaction
圖5可見當轉速為100 r/min時產率最低,原因是底物及產物的擴散速度較低,降低了酶催化的效率。轉速為150 r/min時,產率最高為64.7%。當轉速為200 r/min時,產率有所降低,由于轉速加快,加劇了反應體系中脂肪酶與分子篩、瓶壁之間的碰撞,使固定化的脂肪酶磨損而脫落,改變了部分酶的結構,從而掩蓋了外擴散速度加快帶來的有利影響。故下一輪反應選擇轉速150 r/min。
2.7 酶使用次數的影響
脂肪酶的價格昂貴,所以我們對酶重復使用進行了考察(除酶外,其余反應條件與上一致)。多次使用的結果如圖6所示。
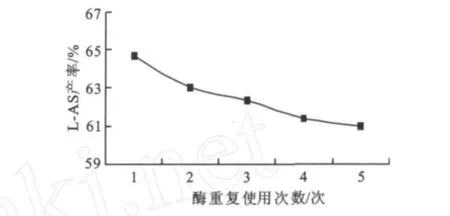
圖6 酶重復使用次數對反應產率的影響Fig.6 Effect of enzyme reused times on the yield of reaction
圖6顯示當酶連續使用5次的催化產率都在61%以上,然而產率隨使用次數增加呈緩慢下降,這與固定化酶的多次使用所造成的部分酶脫落及活性中心失活有關。因此在生產中酶可連續使用5次,保持每次的催化效果與新酶基本相當,這可以明顯降低成本。
3 結 語
成功的用脂肪酶催化L-抗壞血酸與硬脂酸合成了L-抗壞血酸硬脂酸酯,并優化了酶法合成條件,最佳條件下的產率為64.7%,提純工藝簡單有效,酶可多次使用,有很好的發展前景。相對于傳統的化學法合成,選擇用酶法合成L-AS更符合綠色化學的發展要求。目前酶催化法合成L-AS離實現工業化生產有一定距離,為提高酶法合成的產率并降低成本,未來研究的重點將是尋找更高效的催化酶和更優的反應條件以及反應規模的擴大。
[1]黃紹華,胡國華,肖建軍.L-抗壞血酸硬脂酸酯的合成及其抗氧化作用[J].食品工業,1999,(3):28-29.
HUANG Shao-hua,HU Guo-hua,XIAO Jian-jun.Synthesis L-ascorbyl stearate and its antioxidant effect[J].Food Industry,1999,(3):28-29.(in Chinese)
[2]謝文磊,李魁,王宏雁.酯交換法合成L-抗壞血酸硬脂酸酯及其抗氧化性能[J].高校化學工程學報,2002,16(4):441-445.
XIE Wen-lei,LI Kui,WANG Hong-yan.Synthesis of L-ascorbyl stearate by transesterification and its antioxidant effect [J].Journal of Chemical Engineering of Chinese Universities,2002,16(4):441-445.(in Chinese)
[3]雷琳.L-抗壞血酸硬脂酸酯的合成條件探索[J].廣東化工,2009,(6):72-73.
L EI Lin.Study on synthesis condition of L-ascorbyl stearate[J].Guangdong Chemical Industry,2009,(6):72-73.(in Chinese)
[4]李炎.食品添加劑制備工藝[M].廣州:廣東科技出版社,2001.163-164.
[5]張曉鳴,周健,劉巧瑜,等.有機相脂肪酶催化合成技術在食品及相關領域的應用[J].食品與生物技術學報,2006,25 (1):120-126.
ZHANG Xiao-ming,ZHOU Jian,LIU Qiao-yu,et al.Application of lipase-catalyzed synthesis in organic solvent for food and related industry[J].Journal of Food Science and Biotechnology,2006,25(1):120-126.(in Chinese)
[6]Humeau C,Girardin M,Coulon D,et al.Synthesis of 6-O-palmitoyl L-ascorbic acid catalyzed by candida antartica lipase [J].Biotechnol Lett,1995,17(10):1091-1094.
[7]Humeau C,Girardin M,Rovel B,et al.Enzymatic synthesis of fatty acid ascorbyl esters[J].J Mol Catal B:Enzym, 1998,(5):19-23.
[8]Hsien H J,Nair G R,Wu W T.Production of ascorbyl palmitate by surfactant-coated lipase in organic media[J].J Agric Food Chem,2006,(54):5777-5781.
[9]徐鳳杰,譚天偉.生物法合成維生素C棕櫚酸酯[J].生物工程學報,2005,21(6):988-992.
XU Feng-Jie,TAN Tian-Wei.Biologicals Synthesis of L-ascorbyl palmitate[J].Chinese Journal of Biotechnology,2005, 21(6):988-992.(in Chinese)
[10]Chang S W,Yang C J,Chen F Y,et al.Optimized synthesis of lipase-catalyzed L-ascorbyl laurate by novozym 435[J]. J Mol Catal B:Enzym,2009,(56):7-12.
[11]蔡水根,陶冠軍,熊幼翎,等.L-抗壞血酸月桂酸酯的酶法合成、分離及其性質[J].食品工業科技,2008,10(29):211-215.
CAI Shui-gen,TAO Guan-jun,XIONG You-ling,et al.Enzymatic synthesis,separation and properties of L-ascorbyl laurate[J].Science and Technology of Food Industry,2008,10(29):211-215.(in Chinese)
[12]Sakashita K,Miyamoto S,Sakimae A.process for producing ascorbic or erythorbic acid esters:European Patent,0 514 694[P].1992.
[13]Lanne C,Boeren S,Veeger K,et al.Rules for optimization of biocatalysis in organic solvents[J].Biotechnol Bioeng, 1987,(30):81-87.
[14]潘宇.抗壞血酸苯甲酸酯的生物合成與性能研究[D].杭州:浙江大學,2006.
(責任編輯:楊萌)
Lipase-catalyzed Synthesis of L-ascorbyl Stearate in Non-aqueous Phase
YAN Ri-an, J IANG Xin-hui, ZHANG Guang-wen, HUANG Cai-huan, DUAN Han-ying
(Department of Food Science and Engineering,Jinan University,Guangzhou 510632,China)
In this manuscript,the technical conditions of Novozym 435 lipase-catalyzed synthesis of L-ascorbyl stearate(L-AS)in non-aqueous medium were determined with 20%lipase and 1:2 L-ascorbic acid to stearic acid(molar ratio).The optimum reaction conditions listed as follows: 30ml t-butanol with 6.82mmol L-ascorbic acid,13.64mmol stearic acid,0.24g lipase and 3.0g 4A molecular sieves,shaker speed 150r/min,the reaction carried out at 55℃water bath with 48h.Through the separation and purification,the isolated product was finally identified as L-ascorbyl stearate by infrared(IR)and mass spectrometry(MS)detection,the highest yield reached 64.7%.Lipase reused five times,the lowest yield was 61%.
non-aqueous medium,lipase-catalyzed,L-ascorbyl stearate,synthesis
TS 201.2
:A
1673-1689(2010)03-0385-05
2009-05-12
廣東省高校科技成果轉化重大資助項目(cgzhzd0805)。
晏日安(1962-),男,湖南益陽人,工學博士,教授,主要從事食品添加劑制備與應用研究。Email:jxh830923@163.com

