SO42-/杭錦2#土固體超強酸催化合成乙酸正丁酯
魏景芳,郝向英,郭海福,白麗梅,照日格圖
(1.內蒙古師范大學 化學與環境科學學院,內蒙古 呼和浩特 010022;2.肇慶學院 化學化工學院,廣東 肇慶 526061)
乙酸正丁酯是一種無色透明的液體,具有水果香味,被廣泛應用于香料合成和塑料工業中.固體超強酸因具有酸性強、易分離、無腐蝕及對環境友好等優勢,在乙酸正丁酯的合成中顯示出較好的催化性能[1-3];但將其作為催化劑具有成本高及使用壽命短等不足之處,由此制約了其推廣應用[4].
杭錦2#土是內蒙古杭錦旗境內的一種天然礦物材料,其儲量豐富,價格低廉.該土本身具有一定的Lewis酸性,經酸化改性后,比表面積增大,酸性增強.目前對杭錦2#土的研究主要集中在對有機、無機污染物的吸附以及有色物質的脫色方面[5-7],將其用于制備催化劑的研究較少.筆者以酸處理后的杭錦2#土為載體制備了SO42-/杭錦2#土固體超強酸,首次將其用于乙酸正丁酯的合成反應中,顯示出與硫酸為催化劑相當的活性,具有一定的工業開發前景.
1 實驗部分
1.1 催化劑的制備
活性白土的制備:取一定量的杭錦2#土按一定固液比與3.0 mol/L的硫酸混合,在(90±2)℃下恒溫回流攪拌一定時間,冷卻靜置后抽濾,用去離子水洗滌至濾液無Cl-離子存在(0.5 mol/L AgNO3檢驗).濾出物置于110℃溫度的烘箱中干燥3 h,研碎,過篩即得活性白土.
固體超強酸催化劑的制備:分別稱取一定量的上述活性白土,按一定固液比浸漬于一定濃度的硫酸溶液中,室溫下攪拌4 h,抽濾分離;濾出物置于烘箱中在110℃的溫度下干燥后,研磨、過篩,在馬弗爐中于300℃的溫度下焙燒3 h,即制得/杭錦2#土固體超強酸催化劑.
1.2 乙酸正丁酯的合成
在裝有油水分離器、回流冷凝管、磁力攪拌器的三口燒瓶中加入一定量的冰乙酸、正丁醇、環己烷(帶水劑)以及上述固體超強酸催化劑,磁力攪拌,在體系回流溫度為90℃下反應2 h,取樣,按照國標GB1668—81的方法測定其酸值.以酚酞為指示劑,用氫氧化鈉溶液滴定,酯化率的計算公式如下:
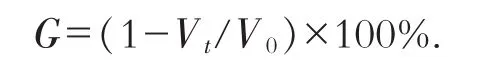
式中:V0—反應前體系消耗NaOH的體積,mL;Vt—反應后體系消耗NaOH的體積,mL.
反應結束后過濾除去催化劑,采用質量分數為10%的碳酸氫鈉溶液中和乙酸,再用飽和的氯化鈉溶液洗至中性,加入無水硫酸鎂干燥;過濾后對粗產品進行蒸餾,收集124~126℃的餾分,得無色透明液體.其紅外光譜圖與乙酸正丁酯的標準譜圖完全一致,分別在1 740 cm-1和1 240 cm-1處出現乙酸正丁酯的 和C─O的特征吸收峰,且折光率nD20為1.394 9,與文獻中的數值[8]相符,證明是乙酸正丁酯.
2 結果與討論
2.1 催化劑用量對酯化率的影響
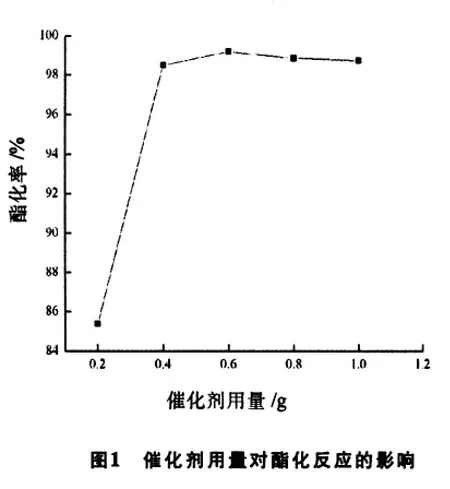
按1.2進行乙酸正丁酯的合成反應,保持醇、酸摩爾比為2:1,反應溫度為90℃,反應時間為2 h的條件不變,改變催化劑的用量,所得酯化率隨催化劑用量的變化結果見圖1.
如圖1所示,催化劑的用量為0.6 g時,反應的酯化率最高;當催化劑的用量小于0.6 g時,酯化率有所下降.由于SO42-/杭錦2#土催化劑的用量少時,活性中心數目太少,不能為反應物提供足夠的有效反應空間,因而酯化率不高.而催化劑用量大于0.6 g時,酯化率又有所降低.這可能是由于催化劑用量過多會造成副反應增加,因此,催化劑的用量控制在0.6 g為宜.
2.2 醇、酸摩爾比對酯化反應的影響
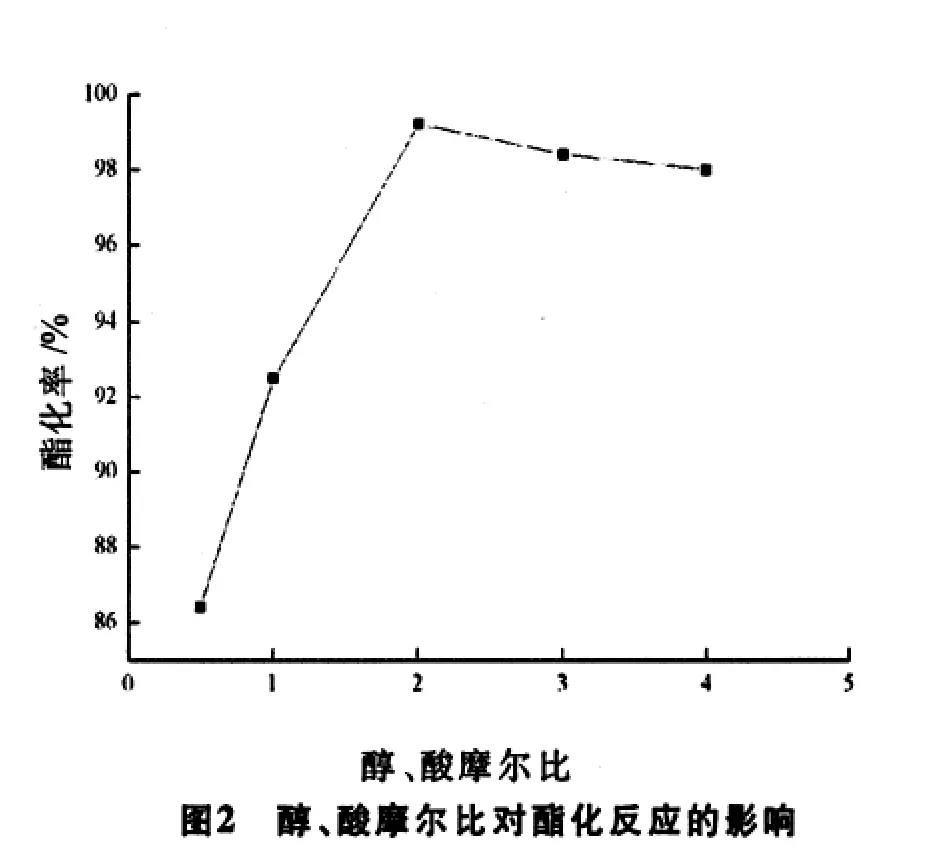
按1.2進行乙酸正丁酯的合成反應,保持催化劑用量為0.6 g,反應溫度為90℃,反應時間為2 h的條件下,改變醇、酸摩爾比,所得酯化率隨醇、酸摩爾比變化的關系曲線如圖2所示.
酯化反應是可逆反應,增大醇的用量,有利于反應向生成酯的方向轉化,從而提高反應的酯化率.醇、酸摩爾比為2:1時,酯化率達到最大值;繼續增大醇的用量,酯化率反而下降.這可能是由于過量的醇降低了酸和催化劑的相對濃度[9],這樣不利于酯化反應的進行,而且大量醇的存在,會促進醇本身發生副反應;因此,在該實驗條件下,醇、酸的最佳摩爾比為2:1.
2.3 反應時間對酯化反應的影響
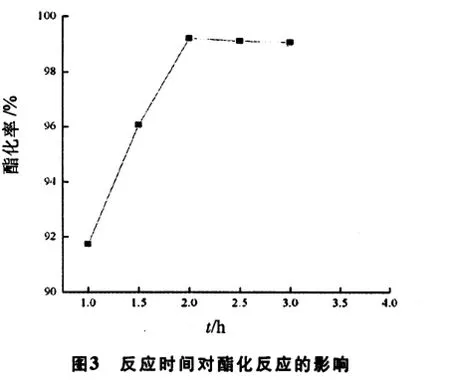
按1.2進行乙酸正丁酯的合成反應,保持催化劑用量為0.6 g,醇、酸摩爾比為2:1,反應溫度為90℃的條件下,改變反應時間,所得酯化率隨反應時間變化的關系曲線如圖3所示.
如圖3所示,反應開始后酯化率持續增大,當反應進行到2 h,酯化率即達到99.2%.這說明若反應時間短,則酯化不完全,酯化率較低;而隨著反應時間的延長,酯化率不斷增大.當反應時間超過2 h后,酯化率基本維持不變.據此,可確定最佳的反應時間為2 h.
2.4 反應溫度對酯化反應的影響
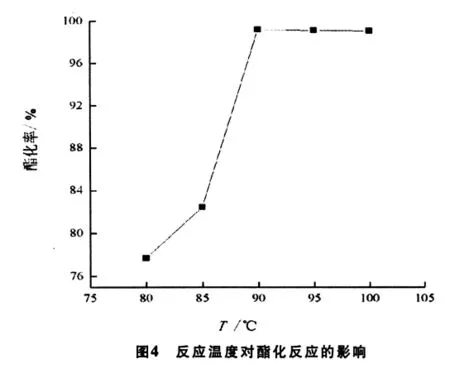
按1.2進行乙酸正丁酯的合成反應,保持醇、酸摩爾比為2:1,催化劑用量為0.6 g,反應時間為2 h的條件下,改變反應溫度,所得酯化率隨反應溫度變化的關系曲線如圖4所示.
圖4表明,隨著反應溫度升高,酯化率也隨之提高,當反應溫度升到90℃時,酯化率達到最大值.繼續升溫,則酯化率趨于平衡.溫度低時體系回流不明顯,反應速度慢,酯化率偏低;而溫度過高時,所得產物的顏色加深,可能生成了副產物,由此增加了后處理的困難,同時影響了產品質量.據此,可確定反應溫度控制在90℃左右為宜.
2.5 催化劑的穩定性
在最佳反應條件下考察催化劑的穩定性.將SO42-/杭錦2#土固體酸催化劑用于乙酸和正丁醇的酯化反應,每次反應2 h,冷卻后濾出催化劑,重復投料反應,連續使用5次,酯化反應結果如表1所示.將反應5次后的催化劑進行再生,用無水乙醇洗滌2遍,在烘箱中于110℃的溫度下烘干,補充浸漬2.5 mol/L的硫酸后再于300℃的溫度下焙燒2 h,將此再生后的催化劑標記為ST(R).
從表1可知,催化劑重復使用5次后,酯化率降至65.6%;重新經酸處理后,酯化率又升至93.2%.由此可見,催化活性降低主要是由于表面的流失所致.另一方面,催化劑表面部分酸中心被覆蓋也可能是活性降低的原因之一.再有,在每次使用、分離的過程中催化劑均有損失,這也會導致活性降低.
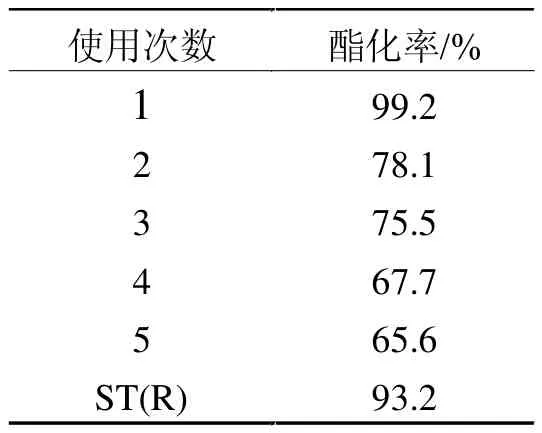
表1 催化劑的穩定性
2.6 酸催化劑的活性比較
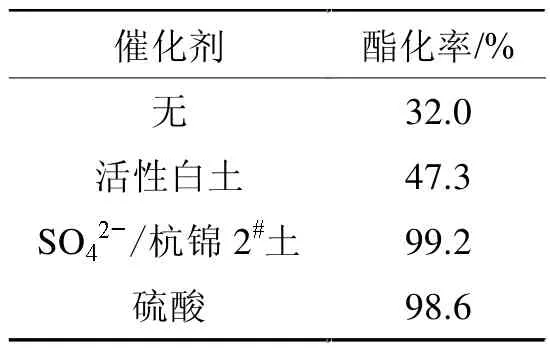
表2 幾種酸催化劑的活性比較
3 結論
以杭錦2#土為原料制備了杭錦2#土固體超強酸,該催化劑對乙酸正丁酯的合成反應具有較高的催化活性.該催化劑成本低廉、制備簡便且可以重復使用.
[1] 張連偉.乙酸正丁酯合成的研究進展[J].當代化工,2005,34(3):173-175.
[2] 李秋榮,趙倩.固體超強酸S/TiO2催化合成乙酸正丁酯[J].工業催化,2006,14(7):35-37.
[3] 古緒鵬,陳同云,萬玉保,等.SZrO2-TiO2-La固體酸催化合成乙酸正丁酯[J].石油化工,2002(5):353-356.
[5] 照日格圖,烏云,寶迪巴特爾,等.杭錦2#土脫色劑的制備及其對植物油脫色性能的研究[J].中國油脂,2004,29(8):19-21.
[6] 烏云,照日格圖,嘎日迪,等.粘土-SA01吸附和分離洛神葵紅色素的研究[J].食品科學,2004,25(11):73-75.
[7] 寶迪.杭錦2#土處理含高氟水的初探[J].內蒙古石油化工,2004,30:1-2.
[8] 劉光啟,馬連湘,劉杰.化學化工物性數據手冊[M].北京:化學工業出版社,2002:426-426.
[9] 戴衛東,李泉,王壽武.納米固體超強酸/ZrO2-Al2O3的制備及催化合成乙酸丁酯[J].應用化工,2008,37(12):1 475-1 478.

