脂肪酸低共熔溶劑對姜黃素的溶解作用
摘要:制備了辛酸(C8)分別與癸酸(C10)、月桂酸(C12)及肉豆蔻酸(C14)形成的 C8-C10、 C8-C12、C8-C14 3 種脂肪酸低共熔溶劑(DES)。C8-C10、C8-C12、C8-C14 對姜黃素的溶解 度分別為 1.11、1.24、1.44 mmol/L,比姜黃素在水中的溶解度分別提高了約 29、32、38 倍。 通過 Gaussian 模擬計算,得到姜黃素與 C8、C10、C12、C14 形成的分子締合物的吉布斯自由 能分別為?48.49、?64.27、?91.26、?120.59 kJ/mol。姜黃素與烷基鏈最長的 C14 形成“三明 治”型分子締合物,具有最強的氫鍵和疏水締合作用,使姜黃素在 C8-C14 脂肪酸 DES 中表現 出最高的溶解度和最強的紫外吸收及熒光發射強度。姜黃素在 C8-C10、C8-C12、C8-C14 3 種 脂肪酸 DES 中均具有顯著提高的穩定性和 1,1-二苯基-2-三硝基苯肼(DPPH)自由基清除能力。
關鍵詞:低共熔溶劑(DES);姜黃素;溶解;氫鍵;疏水作用
中圖分類號:O645.16
文獻標志碼:A
低共熔溶劑(Deep Eutectic Solvent, DES)是由兩 種或兩種以上組分通過氫鍵結合而形成的低熔點混 合物。自 Abbott 等[1] 于 2003 年首次報道 DES 以來, 許多物質包括氯化膽堿、葡萄糖、氨基酸、脂肪酸等 被發現能夠形成 DES。作為一種新型綠色溶劑 , DES 具有成本低廉、制備簡單、生物安全性高、組成 與性質易于調控等優點,被廣泛應用于天然產物提 取[2]、生物質轉化[3] 等領域。
姜黃素是一種從姜黃根莖中提取分離出來的多 酚類天然活性物。研究表明姜黃素具有很高的醫用 價值,如抗氧化[4]、抗腫瘤[5] 等藥理作用。但是,姜黃 素在水中的溶解度很低、穩定性很差,這嚴重限制了 姜黃素的實際應用效果。使用表面活性劑膠束、囊 泡、脂質體以及蛋白質顆粒等包載系統可以有效改 善姜黃素的上述問題[6-7]。但是,這些包載系統還存 在成分安全性低 、制備工藝復雜等缺點。最近 , DES 被用于姜黃素的提取和溶解。Jeliński 等[8] 制備 了氯化膽堿為氫鍵受體與甘油、果糖等氫鍵供體所 形成的 DES,并考察了 DES 對姜黃素的溶解性能。
相比于姜黃素在水中的低溶解性,這些 DES 對姜黃 素具有顯著增強的溶解能力。李佳[9] 使用 12 種 DES 提取姜黃素,發現 DES 的種類、組分物質的量 之比、含水量等條件均可對姜黃素的提取產生影 響。 Shekaari 等[10] 進一步研究了水分對氯化膽堿類 DES 溶解姜黃素的影響,他們通過實驗和活度系數 模型發現含水量的增加不利于 DES 對姜黃素的溶 解。目前報道的研究主要采用低熔點的氯化膽堿類 DES。然而,在與水接觸時,由于親水性銨鹽的氯化 膽堿類 DES 的化學性質不穩定,容易發生分解,使得 人們開始關注和研究疏水性 DES 的制備和應用[11]。
脂肪酸是一類天然羧酸化合物,廣泛存在于動 物脂肪、植物堅果及種子內。脂肪酸可以與氯化膽 堿、醇類等物質共同形成 DES。烷基鏈長度不同的 脂肪酸也能夠通過氫鍵作用形 成 DES。脂肪 酸 DES 已被用于相變材料制備、金屬離子萃取[12] 等方 面。脂肪酸帶有長烷基鏈,從而使脂肪酸類 DES 的 熔點較高,通常需要較高的制備溫度。因此,目前鮮 見脂肪酸類 DES 用于姜黃素的提取和溶解。已有研究表明[13] ,將烷基鏈長度不同的脂肪酸混合,通過調 節脂肪酸分子之間的相互作用,能夠進一步降低脂 肪酸類 DES 的熔點。本文研究烷基鏈長度不同的脂 肪酸形成的 DES 對姜黃素的溶解作用。將辛酸(C8) 分別與癸酸(C10)、月桂酸(C12)和肉豆蔻酸(C14) 混合 ,采用加熱-冷卻方法[14] 制備了 C8-C10、 C8- C12 和 C8-C14 3 種脂肪酸 DES,測定了 3 種脂肪酸 DES 對姜黃素的溶解度,使用 Gaussian 軟件模擬計 算了姜黃素與不同脂肪酸的分子締合作用,并考察 了姜黃素在 3 種脂肪酸 DES 中的紫外和熒光性質、 穩定性和 1,1-二苯基-2-三硝基苯肼(DPPH)自由基清 除性能。
1""" 實驗部分
1.1 試劑和原料
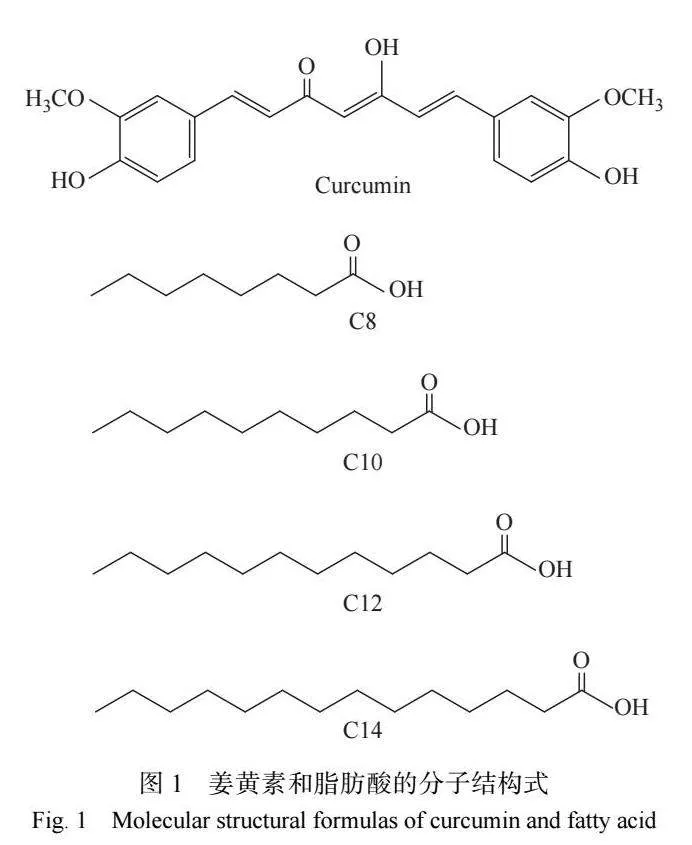
姜黃素(Curcumin):純度gt;70%,阿拉丁生化科技 股份有限公司;C8:純度gt;98%,上海泰坦科技股份有 限公司;C10:純度gt;98%,上海泰坦科技股份有限公 司 ;C12:純度≥99%,國藥集團化學試劑有限公司; C14:純度≥99%,Sigma-Aldrich 試劑有限公司;DPPH: 純度 98%,北京百靈威科技有限公司。實驗用水為 超純水。圖 1 所示為姜黃素和 4 種脂肪酸的分子結 構式。
1.2 脂肪酸 DES 的制備及相變溫度測定
按照一定的物質的量之比將 C8 分別與 C10、 C12、C14 混合,在 60 ℃ 下恒溫攪拌 1 h,然后將脂肪 酸混合物置于烘箱中,于 60 ℃ 繼續干燥 2 h。通過 精細梯度升溫和降溫處理,觀察脂肪酸混合物的相 態變化,記錄樣品的熔點和凝固點。使用差示掃描 量熱儀(DSC,德國 Netzsch 公司 TA200F3)測定脂肪 酸混合物的相變溫度,測試氣體氛圍為 N2,溫度范圍 為?10~80 ℃,升溫和降溫速率均為 5 ℃/min。 在 C8-C10、C8-C12、C8-C14 3 種脂肪酸混合物 中,選擇 C8 與 C10、C12、C14 物質的量之比分別為 2∶1、5∶1 和 6∶1(此時混合物熔點最低)制備 C8- C10、C8-C12 和 C8-C14 脂肪酸 DES,用于姜黃素的 溶解作用研究。
1.3 姜黃素在脂肪酸 DES 中的溶解度測定
在室溫下,將過量的姜黃素加入到脂肪酸 DES 中 ,攪拌 1 h 并靜置 24 h。離心分離后 ,取脂肪酸 DES 的上層清液。同時,配制一系列不同姜黃素濃 度的乙醇溶液,通過測定姜黃素的紫外吸收光譜確 定姜黃素吸光度-濃度標準曲線。定量移取脂肪酸 DES 的上層清液并溶解于乙醇中,然后測定姜黃素 的吸光度。最后,根據姜黃素吸光度-濃度標準曲線 計算姜黃素在脂肪酸 DES 中的溶解度。
1.4 姜黃素與脂肪酸的分子締合作用模擬計算
利用 Sobtop 軟件[15] 與 Multiwfn 軟件[16] 構建姜 黃素(簡寫為 Cur)、C8、C10、C12 和 C14 的分子結 構,然后使用 Gromacs 模擬退火算法對 Cur-C8、Cur[1]C10、Cur-C12 和 Cur-C14 分子締合物進行構象統計, 并使用 Molclus 程序[17] 計算分子締合物的能量。選 擇能量最低的分子締合物構象,使用 Gaussian 軟件 進行構象優化并計算分子締合物的吉布斯自由能。
最 后 , 使 用 Multiwfn 和 Visual" Molecular" Dynamics (VMD)軟件繪制分子締合物的 Core-Pauling-Koltum (CPK)模型。
1.5 姜黃素在脂肪酸 DES 中的紫外吸收光譜和熒 光發射光譜測定
在 298 K 下,使用紫外吸收光譜儀(日本島津公 司 Shimadzu UV-1800 型)測定 10 μmol/L 姜黃素在水 及 C8-C10、C8-C12 和 C8-C14 脂肪酸 DES 中的紫外 吸收光譜。 在 298" K 下 ,使用熒光光譜儀 ( 英 國 Edinburgh Instruments FLS920 型)測定姜黃素樣品的 熒光發射光譜 ,激發波長為 424" nm,掃描范圍為 430~600 nm。在姜黃素的紫外吸收光譜和熒光發射 光譜測定中,均取 3 次測定的實驗平均值。
1.6 姜黃素在脂肪酸 DES 中的穩定性測定
在 298 K 下,使用 Shimadzu UV-1800 紫外吸收 光譜儀測定姜黃素樣品在 0 和 3 h 時的紫外吸光度,考察姜黃素在不同脂肪酸 DES 中的穩定性。
1.7 姜黃素在脂肪酸 DES 中的 DPPH 自由基清除 能力測定
在 298 K 下,將姜黃素樣品與 DPPH 的乙醇溶 液在棕色瓶中混合,使用 Shimadzu UV-1800 紫外吸 收光譜儀測定 0 和 3 h 時樣品在 517 nm 處的紫外吸 光度。
DPPH 自由基清除率(RDPPH)根據式(1)計算:
式中:Asample 為姜黃素樣品與 DPPH 乙醇溶液混合物 的紫外吸光度;Ablank 為姜黃素樣品與無水乙醇混合 物的紫外吸光度;Acontrol 為水與 DPPH 乙醇溶液混合 物的紫外吸光度。
2""" 結果與討論
2.1 脂肪酸 DES 的制備
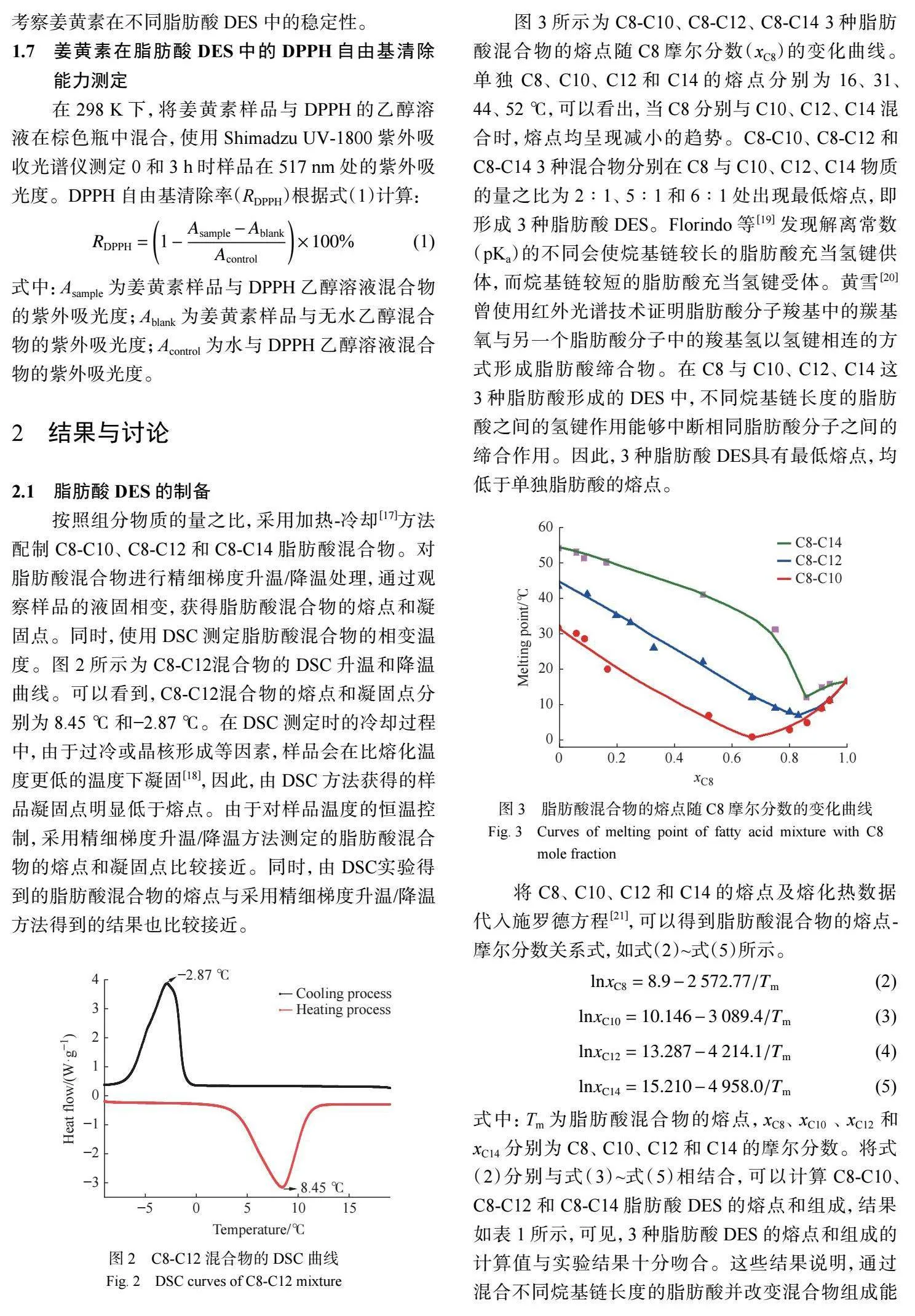
按照組分物質的量之比,采用加熱-冷卻[17]方法 配制 C8-C10、C8-C12 和 C8-C14 脂肪酸混合物。對 脂肪酸混合物進行精細梯度升溫/降溫處理,通過觀 察樣品的液固相變,獲得脂肪酸混合物的熔點和凝 固點。同時,使用 DSC 測定脂肪酸混合物的相變溫 度。圖 2 所示為 C8-C12混合物的 DSC 升溫和降溫 曲線。可以看到,C8-C12混合物的熔點和凝固點分 別為 8.45 ℃ 和?2.87 ℃。在 DSC 測定時的冷卻過程 中,由于過冷或晶核形成等因素,樣品會在比熔化溫 度更低的溫度下凝固[18] ,因此,由 DSC 方法獲得的樣 品凝固點明顯低于熔點。由于對樣品溫度的恒溫控 制,采用精細梯度升溫/降溫方法測定的脂肪酸混合 物的熔點和凝固點比較接近。同時,由 DSC實驗得 到的脂肪酸混合物的熔點與采用精細梯度升溫/降溫 方法得到的結果也比較接近。
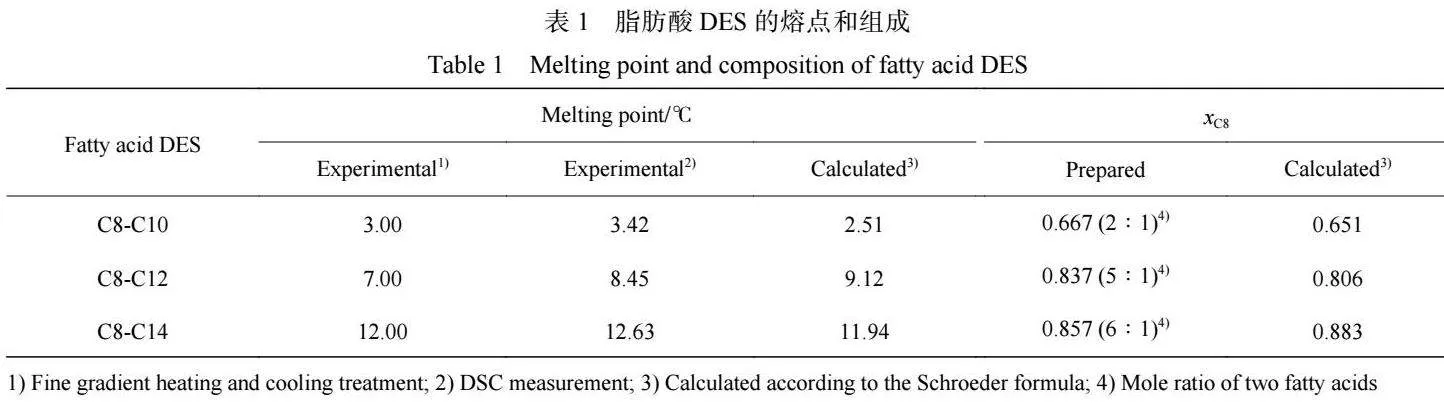
圖 3 所示為 C8-C10、C8-C12、C8-C14 3 種脂肪 酸混合物的熔點隨 C8 摩爾分數(xC8)的變化曲線。 單 獨 C8、 C10、 C12 和 C14 的熔點分別 為 16、 31、 44、52 ℃,可以看出,當 C8 分別與 C10、C12、C14 混 合時,熔點均呈現減小的趨勢。C8-C10、C8-C12 和 C8-C14 3 種混合物分別在 C8 與 C10、C12、C14 物質 的量之比為 2∶1、5∶1 和 6∶1 處出現最低熔點,即 形成 3 種脂肪酸 DES。Florindo 等[19] 發現解離常數 (pKa)的不同會使烷基鏈較長的脂肪酸充當氫鍵供 體,而烷基鏈較短的脂肪酸充當氫鍵受體。黃雪[20] 曾使用紅外光譜技術證明脂肪酸分子羧基中的羰基 氧與另一個脂肪酸分子中的羧基氫以氫鍵相連的方 式形成脂肪酸締合物。在 C8 與 C10、C12、C14 這 3 種脂肪酸形成的 DES 中,不同烷基鏈長度的脂肪 酸之間的氫鍵作用能夠中斷相同脂肪酸分子之間的 締合作用。因此,3 種脂肪酸 DES具有最低熔點,均 低于單獨脂肪酸的熔點。
將 C8、C10、C12 和 C14 的熔點及熔化熱數據 代入施羅德方程[21] ,可以得到脂肪酸混合物的熔點- 摩爾分數關系式,如式(2)~式(5)所示。
式中:Tm 為脂肪酸混合物的熔點,xC8、xC10 、xC12 和 xC14 分別為 C8、C10、C12 和 C14 的摩爾分數。將式 (2)分別與式(3)~式(5)相結合,可以計算 C8-C10、 C8-C12 和 C8-C14 脂肪酸 DES 的熔點和組成,結果 如表 1 所示,可見,3 種脂肪酸 DES 的熔點和組成的 計算值與實驗結果十分吻合。這些結果說明,通過 混合不同烷基鏈長度的脂肪酸并改變混合物組成能夠調節脂肪酸 DES 的熔點。
2.2 姜黃素在脂肪酸 DES 中的溶解度
姜黃素在水中的溶解度為 3.74×10?2 mmol/L,根 據 姜 黃 素 吸 光 度 -濃 度 標 準 曲 線 ( 方 程 為y = 115.845 24x?0.095 61 ,其中,x 表示吸光度,y 表示濃 度。相關系數 R 2=0.998 81),代入測得的各脂肪酸 DES 的吸光度數據 ,即可以計算出姜黃素在 C8- C10、C8-C12 和 C8-C14 3 種脂肪酸 DES中的溶解度 分別為 1.11、1.24、1.44 mmol/L。與水相比,C8-C10、 C8-C12、C8-C14 脂肪酸 DES 能夠使姜黃素的溶解度 分別提高約 29、32 和 38 倍。
姜黃素分子中含有苯環、雙鍵等疏水性基團,不 易與水分子發生作用,因此姜黃素在水中的溶解度 很低。當姜黃素溶解于氯化膽堿 類 DES 中時 , Jeliński 等[8] 發現姜黃素溶解的主要驅動力是姜黃素 與 DES 組分之間的氫鍵作用,同時也歸因于 DES 組 分間的氫鍵網格結構。與表面活性劑對姜黃素的增 溶作用類似,脂肪酸分子中的羧基能夠與姜黃素分 子中的羥基形成氫鍵,同時脂肪酸分子中的烷基鏈 能夠與姜黃素分子中的苯環、雙鍵等疏水性基團產 生疏水作用。因此,不同于其他類型的 DES,氫鍵和 疏水作用均會有助于姜黃素在脂肪酸 DES 中的 溶解。
2.3 姜黃素與脂肪酸的分子締合作用模擬計算
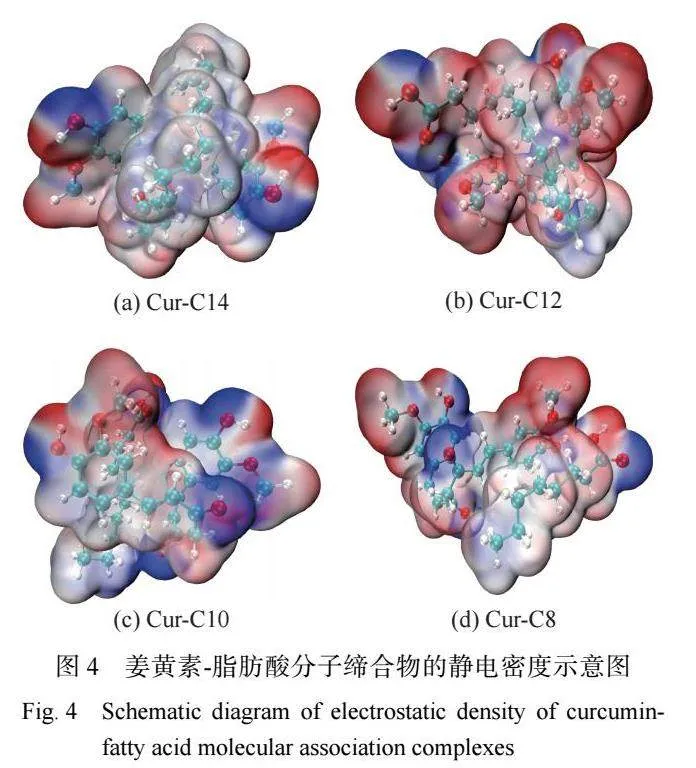
當姜黃素加入到脂肪酸 DES 中時,姜黃素分子 與脂肪酸分子之間存在氫鍵、疏水等弱相互作用,同 時會伴隨著分子構象的變化。使用 Gaussian 軟件對 姜黃素與 C8、C10、C12 和 C14 形成的分子締合物的 構象進行了優化。如圖 4 所示,姜黃素通常采用半展 開的分子形態,其酚羥基能夠與脂肪酸的羧基產生 氫鍵作用,這會使姜黃素分子的兩個苯環彼此遠離, 從而減弱姜黃素分子自身的締合作用[22]。然而,脂肪 酸的烷基鏈長度不同,姜黃素與脂肪酸所形成的分 """ 子締合物呈現不同的構象。在 Cur-C8 分子締合物 中,C8 分子締合于姜黃素分子的外側,二者為并排結構。Cur-C10 分子締合物呈現半并排、半交叉的分子 結象,C10 的烷基鏈部分插入姜黃素的兩個苯環之 間。在姜黃素與 C12 和 C14 形成的“三明治”型分子 締合物中,姜黃素的酚羥基與脂肪酸的羧基產生氫 鍵作用,而姜黃素的苯環、雙鍵會與脂肪酸的烷基鏈 發生強疏水締合作用。通過 Gaussian 模擬計算,姜黃 素與 C8、C10、C12 和 C14 形成的分子締合物的吉布斯 自由能分別為?48.49、?64.27、?91.26、?120.59 kJ/mol。 姜黃素與 C14 形成的分子締合物具有最高負值的吉 布斯自由能,這說明姜黃素與 C14 之間存在最強的 分子締合作用。這個結果也可以解釋姜黃素在 C8- C14 脂肪酸 DES 中具有最高的溶解度。
2.4 姜黃素在脂肪酸 DES 中的光譜性質
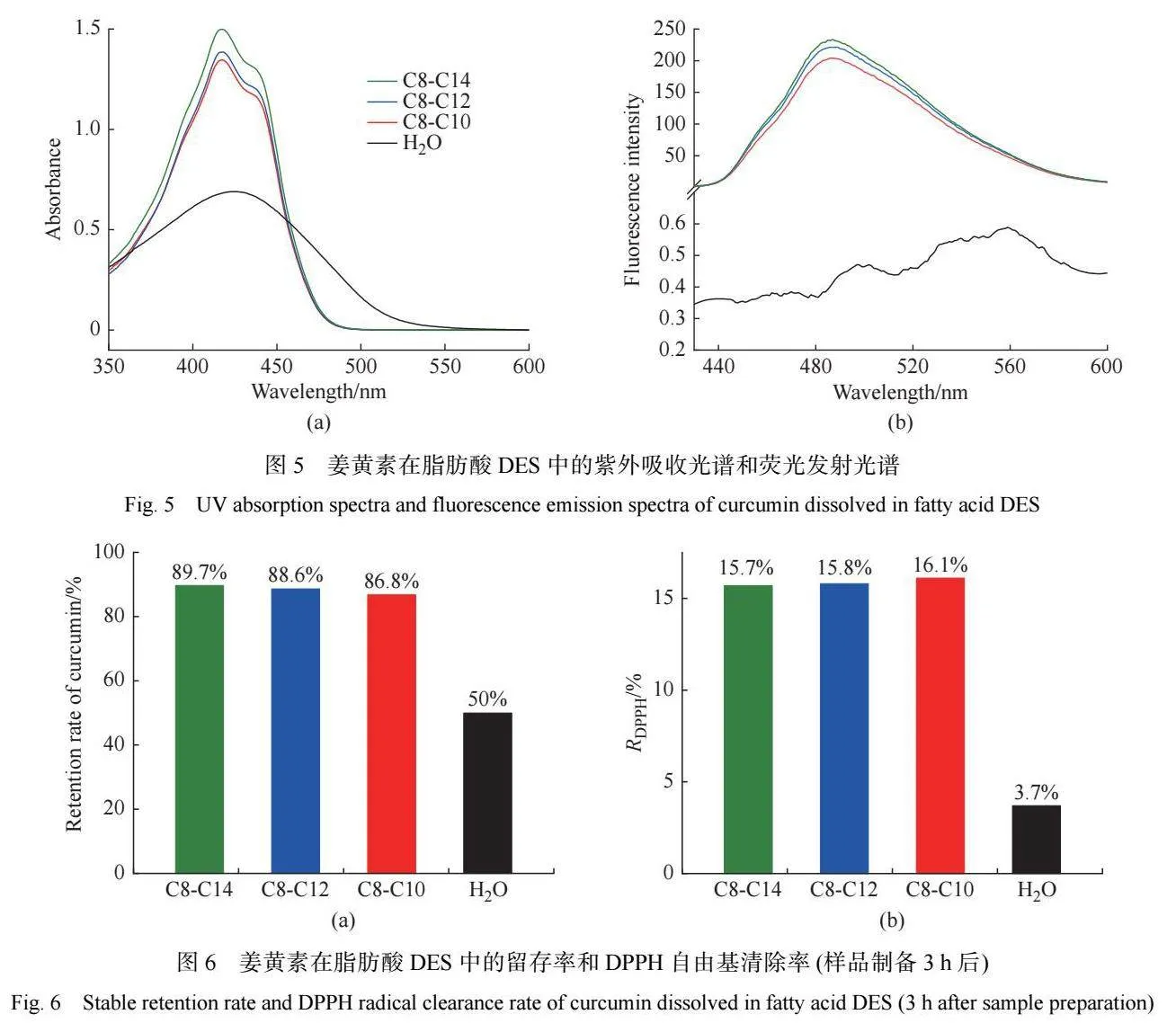
姜黃素是一種高度共軛性分子,其紫外吸收和 熒光光譜性質對周圍環境的變化非常敏感[23]。因此, 紫外吸收光譜和熒光發射光譜可以用來考察姜黃素 在脂肪酸 DES 中的溶解狀態[24]。圖 5 所示為姜黃素 溶解在 3 種脂肪酸 DES 中的紫外吸收光譜和熒光發 射光譜。溶解在水中的姜黃素分別在 425 nm 和 560 nm處呈現較寬的紫外吸收峰和微弱的熒光發射峰。當 姜黃素溶解在脂肪酸 DES 中時,姜黃素與脂肪酸會 形成分子締合物,姜黃素分子的苯環、雙鍵與脂肪酸 分子的烷基鏈之間發生疏水締合作用,能夠為姜黃 素提供疏水環境,從而大大提高姜黃素的紫外吸收 和熒光發射強度。在脂肪酸烷基鏈形成的低極性疏 水環境中,姜黃素分子的 π-π* 躍遷產生的吸收峰會 發生藍移,n-π* 躍遷產生的吸收峰會發生紅移。這 些因素會導致脂肪酸 DES 溶解的姜黃素除了在 417 nm 處呈現明顯的吸收峰外,還在 437 nm 處出現了肩峰[25]。 雖然姜黃素在 3 種脂肪酸 DES 樣品中具有相同的濃 度,但是姜黃素的紫外吸收和熒光發射強度均與脂 肪酸的烷基鏈長度呈現正相關性。姜黃素在 C8- C14 脂肪酸 DES 中具有最高的紫外吸收和熒光發射 強度,這表明 C8-C14 脂肪酸 DES 能夠為姜黃素提供 更疏水的締合微環境[26]。
2.5 姜黃素的穩定性和 DPPH 自由基清除能力
通過測定姜黃素分子和 DPPH 自由基分子的紫 外吸收強度的變化 ,可以考察姜黃素在脂肪 酸DES 中的穩定性和自由基清除能力。在水環境中, 姜黃素分子的酮-烯醇基團容易發生去質子化,因而 姜黃素在水溶液中不穩定[27]。但是,姜黃素分子的 酮-烯醇基團能夠提供氫原子,這使姜黃素分子具有 很強的自由基清除能力[28]。由圖 6 中可以看出,溶解 于水中的姜黃素在 3 h 后降解了 50%,其 DPPH 自由 基清除率為 3.7%。當姜黃素溶解于脂肪酸 DES 中 時,3 h 后姜黃素的留存率可以超過 86%,DPPH 自由 基清除率不低于 15.7%。當被聚合物納米顆粒、表面 活性劑膠束包載時,姜黃素通常能夠表現出顯著提 高的穩定性和 DPPH 自由基清除能力[29-30]。在脂肪 酸 DES 的非水環境中,脂肪酸與姜黃素的氫鍵和疏 水締合作用能夠抑制姜黃素分子中酮-烯醇結構的去 質子化 ,從而提高姜黃素分子的穩定性。當加入 DPPH 自由基時,脂肪酸烷基鏈提供的疏水微環境能 夠促進姜黃素對 DPPH 自由基的還原反應。姜黃素 在 3 種脂肪酸 DES 中的穩定性和 DPPH自由基清除 能力相差不大,這也說明氫鍵作用對脂肪酸 DES 的 形成及姜黃素的溶解具有同樣重要的影響。
3""" 結 論
( 1) 在 C8-C10、 C8-C12、 C8-C14" 脂 肪 酸 DES 中,C8-C14 DES 對姜黃素具有最高的溶解能力。
(2)姜黃素在脂肪酸 DES 中的溶解性和姜黃素 與脂肪酸分子締合物的吉布斯自由能數據一致,這 可歸因于姜黃素與脂肪酸之間的氫鍵、疏水的共同 作用。
(3)脂肪酸 DES 能夠為姜黃素提供低極性疏水 環境,使姜黃素表現出顯著提高的紫外吸收和熒光 發射強度、穩定性及 DPPH 自由基清除能力。作為 一種疏水性 DES,通過改變脂肪酸的種類、組成等條 件,不僅能夠有效調節脂肪酸 DES 的基礎物理化學 性質,也能夠精細調控疏水區域的微觀結構,從而顯 著提高脂肪酸 DES 對姜黃素等難溶性植物活性物的 提取、溶解及應用性能。
參考文獻:
ABBOTT" A" P," CAPPER" G," DAVIES" D" L, et al." Novel solvent properties" of" choline" chloride/urea" mixtures"" elec[1]tronic supplementary information (ESI) available: Spectro[1]scopic data[J]. Chemical Communications, 2003, 1: 70-71.
DUAN L, DOU L L, GUO L, et al. Comprehensive evalu[1]ation" of" deep" eutectic" solvents" in" extraction" of" bioactive natural" products[J]. ACS" Sustainable" Chemistry" amp;" Engi[1]neering, 2016, 4(4): 2405-2411.
GUTIéRREZ" M" C," FERRER" M" L," YUSTE" L, et al. Bacteria" incorporation" in" deep-eutectic" solvents" through freeze-drying[J]. Angewandte Chemie International Edition, 2010, 49(12): 2158-2162.
BASNET P, SKALKO B N. Curcumin: An anti-inflamma[1]tory molecule from a curry spice on the path to cancer treat[1]ment[J]. Molecules, 2011, 16(6): 4567-4598.
李晨晨, 龔飛榮, 程樹軍,等. 姜黃素緩釋膠束的制備、表 征及其抗細胞毒類藥物的多藥耐藥性評價[J]. 華東理工 大學學報 (自然科學版), 2014, 40(5): 562-567.
鄭雨晴, 王小永. 烷基鏈結構對吐溫表面活性劑包載姜黃 素的影響[J]. 華東理工大學學報 (自然科學版), 2023, 49(2): 188-195.
褚翔宇, 王小永. 玉米蛋白/吐溫-20復合納米顆粒對姜黃 素的包載作用[J]. 化學通報, 2018, 81(7): 625-629.
JELI?SKI" T," PRZYBY?EK" M," CYSEWSKI" P." Natural deep" eutectic" solvents" as" agents" for" improving" solubility, stability" and" delivery" of" curcumin[J]. Pharmaceutical Research, 2019, 36(8): 116.
李佳. 天然低共熔溶劑提取姜黃素類化合物的研究[D]. 天津: 天津科技大學, 2020.
SHEKAARI" H," MOKHTARPOUR" M," FARAJI" S, et al. Enhancement of curcumin solubility by some choline chlor[1]ide-based deep eutectic solvents as a new category of green solvents at different temperatures[J]. Fluid Phase Equilibria, 2020, 532. DOI: 10.1016/j.fluid.2020.112917.
BELINDA" S," ARMANDO" J" D," SILVESTRE" P" C, et al. Hydrotropy" and" cosolvency" in" lignin" solubilization" with deep" eutectic" solvents[J]. ACS" Sustainable" Chemistry" amp; Engineering, 2019, 7(14): 12485-12493.
LI D. Natural deep eutectic solvents in phytonutrient extrac[1]tion" and" other" applications[J]." Frontiers" in" Plant" Science, 2022, 13. DOI: 10.3389/fpls.2022.1004332.
馬尚文, 底夢飛, 楊嶸晟, 等. 雙脂肪酸憎水性低共熔溶劑 的合成及富集水中銅離子的研究[J]. 煤炭與化工, 2020, 43(6): 121-128.
ZHAO P, YUE Q, HE H, et al. Study on phase diagram of fatty acids mixtures to determine eutectic temperatures and the" corresponding" mixing" proportions[J]. Applied" Energy, 2014, 115: 483-490.
TIAN" LU." Sobtop," Version" 1.0[EB/OL]." (2022-2-15) [2023-02-01]. http://sobereva.com/soft/sobtop.
TIAN" LU." Multiwfn," Version" 3.8[EB/OL].nbsp; (2022-2-15) [2023-02-01]. http://sobereva.com/multiwfn.
TIAN" LU." Molclus" Program," Version" 1.9.9.9[EB/OL]. (2022-2-15)" [2023-02-01]. http://www.keinsci.com/resear ch/molclus.html.
SIEW W L. Crystallisation and melting behaviour of palm kernel" oil" and" related" products" by" differential" scanning calorimetry[J]. European" Journal" of" Lipid" Science" and Technology, 2001, 103(11): 729-734.
FLORINDO" C," ROMERO" L," RINTOUL" I, et al." From phase change materials to green solvents: Hydrophobic low viscous" fatty" acid-based" deep" eutectic" solvents[J]. ACS Sustainable" Chemistry" amp;" Engineering," 2018," 6(3):" 3888- 3895.
黃雪. 三元低共熔脂肪酸復合相變材料的制備及熱性能 研究[D]. 廣州: 廣東工業大學, 2015.
張寅平, 蘇躍紅, 葛新石. (準)共晶系相變材料融點及融 解熱的理論預測[J]. 中國科學技術大學學報, 1995, 25(4): 474-478.
TONNESEN H H. Solubility, chemical and photochemical stability" of" curcumin" in" surfactant" solutions-studies" of curcumin" and" curcuminolds," XXVIII[J]." Pharmazie," 2002, 57(12): 820-824.
ZSILA" F," BIKáDI" Z," SIMONYI" M." Molecular" basis" of the" cotton" effects" induced" by" the" binding" of" curcumin" to human" serum" albumin[J]. Tetrahedron" Asymmetry, 2003, 14(16): 2433-2444.
SAHU A, KASOJU N, BORA U. Fluorescence study of the curcumin-casein" micelle" complexation" and" its" application as" a" drug" nanocarrier" to" cancer" cells[J]. Biomacromole[1]cules, 2008, 9(10): 2905-2912.
WANG F, WU X, WANG F, et al. The sensitive fluorime[1]tric" method" for" the" determination" of" curcumin" using" the enhancement of mixed micelle[J]. Journal of Fluorescence, 2006, 16(1): 53-59.
PARK" C," MEGHANI" N," LOEBENBERG" R, et al." Fatty acid chain length impacts nanonizing capacity of albumin[1]fatty acid" nanomicelles:" Enhanced" physicochemical"" prop[1]erty" and" cellular" delivery" of" poorly" water-soluble" drug[J]. European Journal of Pharmaceutics and Biopharmaceutics, 2020, 152: 257-269.
WANG" Y" J," PAN" M" H," CHENG" A" L, et al." Stability" of curcumin" in" buffer" solutions" and" characterization" of" its degradation" products[J]. Journal" of" Pharmaceutical" and Biomedical Analysis, 1997, 15(12): 1867-1876.
MORALES" N" P," SIRIJAROONWONG" S," YAMANONT P, et al. Electron paramagnetic resonance study of the free radical scavenging capacity of curcumin and its demethoxy and hydrogenated derivatives[J]. Biological amp; Pharmaceu[1]tical Bulletin, 2015, 38(10): 1478-1483.
盧藝惠. 低共熔介質中姜黃素的提取及其納米顆粒的性 質研究[D]. 江蘇淮安: 淮陰工學院, 2021.
郝興坤, 鄭雨晴, 王倩, 等. 吐溫表面活性劑囊泡對姜黃素 的包載作用[J]. 化學通報, 2021, 84(11): 1243-1247.[24]

