NRG-1通過(guò)SIRT1-NOX2通路減輕血管緊張素Ⅱ誘導(dǎo)的心肌肥大
王有恒 王學(xué)惠
高血壓是心血管疾病的誘因之一,且高血壓發(fā)生率逐年升高[1]。多項(xiàng)研究表明,長(zhǎng)期高血壓可通過(guò)心肌細(xì)胞氧化應(yīng)激、心肌纖維化引起心肌肥大,最終導(dǎo)致心力衰竭[2]。血管緊張素Ⅱ (angiotensin-Ⅱ, Ang-Ⅱ) 是哺乳動(dòng)物體內(nèi)重要的血壓及體液調(diào)節(jié)激素,是腎素-血管緊張素-醛固酮系統(tǒng)(renin-angiotensin-aldosterone,RAAS)的關(guān)鍵效應(yīng)分子[3]。長(zhǎng)期的Ang-Ⅱ水平升高導(dǎo)致心肌肥大、氧化應(yīng)激、纖維化等,促進(jìn)心力衰竭發(fā)生,并激活多種參與心肌肥大的信號(hào)分子,包括沉默信息調(diào)節(jié)因子(silent information regulator,SIRT1)通路、絲裂原活化蛋白激酶(mitogen activated protein kinase,MAPK) 信號(hào)通路等[2,4,5]。過(guò)量的Ang-Ⅱ可導(dǎo)致心肌細(xì)胞中活性氧(reactive oxygen species,ROS)的產(chǎn)生同時(shí)增加心肌細(xì)胞氧化應(yīng)激水平,抑制SIRT1通路[6]。
神經(jīng)調(diào)節(jié)蛋白1(neuregulin 1,NRG-1)是一種從內(nèi)皮細(xì)胞釋放的心臟活性因子,對(duì)心臟發(fā)育、結(jié)構(gòu)和心臟功能完整性是不可或缺的[7]。研究表明,NRG-1通過(guò)促進(jìn)擴(kuò)張型心肌病心肌血管生成來(lái)緩解糖尿病或冠狀動(dòng)脈疾病血管生成反應(yīng)受損[8]。但是,目前NRG-1對(duì)Ang-Ⅱ所誘導(dǎo)的心肌肥大研究較少,且具體機(jī)制尚未完全闡明。基于以上背景,本研究通過(guò)Ang-Ⅱ誘導(dǎo)H9C2細(xì)胞肥大模型,觀察NRG-1處理后對(duì)心肌肥大的影響,并探索其作用機(jī)制,為NRG-1的臨床應(yīng)用提供實(shí)驗(yàn)依據(jù)。
材料與方法
1.藥物、試劑與儀器:NRG-1購(gòu)自以色列ProSpec-Tany TechnoGene公司(貨號(hào):CYT-407),用高壓滅菌后的純水稀釋成濃度為10μmol/L的母液,分裝至EP管中,-80℃冰箱凍存?zhèn)溆谩ng-Ⅱ購(gòu)自鄭州遠(yuǎn)東生物科技有限公司,使用純水稀釋成10mmol/L母液,分裝至EP管中,-80℃冰箱凍存?zhèn)溆谩APDH蛋白抗體購(gòu)自美國(guó)Proteintech 公司;心房鈉尿肽(atrial natriuretic peptide,ANP)、腦鈉肽(brain natriuretic peptide,BNP)、超氧化物歧化酶1(superoxide dismutase 1,SOD1)、SIRT1、NADPH氧化酶2(NADPH oxidase isoform,NOX2)蛋白抗體購(gòu)自萬(wàn)類生物公司;線粒體膜電位試劑盒、鬼筆環(huán)肽染色試劑盒、活性氧檢測(cè)試劑盒、BCA蛋白定量試劑盒均購(gòu)自上海碧云天生物有限公司;1%青霉素/鏈霉素、10%胎牛血清、DMEM培養(yǎng)基購(gòu)自美國(guó)Science Cell公司。CO2培養(yǎng)箱購(gòu)自美國(guó) Thermo 公司;低速離心機(jī)購(gòu)自美國(guó)Thermo 公司;酶標(biāo)儀購(gòu)自美谷分子儀器有限公司;光學(xué)相差顯微鏡購(gòu)自日本Nikon 公司;恒溫孵育箱購(gòu)自中國(guó)常州國(guó)華有限公司、電子天平、-80℃冰箱購(gòu)自美國(guó)Thermo Forma公司;電泳系統(tǒng)(BIO-RAD)、搖床購(gòu)自中國(guó)其林貝爾儀器制造公司;超凈工作臺(tái)購(gòu)自中國(guó)蘇州凈化公司;化學(xué)發(fā)光熒光成像系統(tǒng) Amersham Imager 600購(gòu)自美國(guó) GE 公司。
2.細(xì)胞系和細(xì)胞培養(yǎng):大鼠心肌細(xì)胞系H9C2購(gòu)自中國(guó)科學(xué)院細(xì)胞庫(kù)(上海)(ATCC編號(hào): CRL-1446)。細(xì)胞用10%胎牛血清及1%青霉素/鏈霉素的DMEM培養(yǎng)基培養(yǎng)。培養(yǎng)條件,37℃、5%的CO2。使用胰蛋白酶進(jìn)行消化傳代,細(xì)胞傳代3次后進(jìn)行實(shí)驗(yàn),接種于細(xì)胞培養(yǎng)板中,當(dāng)細(xì)胞密度長(zhǎng)至70%左右加入1μmol/L Ang-Ⅱ繼續(xù)培養(yǎng)24h來(lái)誘導(dǎo)細(xì)胞肥大。
3.CCK-8 試劑盒檢測(cè) H9C2 細(xì)胞活力:將H9C2細(xì)胞接種于96孔板中,每孔接種7000個(gè)細(xì)胞,孵育24h,加入不同濃度的Ang-Ⅱ(0、0.25、0.5、0.75、1、1.25μmol/L)及NRG-1(0、5、10、15、20、25nmol/L)進(jìn)行處理,每個(gè)濃度設(shè)置6個(gè)復(fù)孔,繼續(xù)培養(yǎng)24h,隨后加入100μl培養(yǎng)基洗滌2~3遍,加入10μl的CCK-8試劑,繼續(xù)孵育4h,用酶標(biāo)儀檢測(cè)450nm處的吸光度并進(jìn)行統(tǒng)計(jì)學(xué)分析,實(shí)驗(yàn)重復(fù)3次。
4.H9C2 細(xì)胞骨架染色:將細(xì)胞接種于6孔板中,待使用不用藥物處理后,使用PBS配制3.7%甲醛(避免使用含有甲醇的甲醛)溶液室溫固定細(xì)胞約10~20min。使用1% Triton X-100的PBS洗滌2~4次,每次5min。然后使用含有5%BSA和0.1% Triton X-100的PBS按照1∶100的比例稀釋鬼筆環(huán)肽母液即為工作液,每孔中加入1ml工作液,室溫避光孵育30~60min,使用0.1% Triton X-100的PBS洗滌2~4次,每次5min,隨后熒光顯微鏡進(jìn)行觀察并拍照。使用Image-J軟件進(jìn)行分析并計(jì)算細(xì)胞表面積。每組測(cè)量30個(gè)細(xì)胞進(jìn)行測(cè)量取平均值。
5.檢測(cè)ROS含量:使用無(wú)血清培養(yǎng)基稀釋DCFH-DA母液(10mmol/L)至終濃度(10μmol/L)作為工作液。PBS洗滌分別使用不同藥物處理過(guò)的細(xì)胞,加入DCFH-DA工作液1ml,放入培養(yǎng)箱中繼續(xù)孵育20min,然后使用無(wú)血清養(yǎng)基洗滌細(xì)胞3遍,使用熒光顯微鏡觀察并拍照,使用Image-J軟件進(jìn)行熒光強(qiáng)度測(cè)定。
6.JC-1檢測(cè)細(xì)胞線粒體膜電位:將細(xì)胞接種于6孔板中,配置JC-1工作液:將母液(×200)加入JC-1緩沖液中稀釋200倍配置成為工作液待用。PBS洗滌分別使用不同藥物處理過(guò)的細(xì)胞,加入JC-1工作液1ml,放入培養(yǎng)箱中繼續(xù)孵育20min,然后使用無(wú)血清養(yǎng)基進(jìn)行洗滌,用熒光顯微鏡觀察并拍照,使用Image-J軟件進(jìn)行熒光強(qiáng)度測(cè)定。
7.Western blot法檢測(cè)細(xì)胞中ANP、BNP、SOD1、SIRT1、NOX2蛋白表達(dá):將接種于6孔板中給予相應(yīng)處理后的細(xì)胞,使用PBS沖洗2遍,加入裂解液,使用超聲裂解儀裂解4次,100℃煮蛋白10min使蛋白變性后,冷卻至室溫,離心2min,置于-80℃冰箱中備用。BCA 法測(cè)定蛋白濃度。根據(jù)蛋白濃度調(diào)整上樣量后進(jìn)行電泳。電泳結(jié)束后行濕法轉(zhuǎn)膜,按照1∶1000比例配置相應(yīng)抗體后,一抗孵育過(guò)夜后,使用TBST洗膜3遍,孵育二抗1.0~1.5h,再次用 TBST 洗滌 3 次,配置顯色液曝光。Image-J 軟件分析其灰度值,以目標(biāo)蛋白條帶灰度值/內(nèi)參(GAPDH)灰度值表示相應(yīng)目的蛋白。
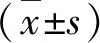
結(jié) 果
1.Ang-Ⅱ及NRG-1對(duì)H9C2細(xì)胞活力的影響:將H9C2細(xì)胞接種于96孔板中,加入不同濃度的Ang-Ⅱ進(jìn)行處理24h,檢測(cè)H9C2細(xì)胞活性。結(jié)果顯示,與空白組比較,隨著Ang-Ⅱ濃度升高,細(xì)胞活力先升高后降低。在1μmol/L Ang-Ⅱ處理細(xì)胞時(shí)活力接近正常水平,選取1μmol/L為實(shí)驗(yàn)濃度,并驗(yàn)證其對(duì)細(xì)胞表面積的影響。同時(shí)測(cè)定不同濃度NRG-1對(duì)細(xì)胞活力的影響,發(fā)現(xiàn)25nmol/L NRG-1對(duì)細(xì)胞具有損傷作用,選取20nmol/L為實(shí)驗(yàn)濃度進(jìn)行后續(xù)實(shí)驗(yàn)(圖1)。
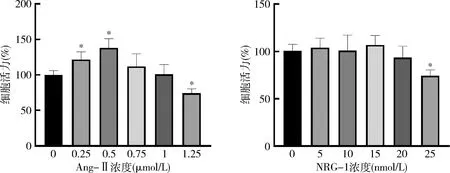
圖1 Ang-Ⅱ與NRG-1處理H9C2細(xì)胞后檢測(cè)其細(xì)胞活力
2.NRG-1對(duì)H9C2細(xì)胞表面積的影響:經(jīng)Ang-Ⅱ(1μmol/L)處理24h后,檢測(cè)H9C2細(xì)胞面積。與空白組比較,模型組細(xì)胞表面積明顯增加(P<0.05),使用濃度為20nmol/L的NRG-1預(yù)處理后,可改善Ang-Ⅱ引起的心肌細(xì)胞表面積增加, 經(jīng)過(guò)NRG-1處理的Ang-Ⅱ+NRG-1組vs模型組細(xì)胞面積為(860.0±101.4μm2vs 1335.6±165.5μm2,圖2)。
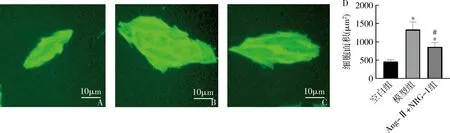
圖2 NRG-1對(duì)Ang-Ⅱ處理后的H9C2細(xì)胞表面積的影響(×400)
3.NRG-1對(duì)Ang-Ⅱ誘導(dǎo)的H9C2細(xì)胞肥大標(biāo)志物的影響:經(jīng)Ang-Ⅱ(1μmol/L)處理24h后,檢測(cè)ANP、BNP肥大相關(guān)蛋白表達(dá)。與空白組比較,模型組ANP、BNP表達(dá)增加(P<0.05)。NRG-1(20nmol/L)可以抑制Ang-Ⅱ誘導(dǎo)的ANP、BNP蛋白表達(dá)(P<0.05),NRG-1能夠有效地抑制Ang-Ⅱ誘發(fā)的心肌肥大(圖3)。
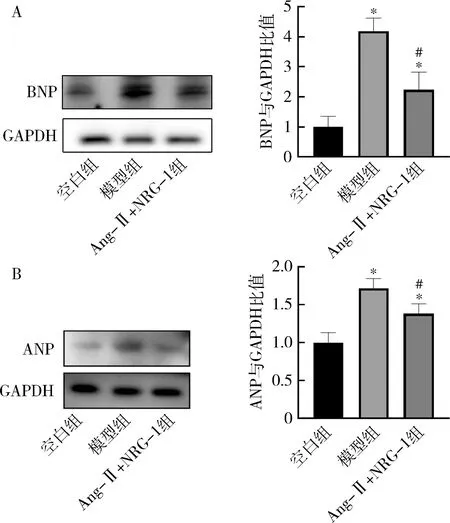
圖3 NRG-1對(duì)Ang-Ⅱ誘導(dǎo)的H9C2細(xì)胞肥大標(biāo)志物表達(dá)的影響
4.NRG-1對(duì)Ang-Ⅱ誘導(dǎo)的H9C2細(xì)胞線粒體膜電位的影響:經(jīng)Ang-Ⅱ(1μmol/L)處理24h后,檢測(cè)H9C2細(xì)胞線粒體膜電位水平。與空白組比較,
模型組可檢測(cè)到線粒體膜電位的下降(P<0.05),而使用NRG-1(20nmol/L)處理后,Ang-Ⅱ所誘導(dǎo)的線粒體膜電位下降明顯逆轉(zhuǎn)(P<0.05,圖4)。
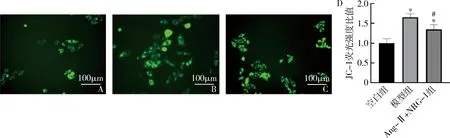
圖4 NRG-1對(duì)Ang-Ⅱ誘導(dǎo)的H9C2細(xì)胞線粒體膜電位的影響(×40)
5.NRG-1對(duì)Ang-Ⅱ誘導(dǎo)的H9C2細(xì)胞ROS的影響:經(jīng)Ang-Ⅱ(1μmol/L)處理24h后,檢測(cè)H9C2細(xì)胞內(nèi)ROS水平。模型組較空白組ROS含量增加(P<0.05),與模型組比較,NRG-1(20nmol/L)組ROS含量較Ang-Ⅱ組明顯下降(P<0.05,圖5)。
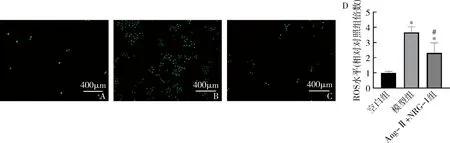
圖5 NRG-1對(duì)Ang-Ⅱ誘導(dǎo)的心肌細(xì)胞內(nèi)ROS表達(dá)的影響(×10)
6.NRG-1對(duì)Ang-Ⅱ誘導(dǎo)的H9C2細(xì)胞氧化應(yīng)激的影響:經(jīng)Ang-Ⅱ(1μmol/L)處理24h后,檢測(cè)NOX2和SOD1氧化應(yīng)激相關(guān)蛋白的表達(dá)水平。NOX2是常見(jiàn)的產(chǎn)生ROS的蛋白,而SOD1是常見(jiàn)的抗氧化蛋白。與對(duì)照組比較,模型組NOX2明顯增加,SOD1顯著降低,而使用NRG-1預(yù)處理后可顯著抑制NOX2的表達(dá),同時(shí)促進(jìn)抗氧化蛋白SOD1的表達(dá)(圖6)。

圖6 NRG-1對(duì)Ang-Ⅱ誘導(dǎo)的H9C2細(xì)胞氧化應(yīng)激水平的影響
7.NRG-1對(duì)H9C2細(xì)胞SIRT1蛋白表達(dá)的影響:經(jīng)Ang-Ⅱ不同濃度(1μmol/L和2μmol/L)處理后,SIRT1表達(dá)顯著下降(P<0.05),但不同濃度Ang-Ⅱ之間處理后SIRT1水平比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。同時(shí)經(jīng)Ang-Ⅱ(1μmol/L)處理24h后,檢測(cè)SIRT1蛋白表達(dá)水平,顯示在Ang-Ⅱ處理后,SIRT1蛋白表達(dá)下降(P<0.05),然而NRG-1(20nmol/L)預(yù)處理后, SIRT1蛋白表達(dá)較模型組增加(P<0.05,圖7)。
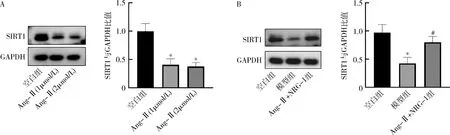
圖7 NRG-1對(duì)Ang-Ⅱ誘導(dǎo)的H9C2細(xì)胞SIRT1蛋白水平的影響
8.SIRT1抑制劑對(duì)H9C2細(xì)胞NOX2蛋白表達(dá)的影響:為進(jìn)一步驗(yàn)證NRG-1的保護(hù)機(jī)制,使用SIRT1抑制劑(EX527)處理H9C2細(xì)胞24h,監(jiān)測(cè)H9C2細(xì)胞中SIRT1表達(dá)顯著下調(diào)(P<0.05)。同時(shí)驗(yàn)證了通路相關(guān)蛋白NOX2表達(dá),在EX527存在的情況下,NOX2蛋白表達(dá)顯著增加(P<0.05,圖8)。
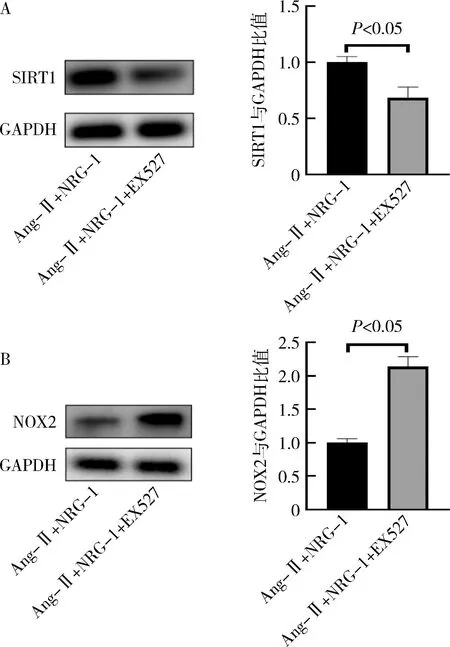
圖8 SIRT1抑制劑EX527對(duì)SIRT1及NOX2蛋白表達(dá)的影響
討 論
多種心臟疾病如高血壓、冠心病、心臟瓣膜病等都可引起心肌肥大,最終導(dǎo)致心力衰竭。病理性心肌肥大是心力衰竭的機(jī)制之一[2]。因此,研究心肌肥大的潛在機(jī)制對(duì)預(yù)防心力衰竭具有重要意義。Ang-Ⅱ?qū)儆赗AAS系統(tǒng),是心臟重塑和心血管疾病的關(guān)鍵介質(zhì)。生理濃度的Ang-Ⅱ?qū)π难芟到y(tǒng)是有益的,但是Ang-Ⅱ過(guò)度分泌引起的心肌纖維化和肥大是導(dǎo)致心臟重構(gòu)的主要因素[9]。Ang-Ⅱ可以作用于心肌細(xì)胞,導(dǎo)致ANP、BNP水平增加。該指標(biāo)已被認(rèn)為可以反映心肌肥大程度及心室收縮和舒張功能情況。本研究使用Ang-Ⅱ處理H9C2細(xì)胞,構(gòu)建心肌細(xì)胞肥大模型,探究NRG-1是否改善心肌肥大并探討其潛在機(jī)制。
研究表明,氧化應(yīng)激是心肌肥大病理過(guò)程中的關(guān)鍵環(huán)節(jié)[10]。氧化應(yīng)激是氧化與抗氧化系統(tǒng)之間失衡的結(jié)果[11]。心血管系統(tǒng)中,ROS主要來(lái)源于線粒體,線粒體功能下降會(huì)導(dǎo)致ROS 產(chǎn)生過(guò)多,增加氧化應(yīng)激水平[12]。NADPH氧化酶與ROS生成密切相關(guān)[13]。NOX2在ROS的生成中起到電子供體的作用[14]。Ang-Ⅱ可以增加NOX2表達(dá),損傷線粒體功能[15]。研究表明,NOX2可加重高脂飲食誘導(dǎo)的小鼠心肌肥厚,其機(jī)制是通過(guò)增加ROS的產(chǎn)生,降低氧化應(yīng)激水平,然而在NOX2基因敲除小鼠中,高脂飲食誘導(dǎo)的小鼠心肌肥厚顯著減輕[16]。
SOD1可以與鋅和銅離子結(jié)合,是體內(nèi)負(fù)責(zé)破壞自由基的三種超氧化物歧化酶之一。作為體內(nèi)一種重要的抗氧化物質(zhì),其可以清除體內(nèi)的ROS[17]。研究表明,在Ang-Ⅱ所誘導(dǎo)的心肌肥大過(guò)程中,SOD1被逐漸消耗,導(dǎo)致ROS 水平增加,引起心肌細(xì)胞損傷[18]。炎癥在心肌肥大中同樣起著至關(guān)重要的作用。NLRP3是炎癥通路中的關(guān)鍵介質(zhì)之一。ROS在整個(gè)NLRP3炎性小體激活過(guò)程中是不可或缺的。ROS可以調(diào)節(jié)NLRP3的啟動(dòng)環(huán)節(jié),進(jìn)而減少白細(xì)胞介素(interleukin,IL)-1β和IL-18的產(chǎn)生,減少炎性反應(yīng)[4]。因此,抑制ROS水平,可以從多方面抑制心肌肥大。
sirtuins是Ⅲ類組蛋白去乙酰基酶,已在人類中發(fā)現(xiàn)了7種Sirtuins亞型,即SIRT1、SIRT2、SIRT3、SIRT4、SIRT5、SIRT6和SIRT7。其中SIRT1研究得最多,它也被稱為核蛋白[19]。SIRT1參與ROS的產(chǎn)生與消耗,其機(jī)制是通過(guò)調(diào)節(jié)NOX2、SOD1在內(nèi)產(chǎn)生和消耗ROS有關(guān)的酶[20,21]。因此,調(diào)節(jié)SIRT1的水平可能成為治療心肌肥大的新靶點(diǎn)[22]。
NRG-1是一種內(nèi)皮細(xì)胞釋放的心臟活性因子,對(duì)心臟發(fā)育、結(jié)構(gòu)和功能是不可或缺的[23],但其改善心肌重構(gòu)的具體分子機(jī)制尚未完全闡明。本實(shí)驗(yàn)中應(yīng)用Ang-Ⅱ誘導(dǎo)心肌細(xì)胞肥大,設(shè)置空白組、模型組、治療組測(cè)定心肌細(xì)胞表面積、線粒體膜電位水平、ROS水平及ANP、BNP、SIRT1、SOD1、NOX2蛋白表達(dá),進(jìn)而探討NRG-1抑制心肌肥大的作用機(jī)制。Ang-Ⅱ誘導(dǎo)的心肌肥大模型中,可以觀察到細(xì)胞表面積增加,線粒體膜電位下降,ANP、BNP、NOX2表達(dá)增加,SIRT1、SOD1表達(dá)下降,而NRG-1能夠有效緩解Ang-Ⅱ引起的變化,表明NRG-1對(duì)Ang-Ⅱ誘導(dǎo)的心肌肥大具有明顯的保護(hù)作用。而使用EX527處理后,NRG-1改善氧化應(yīng)激的能力下降,因此,NRG-1抑制Ang-Ⅱ所致的心肌肥大可能部分是通過(guò)SIRT1-NOX2通路所實(shí)現(xiàn)的。
綜上所述,本實(shí)驗(yàn)驗(yàn)證了NRG-1抗心肌細(xì)胞肥大的作用,同時(shí)了發(fā)現(xiàn)了SIRT1-NOX2通路可能是NRG-1抗心肌肥大潛在機(jī)制之一,但是不能排除NRG-1通過(guò)其他非特異性機(jī)制改善心肌重構(gòu),需要開展進(jìn)一步研究。
利益沖突聲明:所有作者均聲明不存在利益沖突。

