基于BV-2小膠質細胞模型導向分離糙葉五加根的化學成分
陳 楊,肖 瑾,蔣詩琴,羅 姣,劉向前
基于BV-2小膠質細胞模型導向分離糙葉五加根的化學成分
陳 楊,肖 瑾,蔣詩琴,羅 姣,劉向前*
湖南中醫藥大學藥學院,湖南 長沙 410208
基于BV-2小膠質細胞模型導向分離糙葉五加根的化學成分。采用脂多糖(lipopolysaccharide,LPS)誘導的BV-2小膠質細胞建立神經炎癥模型,以MTT法測定細胞毒性,對糙葉五加根的正己烷、醋酸乙酯、正丁醇提取部位進行活性篩選,確定活性部位,根據篩選結果對最佳活性部位進一步采用柱色譜、D101大孔樹脂、半制備液相等方法進行分離純化,根據理化性質和所得到的光譜數據,鑒定化合物的結構。并對其中得到的部分化合物進行活性驗證。糙葉五加醋酸乙酯提取物部位的活性最佳,從中分離得到17個化合物,分別鑒定為 (+)-芝麻素(1)、松柏醛(2)、acuminatolide(3)、芝麻素酮(4)、10-二十九烷醇(5)、(±)--甲基-4-羥基癸酰胺(6)、羅漢松脂素(7)、(1,2,5,6)-6-(3,4-dihydroxyphenyl)-2-(3,4-methylenedioxyphenyl)-3,7-dioxabicyclo[3,3,0]octane(8)、1-辛烯(9)、胡椒醇(10)、(?)-松脂醇(11)、榕醛(12)、丁香醛(13)、丁香脂醇(14)、(?)-表丁香脂素(15)、原兒茶醛(16)、原兒茶酸(17)。其中分離得到的(+)-芝麻素和丁香醛在細胞耐受濃度(5~80 μmol/L)下能減少LPS誘導的BV-2小膠質細胞中一氧化氮(NO)的釋放,且呈劑量相關性。化合物3~10、12、15首次從五加科植物中分離得到,化合物2~12、15~16首次從糙葉五加中分離得到。糙葉五加根中的化合物芝麻素和丁香醛具有潛在的抗神經炎活性。
糙葉五加;抗神經炎活性;五加屬植物;木脂素類;芝麻素;丁香醛
神經炎癥對包括阿爾茨海默癥(Alzheimer’s disease,AD)、帕金森癥(Parkinson’s disease,PD)等在內的多種急性和慢性神經退行性疾病的發生有著密切聯系[1-3],神經炎癥[4]產生的主要病因有膠質細胞的激活、血腦屏障的破壞以及外周免疫細胞進入腦實質內等,膠質細胞的過度激活會導致細胞釋放多種炎性因子,如一氧化氮(NO)、腫瘤壞死因子及前列腺素E2等,造成神經元的損傷和變性。脂多糖(lipopolysaccharide,LPS)具有很強的致炎效應,但對神經元不會產生直接的不良反應,而是通過產生大量的腫瘤壞死因子,從而激活膠質細胞間接引起炎癥反應。此過程也常被用于體外炎癥模型的建立,使用LPS刺激BV-2小膠質細胞,使其活化分泌大量致炎因子如NO、腫瘤壞死因子、前列腺素E2等從而觸發炎癥反應[5-6],其中NO常被用于判斷炎癥反應是否發生的重要指標。
糙葉五加(Oliv.) Harms又名亨利五加,為中國特有的五加屬植物,廣泛分布于湖南、湖北、浙江、安徽、甘肅、四川、河北、山西、陜西等地,資源豐富,生于林緣或灌叢中,其根皮作為“五加皮”收載于《湖南省中藥材標準》。糙葉五加味辛,性溫;具有祛風濕、補肝腎、活血化瘀、壯筋骨等功效,主要用于治療風濕痹痛、拘攣麻木、筋骨痞軟、水腫、跌打損傷、疝氣腹痛等[7-8]。本課題組[9-11]前期圍繞糙葉五加葉、莖、花、果實做了大量相關研究,已證明糙葉五加地上部分中分離的部分化合物具有抗神經炎活性。為了更全面地了解糙葉五加各部分的藥理活性,本研究利用BV-2小膠質細胞的體外炎癥模型對糙葉五加根的正己烷提取物(AH-RH)、醋酸乙酯提取物(AH-RE)、正丁醇提取物(AH-RB)進行細胞毒性實驗和抗炎活性篩選,從活性較好的醋酸乙酯部位(AH-RE)分離得到17個化合物,分別鑒定為 (+)-芝麻素((+)-sesamin,1)、松柏醛(coniferaldehyde,2)、acuminatolide(3)、芝麻素酮(sesaminone,4)、10-二十九烷醇(10-nonacosanol,5)、(±)--甲基-4-羥基癸酰胺(rac--methyl-4-hydroxydecanamide,6)、羅漢松脂素(matairesinol,7)、(1,2,5,6)-6-(3,4-dihydroxyphenyl)-2-(3,4-methylenedioxyphenyl)-3,7-dioxabicyclo[3,3,0]octane((1,2,5,6)-6-(3,4-dihydroxyphenyl)-2-(3,4-methylenedioxyphenyl)-3,7-dioxabicyclo[3,3,0]octane,8)、1-辛烯(1-octene,9)、胡椒醇(piperitol,10)、(?)-松脂醇 [(?)-pinoresinol,11]、榕醛(ficusal,12)、丁香醛(syringaldehyde,13)、丁香脂醇(syringaresinol,14)、(?)-表丁香脂素[(?)-episyringaresinol,15]、原兒茶醛(protocatechuyl aldehyde,16)、原兒茶酸(protocatechuic acid,17),其中化合物3~10、12、15首次從五加科植物中分離得到,化合物2~12、15~16首次從糙葉五加中分離得到。進一步對分離純化的化合物1和化合物13進行細胞毒實驗和抗神經炎活性研究,發現兩者都具有一定的抗神經炎活性,為深入開發應用糙葉五加資源及豐富治療神經炎潛在藥物來源提供了理論依據。
1 材料
1.1 儀器與材料
二氧化碳細胞培養箱(美國賽默飛公司);酶標儀(美國賽默飛公司);超導核磁共振儀(德國Bruker公司);暗箱三用紫外分析儀(上海嘉鵬科技有限公司);LC-10A高效液相色譜儀(日本島津公司);LC-16P半制備高效液相色譜儀(日本島津公司);多級閃蒸器(上海釩幟精密設備有限公司);Kromasil 100-5-C18(250 mm×4.6 mm,5 μm;瑞典Nouryon公司);5C18-MS-II(250 mm×10 mm,5 μm;日本Cosmosil公司);96孔板(海門市天龍實驗器材廠)。
1.2 藥品試劑
DMEM培養基、胎牛血清(FBS)購自GibcoBRL Co.;LPS、3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮、唑溴鹽(MTT)、二甲基亞砜(DMSO)、Griess試劑購自Sigma-Aldrich;正相色譜硅膠(200~300目)、薄層色譜硅膠H、薄層色譜硅膠G購自青島海洋化工有限公司;大孔樹脂(D-101,天津允開樹脂科技有限公司);羧甲基纖維素鈉(上海山浦化工有限公司);YMC Gel ODS-A-HG(50 μm,日本YMC公司)。紫鉚因(butein)為韓國圓光大學藥學院及天然產物研究室自制(HPLC檢測質量分數≥98.5%)。
1.3 藥材
糙葉五加根于2019年8月采自湖南省婁底市新化縣,經湖南中醫藥大學藥學院劉向前教授鑒定為五加科五加屬植物糙葉五加(Oliv.) Harms的根。
1.4 細胞株
小鼠BV-2小膠質細胞來源于韓國圓光大學Park Hyun教授實驗室。
2 方法
2.1 不同極性溶劑提取物的制備
取糙葉五加根干燥粉碎(10.0 kg),依次用正己烷、醋酸乙酯、正丁醇加熱回流提取,濾過,濾液減壓回收溶劑得正己烷提取物(AH-RH,89.5 g)、醋酸乙酯提取物(AH-RE,112.0 g)和正丁醇提取物(AH-RB,206.2 g),取 10 mg精密稱定。
2.2 細胞培養
BV-2小膠質細胞用高糖培養基DMEM(含10%胎牛血清)培養,將培養基置于37 ℃、5%CO2的培養箱中恒溫培養至細胞對數生長期。
2.3 MTT法測定細胞毒性
采用 MTT 法,將對數生長期小膠質BV-2細胞接種于96孔板中(每孔1×105個細胞),置于37 ℃、5% CO2細胞培養箱中溫孵培養12 h后,給藥組分別加入不同質量濃度的正己烷、醋酸乙酯、正丁醇提取物(終質量濃度分別為50、100、200 μg/mL),加入LPS(1 μg/mL)進行誘導,陽性對照組中加入LPS以及10 μmol/L的對照品紫鉚因(butein)。對照組均不加入受試藥物及LPS,但加入體積分數為0.1%的DMSO,模型組加入LPS和培養液,空白組不含細胞只加入培養液。繼續溫孵培養12 h后,取100 μL上清液,加入終質量濃度為100 mg/mL的MTT,置于37 ℃、5% CO2細胞培養箱中孵育0.5 h。形成的甲臜鹽使用酸化異丙醇溶解,置搖床上低速振蕩10 min,在酶標儀540 nm處測定各孔吸光度()值,以未處理組細胞(對照組)的值所對應的細胞存活率為100%,計算細胞存活率。
細胞存活率=(實驗-空白)/(對照-空白)
實驗組為給藥組、模型組或陽性對照組
2.4 對NO的抑制作用
采用Griess法檢測各提取物對LPS誘導下的BV-2小膠質細胞分泌NO的抑制作用。取對數生長期的小膠質(BV-2)細胞,以約1×105個/接孔種于96孔板中,在37℃、5%CO2濃度的培養箱中培養12 h后,進行給藥處理。設定對照組、模型組、陽性對照組及給藥組,陽性對照組和給藥組分別加入100 μL butein及不同濃度的樣品溶液,繼續在該條件下進行培養1 h后,除對照組外(加入等體積DMSO),其余各組均加入100 μL LPS(1 μg/mL)進行刺激,溫孵12 h后,吸取各處理組細胞培養上清液(100 μL)與相同體積的Griess試劑以十字交叉法混勻,在室溫下避光反應5~10 min,在540 nm處使用酶標儀測定混合物的值,計算NO含量。每組設置3個平行實驗。
NO含量=1-(給藥-對照)/對照
2.5 提取與分離
干燥的糙葉五加根(10.0 kg)粉碎后,用醋酸乙酯加熱回流提取2次(2 h/次),合并2次提取液并減壓回收溶劑,濃縮得到醋酸乙酯部位(112.0 g)浸膏。
醋酸乙酯部位(110.0 g)經正相硅膠柱色譜依次以石油醚-醋酸乙酯(100∶1→1∶1)、二氯甲烷-甲醇(200∶1→1∶1)梯度洗脫進行初分,2個洗脫系統分別得到15個組分(Fr. 1.1~1.15)和13個組分(Fr. 2.1~2.13)。
其中Fr. 1.8(石油醚-醋酸乙酯5∶1)經過反復重結晶和純化得到化合物1(41.4 mg);Fr. 1.11(石油醚-醋酸乙酯1∶1)經過反相硅膠柱色譜(20%~100%甲醇梯度洗脫)得到8個亞組分Fr. 1.11.1~1.11.8,Fr. 1.11.4經反相硅膠柱色譜(40%甲醇等度洗脫)得到化合物2(2.5 mg),Fr. 1.11.5(45%甲醇等度洗脫)和Fr. 1.11.8(70%甲醇等度洗脫)分別經過半制備液相進一步純化得到化合物3(6.6 mg)和4(1 mg);Fr. 1.12(石油醚-醋酸乙酯1∶1)經過反相硅膠柱色譜(30%~100%甲醇梯度洗脫)得到5個亞組分Fr. 1.12.1~1.12.5,Fr. 1.12.3經過半制備液相(60%甲醇等度洗脫)得到化合物5(6.4 mg)和6(6.7 mg),Fr. 1.12.4(56%甲醇等度洗脫)和Fr. 1.12.5(50%甲醇等度洗脫)分別經過半制備液相進一步分離純化得到化合物7(24.7 mg)和8(1.6 mg);Fr. 1.13(石油醚-醋酸乙酯1∶1)經反相硅膠柱色譜(30%~100%甲醇梯度洗脫),得2個亞組分Fr. 1.13.1~1.13.2,這2個亞組分再分別經過半制備液相色譜(50%和60%甲醇等度洗脫)得到化合物9(0.4 mg)和10(11.9 mg);Fr. 1.14(石油醚-醋酸乙酯1∶1)經反相硅膠柱色譜(20%~100%甲醇梯度洗脫),得2個亞組分Fr. 1.14.1~1.14.2,其中Fr. 1.14.1經半制備液相色譜(56%甲醇等度洗脫)進一步純化得到化合物11(3.3 mg);Fr. 1.15(石油醚-醋酸乙酯1∶1)經反相硅膠柱色譜(10%~100%甲醇梯度洗脫),得4個亞組分EFr. 1.15.1~1.15.4,其中EFr. 1.15.2經半制備液相色譜(60%甲醇等度洗脫)進一步純化,得到化合物12(0.2 mg)。
Fr. 2.4(二氯甲烷-甲醇100∶1)經反相硅膠柱色譜(30%~100% 甲醇梯度洗脫),得2個亞組分Fr. 2.4.1~2.4.2,其中EFr. 2.4.1經半制備液相色譜(50%甲醇等度洗脫)分離得到化合物13(1.6 mg),Fr. 2.4.2 經半制備液相(50%甲醇等度洗脫)得到化合物14(10.5 mg)和15(1.4 mg);Fr. 2.7(二氯甲烷-甲醇100∶1)經反相硅膠柱色譜(30%~100%甲醇梯度洗脫),得2個亞組分EFr. 2.7.1~2.7.2,EFr. 2.7.1經半制備液相(42%甲醇等度洗脫)得到化合物16(2.5 mg);Fr. 2.8(二氯甲烷-甲醇50∶1)經反相硅膠柱色譜(30%~100%甲醇梯度洗脫),得3個亞組分EFr. 2.8.1~2.8.3,其中EFr. 2.8.2經半制備液相(48%甲醇等度洗脫)得到化合物17(4.8 mg)。
2.6 統計學分析
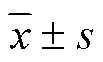
3 結果
3.1 結構鑒定
化合物1:白色針晶(醋酸乙酯)。1H-NMR (500 MHz, C3D6O): 6.90 (2H, d,= 1.7 Hz, H-2, 2?), 6.87 (2H, dd,= 8.0, 1.7 Hz, H-6, 6?), 6.80 (2H, d,= 7.9 Hz, H-5, 5?), 5.97 (4H, s, -OCH2O-×2), 4.68 (2H, d,= 4.1 Hz, H-7, 7?), 4.20 (2H, dd,= 9.1, 7.0 Hz, H-9α, 9?α), 3.82 (2H, dd,= 9.2, 3.8 Hz, H-9β, 9?β), 3.10~3.02 (2H, m, H-8, 8?);13C-NMR (125 MHz, C3D6O): 148.8 (C-4, 4?), 147.8 (C-3, 3?), 136.8 (C-1, 1?), 120.1 (C-6, 6?), 108.7 (C-5, 5?),107.3 (C-2, 2?), 101.9 (-OCH2O-×2), 86.4 (C-7, 7?), 72.2 (C-9, 9?), 55.3 (C-8, 8?)。以上數據與文獻報道基本一致[12],故鑒定化合物1為 (+)-芝麻素。
化合物2:黃色結晶粉末。1H-NMR (600 MHz, C3D6O): 9.64 (1H, d,= 7.7 Hz, H-1), 7.57 (1H, d,= 15.8 Hz, H-3), 7.38 (1H, d,= 2.0 Hz, H-2?), 7.21 (1H, dd,= 8.2, 2.0 Hz, H-6?), 6.92 (1H, d,= 8.2 Hz, H-5?), 6.65 (1H, dd,= 15.8, 7.7 Hz, H-2), 3.93 (3H, s, -OCH3)。13C-NMR (150 MHz, C3D6O): 193.9 (C-1), 154.0 (C-3), 150.8 (C-4?), 148.9 (C-3?), 127.5 (C-1?), 127.1 (C-2), 124.8 (C-6?), 116.2 (C-5?), 111.6 (C-2?), 56.4 (-OCH3)。以上數據與文獻報道基本一致[13],故鑒定化合物2為松柏醛。
化合物3:無色針晶(甲醇-水)。1H-NMR (600 MHz, CDCl3): 6.84 (1H, s, H-6), 6.79 (2H, s, H-2, 3), 5.97 (2H, s, -OCH2O), 4.60 (1H, d,= 6.8 Hz, H-7), 4.53~4.46 (1H, m, H-9β), 4.38~4.28 (2H, m, H-9?β, 9α), 4.19 (1H, dd,= 9.4, 3.7 Hz, H-9?α), 3.43 (1H, td,= 8.9, 3.8 Hz, H-8), 3.13~3.04 (1H, m, H-8?)。13C-NMR和DEPT譜圖數據提示有13個碳信號,分別對應結構中的13個碳原子。13C-NMR (150 MHz, CDCl3): 178.2 (C-7?), 148.4 (C-5), 147.9 (C-4), 132.9 (C-1), 119.8 (C-2), 108.5 (C-3), 106.5 (C-6), 101.4 (-OCH2O-), 86.2 (C-7), 70.2 (C-9), 69.9 (C-9?), 48.5 (C-8), 46.2 (C-8?)。以上數據與文獻報道基本一致[14],故鑒定化合物3為acuminatolide。
化合物4:淡黃色粉末。1H-NMR (600 MHz, CDCl3): 7.53 (1H, dd,= 8.2, 1.7 Hz, H-6), 7.45 (1H, d,= 1.7 Hz, H-2), 6.97 (1H, d,= 1.6 Hz, H-2?), 6.89 (1H, d,= 8.2 Hz, H-5), 6.84 (1H, dd,= 7.9, 1.5 Hz, H-6?), 6.78 (1H, d,= 7.9 Hz, H-5?), 6.07 (2H, s, 3, 4-OCH2O-), 5.96 (2H, s, 3?, 4?-OCH2O-), 4.60 (1H, d,= 9.0 Hz, H-7?), 4.29~4.24 (1H, m, H-9β), 4.16~4.14 (2H, m, H-9α), 4.14~4.12 (1H, m, H-8),3.73 (1H, dd,= 11.2, 4.8 Hz, H-9?β), 3.65 (1H, dd,= 11.2, 5.8 Hz, H-9?α), 2.89 (1H, m, H-8?);13C-NMR (150 MHz, CDCl3): 196.3 (C-7), 170.9 (C=O), 152.4 (C-4), 148.7 (C-3), 148.2 (C-3?), 147.7 (C-4?), 134.0 (C-1?), 131.5 (C-1), 124.9 (C-6), 120.6 (C-6?), 108.4 (C-2), 108.3 (C-5), 108.2 (C-5?), 107.3 (C-2?), 102.2 (-OCH2O-), 101.2 (-OCH2O-), 84.2 (C-7?), 71.1 (C-9), 63.2 (C-9?), 50.3 (C-8?), 49.6 (C-8)。以上數據與文獻報道基本一致[15],故鑒定化合物4為芝麻素酮。
化合物5:白色粉末。1H-NMR (600 MHz, CDCl3): 3.67 (1H, s, H-10), 0.89 (6H, t,= 6.6 Hz, CH, H-1, 29);13C-NMR (150 MHz, CDCl3): 71.1 (C-10), 37.1 (C-9, 11), 31.6 (C-3, 27), 24.9 (C-8, 12), 22.5 (C-2, 28), 14.0 (C-1, 29)。以上數據與文獻報道基本一致[16],故鑒定化合物5為10-nonacosamnol。
化合物6:黃色粉末。1H-NMR (600 MHz, CDCl3): 5.86 (1H, t,= 17.2 Hz, -NH), 3.69 (1H, s, H-4), 2.86 (1H, dd,= 18.0, 6.7 Hz, -OH), 2.54 (1H, dd,= 18.0, 3.9 Hz, H-1?), 2.35 (3H, m, H-2), 1.66 (4H, m, H-3), 1.56~1.49 (2H, m, H-5), 1.43~1.28 (8H, m, H-6~9), 0.91 (3H, t,= 6.8 Hz, H-10);13C-NMR (150 MHz, CDCl3): 174.8 (C-1), 71.8 (C-4), 37.7 (C-5), 33.2 (C-3), 32.2 (C-2), 31.6 (C-8), 29.0 (C-7), 28.9 (C-10), 27.8 (C-1?), 25.2 (C-6), 22.5 (C-9), 14.0 (C-11)。以上數據與文獻報道基本一致[17],故鑒定化合物6為 (±)--甲基-4-羥基癸酰胺。
化合物7:淡黃色油狀物。1H-NMR (600 MHz, C3D6O): 6.72 (1H, d,= 8.0 Hz, H-5?), 6.69 (1H, d,= 2.2 Hz, H-5), 6.68 (1H, d,= 2.0 Hz, H-2?), 6.58 (1H, d,= 2.0 Hz, H-6?), 6.57 (1H, d,= 2.0 Hz, H-2), 4.10 (1H, dd,= 8.8, 7.3 Hz, H-9a), 3.91~3.86 (1H, m, H-9b), 3.80 (3H, s, 3?-OCH3), 3.79 (3H, s, 3?-OCH3), 2.93 (1H, dd,= 14.0, 5.3 Hz, H-7?a), 2.68~2.60 (2H, m, H-8?), 2.54 (1H, d,= 2.4 Hz, H-7), 2.53~2.50 (1H, m, H-8)。13C-NMR和DEPT譜圖數據提示有20個碳信號,分別對應結構中的20個碳原子。13C-NMR (150 MHz, C3D6O): 179.0 (C-9?), 148.3 (C-3?), 148.3 (C-3), 146.2 (C-4?), 146.0 (C-4), 131.1 (C-1), 130.5 (C-1?), 122.9 (C-6?), 122.0 (C-6), 115.7 (C-5), 115.6 (C-5?), 113.7 (C-2?), 113.0 (C-2), 71.6 (C-9), 56.2 (3-OCH3), 56.2 (3?-OCH3), 47.0 (C-8?), 42.2 (C-8), 38.4 (C-7), 35.1 (C-7?)。以上數據與文獻報道基本一致[18-19],故鑒定化合物7為羅漢松脂素。
化合物8:1H-NMR (600 MHz, C3D6O): 6.92 (1H, d,= 1.7 Hz, H-2?), 6.89 (2H, m, H-5?), 6.81 (2H, m, H-6?), 6.73 (1H, m, H-2??), 4.66 (2H, dd,= 25.4, 4.8 Hz, H-2, 6), 4.21 (2H, m, H-4a, 8a), 3.81 (2H, m, H-4b, 8b), 3.06 (2H, m, H-1, 5)。13C-NMR和DEPT譜圖數據提示有19個碳信號,分別對應結構中的19個碳原子。13C-NMR (150 MHz, C3D6O): 147.9 (C-3?), 146.9 (C-4?), 143.8 (C-3??), 142.1 (C-4??), 136.1 (C-1?), 133.6 (C-1??), 119.2 (C-6?), 117.5 (C-6??), 114.4 (C-5??), 113.6 (C-2??), 107.8 (C-5?), 106.4 (C-2?), 101.1 (O-CH2-O), 85.6 (C-2), 85.5 (C-6), 71.5 (C-4), 71.1 (C-8), 54.6 (C-1), 54.3 (C-5)。以上數據與文獻報道基本一致[20],故鑒定化合物8為(1,2,5,6)-6-(3,4-dihydroxyphenyl)-2-(3,4-methylene-dioxyphenyl)-3,7- dioxabicyclo[3,3,0] octane。
化合物9:白色結晶(甲醇-水)。1H-NMR (600 MHz, CDCl3): 5.54 (2H, s, H-1), 3.98 (1H, s, H-2), 3.67 (1H, s, H-3)。13C-NMR和DEPT譜圖數據提示有8個碳信號,分別對應結構中的8個碳原子。13C-NMR (150 MHz, CDCl3): 143.3 (C-2), 114.0 (C-1), 36.7 (C-3), 31.9 (C-6), 29.7 (C-5), 29.4 (C-4), 22.7 (C-7), 14.1 (C-8)。以上數據與文獻報道基本一致[21],故鑒定化合物9為1-辛烯。
化合物10:白色粉末。1H-NMR (600 MHz, C3D6O): 6.93~6.84 (2H, m, H-2, 6?), 6.83-6.76 (2H, m, H-5, 3?), 6.71 (2H, d,= 8.0 Hz, H-6, 2?), 5.97 (2H, s, -OCH2O), 4.65 (2H, dd,= 24.9, 4.7 Hz, H-7, 7?), 4.22 (1H, d,= 6.3 Hz, H-9β), 4.17 (1H, d,= 6.3 Hz, H-9?β), 3.83~3.76 (3H, m, -OCH3), 3.04 (2H, brs, H-8, 8?)。13C-NMR (150 MHz, C3D6O): 148.8 (C-4?), 147.8 (C-4), 145.9 (C-3?), 145.2 (C-3), 137.0 (C-1?), 134.5 (C-1), 120.1 (C-6), 118.4 (C-2?), 114.2 (C-5?), 108.7 (C-5), 107.3 (C-2), 102.0 (-OCH2O-), 86.5 (C-7), 86.4 (C-7?), 72.4 (C-9), 72.0 (C-9?), 55.5 (-OCH3), 55.2 (C-8)。以上數據與文獻報道基本一致[22],故鑒定化合物10為胡椒醇。
化合物11:無色油狀物。1H-NMR (500 MHz, CD3OD), 6.95 (2H, d,= 1.9 Hz, H-2, H-2?), 6.81 (2H, dd,= 8.1, 2.0 Hz, H-6, 6?), 6.77 (2H, d,= 8.1 Hz, H-5, 5?), 4.71 (2H, d,= 4.4 Hz, H-7, 7?), 4.23 (2H, dd,= 9.1, 6.9 Hz, H-9a, 9?a), 3.86 (6H, s, 2×-OCH3), 3.77 (2H, dd,= 9.1, 3.7 Hz, H-9b, 9?b), 3.19~3.08 (2H, m, H-8, 8?)。13C-NMR (125 MHz, CD3OD), 149.1 (C-3, 3?), 147.3 (C-4, 4?), 133.8 (C-1, 1?), 120.1 (C-6, 6?), 116.1 (C-5, 5?), 110.9 (C-2, 2?), 87.5 (C-7, 7?), 72.6 (C-9, 9?), 56.4 (2×-OCH3), 55.4 (C-8, 8?)。以上數據與文獻報道基本一致[23],故鑒定化合物11為 (?)-松脂醇。
化合物12:淡黃色油狀物。1H-NMR (500 MHz, C3D6O): 9.84 (1H, s, H-7?), 7.53 (1H, dd,= 1.5, 1.0 Hz, H-2?), 7.43 (1H, d,= 1.5 Hz, H-6?), 7.06 (1H, d,= 2.0 Hz, H-2), 6.83 (1H, d,= 8.1 Hz, H-5), 6.80 (1H, dd,= 8.1, 2.2 Hz, H-6), 5.70 (1H, d,= 6.8 Hz, H-7), 3.93 (3H, s, 3?-OCH3), 3.85 (2H, d,= 5.1 Hz, H-9), 3.83 (3H, s, 3-OCH3), 3.63 (1H, m, H-8)。13C-NMR和DEPT數據證實了18個碳的存在。13C-NMR (125 MHz, C3D6O): 191.0 (C-7?), 154.9 (C-4?), 148.5 (C-4), 147.7 (C-3?), 145.8 (C-5?), 133.4 (C-1), 132.4 (C-1?), 131.2 (C-3), 121.5 (C-2?), 119.8 (C-6), 115.8 (C-5), 113.3 (C-6?), 110.6 (C-2), 89.9 (C-7), 64.2 (C-9), 56.3 (-OCH3), 56.3 (-OCH3), 53.8 (C-8)。以上數據與文獻報道基本一致[24-25],故鑒定化合物12為榕醛。
化合物13:白色粉末。1H-NMR (600 MHz, C3D6O): 9.82 (1H, s, -CHO), 7.24 (2H, s, H-2, 6), 3.92 (6H, s, -OCH3×2)。13C-NMR和DEPT譜圖數據提示有9個碳原子。13C-NMR (150 MHz, C3D6O): 191.1 (-CHO), 149.0 (C-3, 5), 143.2 (C-4), 129.1 (C-1), 107.8 (C-2, 6), 56.7 (OCH3×2)。以上數據與文獻報道基本一致[26],故鑒定化合物13為丁香醛。
化合物14:淡黃色油狀物。1H-NMR (600 MHz, C3D6O): 7.11 (2H, s, 4, 4?-OH), 6.68 (4H, s, H-2, 2?, 6, 6?), 4.67 (2H, d,= 2.9 Hz, H-7, 7?), 4.29~4.16 (2H, m, H-9, 9?), 3.82 (12H, s, OCH3-3, 3?, 5, 5?), 3.10 (2H, s, H-8, 8?)。13C-NMR和DEPT譜圖數據提示結構中有22個碳原子。13C-NMR (150 MHz, C3D6O), 148.7 (C-3, 3?, 5, 5?), 136.2 (C-4, 4?), 133.3 (C-1, 1?), 104.5 (C-2, 2?, 6, 6?), 86.8 (C-7, 7?), 72.4 (C-9, 9?), 56.7 (3, 3?-OCH3, C-5, 5?), 55.3 (C-8, 8?)。以上數據與文獻報道基本一致[27-28],故鑒定化合物14為丁香脂醇。
化合物15:白色粉末。1H-NMR (600 MHz, C3D6O): 7.08 (2H, d,= 13.3 Hz, H-2?, 6?), 6.69 (2H, s, H-2, H-6), 4.83 (1H, d,= 5.9 Hz, H-7), 4.36 (1H, d,= 7.0 Hz, H-7?), 4.13 (1H, d,= 9.5 Hz, H-9a), 3.86 (2H, dd,= 9.7, 3.5 Hz, H-9b, 9?b), 3.83 (12H, s, H-3, 3?, 5, 5?-OMe), 3.22 (1H, t,= 8.7 Hz, H-8)。13C-NMR和DEPT譜圖數據提示結構中有22個碳原子。13C-NMR (150 MHz, C3D6O): 148.7 (C-3?, 5?), 148.6 (C-3, 5), 136.3 (C-1?), 135.7 (C-4?), 133.4 (C-4), 130.4 (C-1), 104.5 (C-2?, 6?), 104.1 (C-2, 6), 88.7 (C-7?), 82.8 (C-7), 71.6 (C-9), 70.2 (C-9?), 56.7 (3, 3?, 5, 5?-OMe), 55.7 (C-8?), 50.9 (C-8)。以上數據與文獻報道基本一致[29],故鑒定化合物15為 (?)-表丁香脂素。
化合物16:灰白色粉末。1H-NMR (500 MHz, C3D6O), 9.78 (1H, s, -CHO), 7.36 (1H, d,= 1.9 Hz, H-2), 7.34 (1H, d,= 1.9 Hz, H-6), 7.00 (1H, d,= 7.9 Hz, H-5)。13C-NMR和DEPT譜圖數據提示有7個碳信號,分別對應結構中的7個碳原子。13C-NMR (125 MHz, C3D6O), 191.2 (-CHO), 152.3 (C-4), 146.4 (C-3), 131.0 (C-1), 125.5 (C-6), 116.1 (C-2), 115.1 (C-5)。以上數據與文獻報道基本一致[30-31],故鑒定化合物16為原兒茶醛。
化合物17:褐色結晶性粉末。1H-NMR (600 MHz, C3D6O): 7.53 (1H, s, H-2), 7.48 (1H, d,= 8.2 Hz, H-6), 6.90 (1H, d,= 8.2 Hz, H-5)。13C-NMR和DEPT譜圖數據提示有7個碳信號,分別對應結構中的7個碳原子。13C-NMR (150 MHz, C3D6O): 167.8 (-COOH), 150.7 (C-4), 145.5 (C-3), 123.7 (C-6), 123.1 (C-1), 117.5 (C-2), 115.7 (C-5)。以上數據與文獻報道基本一致[32],故鑒定化合物17為原兒茶酸。
3.2 糙葉五加根提取物抗神經炎活性篩選研究
3.2.1 糙葉五加根各提取物在LPS誘導的BV-2小膠質細胞模型下的細胞毒性 為了明確糙葉五加根AH-RH、AH-RE、AH-RB對BV-2細胞的影響,通過MTT法測定不同濃度的糙葉五加根各提取物有無細胞毒性,以確定安全的藥物濃度。MTT實驗表明(圖1),各組受試藥物的不同質量濃度均能提高由LPS誘導細胞炎癥所降低的細胞活力,且細胞存活率均大于60%,因此,可將50、100、200 μg/mL作為后續實驗所用藥物濃度梯度。
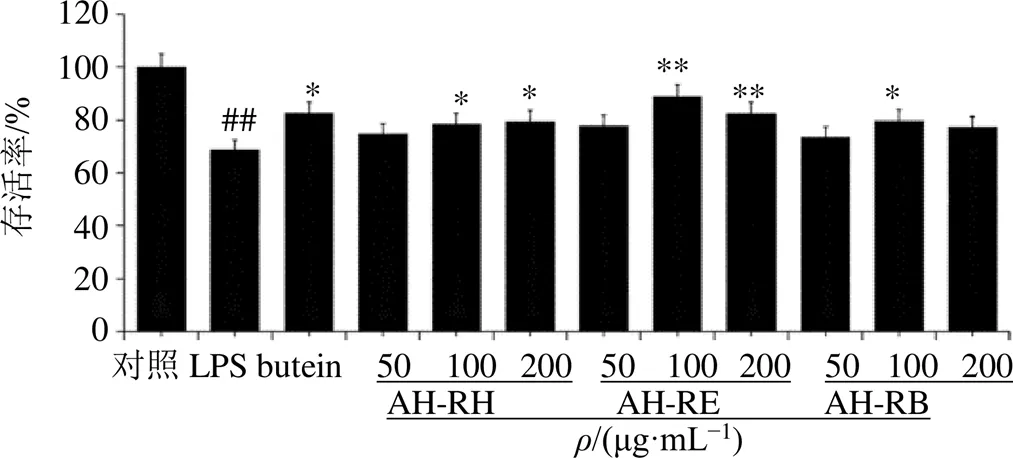
與對照組相比:#P<0.05 ##P<0.01;與LPS組相比:*P<0.05 **P<0.01,下圖同。
3.2.2 糙葉五加根各提取物對BV-2小膠質細胞中NO的影響 炎癥反應的發生伴隨著大量NO的生成,因此,NO被廣泛用作判斷炎癥反應是否發生的篩選指標。本研究以LPS誘導的BV-2小膠質細胞產生NO為模型對糙葉五加根各粗提物進行抗炎活性初篩,結果如圖2所示,與對照組比較,模型組NO濃度顯著升高;與模型組相比,各粗提物均可顯著降低NO水平,其中AH-RE的抑制效果最佳,當AH-RE的藥物濃度為100 μg/mL時,NO水平最低(2.099 μmol/L)。因此,后續實驗重點對AH-RE部位分離純化的化合物進行探討和研究,進一步明確其發揮抗神經炎作用的主要活性成分。
3.3 糙葉五加根中化合物1和13的抗神經炎活性驗證
根據上述各粗提物抗神經炎活性初步篩選結果,對活性較好的AH-RE部位進一步分離純化得到17個化合物,其中分離得到的化合物1、13分別被鑒定為芝麻素(sesamin)和丁香醛(syringaldehyde)。芝麻素是從芝麻中提取出來的一種木脂素,現代研究表明,芝麻素具有抗氧化、抗衰老、調血脂、抗高血壓等作用[33-35];丁香醛是一種黃酮類多酚化合物,具有抗氧化、抗高血糖等多種生理活性[36-37]。本課題組前期相關研究發現,從糙葉五加果實中分離的木脂素類對小膠質細胞中NO的產生具有良好的抑制作用[38]。有研究指出,多酚類物質及其代謝產物能夠通過血腦屏障發揮神經保護效應[39-40]。因此,本研究以分離自糙葉五加根AH-RE部位的化合物芝麻素和丁香醛為主要研究對象,基于LPS誘導的BV-2小膠質細胞作為抗神經炎活性篩選模型,分別對兩者所設定的藥物濃度區間進行了細胞毒實驗并測定了其對由LPS誘導的BV-2小膠質細胞產生NO的抑制作用,初步挖掘芝麻素和丁香醛的抗神經炎的潛在活性能力。
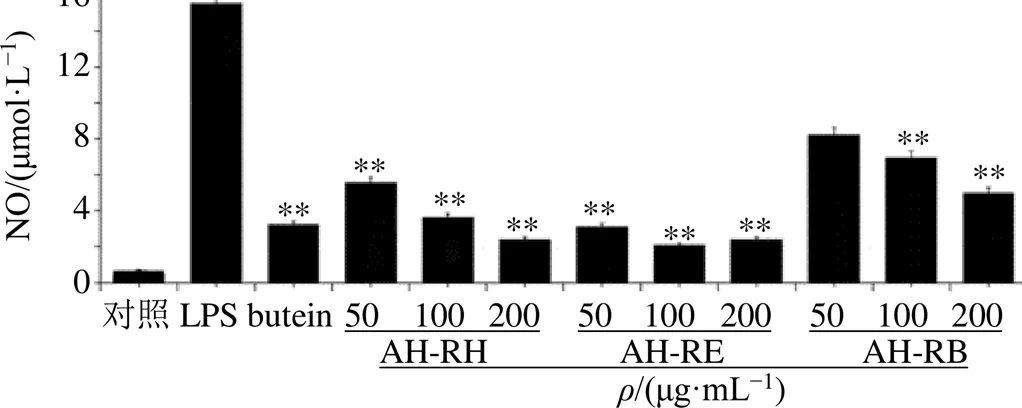
圖2 糙葉五加根各提取物對NO抑制作用(, n = 3)
3.3.1 芝麻素和丁香醛在LPS誘導的BV-2小膠質細胞模型下的細胞毒性 根據實驗結果可知(圖3、4),在5~80 μmol/L下,與對照組相比,芝麻素和丁香醛以此工作濃度梯度對BV-2細胞進行干預會對該細胞系的細胞活力產生一定影響但存活率均大于50%,因此,可將5~80 μmol/L的藥物濃度設置為后續實驗的濃度梯度。
3.3.2 芝麻素和丁香醛對BV-2小膠質細胞中NO的影響 根據實驗結果可知(圖5、6),與對照組相比,模型組的NO水平明顯升高,與模型組相比,不同濃度(5~80 μmol/L)的芝麻素和丁香醛對BV-2細胞處理后,NO水平均呈劑量相關性下降,表明芝麻素和丁香醛均能抑制NO的生成,意味著芝麻素和丁香醛對神經炎可能有一定的治療作用。
4 討論
《湖南省中藥地方標準》將糙葉五加根以“五加皮”收載,是一種具有祛風濕、滋補肝腎、活血化瘀之功效的抗風濕藥物。本課題組已圍繞糙葉五加葉、花、果實、根莖等做了大量研究,表明糙葉五加具有良好的抗炎活性。結合本研究前期對各粗提物的抗炎實驗的初步篩選,表明糙葉五加根醋酸乙酯提取物有更好的抗炎效果。因此,本研究進一步就糙葉五加根AH-RE的化學成分進行毒性、抗神經炎作用方面的研究。通過常規分離手段,共分離得到17個化合物,包括10個木脂素類、3個酚類、1個苯丙素類、3個其他類化合物。為了進一步明確糙葉五加根抗神經炎的主要活性成分,結合本課題組前期的研究成果,選取分離自抗炎活性最佳的AH-RE部位中的化合物芝麻素和丁香醛,利用LPS刺激BV-2小膠質細胞產生NO的體外炎癥模型對其進行抗炎活性驗證,結果表明,證明芝麻素和丁香醛具有一定的抗炎活性,可作為潛在的抗神經炎藥物進行開發。通過此實驗,進一步對糙葉五加的化學成分和藥理活性有了更全面的認識,明確其抗神經炎作用的藥效物質基礎,為糙葉五加根的合理使用及深層次的開發利用奠定理論基礎。
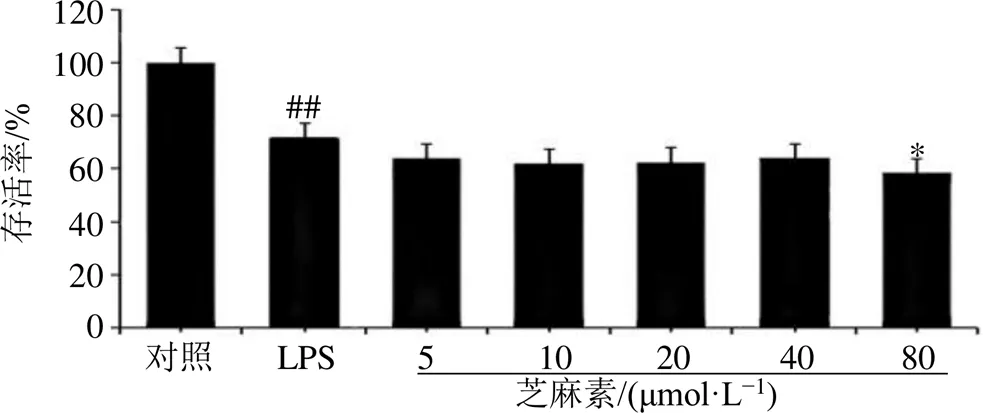
圖3 芝麻素對BV-2小膠質細胞的影響(, n = 3)
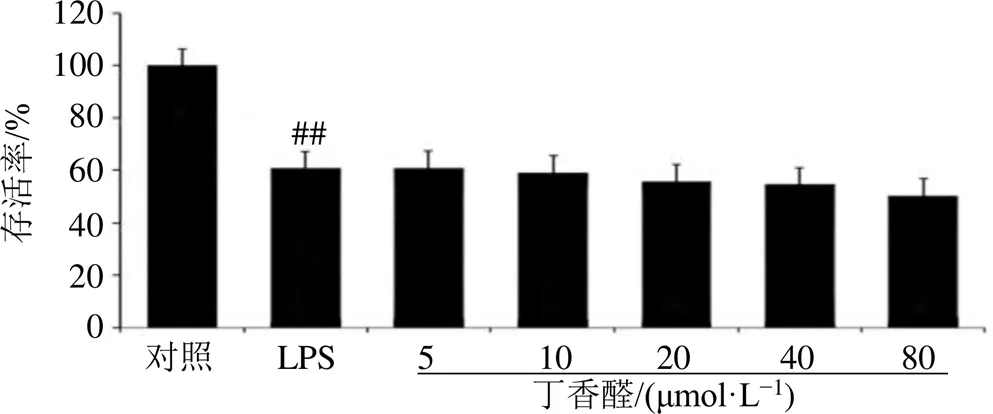
圖4 丁香醛對BV-2小膠質細胞的影響(, n = 3)
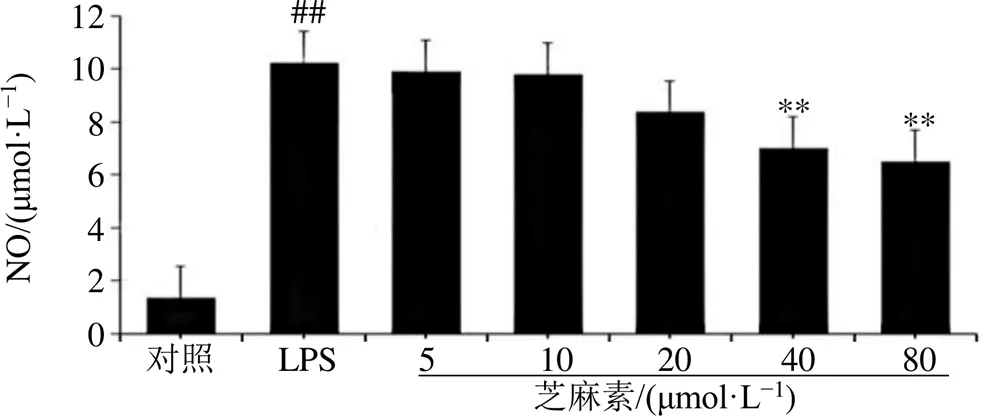
圖5 芝麻素對BV-2小膠質細胞中NO的影響(, n = 3)
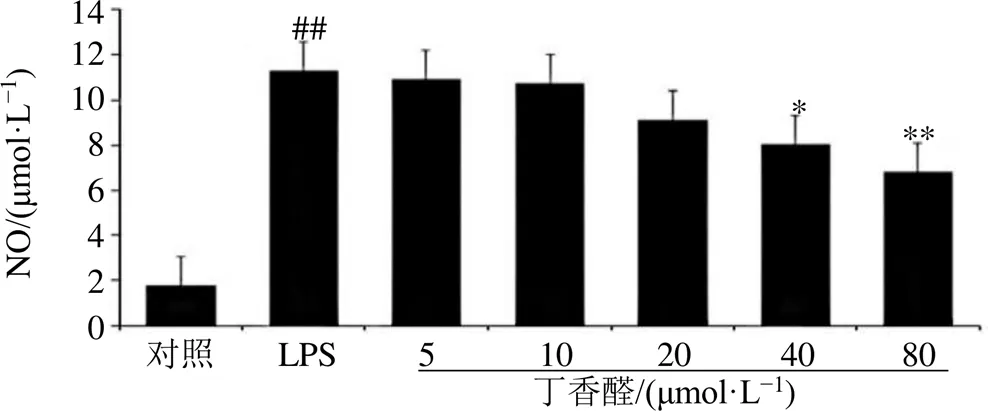
圖6 丁香醛對BV-2小膠質細胞中NO的影響(, n = 3)
利益沖突 所有作者均聲明不存在利益沖突
[1] Heneka M T, Kummer M P, Latz E. Innate immune activation in neurodegenerative disease [J]., 2014, 14(7): 463-477.
[2] de Waal G M, Engelbrecht L, Davis T,. Correlative light-electron microscopy detects lipopolysaccharide and its association with fibrin fibres in Parkinson’s disease, Alzheimer’s disease and type 2 diabetes mellitus [J]., 2018, 8(1): 16798.
[3] Guo Y S, Liang P Z, Lu S Z,. Extracellular αB-crystallin modulates the inflammatory responses [J]., 2019, 508(1): 282-288.
[4] 王超, 張篤偉, 徐沖. 神經炎癥與神經退行性疾病關系探究 [J]. 臨床醫藥文獻電子雜志, 2017, 4(4): 655.
[5] Park T, Chen H Z, Kevala K,. N-docosahexaenoylethanolamine ameliorates LPS-induced neuroinflammation via cAMP/PKA-dependent signaling [J]., 2016, 13(1): 284.
[6] Wang J, Li L X, Wang Z,. Supplementation of lycopene attenuates lipopolysaccharide-induced amyloidogenesis and cognitive impairments via mediating neuroinflammation and oxidative stress [J]., 2018, 56: 16-25.
[7] 馮勝, 劉向前, 張偉蘭, 等. RP-HPLC法測定糙葉五加不同部位中刺五加苷B和E [J]. 中草藥, 2011, 42(6): 1144-1146.
[8] Zhang X D, Liu X Q, Kim Y H,. Chemical constituents and their acetyl cholinesterase inhibitory and antioxidant activities from leaves of: Potential complementary source against Alzheimer’s disease [J]., 2014, 37(5): 606-616.
[9] 李小軍, 金官佑, 張曉丹, 等. 糙葉五加果實乙酸乙酯萃取部位化學成分及抗炎活性研究 [J]. 天然產物研究與開發, 2020, 32(3): 427-434.
[10] 李小軍, 吳賢哲, 金倫喆, 等. 糙葉五加花化學成分及其抗炎活性 [J]. 中成藥, 2019, 41(8): 1856-1862.
[11] 李小軍, 金官佑, 吳賢哲, 等. 糙葉五加莖化學成分研究 [J]. 中草藥, 2019, 50(5): 1055-1060.
[12] Kassim N K, Rahmani M, Ismail A,. Antioxidant activity-guided separation of coumarins and lignan from(Rutaceae) [J]., 2013, 139(1/2/3/4): 87-92.
[13] 馬永鵬, 張紅霞, 孫果, 等. 勐臘毛麝香化學成分研究 [J]. 天然產物研究與開發, 2018, 30(8): 1376-1381.
[14] Zhang W J, Wang Y, Geng Z F,. Antifeedant activities of lignans from stem bark ofDC. against[J]., 2018, 23(3): 617.
[15] 殷軍, 劉志惠, 王勇, 等. 綿萆薢中兩個新二芳基庚酮類化合物的分離和結構鑒定 [J]. 中國現代中藥, 2006, 8(2): 16-19.
[16] Zhang W, Lou H X, Li G Y,. A new triterpenoid fromBroth [J]., 2003, 5(3): 189-195.
[17] Shimotori Y, Nakahachi Y, Inoue K,. Synthesis of optically active γ-lactones via lipase-catalyzed resolution [J]., 2007, 22(5): 421-429.
[18] 王威, 劉小紅, 高華, 等. 東北鐵線蓮地上部位化學成分研究 [J]. 中草藥, 2014, 45(17): 2440-2446.
[19] Sun Y, Liu Y, Sun Y P,. Lanicepsides C-E from the aerial part ofOsbeck [J]., 2020, 37: 95-100.
[20] Urata H, Nishioka Y, Tobashi T,. First chemical synthesis of antioxidative metabolites of sesamin [J]., 2008, 56(11): 1611-1612.
[21] Couperus P A, Clague A D H, van Dongen J P C M,.13C chemical shifts of some model olefins [J]., 1976, 8: 426-431.
[22] Liu H Y, He H P, Yang X W,. Chemical constituents of the flowers of[J]., 2007, 19: 423-426.
[23] In S J, Seo K H, Song N Y,. Lignans and neolignans from the stems ofand their neuroprotective and anti-inflammatory activity [J]., 2015, 38(1): 26-34.
[24] Li Y C, Kuo Y H. Four new compounds, ficusal, ficusesquilignan A, B, and ficusolide diacetate from the heartwood of[J]., 2000, 48(12): 1862-1865.
[25] Zhang P M, Zhang C, Zeng K W,. Lignans and flavonoids from[J]., 2018, 27(6): 429-435.
[26] 任慧, 徐巧林, 董麗梅, 等. 南美蟛蜞菊中的酚酸類化學成分 [J]. 熱帶亞熱帶植物學報, 2015, 23(4): 469-473.
[27] Wang L Q, You X Z, Zhou L,. Lignans fromMarkgr. f. Megalocarpua [J]., 2009, 45(3): 424-426.
[28] Bisoli E, Freire T V, Yoshida N C,. Cytotoxic phenanthrene, dihydrophenanthrene, and dihydrostilbene derivatives and other aromatic compounds from[J]., 2020, 25(14): 3154.
[29] 梁瑞蘭, 史國茹, 庾石山. 大風子中木脂素類化學成分研究 [J]. 中國中藥雜志, 2019, 44(7): 1397-1402.
[30] Li H B, Zhou C X, Pan Y X,. Evaluation of antiviral activity of compounds isolated fromand[J]., 2005, 71(12): 1128-1133.
[31] 粟杰, 馮艷, 林炳鋒, 等. 刺五加化學成分的分離與鑒定[J]. 中草藥, 2021, 52(16): 4783-4788.
[32] Dao P T A, Hai N X, Nhan N T,. Study on DPPH free radical scavenging and lipid peroxidation inhibitory activities of Vietnamese medicinal plants [J]., 2012, 18(1): 1-7.
[33] Ruankham W, Suwanjang W, Wongchitrat P,. Sesamin and sesamol attenuate H2O2-induced oxidative stress on human neuronal cells via the SIRT1-SIRT3-FOXO3a signaling pathway [J]., 2021, 24(2): 90-101
[34] Dalibalta S, Majdalawieh A F, Manjikian H. Health benefits of sesamin on cardiovascular disease and its associated risk factors [J]., 2020, 28(10): 1276-1289.
[35] Ali B H, Al Salam S, Al Suleimani Y,. Ameliorative effect of sesamin in cisplatin-induced nephrotoxicity in rats by suppressing inflammation, oxidative/nitrosative stress, and cellular damage [J]., 2020, 69(1): 61-72.
[36] 呂強華. 丁香醛對沙門氏菌Ⅲ型分泌系統的抑制作用及機制 [D]. 長春: 吉林大學, 2020.
[37] Bozkurt A A, Mustafa G, Tar?k A,. Syringaldehyde exerts neuroprotective effect on cerebral ischemia injury in rats through anti-oxidative and anti-apoptotic properties [J]., 2014, 9(21): 1884-1890.
[38] 唐思琪, 羅姣, 黃浩, 等. 糙葉五加正丁醇萃取部位抗炎活性成分研究 [J]. 天然產物研究與開發, 2021, 33(4): 598-606.
[39] 潘春杏. 氧化白藜蘆醇對LPS誘導的神經炎癥的保護作用及調控機制 [D]. 廣州: 廣東工業大學, 2021.
[40] 徐靜嫻. 白藜蘆醇對脂質炎癥刺激誘導的神經元及小膠質細胞損傷保護作用的體外研究 [D]. 合肥: 安徽醫科大學, 2021.
Chemical constituents of roots ofisolated based on BV-2 microglia model
CHEN Yang, XIAO Jin, JIANG Shiqin, LUO Jiao, LIU Xiangqian
School of Pharmacy, Hunan University of Chinese Medicine, Changsha 410208, China
To study the chemical constituents and anti-neuritis activity of the root of.A neuroinflammation model was established using lipopolysaccharide (LPS)-induced BV-2 microglial cells, and cytotoxicity was measured using MTT method. The n-hexane, ethyl acetate, and n-butanol extracts from the roots ofwere screened for activity to determine the active site. Based on the screening results, the optimal active site was further separated and purified using column chromatography, D101 macroporous resin, and semi-preparative solution methods. Based on the physicochemical properties and obtained spectral data, the structure of compound was identified.The best activity was observed in the ethyl acetate extract site, from which 17 compounds were isolated and identified as (+)-sesamin (1), coniferaldehyde (2), acuminatolide (3), sesaminone (4), 10-nonacosanol (5), rac--methyl-4-hydroxydecanamide (6), matairesinol (7), (1,2,5,6)-6-(3,4-dihydroxyphenyl)-2-(3,4-methylenedioxyphenyl)-3,7-dioxabicyclo[3,3,0]octane (8), 1-octene (9), piperitol (10), (?)-pinoresinol (11), ficusal (12), syringaldehyde (13), syringaresinol (14), (?)-episyringaresinol (15), protocatechuyl aldehyde (16), protocatechuic acid (17), respectively. The isolated sesamin and syringaldehyde can reduce the release of NO in BV-2 microglia induced by LPS in a dose-dependent manner at cell tolerance concentrations (5—80 μmol/L).Compounds 3—10, 12, 15 were isolated from family Araliaceae for the first time. Compounds 3—10, 12, 15 were isolated from theMiq. for the first time. Compounds 2—12, 15—16 were isolated fromfor the first time. The monomeric compounds sesamin and syringaldehyde in the roots ofhave potential anti-neuroinflammatory activities.
(Oliv.) Harms; anti-neuroinflammatory activity;Miq; lignans; sesamin; syringaldehyde
R284.1
A
0253 - 2670(2024)08 - 2533 - 09
10.7501/j.issn.0253-2670.2024.08.004
2023-10-07
湖南省自然科學基金項目(2024JJ7357);湖南省科技廳普惠性政策與創新環境建設計劃項目(2022ZK4039);湖南中醫藥大學“十四五”重點學科-生物工程學科(校行發規字 [2023] 2號);湖南省研究生科研創新項目(QL20220186)
陳 楊,女,碩士研究生,研究方向為中藥及天然藥物活性成分研究。Tel: 16673229122 E-mail: 2200840698@qq.com
通信作者:劉向前,男,博士生導師,教授。Tel: 13308439949 E-mail: lxq0001cn@163.com。
[責任編輯 王文倩]

