藥品上市許可持有人藥物警戒檢查調研分析*
王丹,王濤
(國家藥品監(jiān)督管理局藥品評價中心,國家藥品監(jiān)督管理局藥物警戒研究與評價重點實驗室,北京 100022)
《中華人民共和國藥品管理法》第九十九條規(guī)定“藥品監(jiān)督管理部門應當依照法律、法規(guī)的規(guī)定對藥品研制、生產(chǎn)、經(jīng)營和藥品使用單位使用藥品等活動進行監(jiān)督檢查”。藥物警戒檢查是藥品監(jiān)督檢查的一部分,是對藥品上市許可持有人(以下簡稱“持有人”)以及其他相關單位履行藥物警戒法律法規(guī)等情況進行的符合性檢查,目前藥物警戒檢查的主要對象是持有人。
我國的藥物警戒檢查相對于藥品生產(chǎn)和經(jīng)營檢查起步較晚。藥物警戒是在藥品不良反應報告與監(jiān)測工作基礎上發(fā)展起來的,國內于2015年啟動對制藥企業(yè)藥品不良反應報告與監(jiān)測的檢查試點,2016年將檢查工作正式納入各省的常規(guī)監(jiān)督檢查范疇。2019年修訂的《中華人民共和國藥品管理法》規(guī)定我國建立藥物警戒制度,此后對“藥品不良反應報告與監(jiān)測”的檢查變更為“藥物警戒檢查”,檢查對象由藥品生產(chǎn)企業(yè)變更為持有人。主要檢查內容是持有人執(zhí)行相關法律法規(guī)和《藥物警戒質量管理規(guī)范》[1]《全國疑似預防接種異常反應監(jiān)測方案》[2]等情況,主要檢查依據(jù)是2020—2021年國家藥監(jiān)局出臺的《藥品檢查管理辦法(試行)》[3]和《藥物警戒檢查指導原則》[4]。
1 調研內容與方法
1.1調研內容 調研內容分為兩部分,一是持有人藥物警戒活動開展情況,二是監(jiān)管部門藥物警戒檢查工作組織情況。持有人藥物警戒活動開展情況將結合《藥物警戒質量管理規(guī)范》和《藥物警戒檢查指導原則》中檢查要點,對持有人的藥物警戒體系、藥物警戒活動及質量管理情況進行摸底。監(jiān)管部門藥物警戒檢查工作的組織情況將結合《藥品檢查管理辦法(試行)》《藥物警戒檢查指導原則》的相關要求,從檢查工作承擔的機構和人員、檢查方式和頻率、檢查重點以及對檢查工作的意見和建議等方面進行調查。
1.2調研對象 依據(jù)藥品監(jiān)管職責劃分和屬地管理原則,對持有人的藥物警戒檢查主要由各省級藥品監(jiān)督管理部門組織開展。考慮到近年來各省已經(jīng)開展多輪藥品不良反應報告和監(jiān)測/藥物警戒檢查(以下統(tǒng)稱“藥物警戒檢查”),檢查人員對持有人藥物警戒活動開展情況已經(jīng)有較深入的了解,此外本次調研還著重于藥物警戒檢查工作本身的問題及建議,因此將調研的對象確定為各省、自治區(qū)、直轄市和新疆生產(chǎn)建設兵團具體承擔藥物警戒檢查的相關機構和人員(共32人)。
1.3調查方式 本次調研以線上問卷調查的方式開展。在預調研的基礎上設計制定《藥物警戒檢查相關工作調查問卷》,主要包括三部分內容:①被調查人員的基本信息;②轄區(qū)內持有人藥物警戒工作開展情況;③轄區(qū)內藥物警戒檢查組織情況。每項內容設置若干問題,共設置22個具體問題,題型以選擇題(單選或多選題)和填空題為主,第二部分和第三部分還納入開放式問題。其中第二部分有關持有人藥物警戒工作開展情況,主要通過評分方式進行摸底。要求被調查人員根據(jù)相關法規(guī)和規(guī)范要求,結合近年來檢查工作情況,從以下5個大項為轄區(qū)內持有人藥物警戒活動打分:①機構、人員和資源;②藥物警戒質量管理;③監(jiān)測與報告;④風險識別和評估;⑤風險控制。每大項中又包含細化的評分項,共27小項,例如藥物警戒質量管理又細化為:記錄與數(shù)據(jù)管理、制度與規(guī)程文件及管理、委托管理、內部審核等7小項。各項評分均為五檔,由低至高賦予1~5分。
國家藥品不良反應監(jiān)測中心于2022年8月向各省級不良反應監(jiān)測機構發(fā)出公函,要求省級監(jiān)測機構協(xié)助開展調查工作,每省(自治區(qū)、直轄市)填寫一份調查問卷,問卷填寫人員要求提供真實的姓名和聯(lián)系方式。國家藥品不良反應監(jiān)測中心通過問卷星回收問卷,由專業(yè)技術人員對問卷進行統(tǒng)一匯總和分析,利用問卷星自帶的統(tǒng)計分析功能對選擇題和填空題進行分類統(tǒng)計,對開放式問題進行人工匯總。
2 問卷調研結果分析
截至2022年9月底,共回收在線問卷32份,其中31個省(自治區(qū)、直轄市)和新疆生產(chǎn)建設兵團各1份,有效問卷32份。填寫問卷人員的工作單位除2個為省級藥品監(jiān)督管理局外,其他均為省級藥品不良反應監(jiān)測機構。
2.1持有人藥物警戒活動開展情況
2.1.1總體評分結果 根據(jù)大項的評分結果,5個方面總體情況評分在3~4分(表1),平均3.46分,其中持有人在藥物警戒機構、人員和資源方面得分最高,在藥品風險識別和評估方面得分最低。
目前,我國的智慧城市建設試點城市已超過100個,其中有一些知名旅游城市,如杭州、重慶、昆明等,傳統(tǒng)的旅游資源優(yōu)勢再加上智慧城市的建設將為這些城市打造智慧旅游產(chǎn)業(yè)帶來良好的機遇,同時也為北京市智慧旅游的發(fā)展帶來了競爭壓力與威脅。

表1 持有人藥物警戒活動總體情況評分
2.1.2具體活動的評分結果 具體活動評分結果按分值由高到低排列,見表2,平均3.50分。27小項中“信息注冊與更新管理”和“PSUR/PBRER”兩項達到4分,提示開展情況良好,其他各項均3~4分,“藥品上市后安全性研究”是唯一低于3分的項目,提示開展情況欠佳。
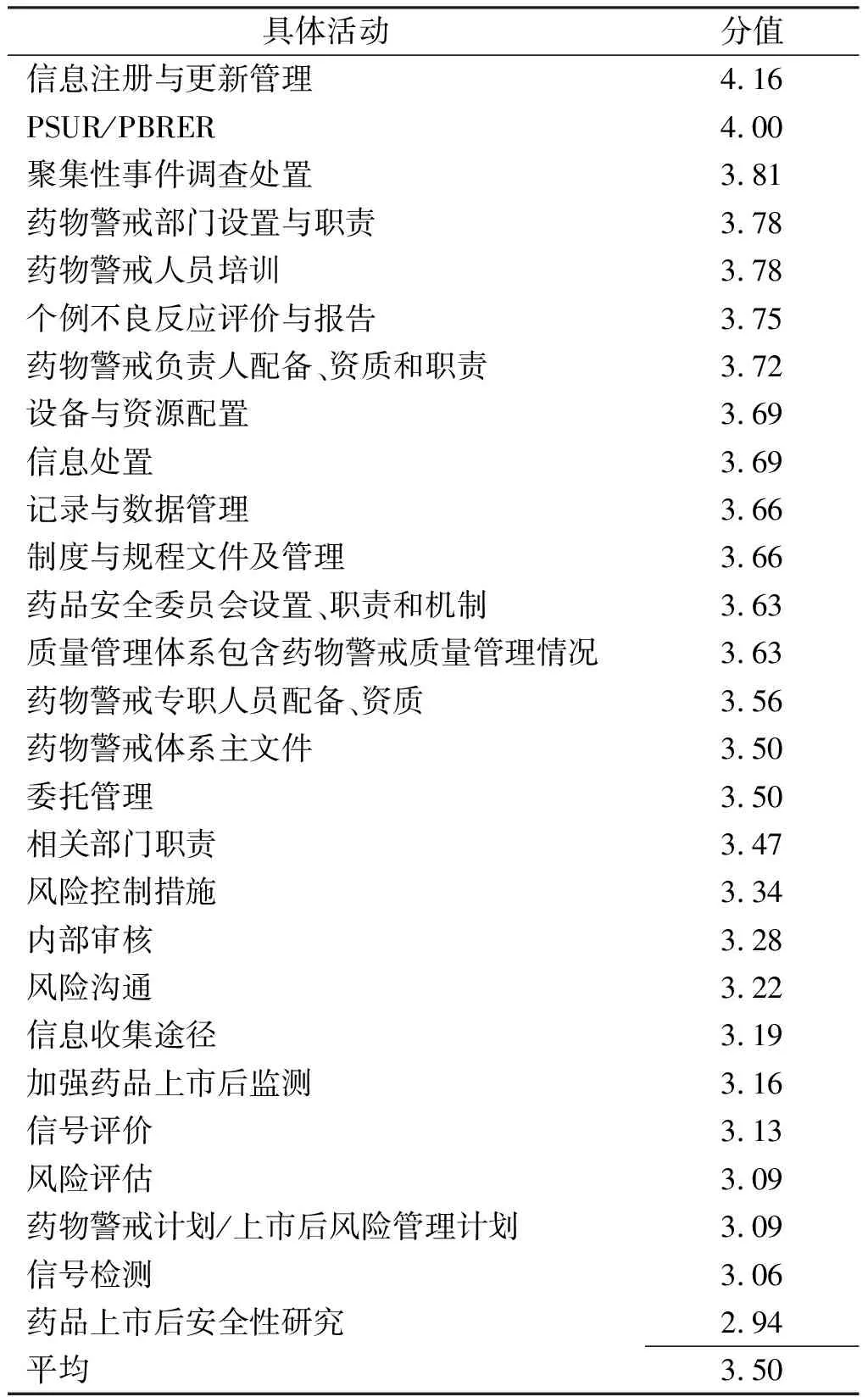
表2 持有人藥物警戒活動細化評分項
2.1.3存在的問題及建議 除評分項外,問卷還設置開放式問題,對當前持有人藥物警戒體系及活動中存在的問題進行調查。根據(jù)調查結果,當前存在的主要問題包括:①企業(yè)藥物警戒專職人員數(shù)量配備不足,技術力量偏弱;②主動收集不良反應報告意識不足,收集渠道需進一步健全;③對藥品風險的識別能力不足,信號檢測、風險評估等核心工作缺乏成熟經(jīng)驗;④主動開展上市后安全性研究的意識相對薄弱;⑤風險控制的手段不夠豐富,風險管理系統(tǒng)還需進一步完善。
調查結果還集中反映持有人當前存在的藥品安全主體責任意識問題,體現(xiàn)在企業(yè)領導對藥物警戒工作重視程度不夠、投入少;企業(yè)對藥物警戒工作心存顧慮,擔心不良反應報告影響產(chǎn)品銷售、企業(yè)信譽,甚至引發(fā)訴訟與賠償。其他較為集中的問題包括:持有人對《藥物警戒質量管理規(guī)范》的理解不夠透徹,不知如何落地實施;外資企業(yè)因其全球集團化管理的特殊性,在執(zhí)行國內規(guī)范上存在不明確的地方;一些企業(yè)藥物警戒工作停留在表面,尤其是缺少創(chuàng)新藥或獨家品種的企業(yè),藥物警戒工作以滿足法規(guī)基本要求為基準,缺乏深入開展的動力。
綜合對持有人的調查結果可以看出,因前期藥品不良反應報告和監(jiān)測工作打下的基礎,持有人在體系建設、不良反應信息收集等方面活動開展情況相對良好;但是對于一些新的規(guī)范要求,如信號檢測、風險評估、上市后安全性研究等,持有人的工作基礎和技術力量還較為薄弱,建議作為今后監(jiān)管部門藥物警戒檢查和工作指導的重點。
2.2藥物警戒檢查組織情況
2.2.1承擔機構和人員 藥物警戒檢查的管理機構是各省級藥品監(jiān)督管理部門。根據(jù)《藥品檢查管理辦法(試行)》,省級藥品監(jiān)督管理部門可依法設置或者指定藥品檢查機構,負責檢查員隊伍的日常管理以及檢查計劃和任務的具體實施。從調查結果看,目前各省承擔藥物警戒檢查的機構主要是省級藥品不良反應監(jiān)測機構(24個),其他依次是省級藥監(jiān)局、省級審核查驗中心和藥監(jiān)局派出/駐機構。一些省份是由多個單位共同承擔藥物警戒檢查工作。實際參加藥物警戒檢查的人員也多來自省級藥品不良反應監(jiān)測中心,其他人員來自地市級不良反應監(jiān)測機構、省級藥監(jiān)局、省級藥監(jiān)局派出/駐機構、省級審核查驗中心。其中,藥物警戒檢查全部由省級監(jiān)測機構人員承擔的有8個省,個別省的地市級市場監(jiān)督管理部門或省藥檢所等單位人員也參加檢查。
根據(jù)《藥監(jiān)局關于加快推進職業(yè)化專業(yè)化藥品檢查員隊伍建設的實施意見》[5],藥品檢查員分為藥品、醫(yī)療器械、化妝品3個檢查序列,藥物警戒檢查員屬于藥品序列。收集的問卷中有24個省(自治區(qū)、直轄市)和新疆生產(chǎn)建設兵團報告了具有藥物警戒檢查能力(指接受過專門藥物警戒檢查培訓或從事過藥物警戒工作,能夠承擔藥物警戒檢查任務的檢查員)的檢查員600余人,約占藥品序列檢查員的10%。
2.2.2檢查頻率和形式 藥物警戒檢查主要分為常規(guī)檢查和有因檢查。藥品監(jiān)管部門依據(jù)風險原則制定藥品檢查計劃,每年對一定比例的持有人開展常規(guī)藥物警戒檢查,一般3~5年可以覆蓋本轄區(qū)內全部的持有人。從各省的檢查頻率來看,9個省為3年全覆蓋,7個省為5年全覆蓋,6個省為4年全覆蓋,少數(shù)省為1~2年全覆蓋。部分省對持有疫苗、集采藥品、創(chuàng)新藥、中藥注射劑等重點品種,以及發(fā)現(xiàn)聚集性事件、報告數(shù)量排名靠前、藥物警戒體系發(fā)生較大變化的企業(yè)加大了檢查頻率。個別省未明確常規(guī)檢查頻率,而是以問題或風險為導向選擇企業(yè)進行檢查。
藥物警戒常規(guī)檢查的形式包括藥物警戒專項檢查,以及根據(jù)《藥品生產(chǎn)監(jiān)督管理辦法》[6]的要求與生產(chǎn)監(jiān)督檢查(GMP檢查)進行并組檢查。根據(jù)調查結果,31個省(自治區(qū)、直轄市)中有18個省同時采取兩類檢查形式,12個省主要采取專項藥物警戒檢查形式,2個省主要采取并組檢查形式。
2.2.3檢查制度 新的法規(guī)、規(guī)范出臺后藥物警戒檢查工作面臨新形勢,各省也根據(jù)《藥品檢查管理辦法(試行)》的要求著手建立本轄區(qū)內的藥物警戒檢查制度,組織制定本轄區(qū)的檢查實施細則和檢查方案等文件。截至調查開始,16個省(自治區(qū)、直轄市)已經(jīng)制定并發(fā)布藥物警戒檢查相關文件,包括藥物警戒質量管理規(guī)范符合性檢查管理程序、藥物警戒年度檢查計劃或方案、藥物警戒檢查工作程序、遠程檢查工作管理辦法、省級藥物警戒檢查要點等。正在制定相關文件的有7個省,個別省還制定了內部工作規(guī)程或檢查報告的模板。
根據(jù)《藥物警戒檢查指導原則》的要求,有17個省(自治區(qū)、直轄市)在藥物警戒檢查相關文件中均規(guī)定重點檢查的藥品,依次為中藥注射劑、創(chuàng)新藥、不良反應大的藥品、聚集性事件頻發(fā)的藥品、集中帶量采購中選品種、多組分生化藥、銷售量大的品種、改良型新藥、附條件批準的藥品、國家藥監(jiān)部門發(fā)布公告提示風險的品種、無菌制劑、社會關注度較高的品種、上市3年或5年內的藥品,其他還包括兒科用藥、孕期和哺乳期用藥、可替代性有限的品種等。
2.2.4近3年檢查情況 本次問卷對近3年藥物警戒檢查的情況進行調查,有28個省(自治區(qū)、直轄市)提供數(shù)據(jù)。2020年1月—2022年7月,28個省(自治區(qū)、直轄市)對2 063家持有藥品制劑注冊證書(不包括原料藥、體外診斷試劑、中藥材、中藥飲片、醫(yī)用氧)的企業(yè)開展藥物警戒檢查,3年內各省檢查覆蓋的制劑企業(yè)比例17.7%~100%。其中12個省開展過有因檢查,檢查主要原因是監(jiān)測工作中發(fā)現(xiàn)可能存在安全風險,其他原因包括不良反應信息遲報、瞞報、漏報,報告質量差,未能及時發(fā)現(xiàn)、評估、控制或溝通相關風險,未按規(guī)定或監(jiān)管部門要求開展藥品上市后安全性研究或制定并實施藥物警戒計劃等。此期間各省均未開展過跨省的藥物警戒檢查工作。
2.2.5存在的問題及建議 調查問卷最后設置兩道開放性問題,主要詢問如何有序推進藥物警戒檢查(包括風險分級管理),以及當前檢查工作存在的主要問題和建議。
關于實施風險分級管理的經(jīng)驗及建議。《藥品檢查管理辦法(試行)》要求監(jiān)管部門對常規(guī)檢查實行分級管理。關于藥物警戒檢查如何實施風險分級管理,省里的意見較為一致,即按照持有人持有品種的風險,或按照持有人藥物警戒工作開展情況以及既往檢查情況確定檢查頻率、周期、優(yōu)先次序。個別省建議采取適當?shù)娘L險分級評定方法來支持風險分級管理,如采用評分法、建立計算機輔助風險評估體系等。
關于檢查員隊伍和能力建設的問題及建議。調研期間,我國職業(yè)化專業(yè)化藥品檢查隊伍正在建立中,藥物警戒檢查沒有專門的檢查員序列。反映的最主要問題之一是職業(yè)化專業(yè)化藥物警戒檢查人員數(shù)量不足,檢查人員專業(yè)素質有待提高。主要建議包括兩方面,一是擴充檢查員隊伍,包括建立專業(yè)藥物警戒檢查員隊伍;二是加強藥物警戒業(yè)務培訓和檢查指導。
關于檢查的職責和分工問題。雖然《藥品檢查管理辦法(試行)》中規(guī)定各級藥品監(jiān)督管理部門依法設置或指定藥品檢查機構開展相關檢查工作,但有的省并未明確指定藥物警戒檢查機構。有的省藥品不良反應監(jiān)測機構和藥品檢查機構(如省級藥品核查中心)在檢查職責上分工不夠清晰,導致檢查工作開展不順暢。基于以上問題,部分省建議由國家或省級監(jiān)管部門明確省級藥物警戒檢查的責任機構;一些人員不足的省級監(jiān)測機構建議將檢查職責交由藥品檢查機構負責,省市監(jiān)測機構人員作為檢查員配合開展檢查工作;個別省則建議將不良反應監(jiān)測機構明確指定為藥物警戒檢查的責任單位。
其他有序推進藥物警戒檢查工作的建議包括:明確藥物警戒檢查的范圍和檢查項目;加強與GMP聯(lián)合檢查,提高檢查效率;統(tǒng)一藥物警戒檢查相關標準;開展國家層面的藥物警戒檢查或督導檢查工作;將檢查情況納入監(jiān)管部門考核指標;完善相關政策制度、法規(guī)和指南文件,逐步提升檢查能力、優(yōu)化檢查手段等。
2.3調研的局限性 本次調研還存在一定的局限性:調研正處于新舊法規(guī)和要求的過渡期,各省的相關配套政策和檢查員隊伍正在建設中,數(shù)據(jù)變化性可能較大;問卷填寫人員主要是省級不良反應監(jiān)測機構人員,對于藥品序列檢查員數(shù)量等真實情況可能無法準確獲得;問卷以個人名義填寫,不排除填寫人員對檢查工作的主觀理解和認知。
3 總結
藥物警戒檢查對規(guī)范持有人開展藥物警戒活動,推動藥物警戒制度的落地實施有著重要的作用[7]。2019—2022年山東[8-9]、江西[10]、海南[11]、上海[12]、重慶[13]等參與藥物警戒檢查的人員對本省市持有人開展藥物警戒檢查的情況進行總結和分析。本次調研從檢查員的角度,以評分的方式對持有人藥物警戒體系及藥物警戒活動開展情況進行摸底。雖然多數(shù)調查項目的評分結果未達到令人滿意的高分,但也達到居中的平均水平。我國藥物警戒制度剛剛起步,對持有人的很多要求都是新的或與國際高標準接軌,需要企業(yè)強化主體責任意識,逐步完善體系和制度,不斷提高藥物警戒的能力和水平。監(jiān)管部門也需要同時加強指導,并利用監(jiān)督檢查的手段來督促持有人合法、合規(guī)履行藥物警戒責任。
從檢查工作本身來看,自2019年國務院規(guī)定我國建立執(zhí)業(yè)化專業(yè)化檢查員隊伍以來[14],藥品監(jiān)管部門已經(jīng)連續(xù)出臺一系列配套政策和辦法,包括檢查員隊伍管理、教育培訓、人員調配、信息管理、廉潔自律等,充分體現(xiàn)政府部門對打造一支“政治過硬、素質優(yōu)良、業(yè)務精湛、廉潔高效”的檢查員隊伍的決心,也體現(xiàn)其強化企業(yè)責任、加強“過程監(jiān)管”的堅定態(tài)度。藥物警戒檢查雖然起步晚,但恰逢新制度建立以及藥品監(jiān)督檢查制度改革的良機,希望監(jiān)管部門能借此機遇,完善藥物警戒檢查各項規(guī)章制度,理順相關部門關系,解決檢查中存在的問題,建立健全藥物警戒檢查員隊伍,有序推進藥物警戒檢查的各項工作,為我國新制度的實施奠定基礎、儲備人才。

