惡性血液病伴碳青霉烯類耐藥菌感染病人死亡風險建模
徐新童,李俏俏,梁春艷,張聰麗,邢海洲
作者單位:鄭州大學第一附屬醫院血液內科,河南 鄭州450052
血液病,尤其是惡性血液病病人,由于其本身特點以及在疾病治療過程中,對免疫功能有損害的藥物被長期應用且其是難以避免的,致使免疫功能較差,細菌感染發生率極高[1-3]。而碳青霉烯類抗生素,對于發生細菌感染的血液病病人來說,是一種最常用的抗生素,曾使眾多病人受益,但在近些年,隨著此起彼伏地出現碳青霉烯類抗生素耐藥菌株,針對感染病人的治療也隨之變得愈發困難,病人的病死率也在不斷上升,國內外研究結果表明伴發碳青霉烯類耐藥菌感染的血液病病人病死率在50%以上,而惡性血液病病人中甚至可達到100%[4-7]。因此,一個行之有效的有能力預測碳青霉烯類抗生素耐藥菌感染死亡風險的評分體系得到建立是十分必要的。本研究旨在探究那些能夠影響已遭受到耐碳青霉烯類藥物細菌感染的惡性血液病病人死亡風險的因素,構造一個惡性血液病伴碳青霉烯類耐藥菌感染病人死亡風險的預測模型,并評測該模型的預測價值。
1 資料與方法
1.1 一般資料本研究借助于電子病歷系統選取和錄入了鄭州大學第一附屬醫院血液內科收治的確定發生有耐碳青霉烯類藥物菌感染的惡性血液病病人的臨床資料信息,時間跨度為2018 年11 月至2021 年2 月,主要收集病人的基本信息、感染前抗生素使用情況、血液病種、血常規及其他部分實驗室檢驗指標、進行過侵入性操作或者手術與否、曾在重癥監護室(ICU)進行治療與否、是否曾應用造血干細胞移植術(HSCT)進行治療以及既往合并患有其他基礎疾病與否等方面的內容。納入標準:臨床資料完整、年齡>14 周歲、符合碳青霉烯類抗菌藥物耐藥菌標準;排除標準:不符合惡性血液病診斷標準、既往發生過碳青霉烯類抗菌藥物耐藥菌感染。病人或其近親屬知情同意,本研究符合《世界醫學協會赫爾辛基宣言》相關要求。
1.2 研究方法按照臨床預測模型統計學要求,2018 年11 月至2020 年10 月的121 例病人的信息資料被選取為建模組。按照建模組樣本量∕驗證組樣本量為3∕1~4∕1 原則,選取2020 年11 月至2021 年2月37 例病人的信息資料為驗證組。再在組內以病人離院時是否死亡作為判定,分為存活亞組和死亡亞組,統計學分析所收集到的信息資料。
1.3 統計學方法應用SPSS 20.0 軟件進行統計學分析。正態分布定量資料以±s表示,兩樣本均數比較采用單因素方差分析,非正態分布定量資料以中位數以及四分位間數表示,組間比較采用Kruskal-Wallis 多重比較;定性資料以例(%)表示,采用χ2(連續校正)檢驗或Fisher 確切概率法。所有檢驗結果均以P<0.05為差異有統計學意義。
將單因素分析結果中所得到的P<0.20 指標(以期更多因素能夠被引入至下一步分析)運行于logistic 回歸分析方程中,篩選出死亡風險因素并根據所得到輸出的相關回歸系數,構建遭受耐藥菌感染的病人死亡風險的預測模型。并對所構建的模型進行評估和驗證,針對于評估模型的價值,采用似然比卡方檢驗;針對于此模型的校準度和區分度,則采用Hosmer-Lemeshow 檢驗以及受試者操作特征曲線(ROC)下面積的統計學方法來評估,應用驗證組數據繪制ROC 曲線對所構建模型的臨床效用進行驗證。本研究的驗證采用的為時段驗證,其為外部驗證中的一種,即利用與構建模型數據來源相同但時間段不同的數據對模型進行驗證[8-13]。
2 結果
2.1 病人基礎資料本次納入的碳青霉烯類抗菌藥物耐藥菌感染病人總共158 例,建模組有121 例,驗證組有37 例。基線數據在建模組與驗證組的差異無統計學意義(P>0.05),見表1。
2.2 建模組病人發生死亡風險的單因素分析建模組中有58 例存活亞組病例,63 例死亡亞組病例,其在耐藥菌感染前住院時間、抗生素使用時間、抗生素使用種類(為住院時應用的總種類數)、最多幾種抗生素聯合使用、使用過碳青霉烯類抗菌藥物與否、應用過其余特殊使用級抗生素與否(如:利奈唑胺、萬古霉素、替考拉寧、多黏菌素、頭孢他啶阿維巴坦以及替加環素等)、中性粒細胞計數、粒缺持續時間以及心腦血管疾病病史等方面進行對比,差異有統計學意義(P<0.05)。見表2。
病人的血液病類型以急性髓系白血病為主,共計56 例(46.3%),存活亞組與死亡亞組在血液原發病疾病譜差異有統計學意義(χ2=13.03,P=0.011),見表3。

表3 建模組碳青霉烯類耐藥菌感染121例血液疾病譜
2.3 感染者死亡風險的logistic 回歸方程因變量為病人的轉歸(存活賦值為0,死亡為1),P<0.20 的單因素分析變量作為因子(即自變量)納入logistic回歸分析方程中,采用逐步向前法(LR)篩選惡性血液病伴耐碳青霉烯類抗菌藥物細菌感染病人的死亡危險因素,將0.10 設為納入變量的顯著性水準、0.15設為剔除變量的顯著性水準。共納入接受過化療與否、耐藥菌感染前的住院時間、感染前抗生素的應用時間、感染前抗生素的使用種類(為住院時應用的總種類數)、最多幾種抗生素聯合應用、感染前使用過碳氫酶烯類抗菌藥物與否、感染前使用過其余特殊使用級抗生素與否、血液疾病譜、感染前中性粒細胞計數、粒缺持續時間、接受過HSCT 與否以及患有心腦血管疾病與否等12項相關風險因素,對這些變量中的分類變量設置啞變量,用數值0,1,2,3,4,5 表示,定量資料則納入其數值,具體賦值情況詳見表4。
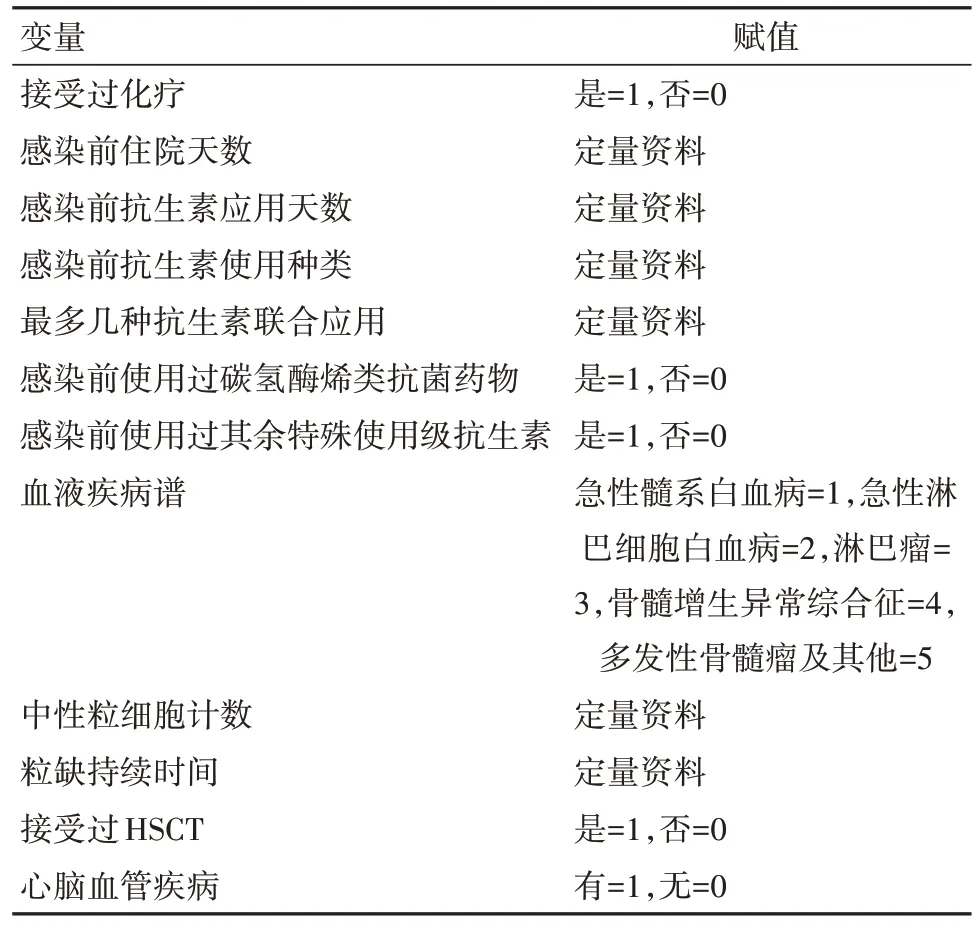
表4 碳青霉烯類抗菌藥物耐藥菌感染158例死亡危險因素多因素logistic回歸方程中因子賦值
由logistic 回歸分析方程可得到,最終保留的自變量有感染前住院時間、感染前使用過其余的特殊使用級性抗生素與否、感染前中性粒細胞計數以及患有心腦血管疾病與否。具體情況見表5。

表5 碳青霉烯類耐藥菌感染158例死亡風險的多因素logistic回歸分析
所得方程:logistic(P)=0.061×a+1.868×b-0.412×c+1.345×d-1.309。
其中感染前住院天數記作a、感染前使用過其余的特殊使用級性抗生素與否記作b、感染前中性粒細胞計數記作c、患有心腦血管疾病與否記作d。
2.4 預測模型的評估與驗證
2.4.1 評估預測模型 對所建立的模型進行似然比χ2檢驗(Likelihood ratio test),結果顯 示:χ2=42.26,P<0.001,故該預測模型與空模型之間進行比較時,差異有統計學意義(P<0.05)。
針對于模型校準度,用H-L(Hosmer-Lemeshow)檢驗進行,獲得結果:chi-square=2.985,P=0.935。P>0.05提示本研究所獲得的預測準確度較高。
針對于預測模型區分度,應用ROC 曲線下面積(AUC)進行檢驗。繪制出ROC 曲線,得出AUC 為0.82,95%CI為(0.79,0.90)。該模型最佳截斷值為0.50,經計算可得靈敏度79.4%,特異度75.9%,約登指數為0.55,判定此模型的區分度較好,預測模型具有臨床意義。
2.4.2 驗證預測模型 為檢驗該模型的預測效能是否具有代表性,將驗證組的病例數據代入方程驗證,繪 出ROC 曲 線,此 中AUC 為0.85,95%CI為(0.71,0.99)。該模型最佳截斷值為0.48,,經計算可得靈敏度81.0%,特異度75.0%,約登指數為0.56,判定此模型的預測價值較好。
3 討論
在臨床的實踐及研究中,我們可以觀察到各種各樣的感染性疾病,尤其是以細菌為病原體的,因為隨著時代的發展與變遷,感染細菌種類以及疾病形態的多樣化在不斷增長,治療的難度也隨之在不斷加大。惡性血液病病人的細菌感染率更是居高不下,并且細菌感染也成為了其死亡的主要原因之一,其中碳青霉烯類抗菌藥物耐藥菌感染對血液病病人的預后結果影響深重尤為需要關注。
通過進行單因素分析,我們能夠觀察到,在存活亞組和死亡亞組之間,包含有血液疾病譜、耐藥菌感染前住院時間、抗生素使用時間、抗生素使用種類(為住院期間應用的總種類數)、最多幾種抗生素聯合使用、使用過碳青霉烯類抗菌藥物與否、使用過其余特殊使用級抗生素與否、中性粒細胞計數、粒細胞缺乏持續時間以及心腦血管疾病病史等的10 項因素差異有統計學意義。雖然罹患惡性血液病的病人體內正常的免疫細胞幾乎均不足,并且多數情況下其無法避免應用化療和(或)免疫抑制治療,但畢竟不同類型的疾病在血細胞數量功能、臨床表現以及疾病所接受的治療方式等方面仍有較大差距,以至于其免疫系統功能具有較大差異,因此當不同疾病的病人均遭受到耐藥菌感染時,其在感染致病菌的清除能力以及對抗菌藥物的耐受與應答能力方面上仍有較大差別。尤為重要的乃是粒細胞缺乏,由于其不僅影響病人對致病的病原體的免疫能力,而且對所應用抗生素的PK(藥物代謝動力學)∕PD(藥物效應動力學)也有關鍵作用。與細胞數較高的病人相比照,粒細胞缺乏病人應用同種藥物可能出現不同的抗菌活性。中性粒細胞減少乃至于缺乏的病人機體免疫能力嚴重不足,對致病菌進行免疫應答的能力遠不及其余病人。另外,粒細胞缺乏的病人由于機體免疫能力差及感染發生時大多無明顯的癥狀體征,以至于發生各種感染后無法實時獲知,病人難以得到及時而有效的治療。而且粒細胞缺乏時間的越久,就越易導致不良預后的發生。在發生感染前較長的住院時間一般會代表著該病人接受了較久治療的可能性大,而惡性血液病病人所接受的治療手段對免疫系統功能難免造成更大的影響,且影響程度隨著時間增長而增大。對罹患感染的病人來說,抗菌藥物尤其是針對于病原菌具備敏感性的抗菌藥物被早期應用,本身具有積極意義,但長期、大量地使用限制性尤其是特殊使用級抗生素會導致病人的身體功能壓力較大、治療成本難以承受,并且難免篩選出其相應的耐藥性菌株,致使不良預后的出現概率增加,因而抗生素的使用時長、種類等情況自然是本研究中的風險因素。同時,長期且(或)大量抗生素的應用也意味著既往可能發生嚴重的難治性感染,耐藥菌感染的產生和與之相關的死亡的出現也就自然而然了。另外,眾所周知,心腦血管疾病會導致罹患該類病癥的病人耐受能力較差,因此當發生細菌感染時,其更易發生不良預后[6,14-22]。
P<0.2 的因素被運行于logistic 回歸方程分析中,惡性血液病病人發生碳青霉烯類耐藥菌感染后死亡的危險因素被輸出,即感染前長時間住院、感染前使用過其余的特殊使用級抗生素、感染前中性粒細胞計數偏低以及罹患心腦血管疾病。正如上文所述,感染前住院時間長、中性粒細胞的數量較低以及心腦血管疾病本身均意味著病人較低的機體免疫力,容易提高不良預后的發生率。而早期使用特殊使用級抗生素對病人免疫功能以及經濟造成較大壓力,當誘使相應耐藥菌出現時會增加選擇抗菌藥物的難度,增加了不良預后的發生率[17-25]。
而根據logistic(P)意為ln(p∕1-p),所得的回歸方程可轉化為p=EXP(0.061×感染前住院時間+1.868×使用過其余特殊使用級性抗生素與否-0.412×中性粒細胞計數+1.345×心腦血管疾病-1.309)∕[1+EXP(0.061×感染前住院時間+1.868×是否使用過其余種類的特殊使用級性抗生素-0.412×中性粒細胞計數+1.345×患心腦血管疾病與否-1.309)]。將待進行風險預測病人的相應數據代入后可計算出p值,若p值小于最佳截斷值,則可認為病人死亡風險較低,反之則可判斷為死亡風險較高。由于不同組別資料的最佳截斷值有一定差異,但一般處于0.5 上下,故在進行臨床應用時可以將其分為三個死亡風險組來進行預測,p≤0.45 為低危組,0.45<p<0.55 為中危組,p≥0.55為高危組。
該模型的建立有助于進行危險度分層、早期識別高風險病人,并采取相應可減少不良預后發生的措施。病人在出現感染前的住院時間的縮短有助于降低發生耐藥菌感染的惡性血液病病人的死亡風險,因而應在保證治療效果的前提下盡可能減少病人在前期的治療周期,當住院時間不可避免地較長以及病人有心腦疾病病史時應針對其不同的生理以及病情狀況選用適宜的抗生素進行防治,但由于使用特殊使用級抗生素對病人的預后有著部分不利影響,故不建議在耐藥菌感染發生前過早進行應用。另外,保證中性粒細胞的數量以及促使粒細胞早期恢復對減少不良預后的發生率更是意義重大。
4 小結
在本研究中得到感染前住院時間長、感染前使用過其余的特殊使用級抗生素、感染前中性粒細胞計數偏低以及心腦血管疾病病史等伴發碳青霉烯類耐藥細菌感染的惡性血液病病人整體死亡率的風險因素;以其作為預測因子,可以得到一個具有良好預測效能的預測模型,可提供參考價值給醫院感染后不良預后的風險評測與預警系統,有助于減少病人不良預后的發生率。

