體質指數正常的多囊卵巢綜合征女性發(fā)生高脂血癥的影響因素研究
劉洋,王宇,,叢晶,宮藝,韓布威,王凱悅,朱夢一,張蓓,吳效科*
1.150040 黑龍江省哈爾濱市,黑龍江中醫(yī)藥大學研究生院
2.150040 黑龍江省哈爾濱市,黑龍江中醫(yī)藥大學附屬第一醫(yī)院婦科一科
3.315000 浙江省寧波市北侖區(qū)人民醫(yī)院中醫(yī)科
4.221000 江蘇省徐州市中心醫(yī)院婦產科
多囊卵巢綜合征(PCOS)作為婦科最常見的內分泌失調和生殖障礙疾病,在育齡期婦女中的患病率高達10%。其臨床表現(xiàn)多樣且伴隨著高雄激素血癥、代謝綜合征(MS)、胰島素抵抗(IR)等[1]。脂代謝異常已被認為是心血管疾病的獨立危險因素,也是PCOS 兇險的遠期并發(fā)癥之一。近年研究發(fā)現(xiàn),PCOS 患者的脂質代謝紊亂發(fā)生率高達70%,血脂異常也是MS 的組成部分,與肥胖和IR 的關系更為密切[2]。有研究表明在BMI 正常的PCOS 患者中具有較高的脂質代謝水平[3]。然而,目前針對BMI 正常的PCOS 人群中血脂異常的文獻較少,因此本研究針對BMI 正常的PCOS 患者伴或不伴高脂血癥的臨床和生化指標水平差異性進行研究,探討B(tài)MI 正常的PCOS 患者發(fā)生高脂血癥的影響因素,為預防和治療PCOS 患者以及可能發(fā)生的心腦血管疾病等并發(fā)癥提供理論依據和個性化治療。
1 對象與方法
1.1 研究對象
本研究是一項二次分析,數據來自“針刺和克羅米芬對多囊卵巢綜合征婦女活產率的影響(PCOSAct)”臨床試驗數據[4]。該臨床試驗在中國大陸的21 個分中心(27 家醫(yī)院)招募了1 000 名年齡20~40 歲的不孕PCOS 患者。當地的機構審查委員會批準了該方案,所有患者及其伴侶在加入研究前提供了書面知情同意。該臨床試驗由一個多學科指導委員會主持,并由一個國際數據和安全監(jiān)測委員會監(jiān)督。這是一項多中心、大樣本的2×2 析因隨機對照試驗,詳細的臨床試驗研究設計、方法、納入與排除標準和主要結果均已發(fā)表[4-5]。臨床試驗編號為NCT01573858。本研究經黑龍江中醫(yī)藥大學附屬第一醫(yī)院倫理委員會審批(批號:2010HZYLL-010)。本研究選取BMI 正常(18.5 kg/m2≤BMI<24.0 kg/m2)的PCOS 患者共428 例。
1.2 納入與排除標準(以PCOSAct 的標準為基礎)
納入標準:(1)年齡20~40 歲;(2)符合PCOS診斷標準;(3)BMI ≥18.5 kg/m2且<24.0 kg/m2;(4)自愿簽署知情同意書。
排除標準:(1)臨床資料不完整;(2)最近3 個月內使用激素或其他藥物。
1.3 診斷標準(以PCOSAct 的標準為基礎)
1.3.1 西醫(yī)診斷標準如下。參與者均符合修訂版鹿特丹PCOS 診斷標準[6]:(1)稀發(fā)排卵或無排卵;(2)高雄激素臨床表現(xiàn)和/或高雄激素血癥;(3)卵巢多囊樣改變,即超聲提示一側或雙側卵巢內直徑為2~9 mm的卵泡≥12 個,卵巢體積≥10 mL;必須滿足(1),其余至少滿足1 條,并排除其他高雄激素的病因和先天性腎上腺皮質增生、庫欣綜合征、分泌雄激素性腫瘤。
1.3.2 根據《中國成人血脂異常防治指南》判斷高脂血癥的評價標準為:總膽固醇(TC)≥6.22 mmol/L 和/或三酰甘油(TG)≥2.26 mmol/L 和/或低密度脂蛋白(LDL)≥4.14 mmol/L 和/或高密度脂蛋白(HDL)<1.04 mmol/L[7]。
1.4 研究指標
1.4.1 基本信息、人體測量學指標:本研究從PCOSAct項目提取了年齡、嘗試妊娠時間、糖尿病家族史、高血壓家族史、體質量、BMI、腰圍(WC)、腰臀比(WHR)、收縮壓、舒張壓等指標的數據。
1.4.2 性激素水平:每個參與者在月經周期的第3 天收集血液樣本。所有血樣運回黑龍江中醫(yī)藥大學核心實驗室測定。檢測指標包括游離睪酮(FT)、睪酮(TT)、黃體生成素(LH)、卵泡刺激素(FSH)、性激素結合球蛋白(SHBG)、抗米勒管激素(AMH)檢查、游離雄激素指數(FAI)。按照公式計算FAI=TT/SHBG×100。
1.4.3 糖脂代謝:檢測指標包括空腹胰島素(FINS)、空腹葡萄糖(FBG)、胰島素抵抗指數(HOMA-IR)、HDL、LDL、TC、TG、載脂蛋白B(ApoB)、載脂蛋白A1(ApoA)、脂蛋白(LP)。HOMA-IR=FINS(mU/mL)×FBG(mmol/L)/22.5。
1.4.4 心肌酶、肝功能指標:包括丙氨酸氨基轉移酶(ALT)、天冬氨酸氨基轉移酶(AST)、乳酸脫氫酶(LDH)、胱抑素C(CysC)、同型半胱氨酸(HCY)、總膽汁酸(TBA)、總膽紅素(TB)、直接膽紅素(DB)、間接膽紅素(IB)。
1.5 統(tǒng)計學方法
采用SPSS 25.0 統(tǒng)計學軟件進行數據分析。符合正態(tài)分的定量資料以(±s)表示,兩組間均數比較采用獨立樣本t檢驗,不符合正態(tài)分布的定量資料以M(QR)表示,兩組間比較采用非參數秩和檢驗。計數資料以相對數表示,組間比較采用χ2檢驗或Fisher's 確切概率法。采用多因素Logistic 逐步回歸分析探討高脂血癥的潛在預測因子。以P<0.05 為差異有統(tǒng)計學意義。
2 結果
2.1 PCOS 患者血脂異常情況
428 例PCOS 患者中138 例被診斷為高脂血癥,TC、TG、HDL、LDL 的異常率分別為7.24%(31 例)、12.15%(52 例)、18.46%(79 例)、7.01%(30 例)。單一表型異常率較高,為21.73%(93 例),多個表型異常率為10.51%(45 例)。根據高脂血癥參考標準將本研究分為兩組:高脂血癥組(138 例)和無高脂血癥組(290 例)。
2.2 兩組患者臨床特征和生化指標比較
與無高脂血癥組相比,高脂血癥組患者年齡、糖尿病家族史占比、體質量、BMI、腰圍、WHR 較大,嘗試妊娠時間較長,差異均有統(tǒng)計學意義(P<0.05)。高脂血癥組中FAI、FINS、HOMA-IR、LDL、TC、TG、APOB、ALT、LDH 水平較無高脂血癥組高,SHBG、AMH、HDL、APOA、TB、DB 水平較無高脂血癥組低,差異有統(tǒng)計學意義(P<0.05),見表1。
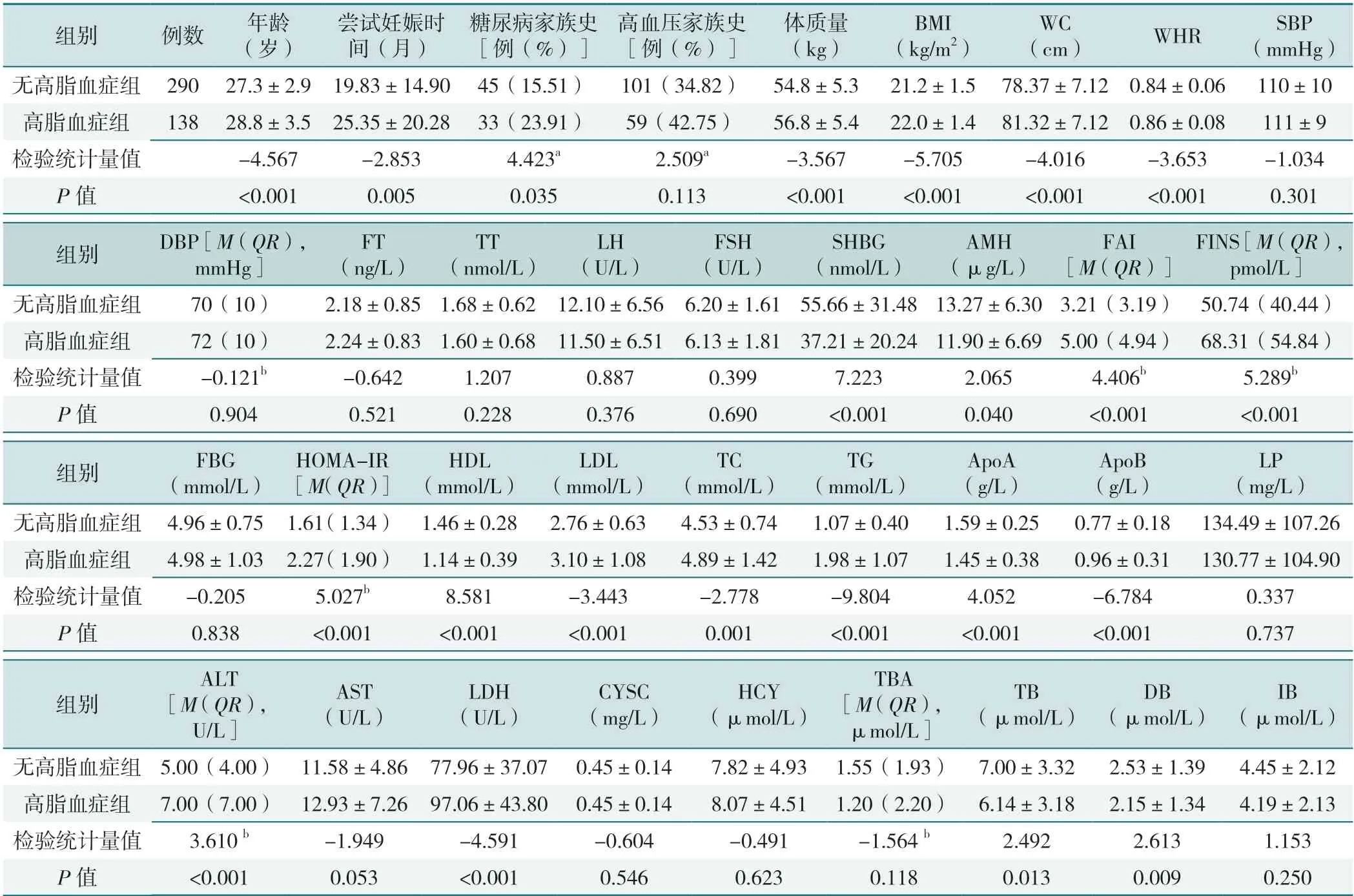
表1 兩組患者臨床特征和生化指標比較Table 1 Comparison of clinical characteristics and biochemical indices between two groups of patients
2.3 BMI 正常的PCOS 患者高脂血癥的影響因素分析
以BMI 正常的PCOS 患者是否伴有高脂血癥為因變量(賦值:是=1,否=0),與無高脂血癥比較差異有統(tǒng)計學意義的指標(賦值為實測值)為自變量,應用逐步向前法分析進行多因素Logistic 回歸分析,結果顯示年齡、BMI、HOMA-IR、LDH 是正常BMI 的PCOS 患者發(fā)生高脂血癥的獨立危險因素(OR=1.170、1.348、1.172、1.009),SHBG 是獨立保護因素(OR=0.979,P<0.05),見表2。
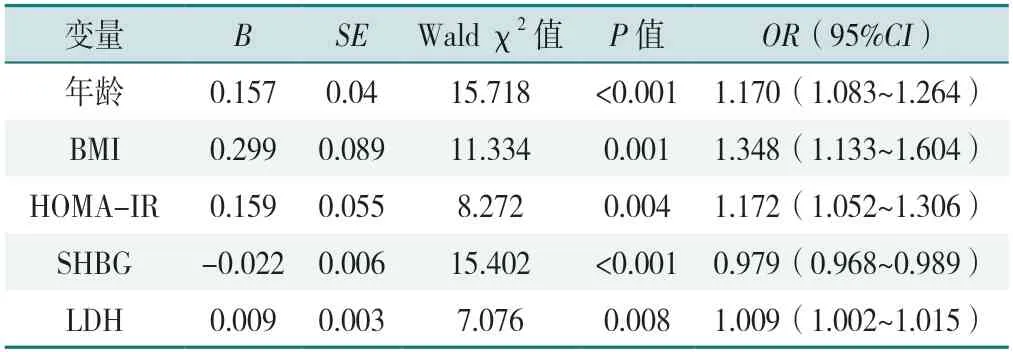
表2 BMI 正常的PCOS 患者高脂血癥患病的多因素Logistic 回歸分析Table 2 Multivariate Logistic regression analysis of the prevalence of hyperlipidemia in PCOS patients with normal BMI
3 討論
PCOSAct 項目是一項在2011—2015年從中國大陸不同地理區(qū)域的不同地點招募PCOS 患者的隨機對照試驗,在中國PCOS 群體中具有普遍的代表性。PCOS 與肥胖關系密切,常伴有高雄激素血癥、IR 和血脂異常等,高脂血癥是導致女性不孕的原因之一,可增加其遠期并發(fā)癥風險。但針對BMI 正常的PCOS 患者伴高脂血癥的研究較少,因此有必要對此類型人群的患病率和影響因素進行研究。本研究通過對BMI 正常的PCOS 患者是否合并高脂血癥進行研究,BMI 正常的PCOS 患者合并高脂血癥的發(fā)生率為32.24%,最常見的血脂異常類型是HDL 水平降低且單一表型較多。在本臨床試驗數據中整體PCOS 患者高脂血癥患病率為41.3%[8],這與其他研究結果相似[9]。因此BMI 正常的中國PCOS 女性中脂代謝異常不應該被忽視。本研究表明年齡、BMI、HOMA-IR、SHBG、LDH 均是BMI 正常的PCOS 女性血脂異常的影響因素。
黃翠玉等[10]對213 例PCOS 患者進行研究,發(fā)現(xiàn)血脂異常組與血脂正常組相比,SHBG、FAI 降低,F(xiàn)INS、HOMA-IR、TG、TC、LDL、APOB 水平升高。本研究結果與之一致。眾所周知,年齡是對脂質水平具有強烈影響的生理因素[11]。本研究表明高脂血癥組較非高脂血癥組年齡偏大,也是BMI 正常的PCOS 女性發(fā)生高脂血癥的獨立危險性因素。TC 和LDL 水平隨著年齡的增長而增加,并優(yōu)先堆積在腹部區(qū)域,也就是內臟脂肪的積累,會導致脂肪細胞及其相關巨噬細胞分泌大量細胞因子的增加,從而導致促炎狀態(tài),干擾胰島素信號轉導通路,引起機體糖脂代謝紊亂。
IR、肥胖、高胰島素血癥、高雄激素血癥、動脈粥樣硬化等病理狀態(tài)與PCOS 血脂異常密切相關,既獨立又相互作用于脂代謝異常[12]。其中IR 是PCOS 患者脂代謝異常的中心環(huán)節(jié),50%~75%的PCOS 患者會伴有不同程度的IR。臨床上常以HOMA-IR ≥2.69 作為IR 的診斷標準,本研究中高脂血癥組的HOMA-IR平均值>2.69,也是發(fā)生高脂血癥的獨立危險因素。腹型肥胖是心血管以及代謝疾病發(fā)生的獨立危險因素。根據國際糖尿病協(xié)會標準中[13],亞洲女性MS 必備指標為WC ≥80 cm,本研究中高脂血癥組的WC 平均值>80 cm,提示在PCOS 正常BMI 人群中多為腹型肥胖,PCOS 女性的血脂異常可能與胰島素抵抗狀態(tài)下的患者一致,血脂異常者和IR 發(fā)生率具有正相關性[14]。既往研究發(fā)現(xiàn)在BMI 正常的PCOS 患者中BMI、WC、FAI、TG 是IR 的獨立危險因素,AMH、TB、磷、HDL是獨立保護因素[15-16]。IR 主要通過刺激脂肪分解、改變脂蛋白脂酶和肝脂酶的表達發(fā)揮關鍵作用[17]。脂質代謝異常可影響卵子質量,也可導致子宮內膜種植窗脂聯(lián)素水平下降,內膜容受性差[18]。
在性激素水平上,有研究顯示PCOS 患者睪酮與血脂異常沒有關系[19]。FAI 由睪酮和SHBG 計算獲得,是評估PCOS 患者高雄激素血癥最敏感的測量指標[20]。SHBG 是運輸雌激素和雄激素的載體,與脂蛋白脂酶活性呈正相關。BMI 被認為是循環(huán)SHBG 濃度的主要決定因素,在本研究中SHBG 是正常BMI 的PCOS 患者發(fā)生高脂血癥的獨立保護因素。在PCOS 女性中SHBG 與IR程度呈負相關,SHBG 可能通過調節(jié)IR 影響脂質代謝。既往研究表明SHBG 可以影響葡萄糖轉運蛋白和PI3K信號轉導通路,與IR 和糖尿病的相關性比較復雜[8,21]。
LDH 是臨床上衡量心臟功能的常用指標,可以輔助診斷心肌梗死。LDH也是參與糖酵解最后一步的催化酶。糖酵解中期腺嘌呤核苷三磷酸生成減少,這也是PCOS患者卵泡發(fā)育不良的主要因素[22]。miRNA 控制糖酵解酶的表達,通過細胞中的Warburg 效應調節(jié)糖酵解[23]。既往研究表明來源卵泡液子的外泌體miR-143-3p/miR-155-5p 通過沉默關鍵酶HK2、PKM2 和LDHA 拮抗PCOS 中顆粒細胞的糖酵解介導卵泡發(fā)育不良[24]。但LDH 與血脂方面的研究較少,本研究顯示LDH 是正常BMI 的PCOS 患者發(fā)生高脂血癥的獨立危險性因素,未來需要更多研究來解釋此機制。
本研究從中國大陸不同地理區(qū)域的不同地點招募PCOS 患者,增加了隊列的普遍性,樣本較大,數據真實可靠。本研究發(fā)現(xiàn)年齡、BMI、HOMA-IR、LDH、SHBG 均是高脂血癥的影響因素,與胰島素抵抗關系密切。對于所有PCOS 患者應該進行血脂測定,避免漏診延誤病情,影響PCOS 患者治療。
本研究存在局限性:本研究未全面、系統(tǒng)地評估生活方式、飲食類型、經濟條件對PCOS女性血脂譜的影響;未對受試者進行長期隨訪,因此本研究無法評估患者真正的心血管健康問題。
綜上,PCOS 合并高脂血癥的發(fā)病機制通常涉及IR,使女性患心血管疾病的風險增加,高脂血癥和IR呈正相關。BMI 正常的PCOS 患者高脂血癥發(fā)生率為32.24%,故不能忽視BMI 正常PCOS 女性的血脂情況。本研究發(fā)現(xiàn)年齡、BMI、HOMA-IR、LDH 是高脂血癥的獨立危險因素,SHBG 是高脂血癥的獨立保護因素。因此無論BMI 是否正常,PCOS 女性應該接受全面的血脂管理和篩查。生活方式的改變是所有PCOS 女性的一線治療,對BMI 正常的PCOS 女性也尤其重要,建議對其加強篩查和管理以減少遠期并發(fā)癥風險。
作者貢獻:劉洋負責研究的構思與設計,數據收集整理以及論文撰寫;王宇、叢晶、張蓓負責統(tǒng)計學分析;宮藝、韓布威、王凱悅、朱夢一參與數據的收集和整理;吳效科負責文章的質量控制與審校,對文章整體負責。
本文無利益沖突。

