內鏡黏膜下剝離術與外科手術治療未分化型早期胃癌的遠期療效對比
趙玉杰 袁 茹 王 峰 郝曉莉
作者單位:450000 鄭州大學第一附屬醫院
早期胃癌是較為常見的一種惡性腫瘤,癌細胞僅局限于黏膜層及黏膜下層,臨床通常采取外科手術治療。但外科手術具有手術時間長、創傷大、并發癥多等缺點,且手術破壞了胃的正常解剖結構,影響術后胃腸功能恢復[1]。近年來內鏡技術不斷發展進步,內鏡黏膜下剝離術(ESD)逐漸應用于臨床,ESD治療早期胃癌可一次性完整切除病灶,取得傳統外科手術的效果[2]。由于未分化型早期胃癌的病變邊界及浸潤深度確定困難,ESD治療后切緣陽性率較高,存在較高的淋巴轉移風險,臨床對于ESD治療未分化型早期胃癌的遠期療效仍存在爭議[3]。有研究表明,在符合ESD擴大適應癥的條件下,采用ESD治療未分化型早期胃癌的復發率、淋巴及遠處轉移率、長期生存率與外科手術相近[4]。基于此,本研究探討ESD與外科手術治療未分化型早期胃癌遠期的遠期療效。
1 資料與方法
1.1 一般資料
回顧性分析2016年1月至2018年12月期間我院收治的82例未分化型早期胃癌患者臨床資料,按治療方式不同分為外科手術組(41例)和ESD組(41例),研究經醫學倫理委員會批準。外科手術組男性25例,女性16例;年齡38~76歲,平均年齡(59.35±7.61)歲;腫瘤直徑11~23 mm,平均直徑(18.30±2.12)mm;合并潰瘍:有14例,無27例;病變縱向位置:上1/3有8例,中1/3有5例,下1/3有28例;病變橫向位置:小彎側17例,大彎側10例,前臂側3例,后壁側11例;分化類型:低分化腺癌26例,印戒細胞癌3例,低分化腺癌伴印戒細胞癌12例;體重指數18.7~27.5 kg/m2,平均體重指數(23.03±1.59)kg/m2。ESD組男性23例,女性18例;年齡40~78歲,平均年齡(58.72±7.96)歲;腫瘤直徑10~26 mm,平均直徑(18.62±2.45)mm;合并潰瘍:有16例,無25例;病變縱向位置:上1/3有12例,中1/3有4例,下1/3有25例;病變橫向位置:小彎側13例,大彎側13例,前臂側5例,后壁側10例;分化類型:低分化腺癌22例,印戒細胞癌6例,低分化腺癌伴印戒細胞癌13例;體重指數18.9~27.4 kg/m2,平均體重指數(23.07±1.55)kg/m2。兩組一般資料均衡無統計學差異(P>0.05)。
1.2 入選標準
(1)納入標準:符合未分化型早期胃癌診斷標準[5];術前經胃鏡或超聲內鏡檢查證實無淋巴結及遠處轉移;隨訪時間3年及以上;ESD組存在部分超ESD擴大適應癥(病變直徑≤20 mm,不伴潰瘍、脈管瘤及神經侵犯)的情況,應患者及家屬要求先行ESD治療;臨床資料完整。(2)排除標準:合并淋巴結轉移、淋巴管或血管侵犯者;有胃癌手術史者;合并其他腫瘤者。
1.3 方法
1.3.1 外科手術組 行外科手術(D1+β或者D2淋巴結清掃術)治療:對患者行全身麻醉,D1+β淋巴結清掃術包括胃左動脈淋巴結(No.7)、肝總動脈淋巴結(No.8a)和腹腔干淋巴結(No.9);患者為遠端胃癌時,D2淋巴結清掃術包括脾動脈近端淋巴結(No.11p)、肝十二指腸韌帶內沿肝動脈淋巴結(No.12a)和腸系膜上靜脈淋巴結(No.14v);患者為近端1/3胃癌時,D2淋巴結清掃術包括脾門淋巴結(No.10)和脾動脈近端及遠端淋巴結(No.11p及No.11d)。術后標本進行病理檢查。
1.3.2 ESD組 行ESD治療:術前采用丙泊酚行靜脈麻醉,確定病灶部位,在病灶外側5 mm位置標記,采用傳統白光內鏡準確評估定位病灶,采用0.0005%腎上腺素1 mL+靛胭脂5 mL+10%甘油100 mL+5%果糖+生理鹽水混合液注射于病灶邊界外≥1.0 cm處黏膜下層進行標記;待注射病灶充分隆起,采用一次性黏膜切開刀對標記外0.5 cm處進行環形切開,充分剝離黏膜下腫瘤組織,完整切除病灶部位;采用氬離子凝固對切口顯現的血管進行止血,對于血管顯露面積較大者,選用止血鉗夾閉血管止血。術后標本進行病理檢查。
1.4 觀察指標
(1)手術質量:比較兩組患者病變部位水平切緣及垂直切緣陽性率,并評價兩組的切除效果,包括整塊切除率(切除病灶完整且獲得單塊標本)、完全切除率(切除病灶完整且水平、垂直切緣均為陰性)。(2)手術情況:統計并比較兩組手術時間、術中出血量及手術切口長度。(3)胃腸功能恢復情況:統計并比較兩組患者術后首次排氣時間、腸鳴音恢復時間、首次進食時間。(4)并發癥發生率:觀察并記錄兩組患者術后發生感染(包括傷口、腹腔、肺部感染等)、穿孔、出血、腸狹窄、急性肝損傷等并發癥情況。(5)隨訪結果:兩組患者術后定期回院復查,行胃鏡及CT檢查,統計3年生存率及復發率。
1.5 統計學方法

2 結果
2.1 兩組手術質量對比
ESD組病變部位水平、垂直切緣陽性率和完全切除率與外科手術組比較(P>0.05),見表1。

表1 兩組手術質量對比(例,%)
2.2 兩組手術情況對比
ESD組手術時間、手術切口長度短于外科手術組,術中出血量少于外科手術組,(P<0.05),見表2。
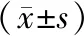
表2 兩組手術情況對比
2.3 兩組患者胃腸功能恢復情況對比
術后首次排氣、腸鳴音恢復、首次進食時間比較,ESD組較短(P<0.05),見表3。
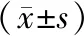
表3 兩組患者胃腸功能恢復情況對比
2.4 兩組并發癥發生率對比
ESD組并發癥發生率低于外科手術組(P<0.05),見表4。

表4 兩組并發癥發生率對比(例,%)
2.5 隨訪結果
隨訪期間,外科手術組有1例(2.44%)患者于術后7個月發生遠處轉移,病灶直徑15 mm,切緣陰性,患者拒絕治療,于術后13個月死亡;另有1例(2.44%)患者于術后29個月發生局部復發,病灶直徑11 mm,切緣陰性,未行治療。ESD組有1例(2.44%)患者于術后10個月發生淋巴結轉移,病灶直徑27 mm,病變部位水平、垂直切緣均為陽性,患者拒絕接受外科手術,于術后25個月死亡。
3 討論
對于胃癌臨床遵循早發現、早診斷、早切除的治療原則[6]。未分化型早期胃癌無明顯的臨床癥狀,其病情發展較為隱匿,通過超聲、內鏡可判斷病變范圍及胃壁結構,為合理選擇治療方式提供指導[7]。傳統外科手術雖能徹底切除胃癌組織,但該治療手段對患者造成的創傷較大,患者預后較差,故在臨床中應用受限[8]。
ESD是一種新型的微創治療手段,可在內鏡下對病變組織進行全面切除,還可清掃部分黏膜下病變組織,達到根治效果[9]。本研究ESD組手術時間、切口長度均較外科手術組短,術中出血量較低,術后胃腸功能恢復時間較短,并發癥發生率較低。說明ESD治療未分化型早期胃癌較外科手術治療對患者造成的創傷更小,利于改善預后。未分化型早期胃癌始發于黏膜和黏膜下層,ESD經口或腸道等自然腔道即可進行病變的剝除,相較于外科手術,其創傷更小,能夠減少術中出血,從而加快術后康復。ESD在內鏡輔助下可重復進行操作,并完整剝離黏膜下腫瘤,為病理科檢查提供完整的標本,評估整體病變,達到與外科手術基本相當的效果[10-11]。本研究中,ESD組僅有3例(7.32%)水平切緣陽性,2例(4.88%)垂直切緣陽性,且隨訪3年僅有1例(2.44%)患者淋巴結轉移,顯著低于既往研究報道[12]。其原因在于,本研究在ESD術前進行精細檢查,精確確定病變范圍,預測浸潤深度,術中標記位于病變邊界外≥1.0 cm處,且在標記外0.5 cm 處切開,通過擴大病變切除范圍降低切緣陽性率。本研究ESD組完全切除率較低,切緣陽性率較高,可能與以下因素有關:ESD術中未完全切除腫瘤組織,導致切緣殘存病變;ESD操作技術和熟練程度存在個體差異性。穿孔、出血是ESD常見的并發癥,ESD術中使用電凝止血預防出血,同時采用鉗夾封閉止血,能夠有效減少穿孔的發生,因而ESD組并發癥發生率更低,與謝小月等[13]研究結果一致。
本研究中外科手術組共有2例患者出現了遠處轉移和局部復發,說明外科手術也不能確保未分化型早期胃癌的絕對治愈。對于此類患者,應進行嚴密隨訪,定期復查,必要時追加外科治療[14]。考慮到ESD能夠達到外科手術相近的治療效果,加上其微創優勢,建議臨床將ESD作為部分未分化型早期胃癌的治療手段,且于術前進行精細檢查,最大程度切除病灶,術后密切隨訪,對于病情復發或轉移者及時予以治療,以盡可能改善患者預后。
綜上所述,ESD治療未分化型早期胃癌可獲得與外科手術基本相當的遠期療效,且手術情況較好,手術切口小,并發癥發生率更低,利于患者術后快速康復,臨床應在滿足ESD適應癥的基礎上擴大ESD的切除范圍,以改善患者預后。

