擬紅紫珠中1個新的木脂素葡萄糖苷化合物
趙 興,劉翰飛,王 歡,林開琴,李金玉,潘衛東,婁華勇*,孫 超*
擬紅紫珠中1個新的木脂素葡萄糖苷化合物
趙 興1, 3,劉翰飛1, 2,王 歡1, 3,林開琴1, 3,李金玉1, 2,潘衛東1,婁華勇1, 2*,孫 超1, 2*
1. 貴州醫科大學 省部共建藥用植物功效與利用國家重點實驗室,貴州 貴陽 550014 2. 貴州省天然產物研究中心,貴州 貴陽 550014 3. 貴州醫科大學藥學院,貴州 貴陽 550025
研究擬紅紫珠的化學成分及其生物活性。利用多種色譜手段(硅膠、Sephadex LH-20、RP-18反相硅膠柱色譜和半制備型HPLC等)進行分離純化,運用理化性質結合現代波譜學(紫外、紅外、核磁、質譜等)技術進行結構鑒定。采用RSL3誘導的HT22小鼠海馬神經元細胞模型鐵死亡抑制活性進行篩選。從擬紅紫珠中分離得到11個化合物,分別鑒定為(7,7?,8,8?,9)-芝麻素-9----葡萄糖苷(1)、(+)-松脂素-4β--葡萄糖苷(2)、(7,7′,7″,7?,8,8′,8″,8?)-4″,4?-二羥基-3,3′,3″,3?,5,5′-六甲氧基-7,9′;7′,9-二環氧-4,8″;4′,8?-雙氧-8,8′-雙新木脂素- 7″,7?,9″,9?-四醇(3)、(7,7′,7″,7?,8,8′,8″,8?)-4″,4?-二羥基-3,3′,3″,3?,5,5′-六甲氧基-7,9′;7′,9-二環氧-4,8″;4′,8?-雙氧-8,8′-雙新木脂素-7″,7?,9″,9?-四醇(4)、泡桐素(5)、4-氧代芝麻素(6)、芝麻素(7)、β-谷甾醇(8)、熊果酸(9)、3β-羥基豆甾-5烯-7-酮(10)和3β-羥基豆甾-5,22-二烯-7-酮(11)。生物活性結果顯示,化合物7、10和11對RSL3誘導的HT22細胞鐵死亡較模型組有明顯的抑制活性,其細胞存活率分別為30.37%、31.93%和36.57%(模型組為23.4%)。化合物1為新化合物,命名為擬紅紫珠苷A。所有化合物均為首次從擬紅紫珠中分離得到,且3個化合物顯示出潛在的鐵死亡抑制活性。
擬紅紫珠;木脂素糖苷;擬紅紫珠苷A;芝麻素;熊果酸;3β-羥基豆甾-5烯-7-酮;鐵死亡抑制
唇形科藥用植物資源豐富,藥用部位廣且藥效多樣,開發潛力巨大[1]。如紫蘇(L.) Britt.的葉、莖、成熟果實可作3種不同藥材入藥[2];羅勒L的莖葉、種子、全草均具有藥用價值,其嫩葉可食用作茶飲,還可用作調香原料、配制化妝品以及牙膏、漱口劑[3]。近年來,本課題組一直致力于黔產唇形科植物中活性物質基礎的挖掘,先后開展了夏枯草[4-5]、貴州鼠尾草[6-7]等藥用植物的系統研究,獲得的結構類型主要包括二萜、三萜、倍半萜、甾體和黃酮等,并從中發現了許多結構新穎的活性先導物。紫珠屬Linn.是唇形科的代表屬植物之一,具有收斂止血、清熱解毒的功效,常用于治療各種內、外出血,也可治療燒傷燙傷,現代藥理研究表明其還具有神經保護等活性[8-9]。與此同時,經系統文獻調研發現,紫珠屬植物擬紅紫珠H. T. Chang的化學成分及其活性研究至今未見系統報道。為了進一步研究該植物的化學成分,闡明其主要的藥效物質基礎。本課題組對采自貴州興義的擬紅紫珠進行了化學成分研究,從中分離獲得了11個化合物,分別鑒定為(7,7?,8,8?,9)-芝麻素- 9--β--葡萄糖苷(1)、(+)-松脂素-4β--葡萄糖苷[(+)-pinoresinol-β--glucopyranoside,2]、(7,7′,7″, 7?,8,8′,8″,8?)-4″,4?-二羥基-3,3′,3″,3?,5,5′-六甲氧基-7,9′;7′,9-二環氧-4,8″;4′,8?-雙氧-8,8′-雙新木脂素-7″,7?,9″,9?-四醇 [(7,7′,7″,7?,8,8′,8″,8?)- 4″,4?-dihydroxy-3,3′,3″,3?,5,5′-hexamethoxy-7′,9′;7′,9-diepoxy-4,8″;4′,8?-bisoxy-8,8′-dineo-lignan-7″,7?,9″,9?- tetraol,3]、(7,7′,7″,7?,8, 8′,8″,8?)-4″,4?-二羥基-3,3′,3″,3?,5,5′-六甲氧基-7,9′;7′,9-二環氧-4,8″;4′,8?-雙氧-8,8′-雙新木脂素-7″,7?,9″,9?-四醇[(7,7′,7″,7?,8,8′,8″,8?)-4″,4?-dihydroxy-3,3′, 3″,3?,5,5′-hexamethoxy-7,9′;7′,9-diepoxy-4,8″;4′,8?- bisoxy-8,8′-dineolignan-7″,7?,9″,9?-tetraol,4]、泡桐素(paulownin,5)、4-氧代芝麻素(4-oxosesamin,6)、芝麻素(sesamin,7)、β-谷甾醇(β-sitosterol,8)、熊果酸(ursolic acid,9)、3β-羥基豆甾-5烯-7-酮(3β-hydroxystigmast-5-en-7-one,10)和3β-羥基豆甾-5,22-二烯-7-酮(3β-hydroxy-stigmast-5,22-dien-7-one,11)。其中化合物1為新化合物,所有化合物均為首次從擬紅紫珠中分離獲得,并評價了所得化合物對RSL3誘導的HT22小鼠海馬神經元細胞模型的鐵死亡抑制活性。
1 儀器與材料
ZX201701048 高分辨液質聯用儀(賽默飛世爾科技有限公司);Chirascane圓二色譜儀(Rigaku/日本);MCP·500旋光儀(Anton·Paar/法國);MPA-100 OptiMelt顯微熔點測定儀(北京泰克儀器有限公司);Agilent 1100高效液相色譜儀(美國安捷倫公司);Waters C18半制備色譜柱(250 mm×10 mm,5 μm);Hei-VAP Digital G3旋轉蒸發儀(德國Heidolph公司);INOVA-600 MHz核磁共振儀(美國Varian公司);ZF-7N智能暗箱式三用紫外分析儀(上海嘉鵬科技有限公司);ME204E/02電子分析天平(瑞士Mettler Toledo公司);DLSB-5/20低溫冷卻液循環泵(鄭州長城科工貿有限公司);柱色譜硅膠(60~80、300~400目,青島海洋化工廠);薄層硅膠板(煙臺江友硅膠發展有限公司);色譜甲醇、氘代甲醇 [薩恩化學技術(上海)有限公司];其他試劑均為分析純,水為超純水。
二氧化碳細胞培養恒溫箱[力申科學儀器(上海)有限公司];十萬分之一電子天平[賽多利斯科學儀器(北京)有限公司];超凈工作臺[孚夏醫療科技(浙江)有限公司];低速離心機[湘立科學儀器(湖南)有限公司];高速離心機[盧湘儀離心機儀器(上海)有限公司];倒置顯微鏡[舜宇光學科技(浙江)有限公司];酶標儀[賽默飛世爾科技(美國)公司];恒溫水浴鍋[鼎鑫宜實驗設備(深圳)有限公司];鼓風干燥箱[蘇珀儀器(紹興)有限公司];移液槍 [艾本德生命科學(德國)公司];立式壓力蒸汽滅菌鍋 [博迅醫療生物儀器股份(上海)有限公司];細胞培養板 [耐思生物科技(上海)有限公司];DMEM高糖培養基(gibco);青鏈霉素混合液(Solarbio);微孔濾膜(BioFIL);胰蛋白酶(Solarbio);噻唑藍(Solarbio);PBS緩沖液 [賽維爾生物科技(武漢)有限公司]。
植物于2021年8月采集于貴州省黔西南興義市的南盤江流域,由貴州省黔西南喀斯特區域發展研究院鄧朝義研究員鑒定為唇形科紫珠屬植物擬紅紫珠H. T. Chang,標本(NHZZ20210801)保存于貴州省天然產物研究中心。
2 方法
2.1 提取與分離
擬紅紫珠全草20.0 kg,粉碎后以95%的乙醇回流提取2次,每次2 h。合并提取液,減壓濃縮后用石油醚和醋酸乙酯分別萃取4次,濃縮干燥得石油醚萃取物192.7 g、醋酸乙酯萃取物253 g。醋酸乙酯萃取物用硅膠柱色譜分離,以二氯甲烷-甲醇(100∶1→1∶1)系統洗脫,得到8個洗脫組分FE. 1~8,其中FE.5(18 g)經反相硅膠柱色譜分離,以50%~100%甲醇梯度洗脫,得到8個組分FE. 5-1~5-8,FE.5-3經正相硅膠柱色譜以二氯甲烷-甲醇(100∶1→1∶1)梯度洗脫后得到2個組分FE.5-3a和5-3b。FE.5-3a經HPLC純化(甲醇-水55∶45,2 mL/min)得化合物1(3 mg,R=25 min)。FE.5-1(2 g)經半制備型高效液相(甲醇-水60∶40,2 mL/min)得3個組分FE.5-1a~1c,FE.5-1b(105 mg)經HPLC純化(甲醇-水33∶67,2 mL/min)得化合物2(5 mg,R=37 min);FE.3(38 g)經反相硅膠柱色譜分離,以40%~100%甲醇梯度洗脫,得到5個組分FE. 3-1~3-5,Fr. 3-3(2 g)經Sephadex LH-20凝膠柱色譜(二氯甲烷-甲醇1∶1)后經HPLC純化(甲醇-水47∶53,2 mL/min),得化合物3(3 mg,R=30 min)和4(4 mg,R=40 min)。
石油醚萃取物采用正相硅膠柱色譜分離,以石油醚-醋酸乙酯(100∶1→0∶1)梯度洗脫,得到10個組分Fr. 1~10,其中Fr. 5(76 g)經反相硅膠柱色譜分離,以50%~100%甲醇梯度洗脫,得到10個組分Fr. 5-1~5-20。Fr. 5-10(1 g)經Sephadex LH-20凝膠柱色譜(二氯甲烷-甲醇1∶1)洗脫后再經HPLC純化(甲醇-水55∶45,2 mL/min),得化合物5(10 mg,R=22 min);Fr. 5-12(118 mg)經Sephadex LH-20凝膠柱色譜(二氯甲烷-甲醇1∶1)后經HPLC純化(甲醇-水60∶40,2 mL/min)得化合物6(9 mg,R=31 min);Fr. 5-20(108 mg)經半制備型高效液相(乙腈-水76∶24,2 mL/min)純化后得到化合物7(10 mg,R=17 min)。Fr. 7(25 g)經正相硅膠柱色譜以石油醚-醋酸乙酯(25∶1→1∶1)梯度洗脫,得到8個組分Fr. 7-1~7-8。其中Fr. 7-6 (300 mg)中有結晶析出,得到化合物8(20 mg)。Fr. 7-8(15 g)經反相硅膠柱色譜分離,以50%~100%甲醇梯度洗脫,得到6個組分Fr. 7-8a~7-8f。Fr. 7-8d(20 mg)經正相硅膠柱色譜以石油醚-醋酸乙酯(25∶1→1∶1)梯度洗脫后得到得化合物9(6 mg);Fr. 7-8e(52 mg)經HPLC純化(甲醇-水30∶70,2 mL/min)得化合物10(8 mg,R=17 min)和11(9 mg,R=19 min)。
2.2 化合物1的水解
取化合物2.0 mg,加入2 mol/L的鹽酸5 mL,在80 ℃條件下水解6 h,水解液用醋酸乙酯萃取即得到苷元和單糖萃取物,單糖萃取物與標準品通過TLC檢識(醋酸乙酯-乙醇-水7∶2∶1),其Rf值和比旋光值與-葡萄糖對照品一致,故確定該糖片段為-葡萄糖。
2.3 化合物1的ECD計算
化合物1經Spartan軟件進行構象搜索后,最優構象用gaussian 16的b3lyp/6-31(d) 基組進行構象優化,確定無虛頻后,得到的構象用gaussian16的b3lyp/6-311+(d, p) 基組進行電子圓二色譜(electrostatic circular dichroism,ECD)計算,得到的數據經 SpecDis軟件生成圖像文件,再與化合物1的測試ECD進行對比,最終確定化合物的絕對構型。
2.4 RSL3誘導的HT22細胞鐵死亡抑制活性測試
用DMEM高糖培養基[含10%胎牛血清(FBS),含青霉素鏈霉素雙抗]培養HT22細胞。將細胞置于37 ℃、5% CO2細胞培養箱中進行傳代培養,取對數生長期細胞用于實驗。將處于對數生長期的HT22細胞按3×103個/mL接種于96孔板,每孔90 μL,設置空白對照、陰性對照、Ferrostatin-1(Fer-1)為陽性對照,每組3個平行,培養24 h,每孔同時加入10 μL RSL3誘導劑(1 μmol/L)和10 μL樣品(20 μmol/L),孵育48 h;加入10 μL的MTT染色劑,4 h后,吸取上清液,加入150 μL DMSO,測定吸光度()值。
3 結構鑒定
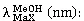
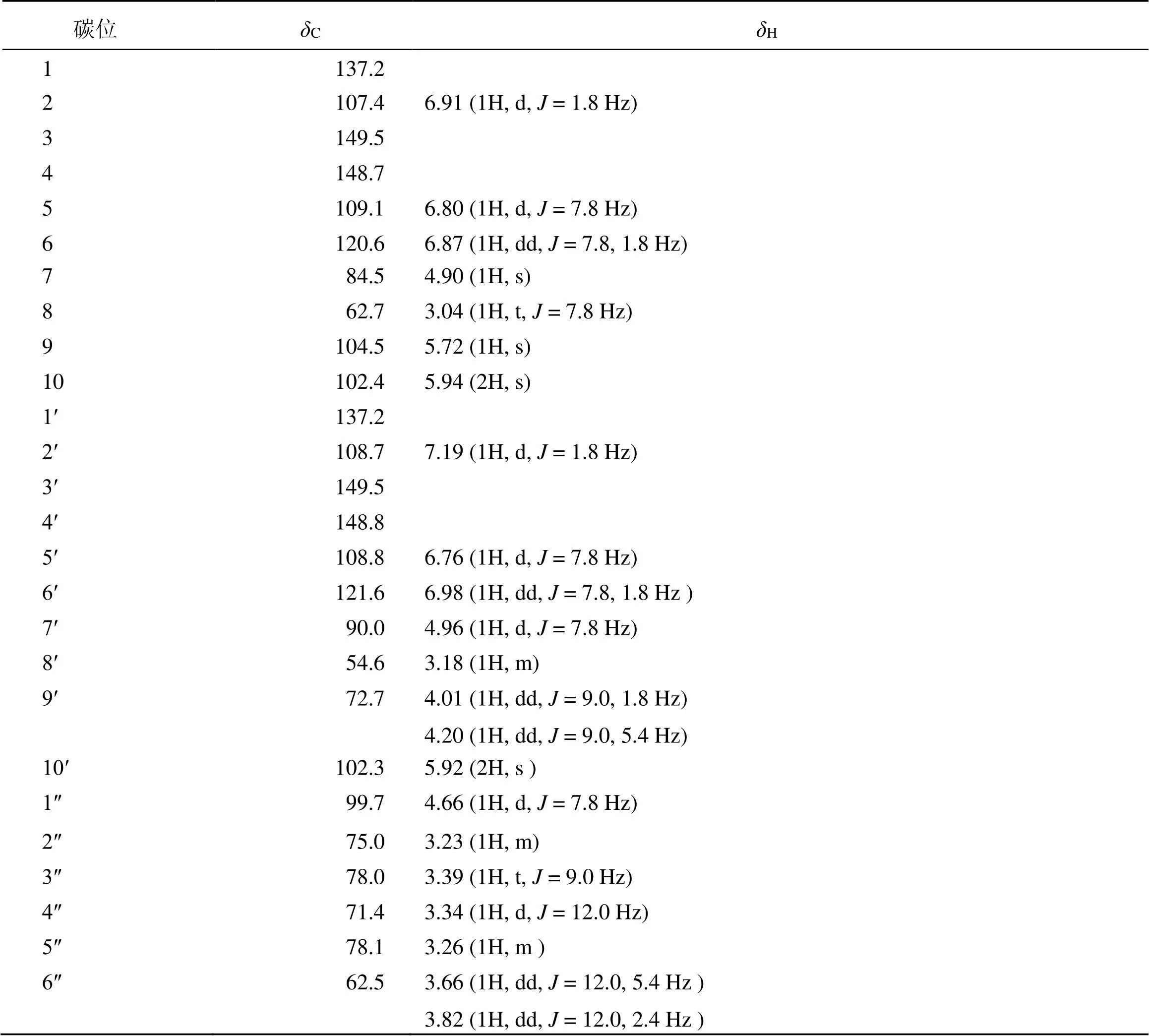
表1 化合物1的1H-NMR和13C-NMR數據(600/150 MHz, CD3OD)
化合物2:白色固體(甲醇),[α]25 D+15.9°(0.32, CDCl3),mp 102~104 ℃, ESI-MS/: 519.4 [M-H]?。分子式為C26H32O11;1H-NMR (600 MHz, DMSO-6):7.04~6.71 (6H, m, Ar-H), 4.87 (1H, d,= 7.2 Hz, Glc-H-1), 4.66 (1H, d,= 4.2 Hz, H-6), 4.60 (1H, d,= 4.2 Hz, H-2), 4.14 (2H, dd,= 6.6, 2.3 Hz, H-4, 8), 3.76 (3H, s, 7′-OMe), 3.76 (3H, s, 7″-OMe), 3.74 (2H, m, H-4, 8);13C-NMR (150 MHz, DMSO-6): 148.9 (C-3′), 147.5 (C-3″), 145.8 (C-4′), 145.8 (C-4″), 135.2 (C-1′), 132.2 (C-1″), 118.7 (C-6″), 118.2 (C-6′), 115.1 (C-5′, 5″), 110.5 (C-2′), 110.4 (C-2″), 100.1 (Glc-C-1), 85.2 (C-6), 84.9 (C-2), 77.0 (Glc-C-5), 77.0 (Glc-C-3), 73.2 (Glc-C-2), 71.0 (C-8), 71.0 (C-4), 69.7 (Glc-C-4), 60.7 (Glc-C-6), 55.7 (-OMe), 55.6 (-OMe), 53.7 (C-1), 53.6 (C-5)。上述數據與文獻報道數據基本一致[13],故鑒定化合物2為(+)-松脂素-4β--葡萄糖苷。
化合物3:白色粉末(甲醇),mp 210~212 ℃,ESI-MS/: 833.3 [M+Na]+,分子式C42H50O16;1H-NMR (600 MHz, DMSO-6):6.91 (2H, t,= 2.4 Hz, H-2″, 2?), 6.71 (2H, m, H-5″, 5?), 6.69 (2H, dd,= 8.4, 1.4 Hz, H-6″, 6?), 6.64 (4H, d,= 1.2 Hz, H-2, 6, 2′, 6′), 4.79 (2H, dd,= 4.8, 3.0 Hz, H-7″, 7?), 4.66 (2H, d,= 3.6 Hz, H-7, 7′), 4.19 (2H, m, H-9β, 9′β), 4.10 (2H′, m, H-8″, 8″), 3.82 (2H, dd,= 9.0, 3.0 Hz, H-9α, 9′α), 3.76 (12H, s, 3, 5, 3′, 5′-OMe), 3.73 (6H, d,= 1.8 Hz, 3″, 3-OMe), 3.70 (2H, d,= 4.8 Hz, H-9″β, 9?β), 3.06 (2H, m, H-8, 8′);13C-NMR (150 MHz, DMSO-6): 152.7 (C-3, 5), 152.7 (C-3′, 5′), 146.9 (C-3″, 3?), 145.2 (C-4″, 4?), 136.8 (C-1, 1′), 134.8 (C-4, 4′), 133.4 (C-1″, 1?), 119.4 (C-6″, 6?), 114.6 (C-5″, 5?), 110.9 (C-2″, 2?), 103.3 (C-2, 6, 2′, 6′), 86.2 (C-7′, 7), 85.1 (C-8″, 8?), 72.0 (C-7″, 7?), 71.4 (C-9, 9′), 53.7 (C-8, 8′), 59.7 (C-9″, 9?), 56.0 (3, 5, 3′, 5′-OMe), 55.5 (3″, 3?-OMe)。上述數據與文獻報道數據基本一致[14],故鑒定化合物3為(7,7′,7″,7?,8,8′,8″,8?)-4″, 4?-二羥基-3,3′, 3″,3?,5,5′-六甲氧基-7,9′;7′,9-二環氧-4,8″;4′,8?-雙氧- 8,8′-雙新木脂素-7″,7?,9″,9?-四醇。
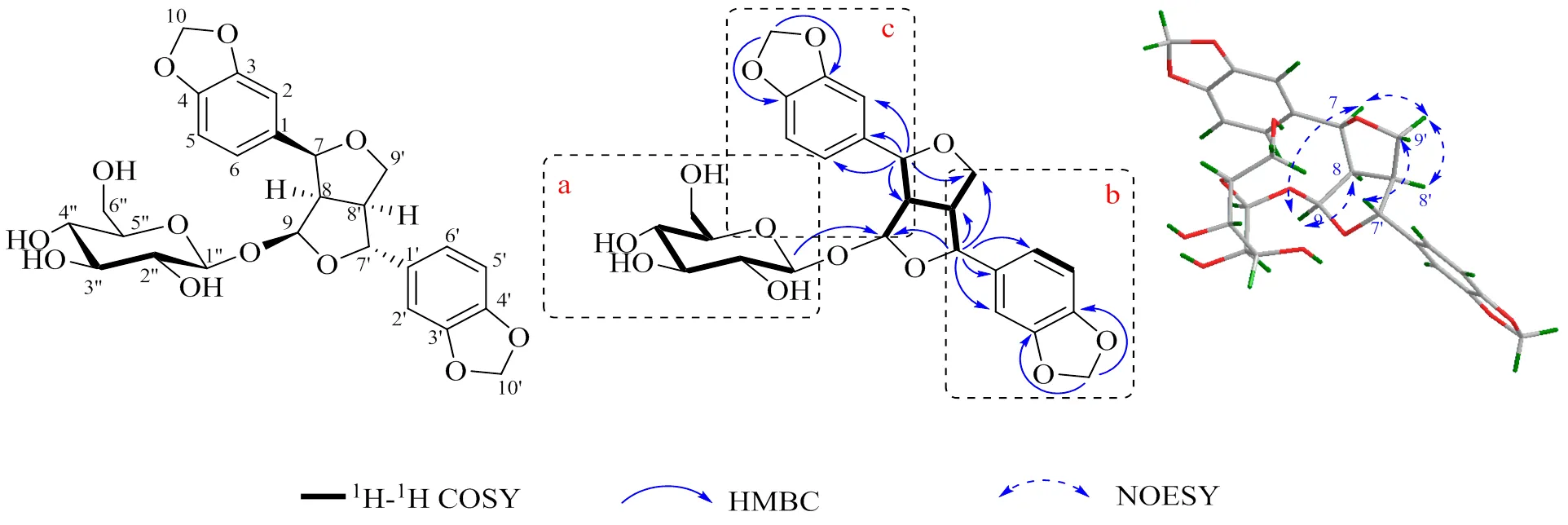
圖1 化合物1的關鍵1H-1H COSY、HMBC和NOESY相關信號
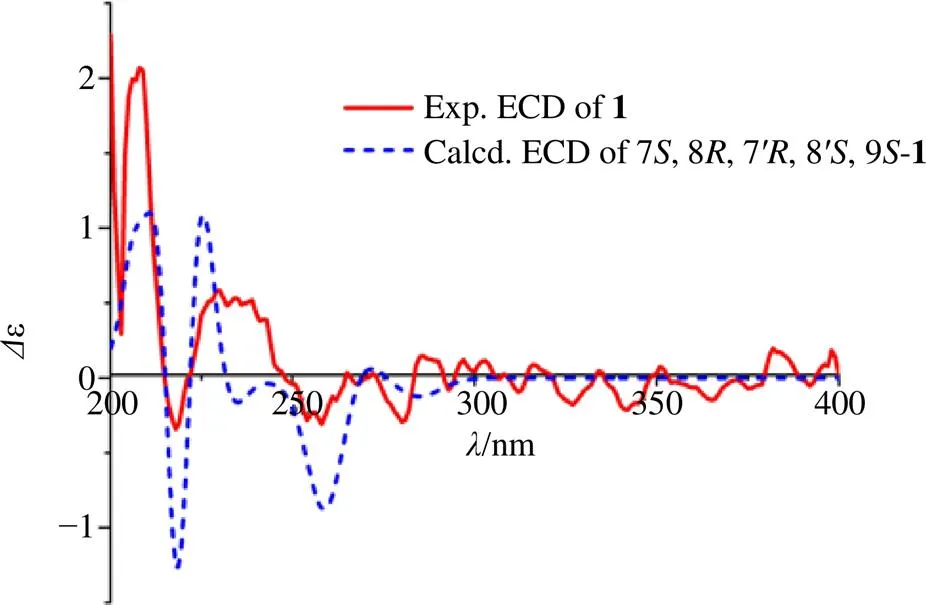
圖2 化合物1的測試和計算ECD譜
化合物4:白色粉末(甲醇),ESI-MS/: 833.4 [M+Na]+,分子式C42H50O16;1H-NMR (600 MHz,DMSO-6): 6.96 (1H, d,= 1.8 Hz, H-2″), 6.91 (1H, t,= 2.4 Hz, H-2?), 6.78 (1H, d,= 7.8 Hz, H-6″), 6.72 (1H, dt,= 7.8, 1.8 Hz, H-6?), 6.69 (2H, m, H-5″, 5?), 6.64 (4H, d,= 2.4 Hz, H-2, 6, 2′, 6′), 4.83 (1H, d,= 4.8 Hz, H-7″), 4.79 (1H, dd,= 4.8, 3.0 Hz, H-7?), 4.66 (2H, d,= 3.6 Hz, H-7, 7′), 4.20 (2H, m, H-9β, 9′β), 4.10 (1H, qd,= 4.8, 2.4 Hz, H-8″), 3.98 (1H, qd,= 4.8, 1.8 Hz, H-8?), 3.82 (2H, m, H-9α, 9′α), 3.76 (6H, s, 3, 3′-OMe), 3.74 (6H, s, 5, 5′-OMe), 3.73 (3H, d,= 1.8 Hz, H-3″), 3.72 (3H, s, 3?-OMe), 3.68 (2H, m, H-9″β, 9β?), 3.38 (2H, ddd,= 11.8, 3.9, 2.4 Hz, H-9α″, 9?α), 3.06 (2H, m, H-8, 8′);13C-NMR (150 MHz, DMSO-6): 152.6 (C-3), 152.6 (C-5), 152.5 (C-3′, 5′), 146.9 (C-3″), 146.8 (C-3?), 145.2 (C-4″, 4?), 136.9 (C-1), 136.8 (C-1′), 134.80 (C-4, 4′), 133.0 (C-1″), 132.8 (C-1?), 119.4 (C-6″), 119.2 (C-6?), 114.5 (C-5″, 5?), 110.9 (C-2″, 2?), 103.3 (C-2, 6, 2′, 6′), 87.0 (C-7), 85.1 (C-7′), 85.1 (C-8″, 8?), 72.10 (C-7″, 7?), 71.3 (C-9, 9′), 60.1 (C-9?), 59.7 (C-9″), 56.0 (3, 5, 3′, 5′-OMe), 55.5 (3″, 3?-OMe), 53.7 (C-8, 8′)。上述數據與文獻報道數據基本一致[14],故鑒定化合物4為 (7,7′,7″,7?, 8,8′,8″,8?)-4″,4?-二羥基-3,3′,3″,3?,5,5′-六甲氧基-7,9′;7′,9-二環氧-4,8″;4′,8?-雙氧-8,8′-雙新木脂素- 7″,7?,9″,9?-四醇。
化合物5:白色粉末(甲醇),ESI-MS/: 371.3 [M+H]+,分子式C20H18O7;1H-NMR (600 MHz, CDCl3): 6.94 (1H, d,= 1.8 Hz, H-2′), 6.91 (1H, d,= 1.8 Hz, H-2), 6.87 (1H, m, H-6, 6′), 6.85 (1H, m, H-5), 6.79 (1H, d,= 8.4 Hz, H-5′), 5.98 (2H, s, -OCH2O-), 5.95 (2H, s, -OCH2O-), 4.84 (1H, d,= 4.8 Hz, H-7′), 4.81 (s, 1H, H-7), 4.50 (1H, dd,= 9.0, 8.4 Hz, H-9′b), 4.04 (1H, d,= 9.6 Hz, H-9b), 3.90 (1H, d,= 9.6 Hz, H-9a), 3.83 (1H, dd,= 9.2, 6.1 Hz, H-9′a), 3.04 (1H, m, H-8′);13C-NMR (150 MHz, CDCl3):148.3 (C-4), 148.2 (C-4′), 148.1 (C-3), 147.4 (C-3′), 134.7 (C-1′), 129.3 (C-1), 120.3 (C-6), 120.0 (C-6′), 108.7 (C-5), 108.4 (C-5′), 107.6 (C-2), 107.0 (C-2′), 101.4 (-OCH2O-), 101.3 (-OCH2O-), 91.8 (C-8), 87.6 (C-7), 85.9 (C-7′), 74.9 (C-9), 71.8 (C-9′), 60.5 (C-8′)。上述數據與文獻報道數據基本一致[15],故鑒定化合物5為泡桐素。
化合物6:白色無定形粉末,ESI-MS/: 369.07 [M+H]+分子式為C20H16O7;1H-NMR (600 MHz, CDCl3):6.76~6.87 (6H, m, H-2, 2′, 5, 5′, 6, 6′), 5.98 (2H, s, -OCH2O-), 5.95 (2H, s, -OCH2O-), 5.31 (1H, d,= 3.6 Hz, H-7′), 5.29 (1H, d,= 3.6 Hz, H-7), 4.32 (1H, dd,= 9.6, 6.6 Hz, H-9α), 4.01 (1H, dd,= 9.6, 4.8 Hz, H-9β), 3.42 (1H, dd,= 9.0, 3.6 Hz, H-8′), 3.20 (1H, m, H-8);13C-NMR (150 MHz, CDCl3): 176.8 (C-9′), 148.5 (C-3′), 148.2 (C-4′), 148.2 (C-3), 147.4 (C-4), 134.5 (C-1′), 133.1 (C-1), 119.2 (C-6′), 118.9 (C-6), 108.7 (C-2′), 108.5 (C-2), 106.1 (C-5′), 105.9 (C-5), 101.6 (-OCH2O-), 101.3 (-OCH2O-), 84.5 (C-7′), 83.5 (C-7), 72.8 (C-9), 53.4 (C-8), 50.1 (C-8′)。上述數據與文獻報道數據基本一致[16],故鑒定化合物6為4-氧代芝麻素。
化合物7:無色針狀(甲醇),mp 119~121 ℃,ESI-MS/: 355.10 [M+H]+,分子式為C20H18O6;1H-NMR (600 MHz, CDCl3): 6.85 (2H, d,= 1.8 Hz, H-2′, 2″), 6.80 (2H, dd,= 8.4, 1.8 Hz, H-6′, 6″), 6.78 (2H, d,= 7.9 Hz, H-5′, 5″), 5.94 (4H, s, -OCH2O-), 4.71 (2H, d,= 4.2 Hz, H-2, 6), 4.23 (2H, dd,= 9.0, 6.6 Hz, H-4eq, 8eq), 3.87 (2H, dd,= 9.0, 3.6 Hz, H-4ax, 8ax), 3.04 (2H, ddt,= 5.4, 3.0, 1.8 Hz, H-1, 5);13C-NMR (150 MHz, CDCl3): 148.1 (C-4′, 4″), 147.2 (C-3′, 3″), 135.2 (C-1′, 1″), 119.4 (C-6′, 6″), 108.3 (C-5′, 5″), 106.6 (C-2′, 2″), 101.2 (-OCH2O-), 85.9 (C-2, 6), 71.8 (C-4, 8), 54.4 (C-1, 5)。上述數據與文獻報道數據基本一致[17],故鑒定化合物7為芝麻素。
化合物8:無色針狀結晶(甲醇),mp 132~134 ℃,ESI-MS/: 415.2 [M+H]+,分子式為C29H50O;10%硫酸乙醇液加熱呈紫紅色,經與β-谷甾醇純品對照后,發現其Rf值一致,故鑒定化合物8為β-谷甾醇。
化合物9:白色針晶(氯仿),mp 285~288 ℃,ESI-MS/: 455.13 [M-H]?,分子式C30H48O3;1H-NMR (600 MHz, DMSO-6): 5.13 (1H, t,= 3.6 Hz, H-12), 3.00 (1H, m, H-3), 1.04 (3H, s, H-27), 0.91 (3H, s,= 6.6 Hz, H-29), 0.90 (3H, s, H-26), 0.80 (3H, s, H-23), 0.81 (1H, d,= 6.6 Hz, H-30), 0.75 (3H, s, H-24), 0.68 (3H, s, H-25);13C-NMR (150 MHz, DMSO-6): 178.3 (C-28), 138.2 (C-13), 124.6 (C-12), 76.9 (C-3), 54.8 (C-5), 52.4 (C-18), 47.0 (C-17), 46.8 (C-9), 41.7 (C-14), 39.1 (C-8), 38.5 C-20), 38.5 (C-4), 38.4 (C-19), 38.3 (C-1), 36.5 (C-10), 36.3 (C-22), 32.7 (C-15), 30.2 (C-7), 28.3 (C-23), 27.6 (C-21), 27.0 (C-2), 23.8 (C-11), 23.3 (C-27), 22.9 (C-16), 21.1 (C-30), 18.0 (C-6), 17.0 (C-29), 16.9 (C-24), 16.1 (C-25), 15.2 (C-26)。上述數據與文獻報道數據基本一致[18],故鑒定化合物9為熊果酸。
化合物10:無色針狀結晶(甲醇),mp 170~171 ℃,ESI-MS/: 429.3 [M+H]+,分子式為C29H48O2;1H-NMR (600 MHz, CDCl3): 5.69 (1H, s, H-6), 3.68 (1H, m, H-3), 1.20 (3H, s, H-19), 0.93 (3H, d,= 6.6 Hz, H-21), 0.84 (3H, d,= 3.6 Hz, H-29), 0.83 (3H, d,= 3.0 Hz, H-26), 0.81 (3H, d,= 6.6 Hz, H-27), 0.68 (3H, s, H-18);13C-NMR (150 MHz, CDCl3): 202.5 (C-7), 165.2 (C-5), 126.3 (C-6), 70.7 (C-3), 54.8 (C-17), 50.1 (C-9), 50.1 (C-14), 46.0 (C-24), 45.6 (C-8), 43.2 (C-13),42.0 (C-4), 38.8 (C-10), 38.4 (C-12), 36. (C-1), 36.2 (C-20), 34.1 (C-22), 31.3 (C-2), 21.4 (C-11), 26.2 (C-15), 28.7 (C-16), 12.1 (C-18), 17.5 (C-19), 19.1 (C-21), 26.5 (C-23), 29.3 (C-25), 20.0 (C-26), 19.2 (C-27), 23.2 (C-28), 12.1 (C-29)。上述數據與文獻報道數據基本一致[19],故鑒定化合物10為3β-羥基豆甾-5烯-7-酮。
化合物11:白色固體,ESI-MS/:427.3 [M+H]+,分子式為C29H46O2;1H-NMR (600 MHz, CDCl3): 5.69 (1H, s, H-6), 5.17 (1H, dd,= 15.0, 8.4 Hz, H-22), 5.02 (1H, dd,= 15.0, 8.4 Hz, H-23), 3.67 (1H, m, H-3), 1.20 (3H, s, H-19), 1.02 (3H, d,= 6.6 Hz, H-21), 0.84 (3H, d,= 6.0 Hz, H-29), 0.81 (3H, d,= 7.2 Hz, H-26), 0.79 (3H, d,= 6.6 Hz, H-27), 0.69 (3H, s, H-18);13C-NMR (150 MHz, CDCl3): 202.4 (C-7), 165.2 (C-5), 138.2 (C-22), 129.6 (C-23), 126.2 (C-6), 70.7 (C-3), 54.8 (C-17), 51.4 (C-24), 50.2 (C-14), 50.1 (C-9), 45.5 (C-8), 43.1 (C-13), 42.0 (C-4), 40.0 (C-20), 38.7 (C-10), 38.4 (C-12), 36.5 (C-1), 32.0 (C-25), 31.3 (C-2), 29.2 (C-16), 26.6 (C-15), 25.5 (C-28), 21.6 (C-26), 21.4 (C-27), 21.2 (C-11), 19.1 (C-21), 17.5 (C-19), 12.4 (C-29), 12.3 (C-18)。上述數據與文獻報道數據基本一致[20],故鑒定化合物11為3β-羥基豆甾-5,22-二烯-7-酮。
4 生物活性測定結果
細胞鐵死亡是一種區別于細胞凋亡、細胞壞死、細胞自噬的新型的細胞程序性死亡方式[21]。越來越多的研究表明,細胞鐵死亡與許多神經系統疾病有關,如神經退行性疾病和中風等,因此抑制細胞鐵死亡是治療神經系統疾病的一種很有前途的策略[22]。紫珠屬植物的現代藥理研究表明具有較好神經保護等活性,但相關的細胞鐵死亡的抑制活性研究報道較少。本研究中,除了量少的化合物3和4外,所有化合物均開展了RSL3誘導的HT22細胞鐵死亡抑制活性評價。結果顯示,與模型組比較(23.4%),化合物7、10和11在20 μmol/L濃度下顯示出了明顯的鐵死亡抑制活性,其細胞存活率分別為30.37%、31.93%和36.57%,而其余化合物在此濃度下未顯示出明顯的鐵死亡抑制活性。
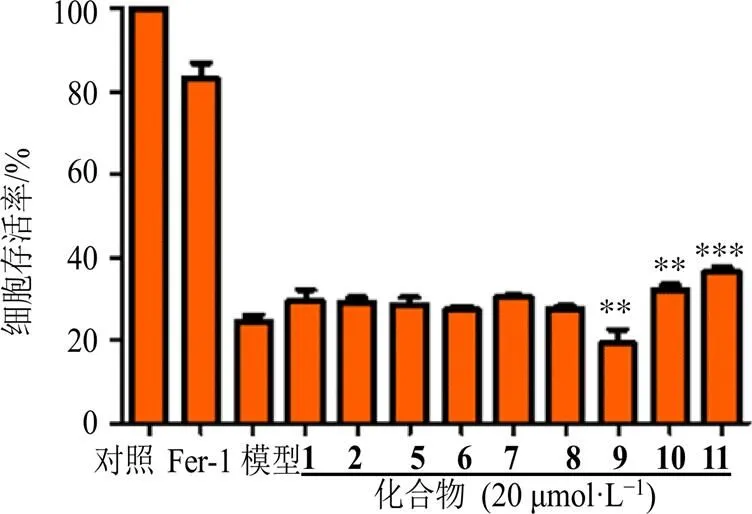
與模型組比較:**P<0.01 ***P<0.001
5 討論
本研究從擬紅紫珠的乙醇提取物的石油醚和醋酸乙酯萃取部位中分離鑒定了11個單體化合物,其中包括7個木脂素、2個三萜和2個甾體,所有化合物均為首次從擬紅紫珠中分離得到。初步的活性篩選發現其中的2個甾體化合物表現出明顯的鐵死亡抑制活性。紫珠屬植物已報道的特征性成分是二萜類化合物,本研究結果顯示木脂素也是該屬植物的特征性成分之一。通過該論文的研究,進一步豐富了紫珠屬植物的化合物結構類型,為深入闡明該屬植物中的特征性成分提供理論基礎,也為該植物的深入開發利用提供科學基礎。
利益沖突 所有作者均聲明不存在利益沖突
[1]邱曉萍, 張懿, 陳煜林, 等. 中國唇形科藥用植物資源及利用現狀和開發潛力 [J]. 應用與環境生物學報, 2023, 29(2): 346-356.
[2]中國藥典 [S]. 一部. 2020:354.
[3]國家中醫藥管理局《中華本草》編輯委員會. 中華本草(藏藥卷) [M]. 上海: 上海科學技術出版社, 2002.
[4]Lou H Y, Zheng S, Li T L,. Vulgarisin A, a new diterpenoid with a rare 5/6/4/5 ring skeleton from the Chinese medicinal plant[J]., 2014, 16(10): 2696-2699.
[5]Lou H Y, Jin L, Huang T,. Vulgarisins B-D, three novel diterpenoids with a rare skeleton isolated fromLinn [J]., 2017, 58(5): 401-404.
[6]梁會, 趙玉敏, 劉翰飛, 等. 貴州鼠尾草中1個新的姜黃素類化合物 [J]. 中草藥, 2022, 53(18): 5593-5599.
[7]趙玉敏, 周謠, 劉翰飛, 等. 貴州鼠尾草化學成分研究 [J]. 熱帶亞熱帶植物學報, 2023, 31(4): 595-601.
[8]楊國棟, 劉昱甫, 劉永林, 等. 紫珠屬的萜類成分和藥理作用研究進展 [J]. 中國藥物化學雜志, 2022, 32(12): 957-973.
[9]中國科學院中國植物志編輯委員會. 中國植物志-第65(1)卷 [M]. 北京: 科學出版社, 1982: 25.
[10]Yuasa K, Ide T, Otsuka H,. Premnafolioside, a new phenylethanoid, and other phenolic compounds from stems ofvar.[J]., 1993, 56(10): 1695-1699.
[11]Zhao H Y, Wang Y Q, Li Y C,. Flavonol glycosides and phenylpropanoid glycosides with inhibitory effects on microglial nitric oxide production from[J]., 2021, 151: 104877.
[12]Zhou L, Han F Y, Lu L W,. Isolation of enantiomeric furolactones and furofurans fromL. with neuroprotective activities [J]., 2019, 164: 122-129.
[13]張冬梅, 胡立宏, 葉文才,等. 白蠟樹的化學成分研究 [J]. 中國天然藥物, 2003, 1(2): 79-81.
[14]夏召, 張海新, 許天啟, 等. 蒼耳子中苯丙素類化學成分的研究 [J]. 中國藥學雜志, 2021, 56(1): 13-22.
[15]馮薇, 楊峻山. 木蹄層孔菌化學成分研究 [J]. 中國藥學雜志, 2010, 45(20): 1528-1530.
[16]李月婷, 龐道然, 朱枝祥, 等. 牡荊子的化學成分與生物活性研究 [J]. 中國中藥雜志, 2016, 41(22): 4197-4203.
[17]Hsieh T J, Chen C H, Lo W L,. Lignans from the stem of[J]., 2006, 1(1): 21-25.
[18]賈瑞芳, 劉荷秀, 黃美玲, 等. 蘇藿香化學成分研究 [J]. 中草藥, 2021, 52(10): 2884-2889.
[19]尚小雅, 王若蘭, 尹素琴, 等. 紫紅曲代謝產物中的甾體成分 [J]. 中國中藥雜志, 2009, 34(14): 1809-1811.
[20]吳蕾, 李金杰, 鐘祥健, 等. 云南兔兒風的化學成分研究 [J]. 廣西植物, 2020, 40(9): 1375-1380.
[21]Dixon S J, Lemberg K M, Lamprecht M R,. Ferroptosis: An iron-dependent form of nonapoptotic cell death [J]., 2012, 149(5): 1060-1072.
[22]Tan Q, Fang Y, Gu Q,. Mechanisms of modulation of ferroptosis and its role in central nervous system diseases [J]., 2021, doi: 10.3389/fphar.2021. 657033.
One new lignan glucoside from
ZHAO Xing1, 3, LIU Han-fei1, 2, WANG Huan1, 3, LIN Kai-qin1, 3, LI Jin-yu1, 2, PAN Wei-dong1, LOU Hua-yong1, 2, SUN Chao1, 2
1. State Key Laboratory of Functions and Applications of Medicinal Plants, Guizhou Medical University, Guiyang 550014, China 2. Natural Products Research Center of Guizhou Province, Guiyang 550014, China 3. School of Pharmaceutical Sciences, Guizhou Medical University, Guiyang 550025, China
To study the chemical constituents ofand their biological activities.The chemical constituents were isolated and purified by silica gel, Sephadex LH-20, RP-18 reversed phase silica gel column chromatography and semi-preparative high performance liquid chromatography (HPLC). Then their structures were elucidated by modern spectroscopic analyses (UV, IR, NMR, and HRESIMS) and physicochemical properties. All isolates were evaluated for their inhibitory effect on RSL3-induced ferroptosis in HT22 mouse hippocampal neuronal cells.A total of eleven compounds were isolated fromand identified as (7,7?,8,8?,9)-sesamin-9--β--glucopyranoside (1), (+)- pinoresinol-4--β--glucopyranoside (2), (7,7′,7″,7?,8,8′,8″,8?)-4″,4?-dihydroxy-3,3′,3″,3?,5,5′-hexamethoxy-7′,9′,7′,9-diepoxy-4,8″,4′,8?- bisoxy-8,8′-dineolignan-7″,7?,9″,9?-tetraol (3), (7,7′,7″,7?,8,8′,8″,8?)-4″,4?-dihydroxy-3,3′,3″,3?,5,5′-hexamethoxy-7,9′, 7′,9-diepoxy-4,8″,4′,8?-bisoxy-8,8′-dineolignan-7″,7?,9″,9?-tetraol (4), paulownin (5), 4-oxosesamin (6), sesamin (7), β-sitosterol (8), ursolic acid (9), 3β-hydroxystigmast- 5-en-7-one (10), and 3β-hydroxystigmast-5,22-dien-7-one (11). Compared with the model group, compounds 7, 10 and 11 exhibited obvious inhibitory activity on RSL3-induced HT22 cells ferroptosis, with the survival rate of 30.37%, 31.93% and 36.57%, respectively (23.4% in model group).Compound 1 is a new compound, named as callicoside A. And all compounds are isolated fromfor the first time. Moreover, compounds 7, 10 and 11 exhibit obvious inhibitory activity against RSL3-induced HT22 cells ferroptosis.
H. T. Chang; lignan glucoside; callicoside A;sesamin; ursolic acid; 3β-hydroxystigmast-5-en- 7-one; anti-ferroptosis activity
R284.1
A
0253 - 2670(2023)21 - 6953 - 08
10.7501/j.issn.0253-2670.2023.21.004
2023-05-27
國家自然科學基金資助項目(32060100);國家自然科學基金資助項目(32100322);貴州省科技計劃項目(黔科合基礎-ZK [2021]534,QKHZC[2021]411,QKHZC [2022]019);貴州省科技計劃項目(黔科中引地[2022]4015)
趙 興(1998—),男,碩士研究生,研究方向為中藥藥效物質基礎研究。E-mail: 2652674828@qq.com
通信作者:婁華勇(1987—),博士,副研究員,研究方向為天然藥物化學。E-mail: loouhy@126.com
孫 超(1970—),學士,研究員,研究方向為藥用植物引種馴化與質量控制。E-mail: chao_sun2000@hotmail.com
[責任編輯 王文倩]

