貝伐珠單抗聯合TC 化療方案對卵巢癌患者血清炎性因子及腫瘤標志物的影響
郎曉東,王虹,朱建鳳
(安丘市人民醫院腫瘤內科,山東濰坊 262100)
“手術-化療-維持治療”是卵巢癌的規范化治療步驟。化療藥物毒性大,臨床緩解率低,現代醫學一直致力于攻破腫瘤患者化療不耐受的難題。 研究證實,血管內皮生長因子(VEGF)在腫瘤病理性新血管生成及腫瘤的生長進展、轉移侵襲等過程中扮演了重要角色[1]。在缺氧或炎癥刺激下,VEGF 的分泌可顯著增加。貝伐珠單抗是美國第一批被批準用于卵巢癌治療的靶向抗血管生成藥物, 并于2018 年首次被批準與常規紫杉醇和卡鉑(TC)化療方案聯合使用以治療卵巢癌。 與單用TC 化療方案相比,聯合靜脈使用貝伐珠單抗可延長卵巢癌患者的無進展生存時間,但對患者體內炎癥的控制效果尚不明確。 基于此,本研究選取安丘市人民醫院腫瘤內科2021 年7 年—2022 年7月收治的100 例卵巢癌患者為對象,探究貝伐珠單抗聯合TC 化療方案對其血清炎性因子及腫瘤標志物的影響。 報道如下。
1 資料與方法
1.1 一般資料
選取安丘市人民醫院腫瘤內科收治的100 例卵巢癌患者為研究對象, 按照隨機數字表法分為兩組,每組50 例。 對照組年齡48~65 歲,平均年齡(56.50±7.72)歲;黏液性卵巢癌11 例,漿液性卵巢癌35 例,透明細胞癌4 例;國際婦產科聯盟(FIGO)分期:Ⅰ~Ⅱ期15 例, Ⅲ~Ⅳ期35 例;47 例為中低分化,3 例為高分化。 觀察組年齡46~66 歲,平均年齡(56.19±8.96)歲;黏液性卵巢癌10 例,漿液性卵巢癌37 例,透明細胞癌3 例;FIGO 分期:Ⅰ~Ⅱ期13 例,Ⅲ~Ⅳ期37 例;46 例為中低分化,4 例為高分化。兩組患者的各項一般資料比較,組間差異無統計學意義(P>0.05),具有可比性。 本研究已獲:醫學倫理委員會批準。
1.2 入選標準
納入標準:符合卵巢癌診斷標準[2],經輔助實驗室檢查、細胞學檢查、病理組織學檢查確診;年齡18~80歲;入組前未接受過放化療;血常規、腎功能等指標符合化療標準;化療前未接受過減瘤手術;簽署知情同意書。排除標準:卵巢轉移性癌;預計生存期<6 個月;合并血液疾病、腦血栓;心、肺等重要器官衰竭;伴有意識障礙或精神認知異常,無法配合本研究。
1.3 方法
兩組患者化療前均采用相同的預處理: 化療前12 h 及化療前6 h,口服20 mg 地塞米松;化療前30~60 min,靜脈滴注300 mg 西咪替丁,并口服50 mg 苯海拉明。
對照組采用TC 化療方案。給予患者紫杉醇注射液(海口奇力制藥股份有限公司,國藥準字H20063169,規格:5 mL:30 mg)靜脈滴注,藥物劑量175 mg/m2,首次靜脈滴注時間為3 h;同時給予患者注射用卡鉑(齊魯制藥有限公司,國藥準字H10920028,規格:0.1 g)靜脈滴注,給藥標準根據Calvert 公式計算:時間曲線下面積(AUC)×[肌酐清除率(Ccr)+25],取值為5。21 d為一個療程,共治療3 個療程。
觀察組在對照組基礎上采用貝伐珠單抗靶向治療。給予患者貝伐珠單抗注射液[海正生物制藥有限公司,國藥準字S20210047,100 mg(4 mL)/瓶]靜脈滴注,藥物劑量15 mg/kg,首次靜脈滴注時間為90 min。1次/周,3 周為1 個療程,兩個療程間需間隔3 周,共治療3 個療程。
1.4 觀察指標
(1)腫瘤標志物。 治療前后,取患者靜脈血3~4 mL,以3 000 r/min 轉速離心10 min,取血清置于EP 管中超低溫保存待檢。 應用貝克曼IAMMGE 采用ELISA 法測定腫癌抗原(CA125)、腫瘤特異性生長因子(TSGF)、腫瘤干細胞標志物CD133、血管內皮生長因子(VEGF)水平。(2)炎性因子。治療前后,取患者靜脈血3~4 mL,以3 000 r/min 轉速離心10min,取血清置于EP 管中超低溫保存待檢。應用BXS05-SN-6105型γ 放射免疫計數器采用放射免疫分析法測定白細胞介素-6(IL-6)、白細胞介素-10(IL-10)、干擾素-γ(INF-γ)水平。 (3)毒副反應。 應用WHO 制定的抗癌藥物毒副反應分級標準評估, 等級分為0~4 級,0 級為無毒副反應,1 級為輕度惡心、嘔吐、出血、脫發、發燒、疼痛、血尿、感染、紅色瘀點、便秘等癥狀,2~4 級為1 級癥狀持續加重,3 級可伴有感覺異常、 運動障礙,4 級可能出現癱瘓或昏迷。
1.5 統計方法
采用SPSS 25.0 統計學軟件進行數據分析。 計量資料用(±s)表示,采用t檢驗;計數資料用[n(%)]表示,采用χ2檢驗;等級資料采用秩和檢驗。P<0.05 為差異有統計學意義。
2 結 果
2.1 兩組腫瘤標志物水平比較
治療前,兩組的CA125、CD133、TSGF、VEGF 水平比較,組間差異無統計學意義(P>0.05);治療后,兩組的各項腫瘤標志物水平均降低, 且觀察組的CA125、CD133、TSGF、VEGF 水平均低于對照組,組間差異有統計學意義(P<0.05)。 見表1。
表1 兩組腫瘤標志物水平比較(±s)
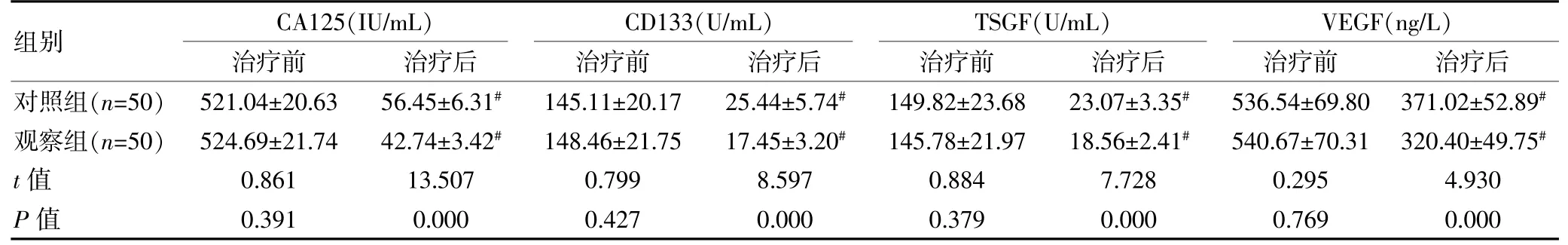
表1 兩組腫瘤標志物水平比較(±s)
注:與同組治療前比較,#P<0.05
?
2.2 兩組炎性因子水平比較
治療前,兩組的INF-γ、IL-6、IL-10 水平比較,組間差異無統計學意義(P>0.05);治療后,兩組的各項炎性因子水平均改善, 且觀察組的IL-6 水平低于對照組,INF-γ、IL-10 水平均高于對照組, 組間差異有統計學意義(P<0.05)。 見表2。
表2 兩組炎性因子水平比較(±s)
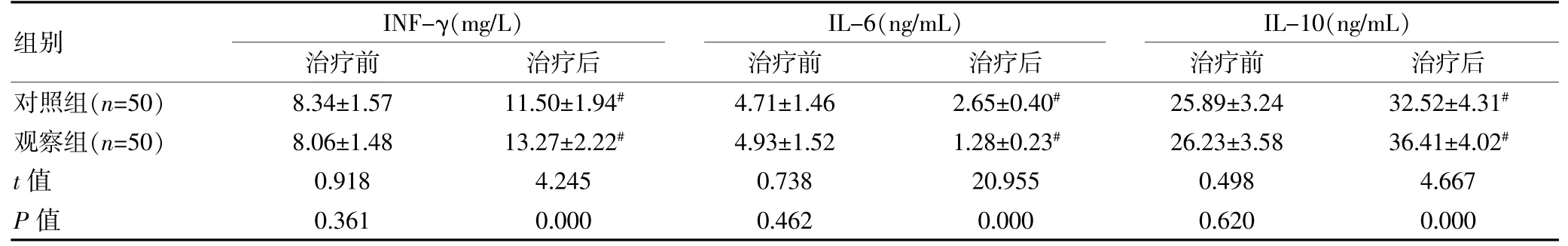
表2 兩組炎性因子水平比較(±s)
注:與同組治療前比較,#P<0.05
?
2.3 兩組毒副反應比較
兩組的毒副反應發生率比較,差異無統計學意義(P>0.05)。 見表3。

表3 兩組毒副反應比較[n(%)]
3 討 論
現階段,臨床針對卵巢癌多采用手術為主,化療、放療等為輔的綜合治療。 部分患者的腫瘤組織較大,手術無法完全切除, 只能通過部分切除減輕瘤負荷,之后采用輔助化療清除術中殘留的癌細胞、腹壁種植結節及腹腔轉移灶。 TC 化療是卵巢癌的一線化療方案,紫杉醇的作用機制是加速微管蛋白聚集,提高微管穩定性,特異性作用于腫瘤細胞周期G 期和M 期,抑制腫瘤細胞的有絲分裂和增殖,從而阻礙腫瘤的細胞復制和促進細胞凋亡[3]。卡鉑則主要通過干擾DNA 螺旋解鏈和合成,抑制細胞復制,殺傷腫瘤細胞[4]。 但傳統的化療方案缺乏靶向性,對腫瘤周圍正常組織及器官存在較大殺傷性,患者需要承受巨大的藥毒痛苦。
貝伐珠單抗為抗血管生成靶向藥物。 王慧萍等[5]的研究指出,采用貝伐珠單抗聯合常規化療治療晚期卵巢癌,能抑制新生血管形成,改善患者免疫狀態。陳遠航等[6]的研究證實,放化療聯合貝伐珠單抗靶向治療可延長晚期卵巢癌患者生存時間。 本研究結果顯示, 觀察組治療后的CA125、CD133、TSGF、VEGF 水平均低于對照組,組間差異有統計學意義(P<0.05),說明貝伐珠單抗聯合TC 化療方案能有效抑制腫瘤血管生成,減少腫瘤細胞的生長。 貝伐珠單抗的作用機制包括:(1)與內源性VEGF 競爭性結合VEGF 受體(VEGFR),抑制VEGF 的生物活性,阻斷腫瘤細胞和基質細胞分泌VEGF,減少新生血管形成,并通過抑制血管內皮細胞DNA 復制, 阻斷腫瘤細胞的營養供應,繼而抑制腫瘤生長;(2)通過調控人體抑癌基因p53、原癌基因人表皮生長因子受體2(HER-2)的表達,使二者水平保持平衡,從而延緩腫瘤細胞的生長與轉移[7-8]。 朱永東等[9]的研究結果顯示,貝伐珠單抗聯合TC 化療方案能降低卵巢癌患者的血清CA125水平,提高其生活質量。
正常的宿主基質細胞、腫瘤細胞和炎性細胞浸潤組成了腫瘤微環境。減弱卵巢癌患者周圍微環境中的炎性因子活性, 能刺激其體內的抗腫瘤免疫反應,逆轉化療藥物的抗性。 張善存等[10]的研究指出,貝伐珠單抗聯合TC 化療方案能有效緩解炎癥,抑制腫瘤生長,延長患者的生存時間。本研究結果顯示,觀察組治療后的IL-6 水平高于對照組,INF-γ、IL-10 水平均低于對照組,組間差異有統計學意義(P<0.05),說明貝伐珠單抗聯合TC 化療方案能有效控制卵巢癌患者體內的炎癥反應,增強機體免疫,提升抗腫瘤反應。考慮原因為,貝伐珠單抗可通過抑制腫瘤新生血管形成而減弱腫瘤組織的炎癥刺激。 本研究結果還顯示,兩組的毒副反應發生率比較,差異無統計學意義(P>0.05),提示卵巢癌患者采用貝伐珠單抗聯合TC 化療方案治療的耐受性良好。
綜上所述,在TC 化療的基礎上聯合貝伐珠單抗靶向治療卵巢癌, 能有效降低其血清腫瘤標志物水平,抑制體內炎癥反應,且毒副反應未明顯增加,患者易耐受,值得臨床推廣使用。

