化學(xué)平衡原理在高中化學(xué)教學(xué)中的應(yīng)用
【摘要】本文論述化學(xué)平衡原理在高中化學(xué)教學(xué)中的應(yīng)用,提出化學(xué)平衡原理在化學(xué)理論層面的應(yīng)用、化學(xué)平衡原理在化學(xué)實驗層面的應(yīng)用、化學(xué)平衡原理在解題訓(xùn)練層面的應(yīng)用等具體做法,旨在幫助學(xué)生牢固掌握判斷化學(xué)平衡原理的方法,促進學(xué)生快速、準(zhǔn)確地解答化學(xué)試題。
【關(guān)鍵詞】高中化學(xué) 課堂教學(xué) 化學(xué)平衡原理
【中圖分類號】G63 【文獻標(biāo)識碼】A
【文章編號】0450-9889(2023)20-0125-04
化學(xué)平衡原理指的是在宏觀條件一定的可逆反應(yīng)中,化學(xué)反應(yīng)的正、逆反應(yīng)速率相等但不等于零,反應(yīng)物與生成物各組分濃度不再發(fā)生改變的狀態(tài)。如果一個已經(jīng)達平衡狀態(tài)的系統(tǒng)被改變,那么該系統(tǒng)會隨之發(fā)生改變而對該改變進行抗衡,所以說這是一種動態(tài)平衡。在高中化學(xué)教學(xué)中,化學(xué)平衡原理有著十分廣泛的應(yīng)用,不僅被應(yīng)用于方程式中,而且被應(yīng)用在化學(xué)實驗、解決化學(xué)問題中。學(xué)生只有掌握化學(xué)平衡原理的判斷方法,才能快速解答化學(xué)問題。因此,教師應(yīng)重視加強對化學(xué)平衡原理的應(yīng)用,不斷提高學(xué)生參與化學(xué)學(xué)習(xí)的積極性,幫助學(xué)生牢固掌握判斷化學(xué)平衡原理的方法,為接下來的解題做好準(zhǔn)備,從而促進學(xué)生快速、準(zhǔn)確地解答化學(xué)試題。
一、化學(xué)平衡原理在化學(xué)理論層面的應(yīng)用
(一)判斷化學(xué)反應(yīng)是否達到平衡狀態(tài)
在高中化學(xué)教學(xué)過程中,學(xué)生會遇到大量的化學(xué)反應(yīng),運用化學(xué)平衡原理來判斷化學(xué)反應(yīng)是否達到平衡狀態(tài),既可以加深對化學(xué)平衡本質(zhì)的理解,又可以借助所學(xué)知識準(zhǔn)確判斷出化學(xué)反應(yīng)中兩種或者多種化學(xué)物質(zhì)是否達到平衡狀態(tài)。在這種情況下,學(xué)生應(yīng)精準(zhǔn)掌握化學(xué)反應(yīng)過程中存在的多種物質(zhì)濃度及方法,假如可以發(fā)生可逆反應(yīng),不僅可以判斷出多種反應(yīng)現(xiàn)象,還可以對比反應(yīng)值逆解讀反應(yīng)相關(guān)數(shù)據(jù),最終判斷出是否真正實現(xiàn)反應(yīng)平衡。
例如,當(dāng)判定密閉容器內(nèi)的化學(xué)反應(yīng)是否達到平衡狀態(tài)時,假如反應(yīng)體系中的氣體總壓強沒有出現(xiàn)變化,即可判定該化學(xué)反應(yīng)處于平衡狀態(tài)。如在體積恒定容器中氮氣和氫氣發(fā)生反應(yīng):N2(g)+3H2(g)?2NH3(g),容器內(nèi)產(chǎn)生的氣體處于混合狀態(tài)時,氣體總質(zhì)量沒有出現(xiàn)變化,容器的體積在化學(xué)反應(yīng)過程中同樣沒有出現(xiàn)變化情況,根據(jù)質(zhì)量守恒定律相關(guān)知識,混合氣體的總壓強并沒有因此再出現(xiàn)變化,所以該化學(xué)反應(yīng)達到平衡狀態(tài)。又如,在一些化學(xué)反應(yīng)中,當(dāng)有有顏色的化學(xué)物質(zhì)參加反應(yīng),而該物質(zhì)的顏色沒有出現(xiàn)變化時,該化學(xué)反應(yīng)也處于平衡狀態(tài)。如在2NO2(g)?2NO(g)+O2(g)化學(xué)反應(yīng)中,由于NO2(g)為有色物質(zhì),當(dāng)該物質(zhì)的顏色不變即濃度不變時,我們就能夠判定這一化學(xué)反應(yīng)處于平衡狀態(tài)。
(二)運用平衡原理書寫化學(xué)方程式
在整個化學(xué)教學(xué)中,無論是初中階段,還是高中階段,化學(xué)方程式都占據(jù)著極為重要的地位,是一項重點學(xué)習(xí)內(nèi)容。在化學(xué)學(xué)習(xí)過程中,有不少化學(xué)題目都是圍繞化學(xué)方程式展開的,學(xué)生不僅要學(xué)會正確寫出化學(xué)方程式,還要真正理解化學(xué)方程式的含義,如此方能正確解答有關(guān)化學(xué)方程式的問題。在高中化學(xué)教學(xué)中,教師要運用化學(xué)平衡原理幫助學(xué)生深刻記憶、透徹理解并牢固掌握化學(xué)方程式,使學(xué)生進一步了解化學(xué)反應(yīng)的原理,繼而深刻分析化學(xué)平衡原理。
例如,對恒定容量的容器來說,當(dāng)反應(yīng)體系內(nèi)的氣體總壓強保持不變時,我們可以確定化學(xué)反應(yīng)達到平衡狀態(tài)。如4NH3+5O2=4NO2+6H2O的化學(xué)方程式中,根據(jù)已學(xué)的質(zhì)量守恒定律可知,容器內(nèi)混合氣體的總質(zhì)量不變,容器內(nèi)的體積也不變,說明當(dāng)反應(yīng)體系內(nèi)的氣體總壓強保持不變時或混合氣體的密度保持不變時,此化學(xué)反應(yīng)達到了平衡狀態(tài)。
二、化學(xué)平衡原理在化學(xué)實驗層面的應(yīng)用
(一)借助實驗教學(xué)契機運用化學(xué)平衡原理
化學(xué)平衡是建立在可逆反應(yīng)基礎(chǔ)之上的,可逆反應(yīng)則是在同一條件下,既能夠正向進行還能逆向進行的一類特殊化學(xué)反應(yīng)。大部分化學(xué)反應(yīng)都具有可逆性,均能夠在不同程度上達到平衡狀態(tài)。實驗教學(xué)是高中化學(xué)教學(xué)過程中最重要的環(huán)節(jié)之一,教師應(yīng)當(dāng)充分借助實驗教學(xué)的契機運用化學(xué)平衡原理開展教學(xué),通過現(xiàn)場演示或者播放案例的方式呈現(xiàn)可逆反應(yīng),指導(dǎo)學(xué)生以可逆反應(yīng)為依托分析與研究化學(xué)平衡原理,使學(xué)生進一步理解化學(xué)平衡的內(nèi)涵,增強學(xué)生的認(rèn)知。
例如,在教學(xué)“濃度變化對化學(xué)平衡的影響”時,教師可以利用重鉻酸根離子與鉻酸根離子之間的轉(zhuǎn)化實驗來探究濃度變化對化學(xué)平衡的影響,指出實驗原理是Cr2O72-+H2O?2CrO42-+2H+,具體實驗步驟是先往K2Cr2O7溶液中緩緩滴入NaOH溶液,當(dāng)溶液顏色由橙變成黃色時,化學(xué)反應(yīng)平衡往正反應(yīng)方向移動,然后往里面加入適量的酸,則溶液顏色由黃色變成橙色。通過觀察這個實驗現(xiàn)象,我們知道化學(xué)反應(yīng)平衡往逆反應(yīng)方向移動。接著,教師帶領(lǐng)學(xué)生總結(jié)濃度變化對化學(xué)平衡影響的規(guī)律,即增大反應(yīng)物的濃度或者減小生成物的濃度,平衡往正反應(yīng)方向移動;減小反應(yīng)物的濃度或者增大生成物的濃度,平衡往逆反應(yīng)方向移動。由此可見,適當(dāng)增加相對廉價的反應(yīng)物或者及時分離出生成物,平衡向正反應(yīng)方向移動,能夠提高產(chǎn)物產(chǎn)量,減少生產(chǎn)成本。
(二)鼓勵學(xué)生做實驗探究體驗化學(xué)平衡原理
在高中化學(xué)教學(xué)過程中,實驗教學(xué)這一重要環(huán)節(jié)不僅是學(xué)生學(xué)習(xí)理論知識的主要途徑,也是學(xué)生研究各種化學(xué)原理、規(guī)則與規(guī)律的關(guān)鍵方式,更是鍛煉學(xué)生動手能力的常規(guī)手段之一。為更好地運用化學(xué)平衡原理,教師需要及時轉(zhuǎn)變教育觀念,堅持以“學(xué)生探究實驗為主,演示實驗為輔”的教學(xué)原則,盡可能為學(xué)生創(chuàng)設(shè)更多親自動手操作實驗的機會,鼓勵他們依托實驗深層次探究化學(xué)平衡原理,切實體會化學(xué)平衡原理的內(nèi)涵,進一步提高學(xué)習(xí)效果。
例如,在“壓強變化對化學(xué)平衡的影響”教學(xué)中,教師可以利用多媒體設(shè)備播放N2(g)+3H2(g)[]2NH3(g)這一可逆反應(yīng)的視頻,帶領(lǐng)學(xué)生一起分析壓強對合成氨的平衡的影響。學(xué)生在觀察實驗視頻的過程中發(fā)現(xiàn)增大壓強時,該化學(xué)平衡往正反應(yīng)方向移動,減小壓強時,化學(xué)平衡往逆反應(yīng)方向移動。接著,教師播放可逆反應(yīng)FeO(s)+CO(g)?Fe(s)+CO2(g)實驗視頻,并通過改變壓強的大小,引導(dǎo)學(xué)生觀察實驗結(jié)果。學(xué)生發(fā)現(xiàn)針對該實驗,通過改變壓強的大小對反應(yīng)的平衡沒有影響。隨后教師指導(dǎo)學(xué)生討論探究其他條件不變,壓強增大或者減小時,N2O4(g)?2NO2(g)反應(yīng)平衡是否移動、移動方向如何?學(xué)生討論后回答,并歸納總結(jié)出“在其他條件不變時,增大壓強,化學(xué)平衡向著氣體總體積減小的方向移動;反之,減小壓強,化學(xué)平衡向著氣體總體積增大的方向移動”的規(guī)律。
(三)轉(zhuǎn)變實驗方式內(nèi)化化學(xué)平衡原理
在高中課程體系中,化學(xué)作為一門以實驗為基礎(chǔ)的自然科學(xué)類科目,涉及大量的實驗研究,尤其是學(xué)生在學(xué)習(xí)化學(xué)平衡原理這一相對抽象的知識時,更是離不開實驗的幫助,通過做實驗學(xué)生可以更加深入地分析化學(xué)平衡原理,進而理解化學(xué)平衡原理的本質(zhì)。對此,高中化學(xué)教師應(yīng)該適當(dāng)轉(zhuǎn)變有關(guān)化學(xué)平衡原理的實驗教學(xué)方式,利用發(fā)現(xiàn)問題的方式引導(dǎo)學(xué)生沿著正確的方向思考,讓學(xué)生深入實驗活動,認(rèn)真觀察實驗程序與反應(yīng)變化,進而內(nèi)化化學(xué)平衡原理。
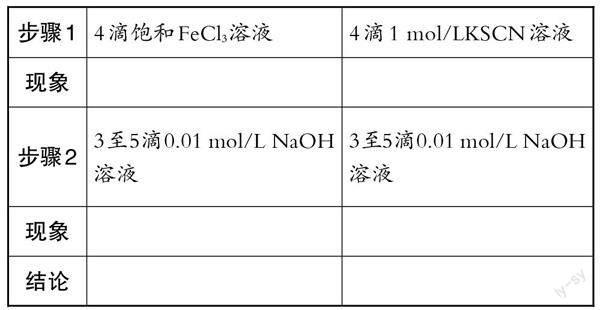
例如,以“化學(xué)平衡的移動”教學(xué)為例,本節(jié)課是以化學(xué)平衡狀態(tài)為基礎(chǔ),通過實驗進行驗證,探究反應(yīng)物的濃度對化學(xué)平衡狀態(tài)的影響。課堂上,在探究反應(yīng)物的濃度對化學(xué)平衡移動的影響時,教師可以轉(zhuǎn)變實驗方式,安排以下實驗教學(xué)環(huán)節(jié)。教師事先準(zhǔn)備好0.05 mol/L的氯化鐵溶液、0.1 mol/L的硫氰化鉀溶液、1 mol/L的硫氰化鉀溶液、0.1 mol/L的氫氧化鈉溶液,以及若干支試管。實驗原理:FeCl3(aq)+6KSCN(aq)?Fe(SCN)3(aq)+6KCl(aq)。實驗步驟:(1)向盛有5 mL 0.05 mol/L FeCl3溶液的試管中加入5 mL 0.1 mol/L KSCN溶液,溶液顯紅色;(2)將(1)中紅色溶液分置于兩支試管中;向其中一支試管中滴加4滴飽和FeCl3溶液,充分振蕩,觀察顏色變化;向第二支試管中滴加4滴1 mol/LKSCN溶液,觀察溶液顏色變化;(3)向(2)的兩支試管中各加入3至5滴0.01 mol/LNaOH溶液,觀察實驗現(xiàn)象,并要求學(xué)生完成下表。
接著,教師組織學(xué)生對上述實驗進行深入思考、討論,并且由學(xué)生代表來解釋實驗現(xiàn)象并得出結(jié)論:增大生成物濃度,平衡向逆反應(yīng)方向移動;減小生成物濃度,平衡向正反應(yīng)方向移動;增大反應(yīng)物濃度,平衡向正反應(yīng)方向移動;減小反應(yīng)物濃度,平衡向逆反應(yīng)方向移動。經(jīng)過深入探討,學(xué)生能夠深刻記憶上述實驗現(xiàn)象、實驗過程和實驗原理。這有助于他們在大腦中形成相對完善的知識體系,進一步加深他們對化學(xué)平衡原理的認(rèn)識和理解。
三、化學(xué)平衡原理在解題訓(xùn)練層面的應(yīng)用
(一)巧用化學(xué)平衡判定方法解答試題
在高中化學(xué)課程教學(xué)中,要想更好地運用化學(xué)平衡原理,教師不僅可以在理論知識講授與實驗操作兩個環(huán)節(jié)運用化學(xué)平衡判定方法,還可以基于解題訓(xùn)練層面切入,圍繞化學(xué)平衡原理的運用設(shè)計有針對性的訓(xùn)練習(xí)題,為學(xué)生創(chuàng)設(shè)運用化學(xué)平衡原理解題的機會,指導(dǎo)學(xué)生學(xué)會巧妙運用化學(xué)平衡判定方法解答試題。因此,高中化學(xué)教師在解題訓(xùn)練中,應(yīng)帶領(lǐng)學(xué)生在解題過程中不斷通過練習(xí)與總結(jié),進而牢固掌握化學(xué)平衡原理的要點,增強他們對化學(xué)平衡知識和判別方法的理解。
例1:在一個密閉的容器內(nèi),化學(xué)反應(yīng)mA(g)+nB(g)?pC(g)+qD(g)達到平衡狀態(tài),不改變溫度條件,將容器體積擴大1倍,當(dāng)化學(xué)反應(yīng)重新達到平衡時,物質(zhì)B的濃度變?yōu)樵瓉淼?5%,那么以下說法正確的有(? )。
A.化學(xué)平衡往逆反應(yīng)方向進行移動
B.物質(zhì)A的質(zhì)量分?jǐn)?shù)提高
C.物質(zhì)A的轉(zhuǎn)化率降低
D.m+n 【分析】當(dāng)容器體積增大時會對化學(xué)平衡產(chǎn)生影響,學(xué)生在解答本題時,可以假設(shè)容器體積變大后不會對化學(xué)平衡產(chǎn)生影響,那么物質(zhì)B和C的濃度均為原來的50%,但反應(yīng)達到平衡時,B的濃度是原來的45%,說明減小壓強平衡向正反應(yīng)方向移動,如此則可說明m+n (二)巧用化學(xué)平衡極限方法解答試題 從本質(zhì)來看,化學(xué)平衡都屬于可逆反應(yīng),即為化學(xué)反應(yīng)中的反應(yīng)物與生成物均不能完全消耗掉。在處理有關(guān)化學(xué)反應(yīng)平衡類的選擇題時,教師提示學(xué)生可以結(jié)合化學(xué)平衡原理的特點將一些不是可逆反應(yīng)的化學(xué)反應(yīng)直接排除,提高他們做題的正確率。此外,在有關(guān)化學(xué)平衡原理的計算題中,教師還可以指導(dǎo)學(xué)生使用極限法,即假設(shè)可逆反應(yīng)的起始反應(yīng)物均完全反應(yīng),以這種極限條件為假設(shè)將會得到生成物的最大值,這樣學(xué)生在解決化學(xué)平衡原理的計算題時就可以快速計算出正確的結(jié)果。 例2:已知在一個恒容密閉的容器中,1 mol的水蒸汽與1 mol的一氧化碳氣體在一定條件下發(fā)生反應(yīng):CO(g)+H2O(g)?CO2(g)+H2(g)且達到平衡狀態(tài),生成0.68 mol的二氧化碳,假設(shè)其他條件不變,再把4 mol的水蒸汽充入到密閉容器中,當(dāng)反應(yīng)再次達到平衡狀態(tài)時,那么生成物二氧化碳的量可能是(? )mol。 A.2? B.1.4? C.0.52? D.0.94 【分析】在處理這類題目時,教師可以指導(dǎo)學(xué)生采用極限假設(shè)法進行計算,將1 mol的水蒸汽與1 mol的一氧化碳氣體反應(yīng)達到平衡時,有0.32 mol CO、0.32 mol水蒸汽、0.68 mol CO2、0.68 mol H2。在此基礎(chǔ)上,再通入4 mol水蒸汽,化學(xué)平衡顯然向右移動,假設(shè)反應(yīng)完全進行,則生成的二氧化碳氣體為1 mol,但是不可能到1 mol,因此只能處于0.68至1 mol范圍之內(nèi),通過對比分析,只有選項D中的0.94在這一范圍內(nèi),符合答案要求。 (三)巧用化學(xué)平衡分割方法解答試題 在化學(xué)可逆反應(yīng)中,外界條件包括催化劑參與、溫度變化、容器體積等,均會影響化學(xué)反應(yīng)平衡,將正反應(yīng)與逆反應(yīng)速率的相等狀態(tài)進行打破,無論遇到有關(guān)化學(xué)平衡原理的任何題型時,學(xué)生都要認(rèn)真審題,仔細研究題干中涉及的環(huán)境變化條件,把起始量不一樣的兩個化學(xué)平衡進行適當(dāng)分割,轉(zhuǎn)變成一樣的起始量,即對分割法的運用,再結(jié)合題干中提供的具體條件進行解題,從而幫助學(xué)生掌握運用化學(xué)平衡原理分割法解答試題的竅門。 例3:在恒容、恒溫的條件下,有兩個體積一樣的甲、乙容器,往甲容器里面分別充入1 g的二氧化硫和氧氣,往乙容器里面分別充入2 g的二氧化硫和氧氣,那么下列說法不正確的有(? )。 A.乙容器中的化學(xué)反應(yīng)速率比甲容器的大 B.乙容器中的化學(xué)反應(yīng)達到平衡狀態(tài)后氧氣濃度比甲容器的大 C.乙容器中的二氧化硫氣體的轉(zhuǎn)化率比甲容器的大 D.乙容器中的化學(xué)反應(yīng)達到平衡狀態(tài)后二氧化硫氣體的體積分?jǐn)?shù)比甲容器的大 【分析】本題主要考查化學(xué)平衡建立過程和化學(xué)平衡的影響因素。選項A為濃度越大反應(yīng)速率越大;選項B為由于乙容器中的量是甲容器中的兩倍,所以反應(yīng)后乙容器中剩余的氧氣多;選項C為由于乙容器中的量是甲容器中的兩倍,氣體物質(zhì)的量越大,壓強越大,因此乙容器中相當(dāng)于增大壓強,平衡正移,二氧化硫的轉(zhuǎn)化率增大;選項D為由C選項可知,乙容器中二氧化硫的轉(zhuǎn)化率變大,所以二氧化硫的體積分?jǐn)?shù)小。綜上可知,D選項錯誤,因此選D。 綜上所述,在高中化學(xué)教學(xué)中,教師應(yīng)充分認(rèn)識化學(xué)平衡原理的重要性。雖然化學(xué)平衡原理學(xué)習(xí)起來有一定的難度,但是化學(xué)平衡原理是有特點、有規(guī)律可循的,教師應(yīng)把握好教學(xué)契機,從理論知識講授、化學(xué)實驗操作與課后解題訓(xùn)練等多個方面加以運用,為學(xué)生創(chuàng)設(shè)更多運用化學(xué)平衡原理的機會,使學(xué)生在實際學(xué)習(xí)過程中不斷積累與歸納運用化學(xué)平衡原理的經(jīng)驗,讓學(xué)生深刻體會到化學(xué)平衡原理的實用性,不斷增強自身的化學(xué)綜合能力。 參考文獻 [1]賀行武.關(guān)于探討化學(xué)平衡原理在高中化學(xué)里的應(yīng)用[J].中學(xué)生數(shù)理化(教與學(xué)),2020(10). [2]范德超.“化學(xué)坐標(biāo)圖像”教學(xué)探索[D].成都:四川師范大學(xué),2022. [3]孫金鳳.高中化學(xué)變化觀念與平衡思想的教學(xué)實踐探索[D].成都:四川師范大學(xué),2021. [4]鄭弘麗.高中化學(xué)建模教學(xué)的實踐研究[D].蕪湖:安徽師范大學(xué),2020. [5]賀中金.淺析如何在高中化學(xué)教學(xué)中巧用化學(xué)平衡原理[J].天天愛科學(xué)(教育前沿),2019(7). 作者簡介:陸采添(1990— ),廣西欽州人,本科,學(xué)士,主要研究方向為高中化學(xué)教學(xué)。 (責(zé)編 林 劍)

