基于OpenFDA對匹伐他汀的不良反應挖掘與分析
韋國麗 黃美琳 蘭鴻章
【摘要】? 目的? ? 利用美國食品藥品監督管理局公共數據開放項目(the US Food and Drug Administration Public Data Open Project,OpenFDA)檢索匹伐他汀的不良反應報告并進行評價,為臨床用藥提供參考。方法? ? 利用OpenFDA數據庫中的ADR端點交互式圖表板塊中的應用程序接口功能,對匹伐他汀在2004年—2021年7月的不良反應報告數據進行分析。結果? ? 共檢索到匹伐他汀相關不良反應報告1 639份,主要為男性、老年患者,上報不良反應的職業分布以醫師等醫務人員為主,約占總數的80%。ADR上報國家主要為日本和美國,用藥的適應證主要為高血壓、血脂異常等心血管類疾病;不良反應主要為惡心、腹瀉、食欲減退等胃腸道系統反應,其次是乏力、發熱等全身反應,基本與藥品說明書記載的吻合,但仍發掘出肺炎、間質性肺炎、呼吸困難等藥品說明書中未記載的不良反應。結論? ? 基于OpenFDA大數據庫可方便快捷地對匹伐他汀的ADR相關信息進行分析,為臨床合理用藥提供參考。
【關鍵詞】? 匹伐他汀;不良反應;美國食品藥品監督管理局公共數據庫;挖掘/分析
Data mining and analysis of the adverse drug reactions for Pitavastatin on Open FDA
Wei Guoli,Huang Meilin,Lan Hongzhang. The People's Hospital of Hechi City,Hechi,Guangxi? 547000
【Abstract】? Objective? ? To detect and evaluate the signal of adverse drug reactions of pitavastatin from the US Food and drug administration public data open project(OpenFDA),so as to provide references for the rational use of this drug in clinical practices. Methods? ? To use the API function in the interactive chart section of the ADR endpoint in the OpenFDA database to analyze the adverse drug reactions(ADR)of pitavastatin from January 2004 to July 2021. Results? ? A total of 1 639 reports of adverse reactions related to pitavastatin,the adverse reactions population was concentrated.About 80% of the reporting occupations were doctors and other-health professionals.Most of the ADR occurred in Japan and the United States.The main indications for the drug were cardiovascular diseas such as hypertension and dyslipidemia.The ADR are mainly gastrointestinal system reactions such as nausea,diarrhoea,anddecreased appetite,followed by systemic reactions such as malaise and pyrexia,which are basically consistent in the drug instructions.However,pneumonia,interstitial lung disease,and dyspnoea not recorded in the drug instructions.Conclusions? ? It is convenient and quick to mining and analysis the adverse reactions of pitavastatin based on the open FDA database,which provides references for the rational use of this drug in clinical practices.
【Key Words】? Pitavastatin;Adverse reactions;OpenFDA;Excavation/analysis
中圖分類號:R969.3? ? ? ? 文獻標識碼:A? ? ? ? 文章編號:1672-1721(2023)10-0117-03
DOI:10.19435/j.1672-1721.2023.10.037
他汀類藥物是一種羥甲基戊二酰輔酶A還原酶抑制劑,主要機制是競爭性抑制內源性膽固醇合成限速酶 HMG-CoA還原酶在肝臟的合成,阻斷細胞內羥甲戊酸代謝途徑,使細胞內膽固醇合成減少,從而反饋性刺激細胞膜表面低密度脂蛋白(LDL-C)受體數量和活性增加,使血清膽固醇清除增加、水平降低,是目前臨床上使用最廣泛的降脂藥物,且是心腦血管疾病一級及二級預防的重要藥物。常用品種有洛伐他汀、辛伐他汀、普伐他汀、氟伐他汀、阿托伐他汀、瑞舒伐他汀和匹伐他汀等,不同種類、不同劑量的他汀類藥物降低膽固醇及LDL-C的幅度不一樣。盡管他汀類藥物單獨使用安全性良好,長期使用也有較好的耐受性,但是在特殊人群中或合并用藥時仍會出現相關不耐受等不良反應,且不同種類的他汀類藥物的不良反應因其吸收、生物利用度、血漿蛋白結合率、排泄和親脂性方面不同而有所不同[1-3]。匹伐他汀是第三代新型他汀類藥物,1999年11月在日本注冊,2003年7月獲得日本醫藥品醫療器械綜合機構批準,之后于2009年8月獲得美國食品藥品監督管理局(FDA)批準,同年中國食品藥品監督管理局(CFDA)也批準其在中國上市。匹伐他汀不同于其他他汀類藥物,其血漿蛋白結合率為 96% ,在肝中廣泛分布,有顯著的肝腸循環,故只需要較小劑量就能發揮治療作用。研究表明[4-9]其不易與其他藥物產生相互作用,具有較高的安全性,尤其適合特殊人群;但由于其入市時間較短,療效和安全性報道不多,臨床實際運用中的不良反應數據報道不全面。因此,對該藥上市后的不良反應進行挖掘與分析有較大的意義。
OpenFDA是美國FDA在2014年啟動的旨在面向公眾開放健康數據庫。該數據庫每年均可收到約150萬份不良事件信息報告,是目前世界上最主要的ADR監測手段,反映真實世界的大量數據。基于搜索的應用程序接口(application programming interface,API)可收集數據庫中的信息,對藥物相關不良反應進行全面了解與評價,為藥物的臨床使用提供更有參考價值的數據[10-11]。本文通過OpenFDA數據庫,對匹伐他汀的藥品不良反應進行檢索與挖掘,以期為臨床用藥提供參考。
1? ? 資料與方法
1.1? ? 資料來源? ? 本研究通過檢索OpenFDA數據平臺,收集藥品不良事件數據信息。
1.2? ? 方法? ? 利用OpenFDA數據庫的APIs 模塊,進入藥品不良事件端口,啟用數據庫交互式圖表板塊,檢索時間段為2004年1月1日— 2021年7月22日。以“pitavastatin為檢索詞在“patient.drug.medicinalproduct”字段中檢索。然后,根據檢索需求(上報國家、性別、年齡分布、ADR 類型、ADR 臨床表現等)進行檢索,獲取相應的數據及圖表信息。
2? ? 結果
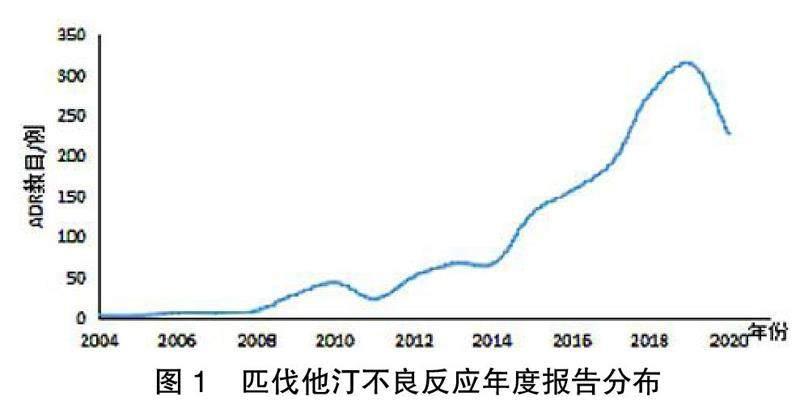
2.1? ? ADR年度報告? ? 檢索結果顯示,在檢索時間段內,FDA共收到1 639份關于匹伐他汀的不良反應報告。按年度分布如圖1所示,匹伐他汀的不良反應報告數量從2014年開始呈現急劇增長的趨勢,至2019年達到頂峰,為315份。
2.2? ? 患者性別及年齡? ? 匹伐他汀的1 639份ADR報告中男性828份,占50.52%;女性683份,占41.67%;未知性別128份,男性的ADR報告份數明顯多于女性。年齡分布上,老年人(≥65歲)占62%,成年人(18~64歲)占37%,未有關于未成年的數據上報。
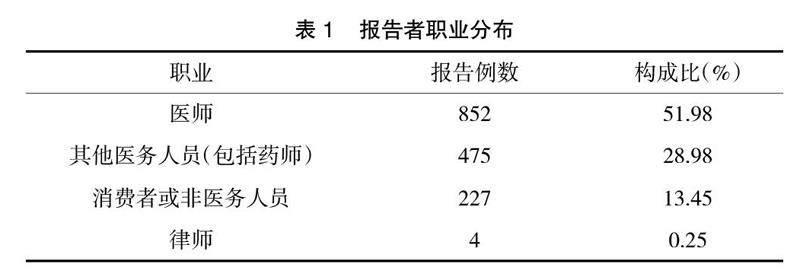
2.3? ? 報告者職業分布? ? 匹伐他汀ADR 報告中約95%上報者填報了自己的職業情況,共1 558份。可以看出醫師是最主要的報告群體,共852份,占總數的51.98%;其次為其他醫務人員(包括藥師),共475份,占28.98%左右;其余上報的人員包括消費者或非醫務人員、律師等,見表1。
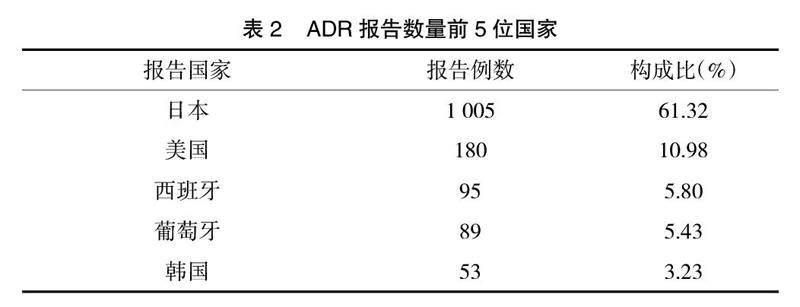
2.4? ? ADR發生國家? ? 檢索結果顯示,日本報告的匹伐他汀不良反應數量最多,高達61.32%,隨后是美國、西班牙、葡萄牙、韓國,見表2。
2.5? ? 藥物適應證? ? 1 639份匹伐他汀的ADR 報告中,藥物適應證不明確或者信息缺失的有597份,而有些報告上報的適應證為多個。通過統計,其排前10位的適應證為高血壓、血脂異常、高脂血癥等,見表3。
2.6? ? 常見ADR發生類型? ? 在上報的1 639 份匹伐他汀不良反應報告中均明確上報了ADR 類型,且有些報告涉及多個系統 ADR。其常見的不良反應包括乏力、惡心、腹瀉、發熱、肌痛等,涉及多個系統(胃腸道系統、骨骼肌系統、呼吸系統、腎臟系統等),見表4。
2.7? ? 患者的轉歸? ? 患者發生ADR的轉歸是指截至最后觀察時間時患者轉歸的情況,但因為上報的病例可不斷更新,因此可能會出現患者轉歸情況例次多于總報告份數,轉歸結果也可能會由于不同的觀察時間點不同,見表5。
3? ? 討論
從報告分布時間及報告來源來看,2014年后匹伐他汀的 ADR報告呈現急劇增長的趨勢,這可能與2014年FDA要求生產商就藥物上市后應開展相關風險研究相關;2020年的ADR報告數較前下降,可能受全球新型冠狀病毒疫情的影響。在報告人員職業分布中,醫師和其他醫務人員是主要的上報人員,約占80%;表明匹伐他汀相關的ADR主要受到醫務人員的重點關注,而其他消費者關注較少。數據顯示,日本和美國是匹伐他汀不良反應報告的主要國家,原因可能是數據庫來源于美國,而匹伐他汀的生產商來自日本,而在其他國家上市時間較晚。報告中匹伐他汀用藥適應證為高血壓、血脂異常、2型糖尿病等心血管疾病,因為這些患者往往合并血脂異常,故基本與相關適應證符合。但值得關注的是,其中有 597例(36.42%)患者藥品使用適應證不明,警惕該藥物在臨床應用時應嚴格掌握其適應證,避免不合理用藥。匹伐他汀不良反應主要為惡心、腹瀉、食欲減退等胃腸道系統不良反應,其次是乏力、發熱等全身反應,還有肌痛、橫紋肌溶解、肝酶升高、肝功能異常等常見ADR。通過比對藥品說明書,本文挖掘的不良反應結果基本與匹伐他汀說明書收錄的吻合。但肺炎、間質性肺炎、呼吸困難為說明書中未記載的不良反應,臨床使用時也應注意觀察患者是否出現上述ADR表現。對于患者轉歸情況中有147例死亡,37例患者存在后遺癥,提示臨床用藥中一旦發現疑似ADR,應立即采取不良反應的對癥處理措施,避免出現嚴重不良事件。總體來說,本研究結果顯示匹伐他汀相關不良反應較輕且較為明確,具有較高的安全性,與目前大多數研究[4-9]結果一致;說明匹伐他汀是一種理想的降脂的藥物,尤其適合特殊人群。但由于價格、醫生用藥習慣問題,匹伐他汀在臨床仍作為非首選他汀類降血脂藥物。
OpenFDA是基于FAERS的自發呈報數據庫,為藥品不良反應事件的大數據庫,能夠快速獲取真實世界臨床使用數據,對藥品不良反應數據分析具有重要意義。但由于數據庫的缺陷,只能看到結果信息,無法獲取患者用藥相關的完整信息,故會導致數據的質量及完整性存在一定偏倚;但合理利用分析工具對其深入研究并數據挖掘,對 ADR 的監測與研究具有重要意義。
本研究通過檢索OpenFDA 數據庫,全面挖掘分析匹伐他汀實際臨床應用中的ADR發生情況,總體表明其安全性較高;但在臨床應用時應嚴格掌握其適應證,除說明書記載的不良反應外,還需關注肺部系統相關的不良反應。
參考文獻
[1]? ? 諸駿仁,高潤霖,趙水平,等.中國成人血脂異常防治指南(2016年修訂版)[J].中華心血管病雜志,2016,44(10):833-853.
[2]? ? 中華醫學會,中華醫學會雜志社,中華醫學會全科醫學分會,等.血脂異常基層診療指南(實踐版·2019)[J].中華全科醫師雜志,2019(5):417-421.
[3]? ? MACH F,BAIGENT C,CATAPANO A L,et al.2019 ESC/EAS Guidelines for the management of dyslipidaemias:lipid modification to reduce cardiovascular risk[J].Eur Heart J,2020,41(1):111-188.
[4]? ? R? tz Bravo A E,Tchambaz L,Kr? henbühl-Melcher A,et al.Prevalence of potentially severe drug-drug interactions in ambulatory patients with dyslipidaemia receiving HMG-CoA reductase inhibitor therapy[J].Drug Saf,2005,28(3):263-275.
[5]? ? TAGUCHI I,IIMURO S,IWATA H,et al.High-Dose Versus Low-Dose Pitavastatin in Japanese Patients With Stable Coronary Artery Disease(REAL-CAD):A Randomized Superiority Trial[J].Circulation,2018,137(19):1997-2009.
[6] STENDER S,BUDINSKI D,HOUNSLOW N.Pitavastatin demonstrates long-term efficacy,safety and tolerability in elderly patients with primary hypercholesterolaemia or combined(mixed)dyslipidaemia[J].Eur J Prev Cardiol,2013,20(1):29-39.
[7]? ? BRAAMSKAMP M J,STEFANUTTI C,LANGSLET G,et al.Efficacy and Safety of Pitavastatin in Children and Adolescents at High Future Cardiovascular Risk[J].J Pediatr,2015,167(2):338-343.e5.
[8]? ? 李麗珍,周新明,王寶,等.匹伐他汀鈣與阿托伐他汀鈣治療老年性高血脂的療效比較[J].北方藥學,2020,17(10):18-20.
[9]? ? 杜萍.匹伐他汀鈣與辛伐他汀治療老年冠心病的有效性比較[J].臨床合理用藥雜志,2021,14(20):41-43.
[10]? ? 施雯慧,陳穎,姚捷,等.FDA公共數據開放項目中屈螺酮炔雌醇片的分析研究[J].中國藥物警戒,2015,12(9):552-555.
[11]? ? 蒙龍,唐學文,季歡歡,等.他汀類藥物相關不良反應的信號挖掘與評價——基于美國OpenFDA公共數據開放項目的數據挖掘研究[J].中國新藥雜志,2019,28(2):244-248.
(收稿日期:2023-01-19)

