基于網絡藥理學和實驗驗證的甘麥大棗湯抗抑郁的物質基礎及作用機制研究*
蒲蓮蓮,劉漫,楊穎,嵇晶,何苗,程建明,劉陶世
1 南京中醫藥大學藥學院 江蘇南京 210023
2 江蘇省經典名方工程研究中心 江蘇南京 210023
3 太極四川綿陽制藥有限公司 四川綿陽 621000
甘麥大棗湯為“醫圣”張仲景所創,載于《金匱要略》[1]曰:“婦人臟躁,喜悲傷欲哭……甘麥大棗湯主之。甘草三兩,小麥一斤,大棗十枚……亦補脾氣。”該方組成簡單,僅有甘草、小麥、大棗三味,可謂藥簡效彰。方中小麥補營益陰,寧心安神為君藥;甘草補養心氣,和中緩急為臣藥;大棗補中益氣,養血安神為佐使藥;三物合用,共奏甘潤滋養,養心寧神,和中緩急之功[2]。歷來醫家常用于臟躁、郁癥等情志類疾病。有統計[3]分析古籍中治療類似抑郁癥的方劑中,該方使用頻數占其匯總方劑的榜首。現代臨床常用于各類抑郁癥、失眠、更年期綜合征等的治療[4-6]。甘麥大棗湯的長期臨床應用已證明其療效確切,但對其研究多集中于藥理作用、臨床療效等方面,缺乏對其復方中化學成分的系統分析,嚴重限制了該方藥效物質基礎研究及質量控制指標的確定。
UPLC-Q-TOF-MS是一種高通量、高靈敏度、快速高效的非靶向分析方法,廣泛應用于單味或復方中藥化學成分的系統分析。網絡藥理學是一種基于系統生物學理論,選取特定信號節點(Nodes)進行多靶點藥物分子設計的方法。應用于中藥研究,形象的反應了中藥發揮療效的多成分、多靶點、多途徑的特點。本研究采用UPLC-Q-TOF-MS 技術結合網絡藥理學及動物實驗,探討甘麥大棗湯抗抑郁的關鍵成分及作用機制。
材 料
1 儀器
LC-30A超高效液相色譜儀(日本島津);Triple Tof5600 +質譜儀(美國ABSCIEX);超聲波清洗器(昆山禾創超聲儀器有限公司);離心機(上海安亭科學儀器廠);電熱套(鞏義市予華儀器有限責任公司);電子分析天平(賽多利斯科學儀器有限公司)。
2 藥材和試劑
方中甘草、淮小麥、大棗三味,均購置于安徽亳州中藥材市場,經鑒定甘草為豆科植物甘草Glycyrrhiza uralensis Fisch.的根和根莖;淮小麥為禾本科植物小麥Triticum aestivum L.的穎果;大棗為鼠李科植物棗Ziziphus jujuba Mill.的果實。
甘草酸銨對照品(中檢所,110731-202021);甘草苷對照品(批號111610-201908,99%);熊果酸對照品(批號L03A6Y1,99%);齊墩果酸對照品(批號H04J9262784,99%);鹽酸氟西汀(上海中西制藥有限公司);LPS(Biosharp公司);甲醇(美國TEDIA公司);乙醇(無錫市亞盛化工有限公司);生理鹽水(四川科倫藥業股份有限公司);乙腈(德國默克公司);甲酸(阿拉丁試劑(上海)有限公司);小鼠ELISA試劑盒(南京翼飛雪生物科技有限公司)。
3 實驗動物
Babl/c雄性小鼠50只,體質量18~20 g,上海斯萊克實驗動物有限責任公司,生產許可證號SCXK(滬)2022-0004。適應性喂養7 d,自由飲食和飲水。南京中醫藥大學實驗動物倫理委員會審查并批準(202207A062)。
方 法
1 色譜條件
色譜柱:Kromasil (250 mm×4.6 mm,5 μm),柱溫:40 ℃,流動相A為0.1%甲酸水(v/v),流動相B為乙腈。梯度洗脫:0~3 min,10% B;3~39 min,90%B;39~41 min,90% B;41~42 min,10% B;42~45 min,0 B。流速為1mL/min,進樣量為20 μL。
2 質譜條件
電噴霧離子源(ESI),離子源溫度(TEM)550 ℃,氣簾氣(CUR)40 psi,霧化氣(GSI)55 psi,輔助加熱氣(GS2)55 psi,離子源噴霧電壓(IS)5500 V/-5500 V,碰撞電壓(CE)10V/-10V,去簇電壓(DP)100 V/-100V,掃描范圍為m/z 50~1500。
3 供試品溶液制備
3.1 對照品溶液 分別取甘草酸銨、甘草苷、熊果酸、齊墩果酸對照品各10 mg,置10 mL容量瓶中,甲醇超聲溶解,定容,制成1mg/mL的對照品溶液。分別量取各對照品溶液液適量,混合后加入甲醇稀釋,備用。
3.2 甘麥大棗湯樣品溶液 取甘草9 g、淮小麥30 g、大棗15 g,10倍量水浸泡30 min,加熱至沸騰后煎煮60 min,過濾,再加8倍量水煎煮50 min,濾過,取濾液8000 r.min-1離心10 min,取上清液過0.22μm微孔濾膜,備用。取上述所得甘麥大棗湯濾液,濃縮至生藥量1g/m L。
3.3 甘麥大棗湯總黃酮溶液 取甘草9 g、淮小麥30 g、大棗15 g,10倍量乙醇浸泡30 min,回流提取60 min,濾過,濃縮至無醇味,加水稀釋至生藥量1 g/m L。
3.4 鹽酸氟西汀溶液 取適量藥品,以生理鹽水配制為2mg/mL藥物溶液。
4 化合物結構分析
照“1”“2”項下條件,采集甘麥大棗湯正、負離子模式下的質譜數據。首先,通過SciFinder、本草組鑒(HERB)以及文獻,收集整理甘草、淮小麥、大棗的化學成分信息,構建甘麥大棗湯化學成分數據庫。其次,采用Peakview 1.2軟件對一級質譜提供的精確準分子離子峰進行分析,計算其未知化合物的元素組成和可能的分子式(誤差±5.0×10-6),對各色譜峰進行初步鑒定。最后,將目標化合物的二級質譜碎片信息與對照品、數據庫及文獻提供的保留時間、裂解規律等進行對比分析。
5 網絡藥理學分析
5.1 甘麥大棗湯潛在活性成分 通過PubChem數據庫獲取已鑒定各成分的SMILES號或2D結構,導入SwissADME數據庫,根據ADME參數篩選潛在活性化學成分。篩選條件GI absorption為High,Lipinski為Yes[7-8],少數不符合條件者,但有研究證明其為主要有效成分,亦將其作為潛在活性成分。如甘草苷、甘草酸[9-10]。
5.2 甘麥大棗湯潛在作用靶點 將潛在活性成分導入SuperPred和SwissTargetPrediction 數據庫,預測其靶點,整合去重。在GeneCards、DrugBank、PharmGKB、TDD數據庫,以“depression”為關鍵詞檢索,整合去重得到抑郁癥疾病靶點。分別將成分和疾病靶點輸入Venny 2.1網站,繪制Venn圖,獲取交集靶點,即為潛在作用靶點。
5.3 成分—靶點網絡構建 將活性成分、疾病及靶點輸入Cytoscape 3.9.1軟件,構建成分-疾病-靶點網絡。通過CytoNCA插件對網絡進行拓撲分析,根據degree大小篩選甘麥大棗湯抗抑郁的關鍵成分。
5.4 PPI網絡構建 將潛在作用靶點輸入String11.5數據庫,物種選擇“Homo sapiens”,其他參數默認不變,獲取PPI網絡。將結果導入Cytoscape 3.9.1軟件,繪制PPI網絡圖,利用其CytoNCA功能對PPI網絡信息進行拓撲分析,得到甘麥大棗湯治療抑郁癥的核心靶點。
5.5 GO功能與 KEGG 通路富集分析 將篩選出的交集靶點輸入Metascape數據庫,以P<0.01 作為條件,進行GO功能與 KEGG通路富集分析,并采用“微生信”云平臺進行數據可視化。最終,構建甘麥大棗湯抗抑郁作用的“成分-靶點-通路”關聯網絡。
6 動物實驗
6.1 分組及給藥 小鼠適應性喂養7天后,按體重隨機分為空白組、模型組、鹽酸氟西汀組、甘麥大棗湯組、甘麥大棗湯總黃酮組,每組8只小鼠。各組小鼠均灌胃給藥,2次/d(隔12 h)連續給藥7d。空白組、模型組灌胃純水,其他組灌胃各組對應藥物。灌胃體積均為10 mL/kg。
6.2 急性抑郁造模方法 在實驗第8天,以LPS腹腔注射方式造模。除空白組外,各組小鼠腹腔注射LPS溶液(.83 mg/kg),給藥體積10 mL/kg,空白組注射等體積生理鹽水。4.5 h后開始行為學檢測,評價小鼠抑郁癥狀。造模6 h后收集小鼠外周血清及腦組織,分別于-20℃及-80℃保存待測。
6.3 行為學檢測方法
6.3.1 懸尾實驗 在小鼠尾尖約2cm處固定,將小鼠頭朝下懸掛于一四周封閉紙箱內6min,距離底部約10cm,記錄小鼠2~6min內的累計不動時間。
6.3.2 強迫游泳實驗 將小鼠置于一直徑10cm,水深20cm容器內,水溫24℃左右,觀察6min內小鼠游泳情況,記錄小鼠2~6min內的累計不動時間。
6.4 小鼠外周血清IL-1β、TNF-α、5-HT、NE含量檢測 各組小鼠血清均采用ELISA法檢測TNF-α、IL-1β、NE、5-HT的含量,實驗步驟按試劑盒方法操作。
結 果
1 甘麥大棗湯化學成分的鑒定
采用UPLC-Q-TOF-MS/MS 技術以質譜條件項下質譜條件對甘麥大棗湯樣品進行正、負離子全掃,其總離子流圖見圖1。照化合物結構分析項下數據處理方法,在甘麥大棗湯中共鑒定出95個化合物,包括45個黃酮類、19個萜類、12個有機酸類、4個氨基酸類以及15個其他類化合物。各化合物的保留時間(tR)、碎片離子等信息,見表1。
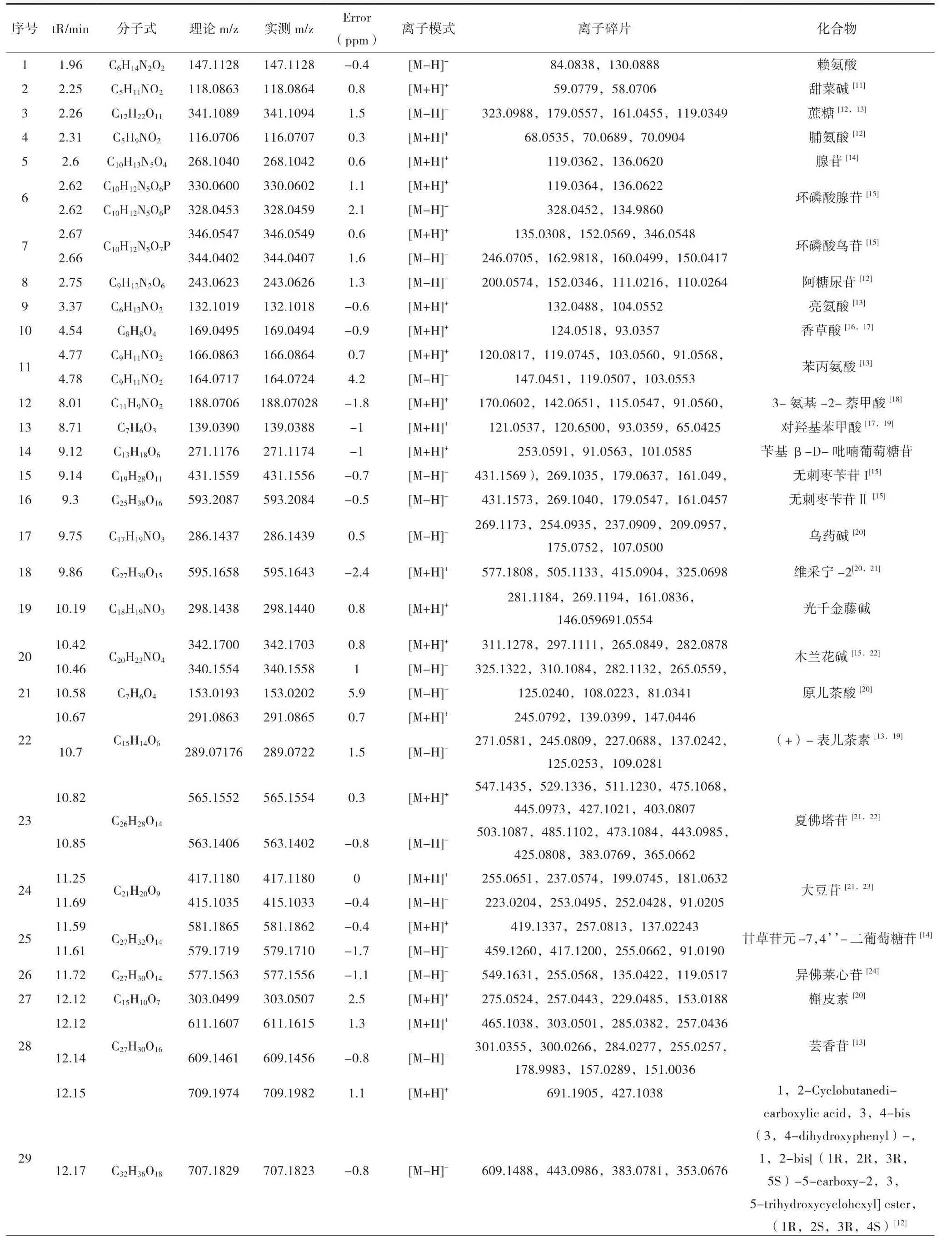
表1 甘麥大棗湯化學成分鑒定分析
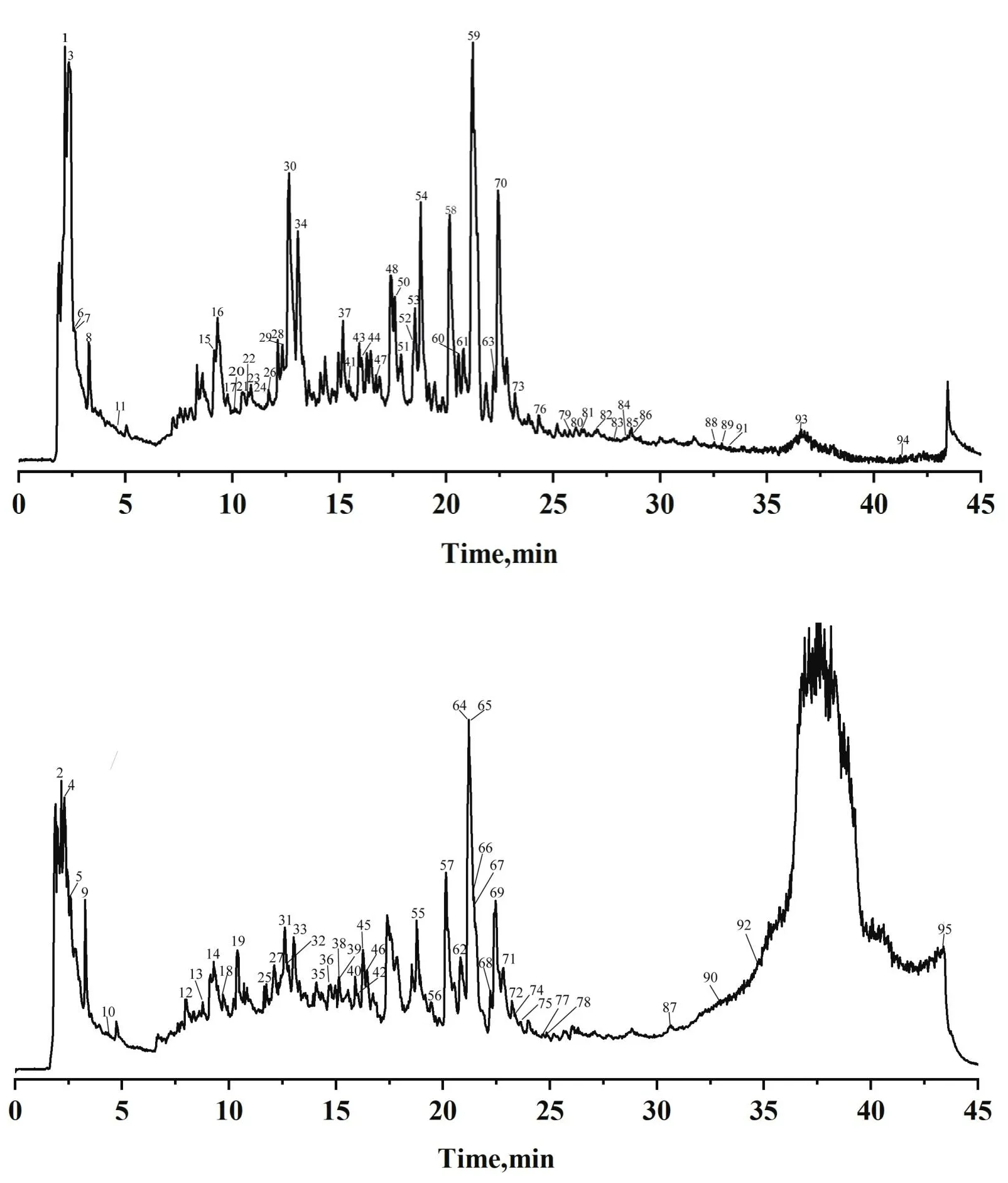
圖1 甘麥大棗湯的負離子(A)和正離子(B)模式下 TIC 圖
2 網絡藥理學分析
2.1 甘麥大棗湯化學成分及其潛在作用靶點 共篩選獲得59個活性成分,對活性成分別進行靶點的預測和收集,獲得成分靶點366個和602個,整理去重共得成分靶點155個。以“depression”為關鍵詞,進行數據庫檢索,合并去重,最終得到1037個疾病靶點。繪制成分和疾病靶點Venn圖,獲得潛在靶點40個,見圖2。

圖2 成分靶點與疾病靶點韋恩圖
2.2 成分—靶點網絡構建 將甘麥大棗湯活性成分、疾病及交集靶點輸入Cytoscape 3.9.1 軟件,構建甘麥大棗湯成分-靶點網絡(圖3)。通過拓撲分析,以degree計,大于中位數的即為甘麥大棗湯抗抑郁的關鍵成分,共12個,即芹菜素、N-去甲(基)荷葉堿、山奈酚、大豆素、柚皮素、甘草黃酮C、烏拉爾醇、甘草黃酮醇、甘草寧C、甘草次酸、烏藥堿、巴婆堿。
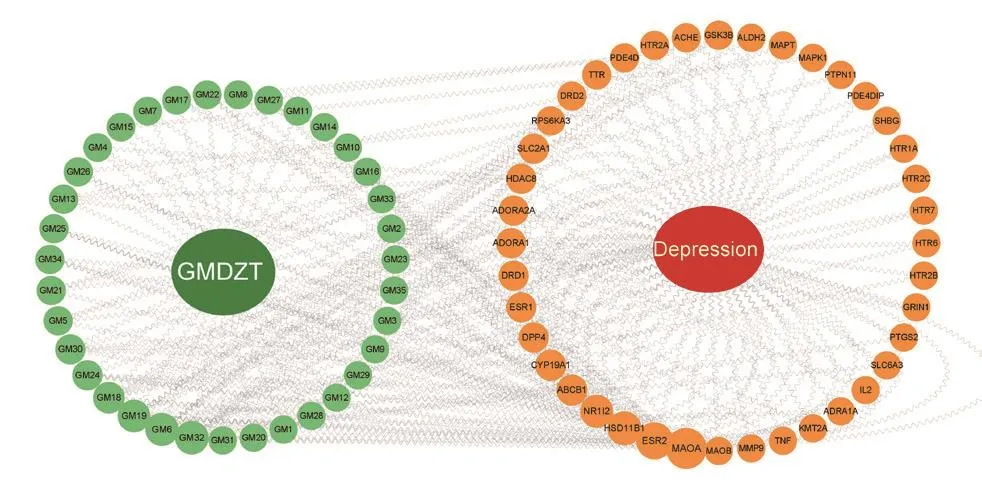
圖3 成分-靶點網絡圖
2.3 PPI網絡的構建及核心靶點篩選 將潛在作用靶點導入String11.5數據庫,獲取靶點間相互作用關系,構建PPI網絡,見圖4。以degree、betweenness、closeness 3 個重要拓撲參數均大于其中位數進行篩選,并以degree計,TNF、SLC6A3、ESR1、MAOB、MAPK1、PTGS2、MAOA等16個靶點可能為甘麥大棗湯抗抑郁作用的核心靶點。
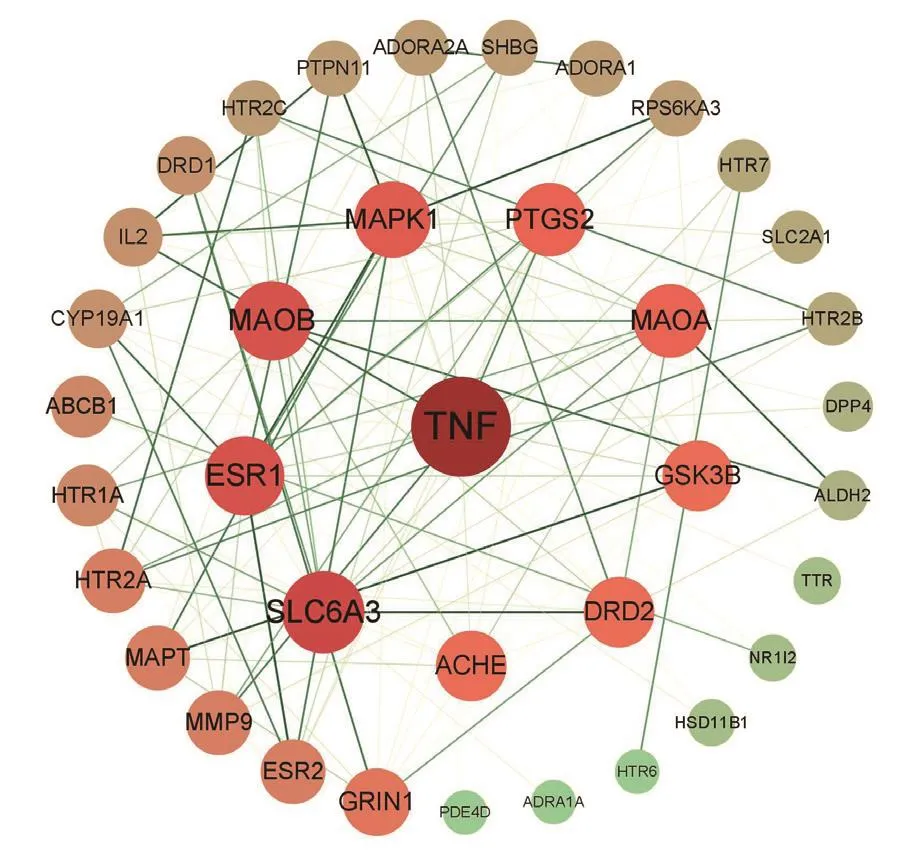
圖4 交集靶點 PPI 網絡圖
2.4 GO功能KEGG信號通路分析 對個16核心靶點進行GO功能和KEGG信號通路富集分析,共獲得個GO條目284個,分別為生物過程(BP)條目248 個,細胞組成(CC)條目28 個,分子功能(MF)條目8 個,見圖5。生物過程主要涉及到神經遞質水平調節、跨突觸信號調節、認知、學習和記憶等;細胞組成主要是樹突、膜筏、軸突、突觸膜等;分子功能主要包括胺結合、神經遞質受體活性、蛋白酶結合、磷酸酶結合、氧化還原酶活性等。
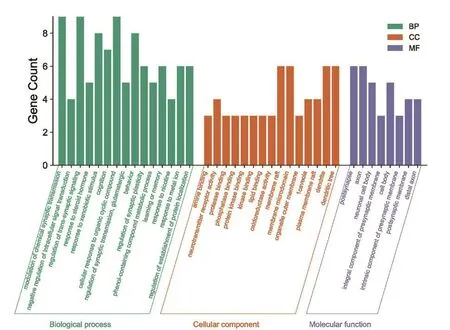
圖5 GO 富集分析
通過 KEGG 富集分析得到信號通路37條,取前20條通路進行可視化見圖6。結果顯示,與甘麥大棗湯抗抑郁有密切聯系的信號通路主要有神經退行性病變-多種疾病通路)、5-羥色胺能突觸、環磷酸腺苷信號傳導、帕金森病、神經活性配體-受體相互作用等神經相關通路;乳腺癌、催乳素信號通路、內分泌抵抗、雌激素信號通路等內分泌相關通路;IL-17信號通路、人類乳突病毒感染、T細胞受體信號通路等炎癥免疫相關通路。構建甘麥大棗湯抗抑郁作用的“關鍵活性成分-靶基因-信號通路”網絡,見圖7。
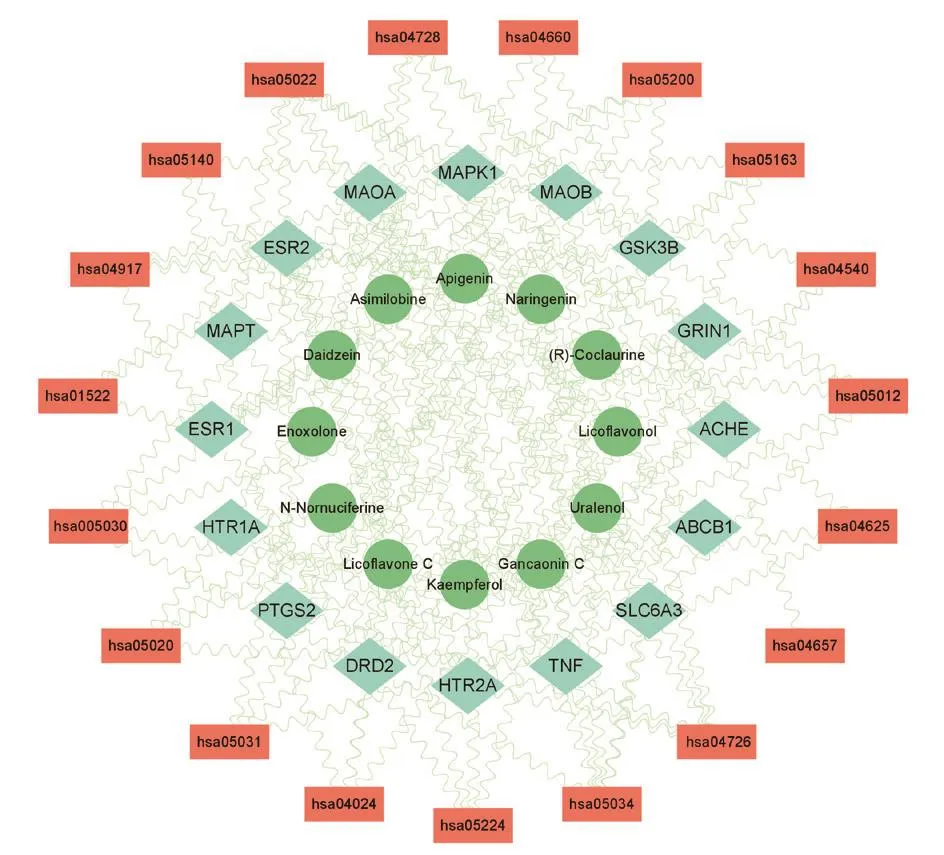
圖7 成分-靶點-通路網絡
3 動物實驗
3.1 小鼠行為學檢測結果 結果如表2所示,與空白組比較,模型組懸尾及強迫游泳累計不動時間均明顯延長,表明造模成功。與模型組相比,各組懸尾及強迫游泳累計不動時間均顯著降低。
表2 各組對LPS致急性抑郁小鼠抑郁樣行為的影響( ±s,n=8)

表2 各組對LPS致急性抑郁小鼠抑郁樣行為的影響( ±s,n=8)
注:與空白組比較 # P<0.01,與模型組比較 * P<0.01
組別劑量懸尾累計不動時間/s強迫游泳累計不動時間/s體重/g空白組—47.69±13.2385.77±17.7924.25±0.77模型組—86.13±16.95#141.11±16.75#24.26±1.58鹽酸氟西汀組20mg/kg27.05±7.37*47.76±14.99*23.41±0.57甘麥大棗湯組10g/kg53.91±13.47*48.67±11.19*23.90±0.81甘麥大棗湯總黃酮組10g/kg49.45±12.22*55.90±12.51*24.03±1.37
3.2 小鼠外周血清IL-1β、TNF-α含量結果 結果如表3所示,與空白組比較,模型組小鼠外周血清中的 IL-1β、TNF-α含量均顯著升高。與模型組相比,各給藥組均可明顯降低小鼠血清中IL-1β、TNF-α含量,其中甘麥大棗湯組較其總黃酮組低,差異具有顯著性。
表3 各組對LPS致急性抑郁小鼠炎性因子及神經遞質的影響( ±s,n=8)
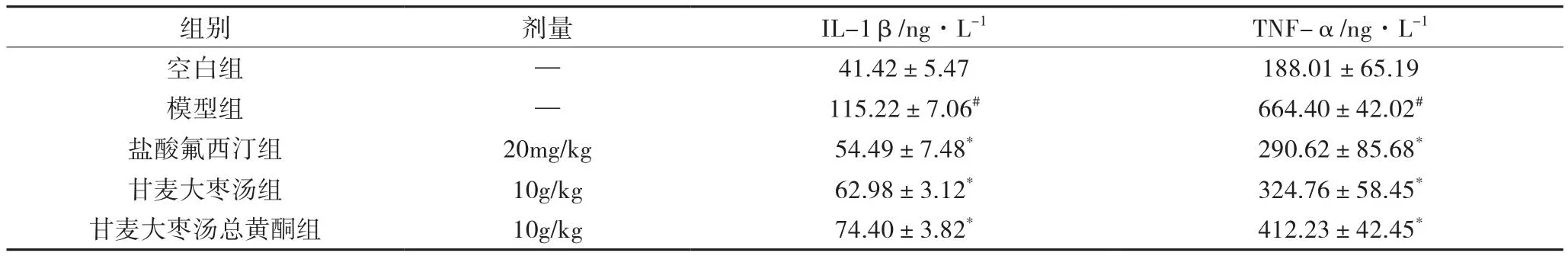
表3 各組對LPS致急性抑郁小鼠炎性因子及神經遞質的影響( ±s,n=8)
注:與空白組比較 # P<0.01,與模型組比較 * P<0.01
組別劑量IL-1β/ng·L-1TNF-α/ng·L-1空白組—41.42±5.47188.01±65.19模型組—115.22±7.06#664.40±42.02#鹽酸氟西汀組20mg/kg54.49±7.48*290.62±85.68*甘麥大棗湯組10g/kg62.98±3.12*324.76±58.45*甘麥大棗湯總黃酮組10g/kg74.40±3.82*412.23±42.45*
3.3 小鼠外周血清5-HT、NE含量結果 結果如表4所示,與空白組相比,模型組小鼠腦組織中的5-HT、NE含量明顯降低。與模型組相比,各給藥組5-HT、NE含量不同程度升高。甘麥大棗湯組較其總黃酮組高,差異具有顯著性。
表4 各組對LPS致急性抑郁小鼠5-HT、NE的影響( ±s,n=8)
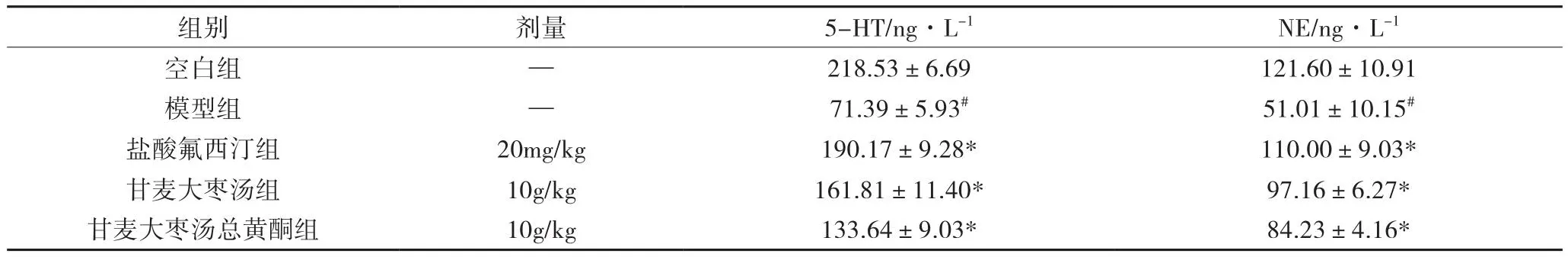
表4 各組對LPS致急性抑郁小鼠5-HT、NE的影響( ±s,n=8)
注:與空白組比較 # P<0.01,與模型組比較 * P<0.01
組別劑量5-HT/ng·L-1 NE/ng·L-1空白組—218.53±6.69121.60±10.91模型組—71.39±5.93#51.01±10.15#鹽酸氟西汀組20mg/kg190.17±9.28*110.00±9.03*甘麥大棗湯組10g/kg161.81±11.40*97.16±6.27*甘麥大棗湯總黃酮組10g/kg133.64±9.03*84.23±4.16*
討 論
本研究從甘麥大棗湯的水煎液中共鑒定出95個化學成分,包括黃酮類、萜類、有機酸等,經篩選獲得59個活性成分。在此基礎上,運用網絡藥理學分析預測了甘麥大棗湯抗抑郁作用的關鍵活性成分、核心靶點和作用機制。篩選出的芹菜素、N-去甲(基)荷葉堿、甘草黃酮C、甘草黃酮醇、甘草次酸等12個關鍵活性成分,其中8個為黃酮類成分。已有研究證實[32],多種黃酮類化合物具有抗抑郁作用,其作用機制可能與透過血腦屏障作用于中樞神經系統,影響單胺神經遞質、調節HPA軸相關。其中,芹菜素可調節大腦中的5-HT水平發揮抗抑郁作用。甘草黃酮能上調BDNF及其受體Trk B的蛋白表達發揮抗抑郁作用[33]。甘草次酸通過抑制炎性因子TNF-α、IL-6釋放產生抗抑郁作用[34]。因此,可認為黃酮類成分、甘草次酸可能是甘麥大棗湯抗抑郁作用的主要物質基礎。此外,獲得了TNF、SLC6A3、MAOB等16個核心靶點,其中TNF是一種促炎細胞因子,而抑郁癥的發生、發展與促炎細胞因子的中樞和外周濃度升高密切相關[35],機體應激后情緒、行為的改變也與炎性因子密切相關[36]。許一凡[37]等研究發現甘麥大棗湯能明顯改善LPS急性抑郁模型小鼠抑郁樣行為,顯著降低外周及中樞IL-1β、TNF-α含量,抑制IL-1β基因表達。因此,可表明預測的潛在靶點TNF是甘麥大棗湯主要成分抗抑郁的靶點。DA、5-HT、NE等單胺類神經遞質異常主流認為是抑郁發生的主要因素。SLC6A3是一種多巴胺轉運蛋白,在神經遞質調節方面起著重要作用,與多種精神類疾病發生相關[38]。MAOB(MAOA)是一種單胺氧化酶,與5-HT代謝密切相關[39]。因此,可從炎性因子、多巴胺、5-HT能神經系統調控等角度開展甘麥大棗湯抗抑郁的作用機制研究。
GO功能富集分析,甘麥大棗湯可通過神經遞質水平調節、跨突觸信號調節、認知、學習和記憶等BP;樹突、膜筏、軸突、突觸膜等CC;胺結合、神經遞質受體活性、蛋白酶結合、磷酸酶結合等MF抗抑郁。KEGG通路富集分析了37條信號通路,包括神經退行性病變-多種疾病通路、5-羥色胺能突觸、阿茲海默病等。其中5-羥色胺能突觸通過調控相關5-HT的水平及相應受體數量或功能改善抑郁癥狀[40],也可影響γ-氨基丁酸、多巴胺等其他神經遞質釋放,還可以調控HPA軸發揮抗抑郁作用[41]。神經退行性病變-多種疾病通路與阿爾茨海默、帕金森、腦萎縮等各種神經損害性疾病密切相關,表現為大腦或脊髓特定區域神經元死亡[42]。有研究[43]表明神經退行性疾病和抑郁癥狀有一定的關聯度,兩者之間擁有共同的發病機制或病理生理學變化,神經退行性疾病可能直接參與抑郁癥的發生發展。
LPS腹腔注射建立急性抑郁動物模型,已廣泛應用于研究藥物抗抑郁作用與抑制炎癥反應關系的模型載體[44-45]。本研究動物實驗結果顯示,經LPS應激后,與空白組比較,模型組小鼠強迫游泳和懸尾不動時間均顯著增加,表明LPS可誘導小鼠行為學異常,抑郁造模成功。與模型組相比,各給藥組均可改善LPS誘導的小鼠抑郁樣行為,表現出抗抑郁作用,同時甘麥大棗湯及其總黃酮組可降低小鼠血清中IL-1β、TNF-α含量,上調5-HT、NE含量。該結果與網絡藥理學研究所預測的靶點TNF、MAOB、通路5-HT能突觸及黃酮類成分相符,表明網絡藥理學結果具有一定的準確性。
綜上所述,本研究首次采用液質聯用技術結合網絡藥理學初步闡明了甘麥大棗湯中關鍵活性成分、潛在作用靶點及通路,并通過動物實驗進行驗證,表明甘麥大棗湯抗抑郁作用的發揮與下調IL-1β、TNF-α含量、上調5-HT、NE含量相關。為該方進一步的藥效物質基礎和作用機制研究提供了參考依據。

