靜脈輸注利多卡因對心臟外科手術患者術后并發癥和死亡率的影響*
吳德華,譚 鋼,吳鏡湘,徐美英,吳玉蘭,李瓊珍△
(1.上海交通大學醫學院附屬胸科醫院麻醉科 200032;2.上海市松江區中心醫院麻醉科 201600;3.南京軍區福州總醫院麻醉科 350025)
體外循環下心臟手術的患者可能發生多種術后并發癥[1-2],包括呼吸功能不全、心功能不全、腎功能不全、房顫、認知功能障礙。有研究[3-4]報道心外科術后腎功能不全發生率為5%~20%,術后神經損害也受廣泛關注。研究顯示術后認知功能障礙發生率在36%左右[5]。而房顫是心臟外科手術術后常見的并發癥之一,EIKELBOOM等[6]研究表明心臟外科手術術后房顫發生率達23.7%。患者一旦出現重要器官并發癥,死亡率明顯增加[1-2]。研究顯示心臟外科患者術后30 d內死亡率為2%,術后出現腎功能不全的患者死亡率進一步增加[3]。
利多卡因作為Na+通道阻滯劑具有潛在的抗炎性反應效應,其效果與皮質類固醇激素和NSAIDs藥物效果相當[7],通過干預細胞的吞噬、遷移、胞吐和細胞代謝影響炎性進展,抑制炎性因子釋放[8],調節圍術期交感-迷走的失衡[9],具有良好的心肌保護作用[8]。另外,利多卡因對術后胃腸功能的恢復,術后疼痛的改善,以及減輕圍術期炎性反應和免疫抑制,促進術后快速恢復等均具有積極作用[10]。盡管利多卡因具有諸多優勢,但其是否能夠有效改善體外循環下心臟手術患者術后并發癥的發生和術后死亡的結局仍有待明確。
1 資料與方法
1.1 一般資料
擇期行體外循環下心臟手術的患者1 408例,ASA分級Ⅰ~Ⅳ級,年齡18~80歲,體重35~104 kg,排除術前有心律失常病史、術前中度及以上肝、腎功能損害、術前有重度心功能不全、術前有癡呆或譫妄、對利多卡因過敏或使用禁忌、術中深低溫停循環、CPB≤30 min、大量失血的患者。
1.2 分組方法
采用隨機數字表法分為利多卡因組(L 組,n=704)和對照組(C組,n=704)。L組采用三階段靜脈注射利多卡因:負荷量、3 h和21 h維持量。麻醉誘導后開始輸注1.5 mg/kg利多卡因作為負荷量,最大劑量控制在按照理想體重計算利多卡因劑量的150%,持續輸注5 min;之后采用2.3 mg·kg-1·h-1利多卡因維持3 h,最大劑量控制在按照理想體重計算利多卡因劑量的120%;繼續采用0.8 mg·kg-1·h-1利多卡因維持21 h,最大劑量控制在按照理想體重計算利多卡因劑量的120%。理想體重的計算應用Broca改良式:男性標準體重(kg)=身高-105(cm);女性標準體重(kg)=身高-105-2.5(cm)。C組患者靜脈輸注生理鹽水,輸注量、輸注速度和輸注時間段均同L組。兩組患者進入手術室后,按照上海交通大學醫學院附屬胸科醫院心臟手術圍術期管理常規進行,參考文獻[11]。本研究已獲得上海交通大學醫學院附屬胸科醫院醫學倫理委員會批準(KS1459),患者或家屬簽署知情同意書。記錄兩組患者年齡,體重,性別,身高,ASA分級,內科合并癥,手術類型,CPB時間,主動脈阻斷時間,外科手術時間,麻醉用藥劑量,失血量,尿量,ICU停留時間,手術后住院時間,住院總費用,術后主要并發癥(包括房顫、呼吸功能不全、循環功能不全、急性腎功能不全、神經功能損害)和術后30 d全因死亡情況,患者出院后采用電話隨訪。
1.3 血漿利多卡因監測
兩組前30例患者在手術結束時和利多卡因輸注結束時2個時間點采集頸內靜脈血液檢測利多卡因水平。如果患者術后出現利多卡因中毒癥狀,如耳鳴、口周麻木、口中有金屬味或視覺模糊等,停輸利多卡因,并檢測患者血漿利多卡因水平。
1.4 統計學處理
2 結 果
2.1 兩組患者基本情況
L組2例患者被剔除,其中1例術中采用了深低溫停循環選擇性腦灌注技術,另1例術中出血量超過1 500 mL;C組4例患者因術中出血量超過1 500 mL被剔除。最終L組702例、C組700例患者納入統計分析。兩組患者術前一般情況、手術類型、左心房大小、心功能、術前合并癥、ASA分級差異無統計學意義(P>0.05),見表1。
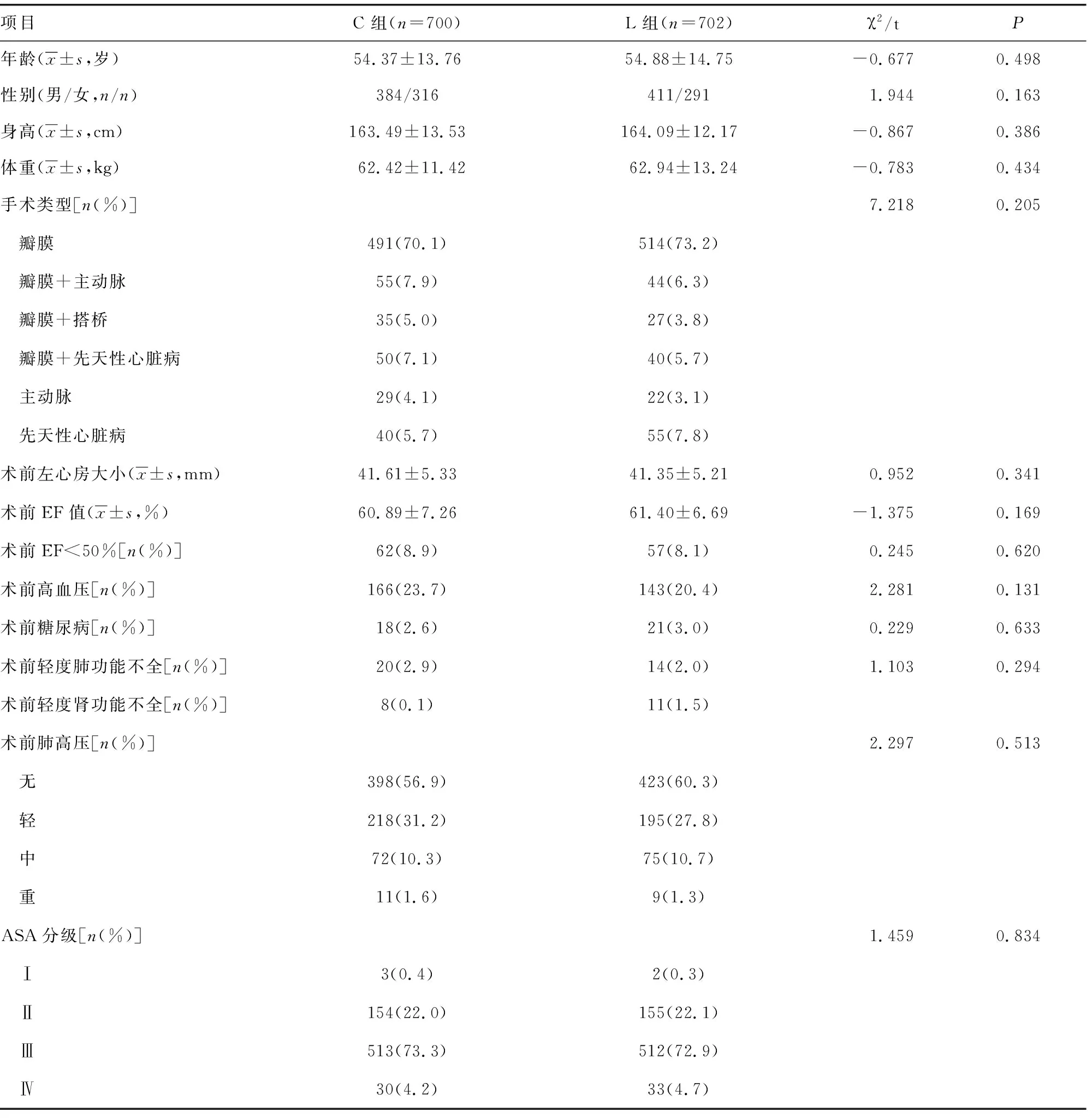
表1 兩組患者術前一般情況、手術類型等比較
2.2 兩組患者術中情況
L組患者術中異丙酚和舒芬太尼的用量小于C組[(527.45±252.15) mgvs.(619.69±259.28)mg,P<0.001;(150.54±27.68)μgvs.(171.95±29.95)μg,P<0.001],兩組患者手術時間、體外循環時間、維庫溴銨用量、出入量的差異無統計學意義(P>0.05),見表2。
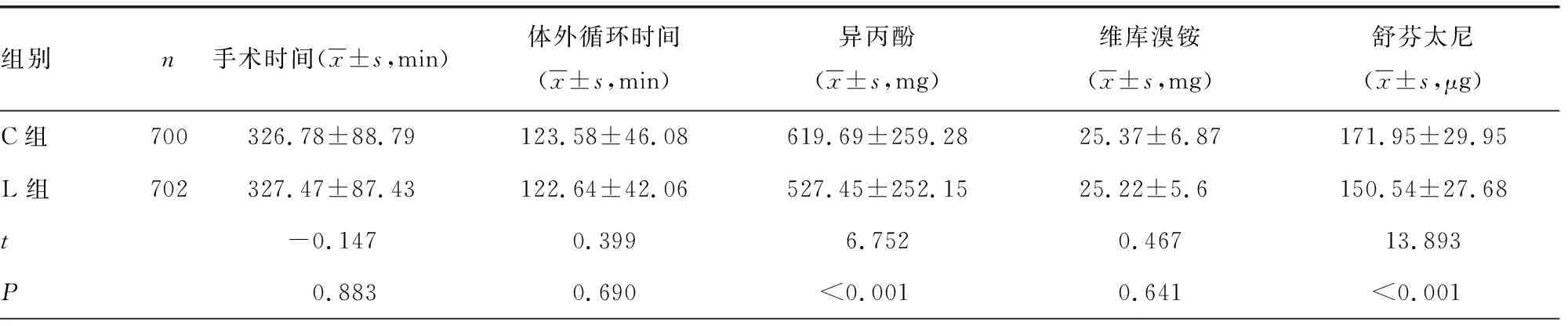
表2 兩組患者手術時間、麻醉用藥和出入量比較
2.3 L組患者利多卡因血藥濃度和中毒情況
L組患者手術結束時和利多卡因輸注結束時血漿利多卡因水平分別為(3.3±0.4) μg/mL和(2.2±0.5) μg/mL。所有患者術后未出現利多卡因中毒表現。
2.4 兩組患者術后主要并發癥
與C組比較,L組患者術后房顫發生率降低(10.0%vs.24.7%,P<0.001)。兩組患者術后主要并發癥(包括呼吸功能不全、循環功能不全、急性腎損害和神經功能損害)發生率之間無差異,見表3。
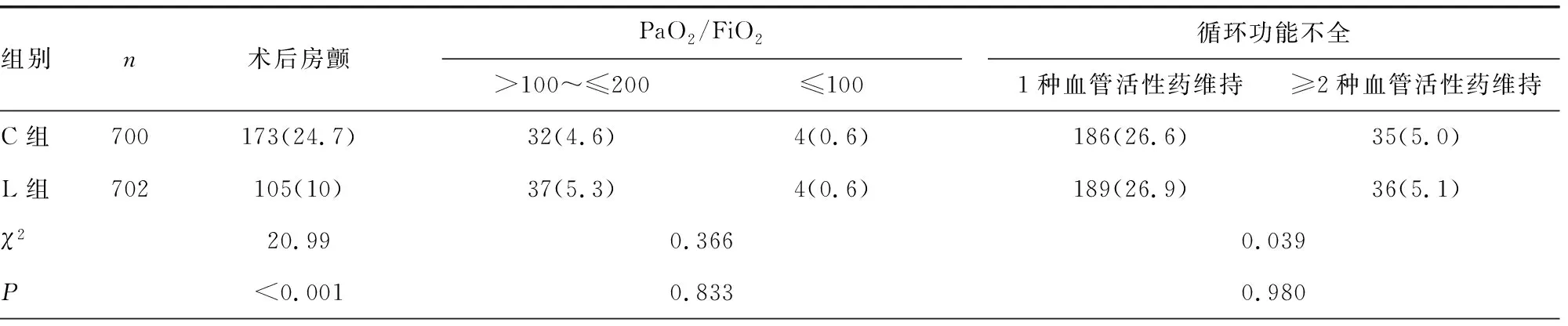
表3 兩組患者術后并發癥和死亡情況比較[n(%)]
2.5 兩組患者術后住院時間和總費用
與C組比較,L組患者術后ICU停留時間縮短[(1.75±0.87)dvs.(1.99±1.32)d,P<0.001],住院時間縮短[(10.15±2.69)dvs.(10.99±4.09)d,P<0.001],總費用降低[(11.43±3.45)萬元vs.(11.79±3.33)萬元,P=0.045],見表4。
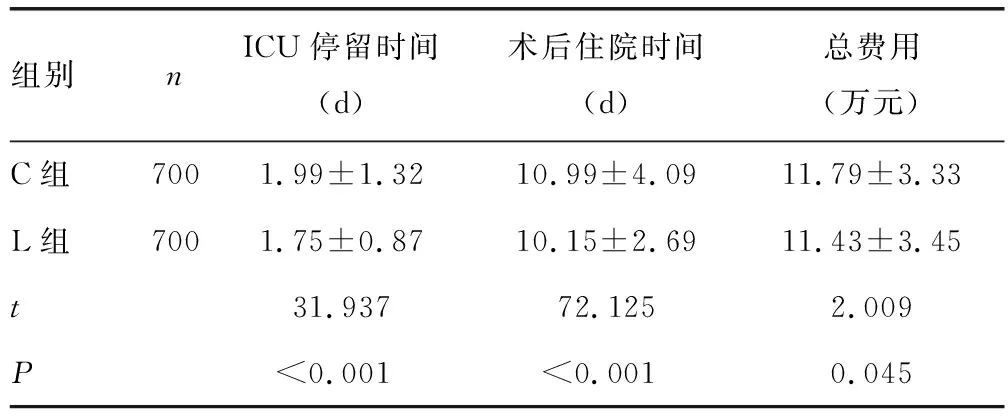
表4 兩組患者術后ICU停留時間、術后住院時間、費用比較
2.6 兩組患者術后30 d全因死亡率
C組患者術后30 d內15例(2.1%)死亡,其中院內死亡11例,出院后死亡4例;L組患者11例(1.6%)死亡,其中院內死亡9例,出院后死亡2例,組間比較差異無統計學意義(P=0.424),見表3。院內死亡原因:C組死亡原因包括多器官衰竭3例,右心衰合并多器官衰竭3例,感染性休克合并多器官衰竭2例,低心排2例,腹腔干栓塞合并多器官衰竭1例;L組死亡原因包括多器官衰竭3例,腦死亡1例,術后主動脈破裂1例,室顫1例,低心排2例,感染性休克1例。出院后死亡原因:C組心力衰竭合并腎衰竭1例,其余5例死亡原因不詳。
3 討 論
本研究表明靜脈輸注利多卡因患者術后房顫發生率降低(10.0%vs.24.7%)。利多卡因不但有Na+通道阻滯作用,還有促進心肌細胞內K+外流的作用,可降低心肌的自律性,具有良好的穩定心律的作用[12]。還能有效降低血漿促炎因子的產生[13]。此外利多卡因還能通過聯合阿片類鎮痛藥增強抗傷害性刺激、減少圍術期心肌損傷,從而減少術后房顫的發生。
術前肺功能不全是心臟手術患者圍術期并發癥和死亡率增加的獨立危險因素。術前肺功能正常的患者術后肺部并發癥發生率2%~11%,術后1年內的全因死亡率為3%[2]。本研究選擇的患者術前肺功能正常或少數患者輕度肺功能不全(占2%~3%),結果顯示兩組患者術后中-重度肺功能不全(PaO2/FiO2≤200)發生率為5%~6%,與文獻[2]報道的發生率相似。WANG等[14]研究顯示,靜脈輸注利多卡因對術后PaO2/FiO2、呼吸動力學參數(驅動壓、呼吸指數、動態順應性)及術后血流動力學并沒有影響,與本研究結果類似。盡管利多卡因具有抗全身炎性反應和抗傷害性應激作用,但可能仍不足以對抗體外循環下心臟手術帶來的肺損傷作用。
圍術期心功能不全也是術后并發癥發生和患者死亡的一個重要因素。ZANGGRILLO等[15]研究納入了6 478例心臟手術患者,其中506例(7.8%)患者出現嚴重的圍術期心功能不全,術后30 d內死亡患者占心功能不全患者的13%,占總體患者的1%。本研究結果顯示不管是采用1種血管活性藥物還是≥2種血管活性藥物支持術后循環功能,心功能不全的發生率差異無統計學意義。說明靜脈輸注利多卡因對心臟手術術后循環功能無明顯影響。
本研究兩組患者急性腎損害發生率約為10%,低于文獻報道的30%[16]。心臟手術后急性腎功能不全的發生原因包括:體外循環的使用、圍術期低心排、心臟停搏復跳導致的缺血再灌注損傷、過氧化應激及全身炎性反應等。本研究顯示,靜脈輸注利多卡因對術后急性腎損害無明顯影響,考慮與本研究選擇的樣本均為術前沒有明顯合并癥的患者有關。
利多卡因對心臟手術患者術后神經認知損害的影響報道不一。研究顯示,靜脈輸注利多卡因可降低心臟術后10 d以內的POD,但對10周及1年內的POD無影響,認為利多卡因可通過降低線粒體的損害提供神經保護效應、改善術后的認知功能[17]。MATHEW等[18]研究顯示,靜脈輸注利多卡因不能降低總體心臟手術后的認知障礙,但對于術前有糖尿病的患者,利多卡因對術后認知障礙有一定的保護作用。本研究結果顯示,利多卡因同樣對心臟手術患者術后神經認知功能無影響,與上述結果相似。
心臟手術患者術后死亡率報道不一。有研究顯示出院后30 d內全因死亡率為0.2%~0.8%,術后1年的死亡率達2.1%~9.3%[19]。另有研究顯示,術后30 d死亡率為3%~5%[20]。體外循環誘導的全身炎性反應容易導致術后主要器官功能障礙,術后24 h達到高峰,是心臟手術后死亡率較高的主要原因之一。一篇Meta分析[21]顯示,靜脈輸注利多卡因并不影響心臟手術患者術后的死亡。雖然利多卡因靜脈輸注可降低心臟手術術后疼痛評分,減少芬太尼的使用劑量,甚至輕微改善術后FEV1,但利多卡因輸注并不影響術后總體死亡率[21]。本研究顯示,對照組患者術后30 d內全因死亡率2.1%,利多卡因組為1.6%,組間差異無統計學意義,表明利多卡因并不能有效降低心臟手術后30 d的全因死亡率。
總之,圍術期輸注利多卡因可減少術后房顫的發生,縮短ICU停留時間和術后住院時間,降低住院總費用;但對術后主要并發癥發生率和全因死亡率無影響。

