柴胡疏肝散異病同治2型糖尿病、非酒精性脂肪肝和抑郁癥的作用機制
常 碩,劉懷珍,陶慶雪,郭錦晨
1.安徽中醫藥大學第一臨床醫學院(合肥230031);2.安徽中醫藥大學第一附屬醫院老年病中心-內分泌科(合肥230031);3.安徽中醫藥大學新安醫學教育部重點實驗室(合肥 230038)
2型糖尿病(type 2 diabetes mellitus,T2DM)是臨床最常見、最重要的代謝性疾病之一,其發病主要與胰島素缺陷和(或)胰島素抵抗有關。抑郁癥(depressive Disorders,DD)和非酒精性脂肪肝(non-alcoholic fatty liver disease,NAFLD)是T2DM 患者常見的并發癥。現代研究認為,T2DM、NAFLD 與DD 之間存在某些相互作用,增加了三種疾病發病機制的復雜性,也為臨床治療三種疾病帶來了諸多挑戰[1]。臨床上,T2DM人群患NAFLD 和DD 的概率遠大于普通人群[2-3],這不僅加重了T2DM 患者的致殘率、死亡率,更為T2DM 患者的治療帶來了巨大挑戰。而傳統中醫的“異病同治”理念對疾病共病的治療優勢尤為突出,是中醫辨證論治的生動體現,它將辨病與辨證有效地連接在一起,促進了中西醫結合的發展[4]。
柴胡疏肝散一方出自《醫學統旨》,由芍藥、川芎、香附、柴胡、甘草、陳皮、枳殼7 味中藥組成,全方謹遵《內經》“木郁達之”之旨,具有疏肝解郁,行氣止痛之效。秦伯末《謙齋醫學講稿》中指出:“本方即四逆散加川芎、香附和血理氣……專以疏肝為目的。”現代藥理學研究顯示柴胡疏肝散具有抗炎、調節脂質代謝、保肝、抗纖維化、干預神經傳遞等作用[5]。并且已有臨床研究證實此方治療T2DM[6]、NAFLD[7]、DD[8]療效確切。本文采用網絡藥理和分子對接技術探討柴胡疏肝散異病同治T2DM、NAFLD 及DD 的作用機制,為柴胡疏肝散治療三病共病提供科學依據,以供臨床參考。
1 方法
1.1 柴胡疏肝散藥物活性成分的篩選
將柴胡疏肝散全方中的芍藥、川芎、香附、柴胡、甘草、陳皮、枳殼分別輸入中藥系統藥理學數據庫平臺(TCMSP)中,以口服生物利用度(OB)≥30%、類藥性(DL)≥0.18 為條件進行篩選,把結果錄入EXCEL 表格中。
1.2 柴胡疏肝散潛在作用靶點篩選及基因名標準化
把1.1 中篩選得到的化合物ID(Mol ID)輸入TCMSP數據庫,收集每個活性成分的潛在靶點信息,并錄入EXCEL中保存。進入UniProt(http://www.uniprot.org)數據庫,收集所有已經驗證過的人類基因,錄入EXCEL,以此基因名作為標準將上一步在TCMSP 數據庫中收集到的潛在靶點做標準化命名并保存。
1.3 疾病靶點的篩選
為保證數據的準確與統一,疾病的靶點均在Gene Cards(http://www.genecards.org)數據庫中篩選,分別以Type 2 diabetes、Nonalcoholic fatty liver disorder、depressive disorder為檢索詞,獲取疾病的相關靶點。將1.2中標準化后的靶點與疾病靶點分別導入Venny2.1在線平臺取交集,得到藥物-疾病的共同作用靶點。
1.4 藥物-成分-靶點-疾病網絡圖構建
將柴胡疏肝散中單味藥及活性成分,藥物-疾病共同靶點導入到Cytoscape 3.7.0軟件中,構建成分-靶點-基因-疾病網絡圖。
1.5 蛋白質互作網絡的構建
將1.4 中得到的共同靶點輸入到STRING 數據庫,以“Homo sapiens”為條件,構建蛋白質互作(PPI)網絡圖。并將此數據庫的分析數據以“tsv”格式保存,導入Cytoscape3.7.0 軟件中,以度值(Degree)、介數中心性(Betweenness Centrality)為條件篩選出柴胡疏肝散異病同治T2DM、NAFLD 和DD 的核心靶點,并在Cytoscape3.7.0軟件中構建核心靶點網絡圖。
1.6 基因功能和通路富集分析
將1.5 中得到的核心靶點導入DAVID(https://david.ncifcrf.gov/)在線數據庫平臺,以“OFFICE_GENE_SYMBOL”與“Homo sapiens”為條件,對靶點分別進行生物過程(Biological process,BP)、細胞組分(Cellular component,CC)、分子功能(Molecular function,MF)分析及Kyoto encyclopedia of genes and gnomes(KEGG)富集通路分析。
1.7 分子對接驗證
在PubChem 數據庫找出活性成分的2D 結構,在RCS PDB 數據庫找出靶蛋白的3D 結構,通過Pymol 2.4.0軟件及AutodockTools 1.5.7軟件對兩者預處理后,在Autodockvina 1.1.2軟件中進行對接驗證。
2 結果
2.1 藥物活性成分的篩選
在TCMSP 數據庫中篩選出柴胡疏肝散中各藥物有效活性成分數目分別為:陳皮5個、柴胡13個、川芎6個、香附16 個、枳殼5 個、芍藥8 個、甘草88 個,刪除重復值后,共有123個符合條件的化合物,并將不同藥物中相同的活性成分進行統計,見表1。

表1 柴胡疏肝散藥物中的共有活性成分Table 1 Common active ingredients in Chaihu Shugan Powder
2.2 藥物靶點篩選及基因名標準化
在TCMSP 數據庫共篩選出柴胡疏肝散2 995 個潛在作用靶點,其中陳皮95 個、柴胡348 個、川芎42 個、香附496個、枳殼123個、芍藥123個、甘草1 768個,將得到的潛在靶點進行標準化處理,刪除重復后剩余251個有效靶點。
2.3 藥物與疾病交集靶點篩選
對1.3 中獲得的3 種疾病的基因靶點進行多次“Relevance score”參數截取,篩選出T2DM相關靶點1 622個、NAFLD相關靶點1 513個,DD相關靶點1 600個,將上述靶點與2.2篩選到的藥物靶點取交集,得到交集靶點共70個,見圖1。
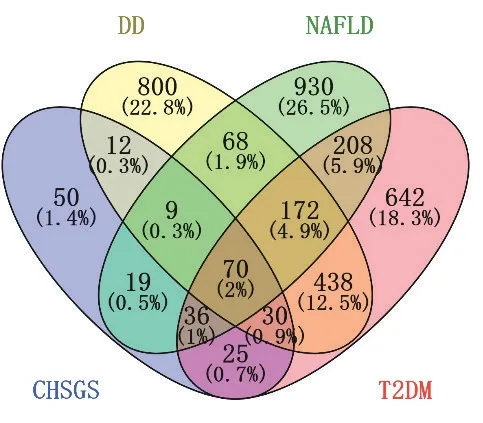
圖1 交集靶點VEEN圖Figure 1 Venn diagram of intersecting targets
2.4 藥物-成分-疾病-靶點網絡圖構建
利用Cytoscape3.7.0 軟件構建“藥物-成分-疾病-靶點”網絡關系圖,見圖2。其中粉色菱形代表藥物名稱(CX為川芎,CP為陳皮,CH為柴胡,BS為白芍,ZK為枳殼,XF為香附,GC為甘草),黃色圓形和紫色圓形代表藥物成分(XF1-XF10 分別代表香附的10 種不同活性成分),紫紅色六邊形代表藥物之間的相同成分(各字母含義見表1),橙色正方形代表藥物與疾病之間的共同靶點,綠色箭頭形狀代表3種疾病。

圖2 藥物-成分-疾病-靶點網絡圖Figure 2 Network diagram of Drug-Ingredient-Disease-Target
2.5 PPI網絡圖及核心靶點網絡圖構建
根據1.5 步驟篩選得到柴胡疏肝散異病同治T2DM、NAFLD和DD的19個核心靶點。為提高所篩選到的核心靶點的準確性,按照1.4 與1.6 步驟找出柴胡疏肝散分別治療T2DM、NAFLD、DD 的核心靶點各有39 個、31 個、26 個,將此3 組核心靶點取交集后與上述19 個核心靶點再次取交集,最終得到18 個核心靶點。此18 個核心靶點均在上述19 個靶點中,故以70 個靶點篩選出的核心靶點為依據,構建交集核心靶點網絡圖,及其可視化分析,見表2、表3 與圖3。其中IL6、TNF、AKT1、IL1B、VEGFA 的度值較大,且在2.6 KEGG富集通路中出現的頻次分別為11、12、19、8、7次,提示此5個靶點可能為柴胡疏肝散異病同治T2DM、NAFLD和DD的關鍵靶點。
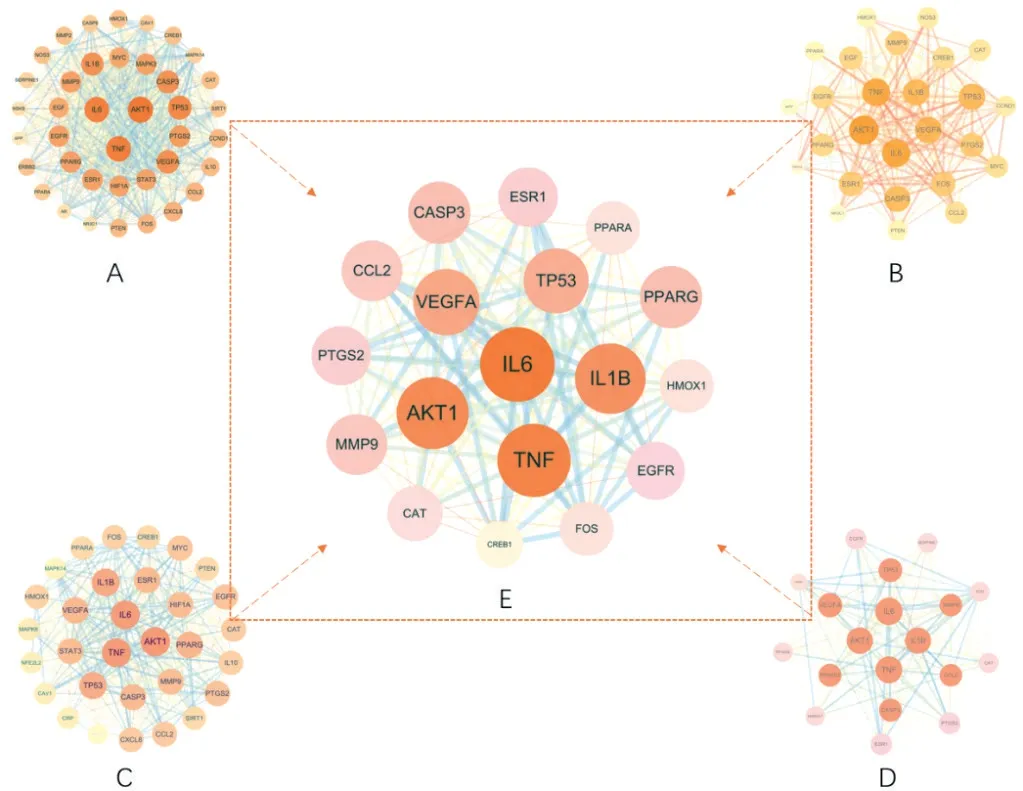
圖3 關鍵靶點的PPI網絡圖Figure 3 PPI network diagram of key targets

表2 核心靶點的篩選Table 2 Screening of core targets
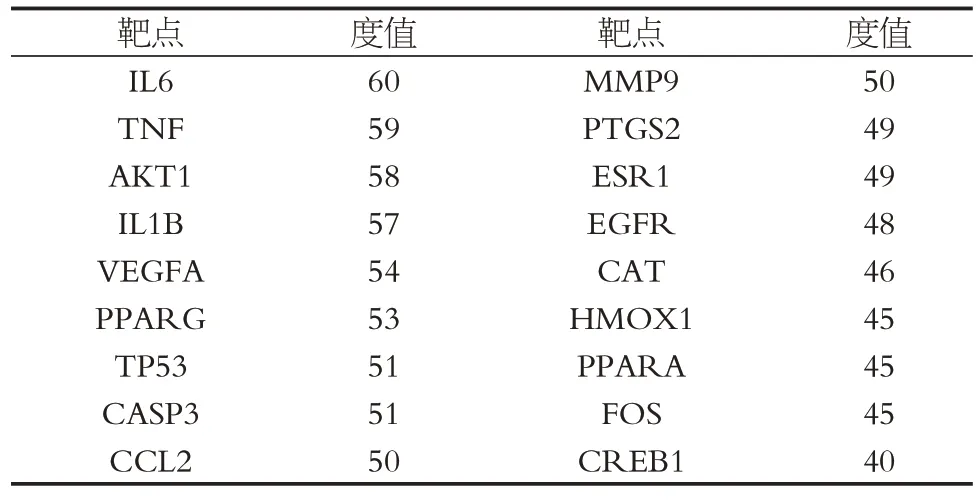
表3 關鍵靶點信息Table 3 Information of key targets
2.6 基因功能分析和KEGG分析
將得到的70 個交集靶點導入至DAVID 在線數據庫平臺,進行基因功能GO 分析和KEGG 分析,分別得到BP、CC、MF 條目597、55、78 個,以及151 條KEGG 信號通路。以P≤0.01為篩選條件,按P值大小分別選取GO 分析中的前10 條繪制成氣泡圖,見圖4。選取KEGG 分析中的前20 條信號通路(刪除與本研究無關的信號通路,如Pathways in cancer,Human cytomegalovirus infection,Amoebiasis 等)做KEGG 基因富集分析圖,見圖5。
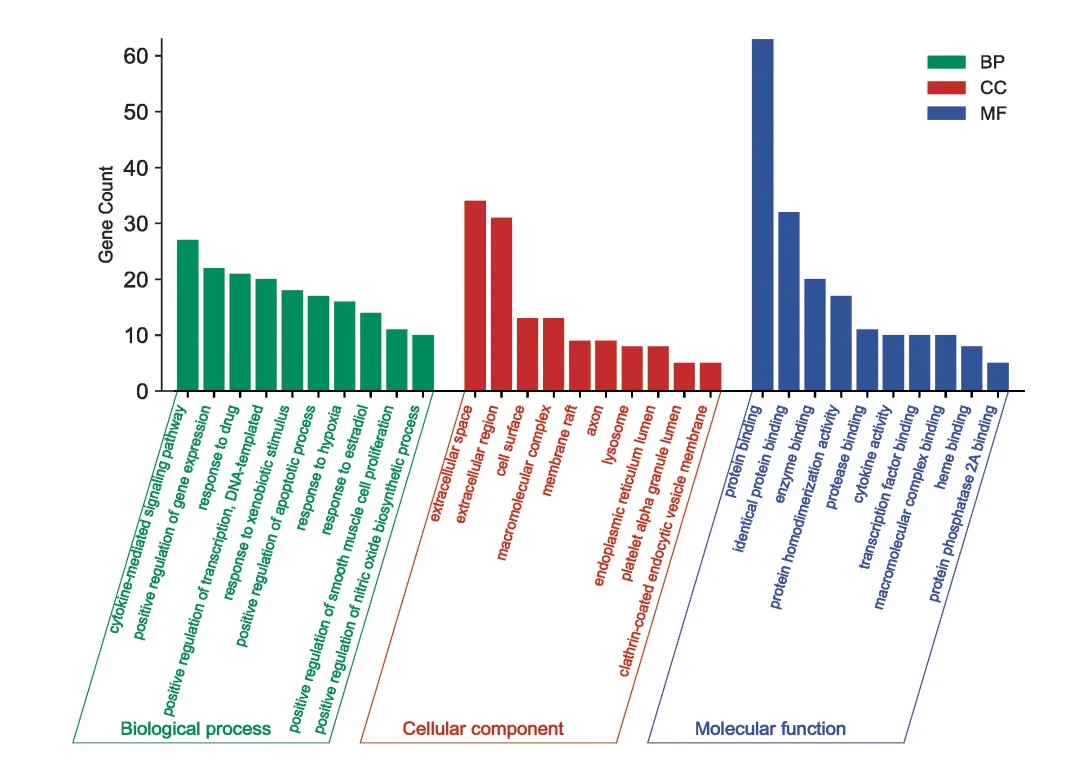
圖4 GO富集分析Figure 4 GO enrichment analysis
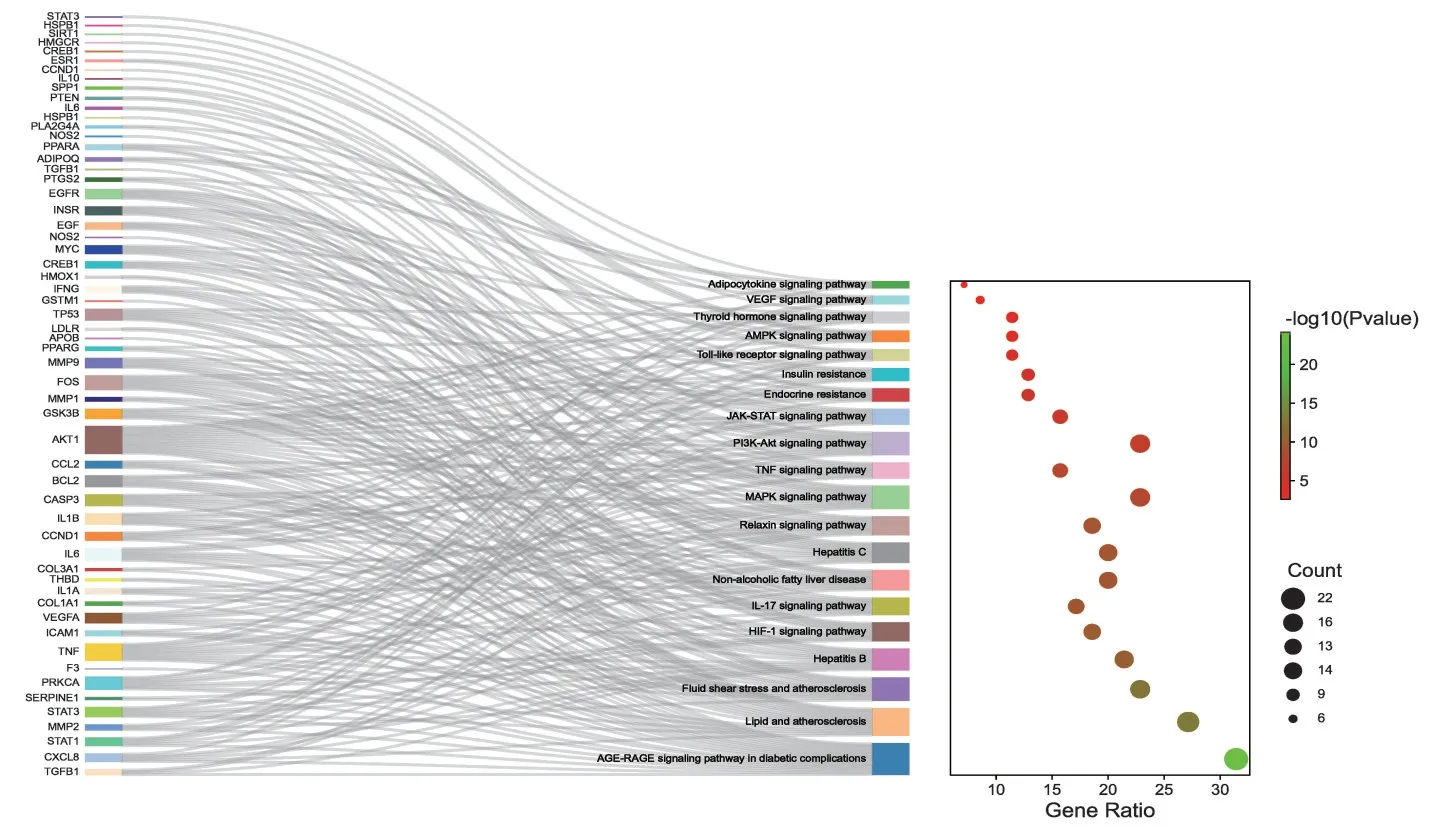
圖5 交集靶點KEGG富集分析Figure 5 KEGG enrichment analysis of intersecting targets
2.7 分子對接驗證
現代藥理學研究表明[9-10],柴胡中的主要成分柴胡皂苷a 和柴胡皂苷d 在抗炎、抗抑郁、免疫調節具有顯著作用。柴胡是柴胡疏肝散中的君藥,故將上述兩個主要成分以及表2 中Degree 值靠前的6 個藥物成分與核心靶點(TNF、IL6、VEGFA、PPARG、IL1B、AKTI)進行虛擬分子對接,結果顯示結合能均≤-6.0 kcal/mol,表明以上活性成分與預期篩選的靶點能夠穩定結合,現將所有對接結合能結果制作成熱圖展示并選取其中結合能較好的對接體進行可視化展示,見圖6、圖7。
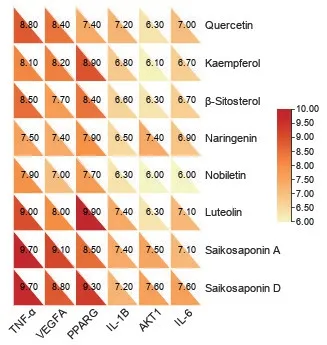
圖6 分子對接熱圖Figure 6 Heat map of molecular docking
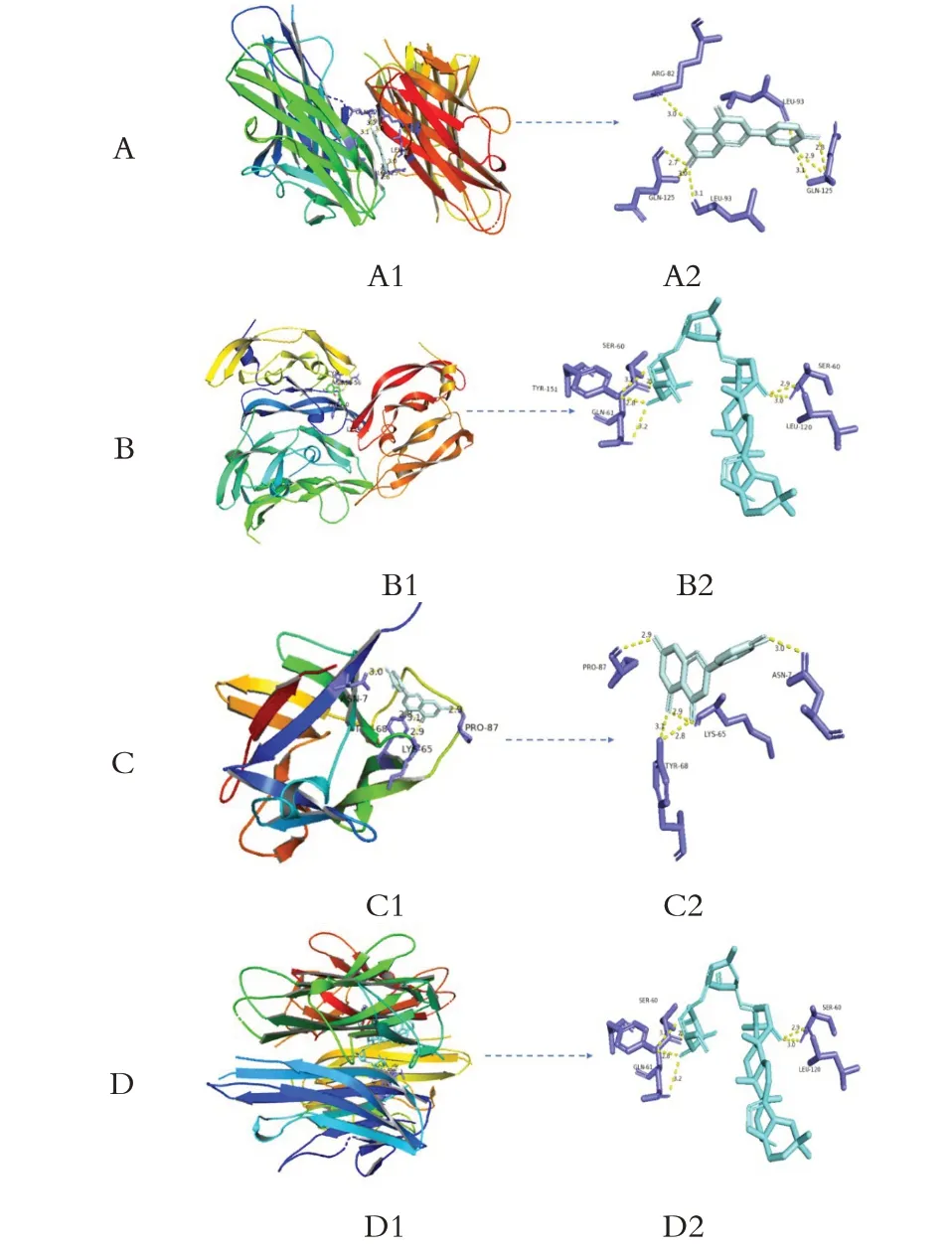
圖7 分子對接結果Figure 7 Results of molecular docking
3 討論
胰島素抵抗與慢性炎癥反應貫穿著T2DM 與NAFLD 的發生發展過程,其中胰島素抵抗的發生可進一步加重炎癥反應與脂代謝紊亂,這兩種病理過程又分別是DD 和NAFLD 發病的關鍵機制,由此可見,T2DM、NAFLD 與DD 之間存在復雜的病理反應,使三病互為因果。傳統中醫認為T2DM 屬于“消渴”范疇;NAFLD歸屬于“肝癖”病[11];抑郁癥則屬于“郁證”范疇。此三病雖歸屬于不同系統疾病,但綜合分析三病核心病機總不離“肝郁氣滯”[12-14]。《丹溪心法》指出:“氣血沖和,萬病不生。一有怫郁,諸病生焉”,故臨床常以柴胡疏肝散異病同治。全方融疏肝、養肝、健脾于一體,“辛疏酸斂合法,肝脾氣血兼顧”,切合消渴、肝癖與郁證的核心病機。
經篩選,發現柴胡疏肝散異病同治T2DM、NAFLD和DD 的主要有效化學成分為槲皮素、山奈酚、β-谷甾醇、柚皮素等。槲皮素和山奈酚都屬于黃酮類化合物,兩者均可改善胰島素抵抗和減輕炎癥反應。現代藥理學研究認為黃酮類化合物具有抗炎、保護神經、維持血糖平衡等藥理作用[15]。有實驗驗證[16],槲皮素可以通過改善胰島素抵抗而對NAFLD有顯著療效,既證明了槲皮素對2 型糖尿病的作用,又闡釋了槲皮素治療NAFLD 的機制。β-谷甾醇對脂代謝有積極作用[17],目前常應用于非酒精性脂肪肝的治療和預防。柚皮素屬于二氫黃酮類化合物,具有抗炎、降血脂、抗菌、抗氧化、抗癌抗腫瘤等廣泛藥理作用,在治療炎癥和胰島素抵抗引發的各種疾病中具有積極意義,如T2DM、NAFLD等[18-19]。
由表3 可知IL6、TNF、IL1B、VEFGA、PPARG 等靶點在藥物治療疾病中可能起著關鍵作用。TNF-α 與IL6 已被證實為炎癥反應的標志物[20],其中IL6 是一種促炎癥細胞因子,其濃度常在炎癥反應過程中增加,TNF-α則可以刺激免疫細胞合成IL6、IL1B等炎性細胞因子。IL1β是趨化因子家族中IL1存在的分子形式之一,其過度表達可誘導下游細胞因子的表達,如IL4、IL6、VEGF 等[21],他們可直接加重炎癥反應,影響神經發生和干擾神經可塑性的調節,而抑郁癥的發生則與此有關[22]。另外有實驗數據表明[23],IL1β 亦是治療T2DM的關鍵靶點,在T2DM患者中使用IL1β受體拮抗劑可顯著降低血糖濃度,改善胰島B 細胞功能。過氧化物酶體增殖物激活受體(PPARG)是一種轉錄因子[24],可參與脂肪代謝、炎癥反應、胰島素抵抗等過程。VEGFA 可正向調節海馬神經的發生與增殖,提高抑郁患者的認知功能,減少抑郁患者的不良情緒[25]。
GO、KEGG分析結果發現,柴胡疏肝散異病同治過程主要涉及糖尿病并發癥中的AGE-RAGE 信號通路、HIF-1 信號通路、MAPK 信號通路、Toll 樣受體信號通路等。糖基化終末產物(AGEs)是在高血糖狀態在經過非酶糖基化反應產生的一種病理產物,是加重糖尿病及其并發癥的關鍵因素,并且其形成過程是不可逆的。AGEs與相應受體(RAGE)相互結合所形成的通路介導了炎癥反應、氧化應激反應等過程,加重了胰島素抵抗和脂代謝紊亂[26-27]。有實驗證實[28],葡萄糖依賴性促胰島素多肽(GIP)的信號表達可能與缺氧誘導因子-1α(HIF-α)基因表達及其依賴的信號通路有關,其最終結果加重了脂肪組織中的炎癥與胰島素抵抗,當HIF-α基因沉默時,GIP及其誘導的炎癥因子表達隨之減少。絲裂原活化蛋白激酶(MAPK)信號通路是介導細胞內外信號傳導的重要通路之一,眾所周知,MAPK信號通路參與了抑郁癥的發病機制[29]。在慢性不可預知輕度應激(CUMS)誘導的抑郁小鼠模型中,MAPK信號通路的活化與小鼠抑郁癥狀及小鼠體內炎癥因子的過度表達相關[30],且有報告指出,對p38MAPK 信號通路的阻斷不僅可以降低IL6、TNF-α等炎癥因子的表達,亦可有效發揮抗非酒精性脂肪性肝炎(NASH)作用[31]。Toll 樣受體(TLRs)信號通路已經被證實與胰島素抵抗及神經炎癥有密切聯系,Luteolin干預慢性炎癥及改善胰島素功能即是主要通過參與此信號通路完成的[32-33]。
分子對接結果表明,通過網絡藥理學篩選出的柴胡疏肝散的有效活性成分以及柴胡的主要成分與有效靶點之間具有良好的結合能,證明了柴胡疏肝散所含的活性成分與靶點可以有效作用于T2DM、NAFLD 和DD。
4 結論
本文通過網絡藥理學數據和分子對接技術闡釋了柴胡疏肝散通過多靶點、多通路異病同治T2DM、NAFLD 和DD 的作用機制,為中醫異病同治理念提供了科學支撐,為T2DM 及其并發癥的治療提供了治療方案。

