基于正交試驗結合基準關聯度和AHP-熵權法優化經典名方黃連湯提取工藝
王曉麗,沈哲苑,李麗萍,梅 茜,何天雨,趙曉莉,毛 靖,侯金才,郭 勇,毛春芹,崔恩忠, 3*,陸兔林*
·藥劑與工藝·
基于正交試驗結合基準關聯度和AHP-熵權法優化經典名方黃連湯提取工藝
王曉麗1,沈哲苑1,李麗萍1,梅 茜1,何天雨1,趙曉莉1,毛 靖1,侯金才2,郭 勇2,毛春芹1,崔恩忠1, 3*,陸兔林1*
1. 南京中醫藥大學藥學院,江蘇 南京 210023 2. 神威藥業集團有限公司,河北 石家莊 051430 3. 東部戰區總醫院 藥劑科,江蘇 南京 210002
應用正交試驗設計,結合基準關聯度和層次分析法-熵權法優化經典名方黃連湯的提取工藝。以黃連堿、巴馬汀、小檗堿、6-姜辣素、甘草苷、甘草酸、指紋圖譜相似度及干膏率為關鍵質量屬性,以加水量、浸泡時間、提取時間為關鍵工藝參數,采用單因素確定各因素水平,正交試驗設計優化工藝參數。計算不同提取參數的各評價指標下各樣品與基準樣品的基準關聯度,采用AHP-熵權法確定各評價指標的綜合權重系數,進行綜合評分。正交試驗設計聯用基準關聯度和AHP-熵權法建立的工藝評價函數模型為綜合評分=相對偏差(relative deviation,SR),黃連堿×30%+SR,巴馬汀× 24%+SR,小檗堿×28%+SR,6-姜辣素×5%+SR,甘草苷×5%+SR,甘草酸×6%+SR,干膏率×2%,該模型穩定可靠,確定提取工藝為全方飲片加6倍量水,浸泡60 min,煎煮45 min。驗證實驗綜合評分均值為90.11,RSD為1.09%,符合基準樣品的要求,且方法具有適用性。篩選的黃連湯現代提取工藝參數具有可行性,可為其他經典名方的開發利用提供理論依據。
經典名方;黃連湯;提取工藝;基準關聯度;層次分析法;正交設計;信息熵權法;質量源于設計;關鍵質量屬性;關鍵工藝參數;黃連堿;巴馬汀;小檗堿;6-姜辣素;甘草苷;甘草酸;指紋圖譜
經典名方黃連湯(Huanglian Decoction)出自《傷寒論》(東漢·張仲景),被收載于《古代經典名方目錄(第一批)》[1]。全方由黃連、甘草(炙)、干姜、桂枝(去皮)、人參、半夏(洗)、大棗(擘)7味藥組成,主治傷寒胸中有熱,胃中有邪氣,腹中痛,欲嘔吐者[2]。現代黃連湯及其加減方常用于治療胃腸疾病、婦科疾病及其他疾病,效果顯著[3-4]。經典名方制劑研發是近年來中藥新藥研發熱點。根據國家藥品監督管理局發布《古代經典名方關鍵信息表(25首方劑)(征求意見稿)》[5]、《按古代經典名方目錄管理的中藥復方制劑藥學研究技術指導原則(試行)》[6](簡稱《原則》),制劑研究應以制劑質量與基準樣品質量基本一致為目標。但在現代大生產中,中試產品的質量易受提取方式、提取容器等眾多因素的影響,難以實現現代提取工藝與傳統制法的質量一致性。質量標志物(quality marker,Q-Marker)最早于2016年由劉昌孝院士[7]提出,通過風險評估、試驗設計等手段確定生產工藝的關鍵質量屬性、關鍵物料屬性與關鍵工藝參數間的關系模型,提高工藝穩健性和產品質量可控性[8-9]。基準關聯度(standard relation,SR)可評價現代提取工藝下各樣品與基準樣品間質量的一致性,進而確定與傳統工藝最接近的現代工藝。層次分析法(analytic hierarchy process,AHP)-熵權法可確定各個測定指標的權重系數,將主觀賦權法和客觀賦權法結合,實現主客觀內在統一[10],使篩選出的現代提取工藝參數更加科學可信。本研究基于質量源于設計(quality by design,QbD)理念,計算不同提取參數的各種評價指標下各樣品與基準樣品的基準關聯度,結合AHP-熵權法對方中君臣佐使分別主觀賦權,確定各評價指標的權重系數,以保證在所篩選的提取工藝參數下制備的樣品與基準樣品保持質量一致,確保提取工藝穩定可靠,為黃連湯的后續中試工藝和工業化生產提供科學依據。
1 儀器與材料
1.1 儀器
Waters 2695型高效液相色譜儀,配備四元泵、柱溫箱、自動進樣器、2998檢測器、Empower3色譜工作站,美國Waters公司;Milli-Q型超純水機,美國Millipore公司;FA1104型電子分析天平,=0.1 mg,上海精密科學儀器有限公司;MS105DU型電子分析天平,=0.01 mg,瑞士梅特勒-托利多公司;KQ-500E型超聲波清洗器,昆山超聲儀器有限公司;DHG-9140A型電熱恒溫鼓風干燥箱,上海精宏實驗設備有限公司;AE-1106A型多功能紅外爐,中山市愛米生活電器有限公司。
1.2 試藥
對照品鹽酸小檗堿(批號110713-201814,質量分數86.7%)、鹽酸巴馬汀(批號110732-201611,質量分數86.8%)、鹽酸黃連堿(批號112026-201601,質量分數95.1%)、甘草苷(批號111610-201607,質量分數93.1%)、甘草酸銨(批號110731-201720,質量分數97.7%)、6-姜辣素(批號111833-201806,質量分數99.9%)均購自中國食品藥品檢定研究院。磷酸二氫鉀,色譜級,上海阿拉丁生化科技有限公司;乙腈,色譜級,默克股份兩合公司;甲醇,色譜級,江蘇漢邦科技有限公司;磷酸,色譜級,上海阿拉丁生化科技有限公司;其他試劑為分析級。黃連(批號22041211)、干姜(批號22041811)、水炙甘草(批號22041311)、桂枝(批號22041511)、人參(批號22041711)、湯洗半夏(批號22042011)、大棗(批號22041711)均由神威藥業集團有限公司提供,均經過南京中醫藥大學藥學院陳建偉教授鑒定,黃連為毛茛科黃連屬植物黃連Franch.的干燥根莖、干姜為姜科姜屬植物姜Rosc.的干燥根莖、水炙甘草為豆科甘草屬植物甘草Fisch.的干燥根和根莖、桂枝為樟科樟屬植物肉桂Presl的干燥嫩枝、人參為五加科人參屬植物人參C. A. Mey.的干燥根和根莖、湯洗半夏為天南星科半夏屬植物半夏Breit的干燥塊莖、大棗為鼠李科棗屬植物棗Mill.的干燥成熟果實,均符合《中國藥典》2020年版[11]飲片標準。
2 方法與結果
2.1 基準樣品的制備
對黃連湯煎煮工藝進行研究,確定最佳工藝:稱取黃連41.40 g,甘草(水炙)41.40 g,干姜41.40 g,桂枝41.40 g,人參27.60 g,半夏(湯洗)60.00 g,大棗42.00 g于砂鍋中,加2000 mL水,浸泡60 min,以武火(2200 W)煮沸后,調節火力至文火(900 W)保持微沸,煎煮約60 min后,趁熱濾過,濾液放涼后加水調整體積至1200 mL,即得黃連湯基準樣品。
2.2 干膏率的測定
精密量取黃連湯基準樣品10 mL于恒定質量后的蒸發皿中,水浴蒸干后,105 ℃干燥3 h,記錄質量,計算干膏率。
干膏率=/
為黃連湯湯干膏粉的質量,為全方飲片質量
2.3 指紋圖譜的測定[16]
2.3.1 色譜條件 Merck Purospher Star LP RP-18endcapped色譜柱(250 mm×4.6 mm,5 μm);流動相為乙腈-水(含0.05 mol/L磷酸二氫鉀,磷酸調節pH 3.0);梯度洗脫:0~7 min,10%~22%乙腈;7~19 min,22%~23.5%乙腈;19~28 min,23.5%~24%乙腈;28~42 min,24%~35%乙腈;42~52 min,35%~63%乙腈;52~54 min,63%~10%乙腈;54~56 min,10%乙腈;體積流量1 mL/min;檢測波長280 nm;柱溫25 ℃;進樣體積10 μL。
2.3.2 方法學考察[16]參考本課題組前期研究基礎進行,結果均滿足分析要求。
2.3.3 供試品溶液的制備 精密量取黃連湯基準樣品及正交水提液2 mL置10 mL量瓶中,加入甲醇7 mL,再加水至刻度,使甲醇體積分數為70%,稱定質量,超聲處理30 min,放冷,用70%甲醇補足減失的質量,搖勻,濾過,取續濾液,即得供試品溶液。
2.3.4 指紋圖譜的建立及其相似度分析 分別取“2.3.3”項下方法制得基準樣品供試品溶液及正交水提液供試品溶液,按“2.3.1”項下色譜條件進樣,測定指紋圖譜。將色譜結果以cdf.的格式導入2012年版《中藥色譜指紋圖譜相似度評價系統》進行評價。以基準樣品的指紋圖譜為參照圖譜,時間窗寬度為0.1 s,采用中位數法,進行全譜峰匹配,計算相似度。圖譜見圖1。
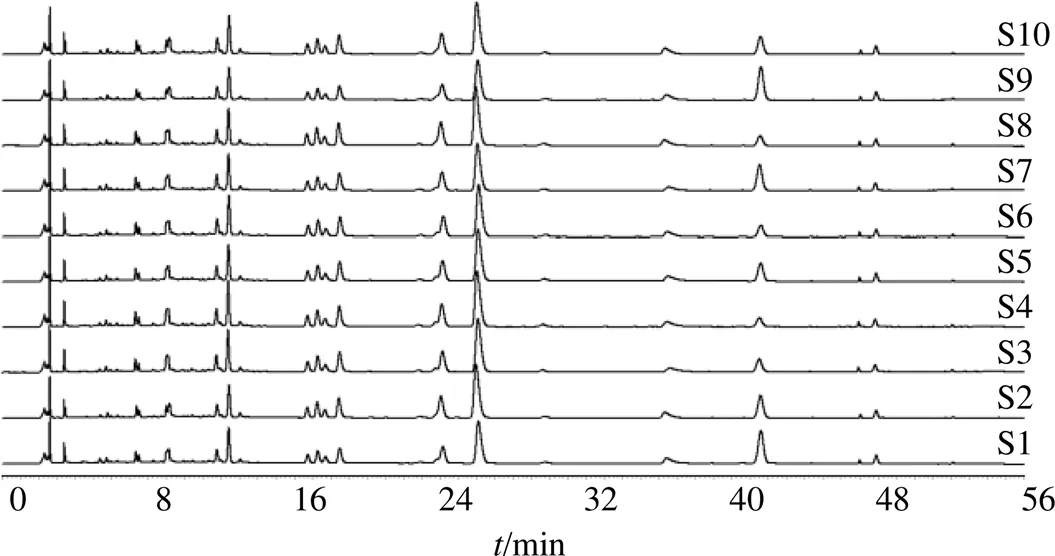
S1-基準樣品的指紋圖譜 S2~S10-正交試驗1~9號樣品的指紋圖譜
2.4 指標成分的含量測定[17]
2.4.1 色譜條件 檢測波長237、280、345 nm,色譜柱等其余條件與“2.3.1”項下一致。典型色譜圖見圖2。
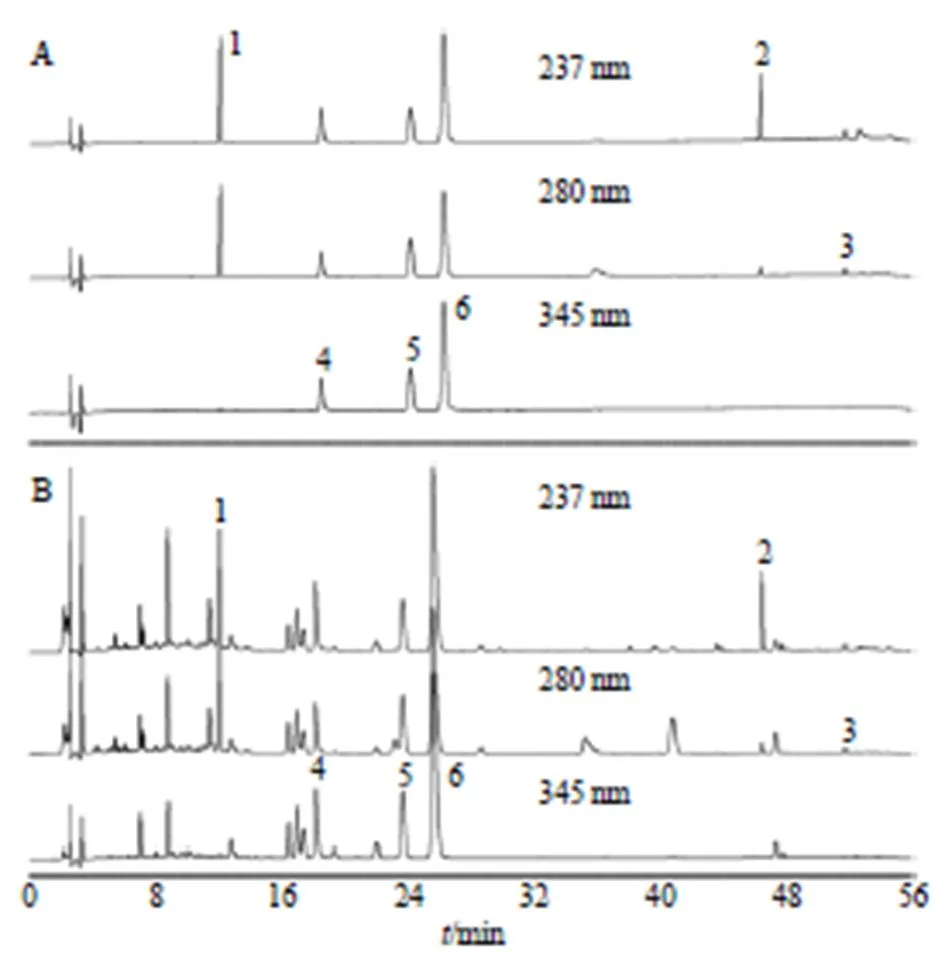
1-甘草苷 2-甘草酸 3-6-姜辣素 4-黃連堿 5-巴馬汀 6-小檗堿
2.4.2 方法學考察[17]參考本課題組前期研究基礎進行,結果均滿足分析要求。
2.4.3 對照品溶液的制備 精密稱取各對照品適量,加入甲醇配制成分別含鹽酸小檗堿483.92 μg/mL、鹽酸黃連堿103.83 μg/mL、鹽酸巴馬汀124.66 μg/mL、甘草苷292.80 μg/mL、甘草酸單銨鹽493.61 μg/mL、6-姜辣素58.98 μg/mL的混合對照品溶液。
2.4.4 供試品溶液的制備 同“2.3.3”項下供試品溶液的制備方法。
2.5 黃連湯基準樣品干膏率及指標成分的測定
取制得的基準樣品,按“2.2”~“2.4”項下方法,平行制備2份供試品溶液,測定黃連湯基準樣品的干膏率及各指標成分含量,算取平均值。
2.6 單因素考察
2.6.1 加水量考察 依次稱取處方量的飲片于5 L圓底燒瓶中,分別加入4、6、8、10、12倍處方量的去離子水進行回流提取,分別浸泡60 min,提取60 min。按“2.3.3”項下方法平行制備2份供試品溶液,測定水提液中黃連堿、巴馬汀、小檗堿、6-姜辣素、甘草苷、甘草酸及干膏率,算取平均值,結果見表1。隨著加水量增加,黃連堿、巴馬汀、小檗堿、甘草苷、甘草酸含量及干膏率呈上升趨勢,超過10倍水后,6-姜辣素含量下降。結合隨性物質基準考察指標,加水量的低水平及高水平分別為6倍量水和10倍量水。
2.6.2 浸泡時間考察 依次稱取處方量的飲片于5 L圓底燒瓶中,加入8倍處方量的去離子水進行回流提取,分別浸泡20、40、60、80 min,提取60 min。按“2.3.3”項下方法平行制備2份供試品溶液,測定水提液中黃連堿、巴馬汀、小檗堿、6-姜辣素、甘草苷、甘草酸及干膏率,算取平均值,結果見表2。隨著浸泡時間增加,黃連堿、巴馬汀、小檗堿、6-姜辣素的含量呈緩慢上升趨勢,超過60 min后,甘草苷、甘草酸含量略有下降,干膏率無明顯變化。因此,浸泡時間的低水平及高水平分別為20、60 min。
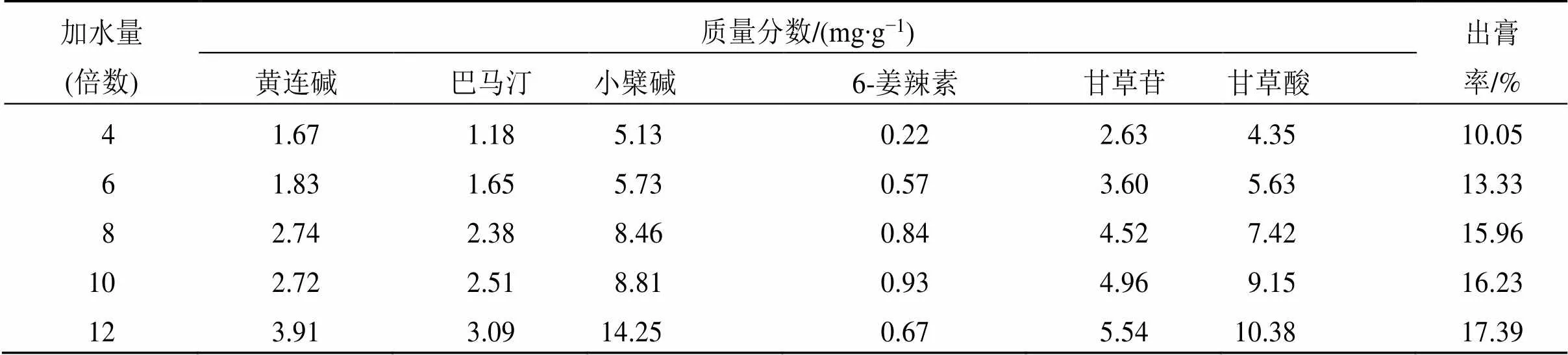
表1 加水量考察結果
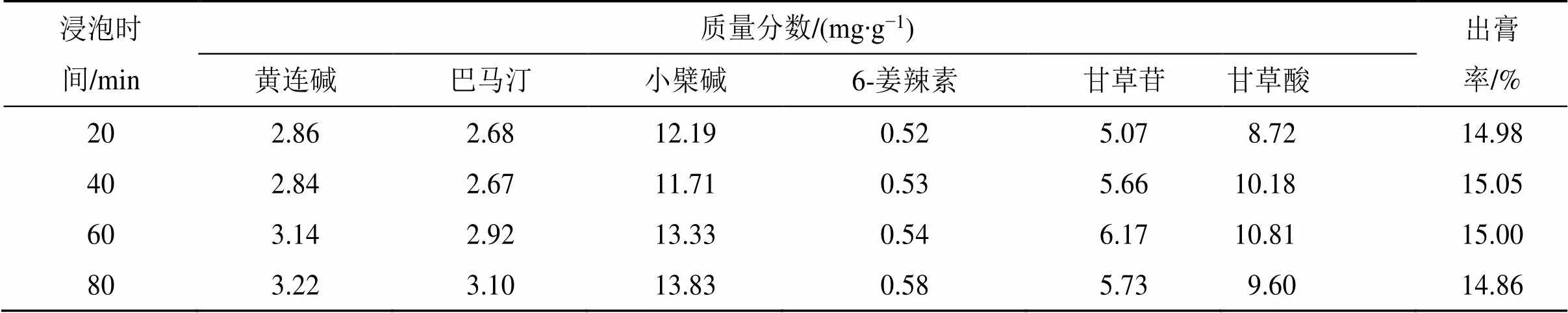
表2 浸泡時間考察結果
2.6.3 提取時間考察 依次稱取處方量的飲片于5 L圓底燒瓶中,加入8倍處方量的去離子水進行回流提取,浸泡60 min,分別提取30、40、50、60 min。按“2.3.3”項下方法平行制備2份供試品溶液,測定水提液中黃連堿、巴馬汀、小檗堿、6-姜辣素、甘草苷、甘草酸及干膏率,算取平均值,結果見表3。隨著提取時間增加,黃連堿、巴馬汀、小檗堿的含量和干膏率呈上升趨勢,6-姜辣素的含量無明顯趨勢,提取時間超過50 min后,甘草苷上升緩慢且甘草酸含量下降。結合物質基準的各項指標,由此確定提取時間的低水平及高水平分別為30、60 min。
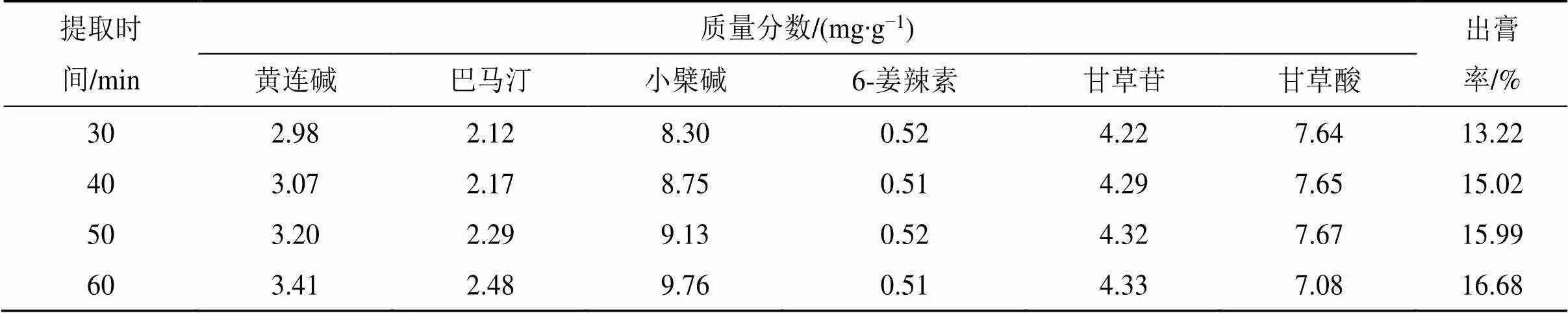
表3 提取時間考察
2.7 提取正交試驗
(1)關鍵質量屬性(critical quality attributes,CQAs)和關鍵工藝參數(critical process parameters,CPPs)的確定:基于前期研究,物質基準初步預測黃連堿、巴馬汀、小檗堿、甘草苷、甘草酸、桂皮醛、6-姜辣素為黃連湯潛在的質量標志物(Q-Marker)[16]。由于桂皮醛在制劑中的濃縮、干燥階段損耗較大,故先提取桂枝揮發油,后用β-環糊精進行包合,在制粒環節加入顆粒中。因此,在提取正交試驗中,選擇6個指標成分含量(黃連堿、巴馬汀、小檗堿、甘草苷、甘草酸、6-姜辣素)、干膏率及指紋圖譜相似度作為黃連湯提取工藝的CQAs。結合文獻分析,選擇料液比(A)、浸泡時間(B)、提取時間(C)3個因素作為黃連湯制劑工藝的CPPs。
(2)正交試驗設計:稱取與傳統工藝相同處方量的同一批的藥材飲片,共9份,以料液比(A)、浸泡時間(B)、提取時間(C)3個因素為考察對象,以提取物中黃連堿、巴馬汀、小檗堿、6-姜辣素、甘草苷、甘草酸含量,指紋圖譜相似度以及干膏率為評價指標,按L9(34)正交表進行提取,檢測結果見表4。
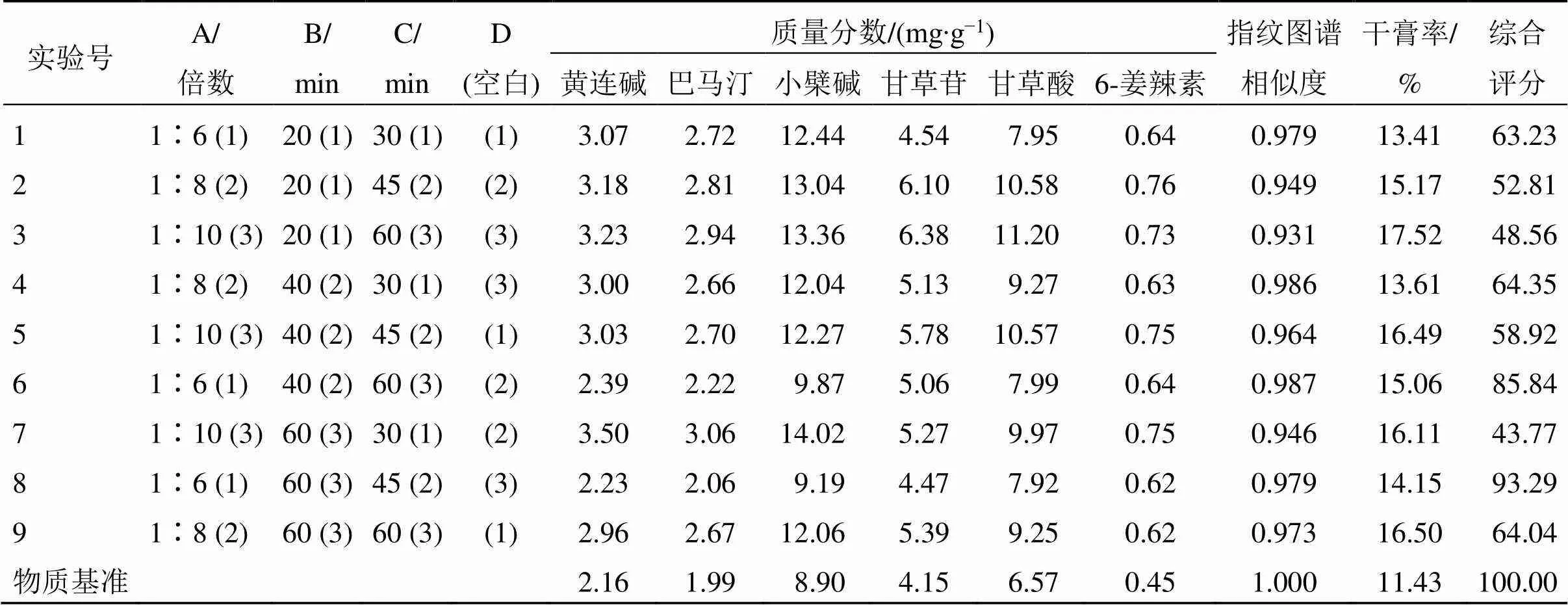
表4 正交試驗設計與響應值
2.8 基準關聯度的原理方法
2.8.1 評價對象的確定 基準關聯度是評價某樣品與基準樣品的相似度的關鍵參數,應首先確定樣品評價的指標數目和樣品數目,本方法的基本路線如圖3所示。本研究將正交試驗設計生成的9個樣品與基準樣品相比,以提取物中黃連堿、巴馬汀、小檗堿、6-姜辣素、甘草苷、甘草酸含量,指紋圖譜相似度以及干膏率為評價指標,以X,j、S為評價對象,X表示正交試驗的第(=1,2,…,)個樣本的第(=1,2,…,)個指標下的測量值,S表示基準樣品的第(=1,2,…,)個指標下的測量值。
2.8.2 相對偏差(relative deviation,RD)值的計算 RD表示第(=1,2,…,)個樣本的第(=1,2,…,)個指標下的RD,RD越小則表明代表X相對于S的偏差越小,即該條件下制得樣品質量與基準樣品相似度更高。根據公式(1)計算RD。
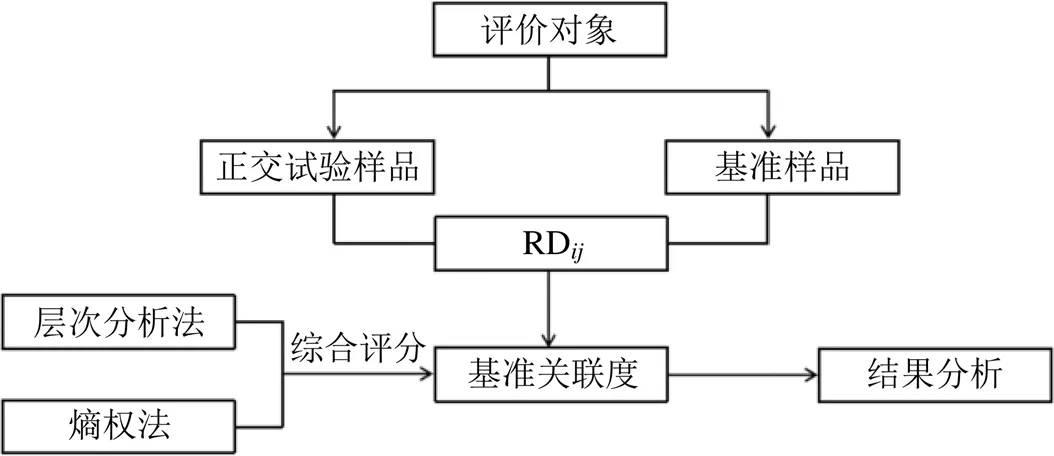
圖3 方法流程圖
RD=|X-S|/S(1)
2.8.3 基準關聯度(standard relation,SR)的計算 以基準樣品質量為標準值(),以正交試驗設計下的各樣品質量為測得值(),以不同的指標為評價指標,按公式(2)計算所得結果,稱為基準關聯度,結果見表5。SR表示第(=1,2,…,)個樣本的第(=1,2,…,)個指標下的基準關聯度。SR越接近100%,在該指標下的工藝參數制得的樣品與基準樣品相似度越高。
SR=1-RD=1-|X-S|/S(2)
計算公式如公式(2)所示,計算結果表明,當以黃連堿、巴馬汀、小檗堿、甘草苷、甘草酸為評價指標時,與基準樣品最為接近的是試驗8;當以6-姜辣素為評價指標時,與物質基準最為接近的是試驗9;當以指紋圖譜相似度為評價指標時,與物質基準最為接近的是試驗6;當以干膏率為評價指標時,與物質基準最為接近的是試驗1。由此可得,當以單一因素為評價指標時,試驗所得最優結果會根據評價指標的變化而變化,因此需進行綜合評分后才能確定提取工藝參數。
2.9 AHP-熵權法組合權重的計算
2.9.1 AHP主觀賦權
(1)構建判斷矩陣:根據君臣佐使原則[12],黃連湯方中黃連和干姜為君藥,黃連苦寒,清胸中之熱、兼和胃氣,干姜辛溫,以溫胃中之寒;臣藥為桂枝和半夏,桂枝辛散溫通、祛寒止痛,半夏和胃降逆止嘔,寬胸散結消痞;佐藥為人參和大棗,兼得益氣健脾、緩和藥性之效;使藥為甘草,甘草甘平,緩腹中之痛[13]。諸藥合用,可平調寒熱、和胃降逆。
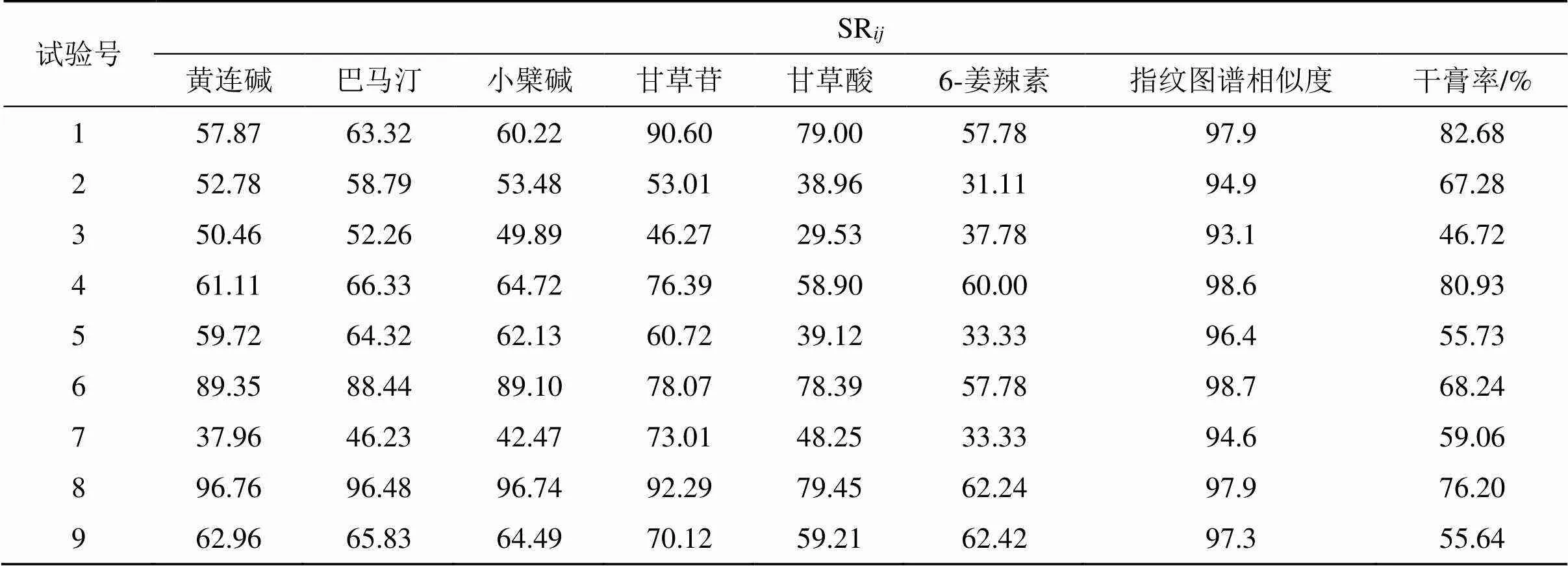
表5 正交試驗的SRij
本研究參考《中藥新藥質量標準研究技術指導原則(試行)》要求[14],根據黃連湯的處方組成,結合各味藥中指標性成分的實際測得性和穩定性,選擇君藥黃連中的黃連堿、巴馬汀、小檗堿,君藥干姜中的6-姜辣素,以及使藥甘草中的甘草苷、甘草酸為6個指標性成分,同時兼顧干膏率和指紋圖譜。通過干膏率反映提取工藝的穩定性,指紋圖譜體現制劑過程中小分子成分的輪廓及定性特征。
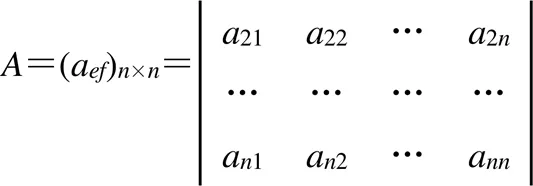
指紋圖譜可反映小分子成分輪廓和定性特質,但與含量測定的指標性成分相比,其所包含的質量信息仍較少[15],故將其重要程度視為與干膏率同等重要。故按黃連堿=巴馬汀=小檗堿>6-姜辣素>甘草苷=甘草酸>指紋圖譜相似度≈干膏率的順序,再根據AHP理論判斷矩陣1~9標度,對同一層次內個指標的相對重要程度進行打分,結果見表6。黃連堿、巴馬汀、小檗堿為君藥黃連的主要藥效成分,相對于6-姜辣素較明顯重要,故標為4,相對于甘草苷、甘草酸明顯重要,故標為5,相對于指紋圖譜相似度和干膏率明顯更為重要,標為6,以此類推,根據公式(3)構建判斷矩陣,數據見表7,用a表示因素相對于因素的比較結果。
(2)計算主觀權重系數(WS):首先對判斷矩陣進行幾何平均(方根法),按公式(4)計算得到初始權重系數(W′),a表示第(=1,2,…,)個指標因素對第(=1,2,…,)個指標因素的比較結果,然后按照公式(5)計算歸一化WS,得到5個指標的WS,結果見表8。

表6 AHP構建判斷矩陣的標準
W′=(a1a2…a)1/n(4)
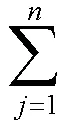
(3)一致性檢驗:對矩陣進行一致性檢驗。首先根據公式(6)計算最大特征根(max),再根據公式(7)計算一致性指標(consistency index,CI),得到CI為0.03,一致性比例(consistency ratio,CR)(CR=CI/RI,RI為自由度指標)為0.02,均小于0.1,表明該矩陣具有一致性[10]。
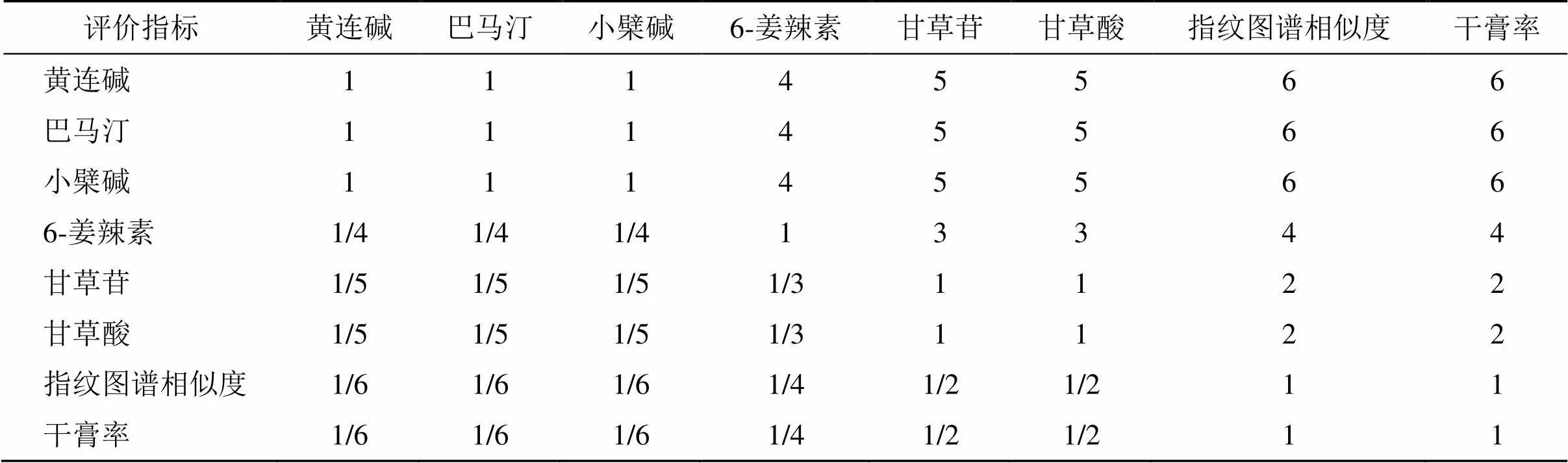
表7 指標成對比較的判斷優先矩陣
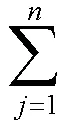
CI=(max-)/(-1) (7)
2.9.2 信息熵客觀賦權
(1)建立正交試驗原始數據矩陣:現有個樣本,個評價指標,原始數據矩陣=(X,j)×n,以黃連堿、巴馬汀、小檗堿、6-姜辣素、甘草苷、甘草酸含量,指紋圖譜相似度及干膏率8個指標為評價指標,建立原始數據矩陣()。
(2)將原始數據轉化為概率矩陣:根據公式(8)將原始數據矩陣轉化為概率矩陣(),P表示在第個指標下第個樣本的概率。
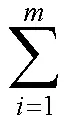
(3)計算各指標的信息熵(H)和客觀權重系數(WO):H越小,代表指標下的數據離散程度越高,則其所提供的信息量就越大[10]。根據公式(9)計算出各指標的H依次為0.996 1、0.996 9、0.996 4、0.998 3、0.997 0、0.996 4、0.999 9、0.998 2,按照公式(10)計算各指標的WO。
H=?PlnP,=1/ln(9)
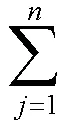
2.9.3 綜合權重系數(W)的確定 采用AHP得到WS,熵權法得到WO,根據公式(11)計算各指標的W,結果見表8。
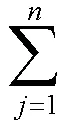
2.10 綜合評分
通過AHP-熵權法得到的W,可知黃連堿占比30%,巴馬汀占比24%,小檗堿占比28%,6-姜辣素占比5%,甘草苷占比5%,甘草酸占比6%,干膏率占比2%。根據公式(12)計算綜合評分,結果見表4。由表4中結果可知,試驗8綜合評分最高,結果表示與古法最相似的現代工藝參數為A3B1C2,即以6倍量的水浸泡1 h煎煮45 min得到的樣品與基準樣品的質量最為一致。
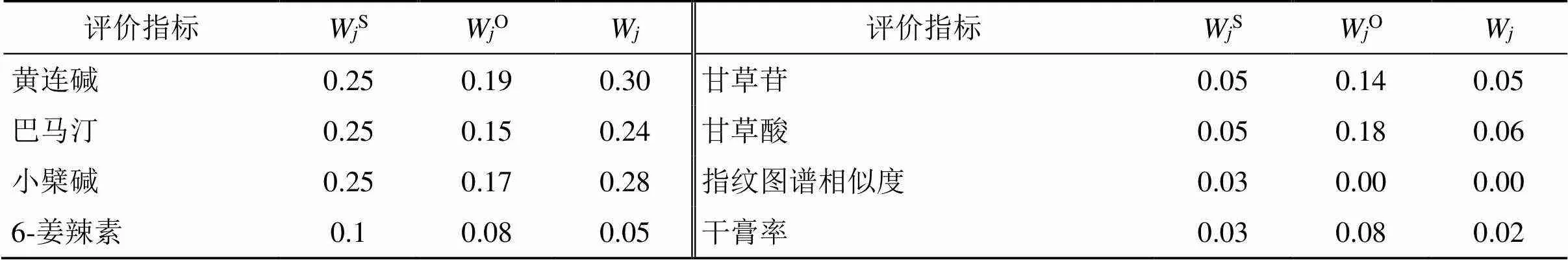
表8 組合權重
綜合評分=SR,黃連堿×30%+SR,巴馬汀×24%+SR,小檗堿×28%+SR,6-姜辣素×5%+SR,甘草苷×5%+SR,甘草酸×6%+ SR,干膏率×2% (12)
2.11 驗證試驗
對優化后的提取工藝參數進行驗證,重復試驗3次,測定黃連堿、巴馬汀、小檗堿、6-姜辣素、甘草苷、甘草酸含量,指紋圖譜相似度及干膏率,計算綜合評分,結果見表9。驗證試驗的綜合評分均值為90.11,與基準樣品質量接近,且符合《按古代經典名方目錄管理的中藥復方制劑藥學研究技術指導原則(試行)》[6]中對制劑生產研究的要求。綜合評分的RSD值為1.09%,說明該方法確定的提取工藝穩定可靠且重復性良好。
3 討論
黃連湯作為平調寒熱、和胃降逆治法的代表方,自古至今一直被眾多醫家廣泛使用,對其進行經典名方制劑的開發研究意義重大。課題組前期已根據古籍記載制備了黃連湯標準湯液,并建立了其質量標準[16-17]。本研究基于QbD理念,選用正交試驗設計,建立以黃連堿、巴馬汀、小檗堿、6-姜辣素、甘草苷、甘草酸、指紋圖譜相似度和干膏率為主的質量控制體系,確定以加水倍量、浸泡時間、提取時間作為關鍵工藝參數,采用單因素實驗確定各因素水平,應用正交設計優化經典名方黃連湯的提取工藝。AHP作為主觀賦權法,由人為確定各個評價指標的權重系數,受人為影響較大;熵權法作為客觀賦權法,根據數據變化規律得出最終權重系數,但不能體現中藥復方的君臣佐使關系。
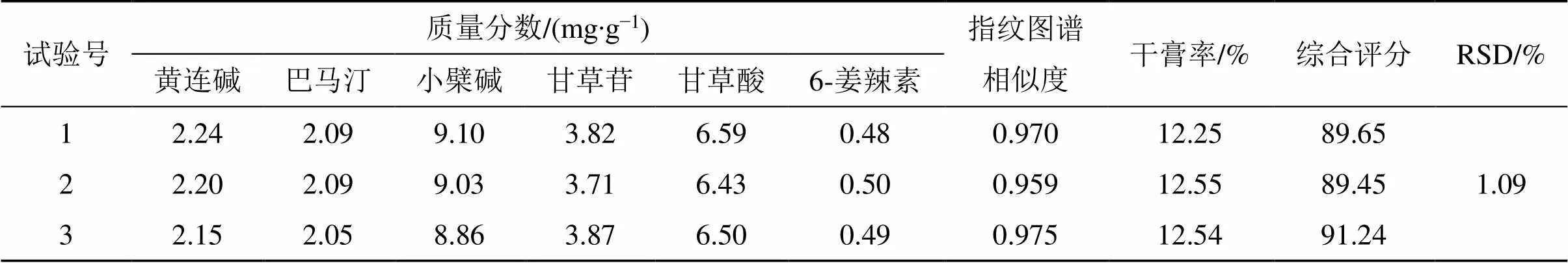
表9 驗證試驗結果
本研究結合基準關聯度和AHP-熵權法對質量評價體系進行賦權,明確8個指標在質量控制體系中的權重系數,以此優化黃連湯現代提取工藝為加6倍量水、浸泡60 min、提取45 min。所得工藝可保證工業生產的可行性及產品質量的穩定性,符合經典名方“傳承精華、古為今用、古今銜接”的基本研究原則,實現了傳統工藝向現代工業生產的關鍵一步。
利益沖突 所有作者均聲明不存在利益沖突
[1] 國家中醫藥管理局. 國家中醫藥管理局關于發布《古代經典名方目錄(第一批)》的通知[EB/OL]. (2018-04-13). [2022-12-18]. http://kjs.satcm.gov.cn/zhengcewenjian/ 2018-04-16/7107.html.
[2] 漢·張仲景著. 厲暢, 梁麗娟點校. 傷寒論 [M]. 北京: 中醫古籍出版社, 1997: 42.
[3] 于雷, 劉納文, 陳重, 等. 黃連湯治療幽門螺桿菌陽性脾虛濕熱型慢性非萎縮性胃炎的療效分析 [J]. 中國慢性病預防與控制, 2020, 28(12): 921-923.
[4] 謝躍麗. 阿奇霉素聯合黃連湯治療急性宮頸炎效果觀察 [J]. 實用中醫藥雜志, 2019, 35(4): 446-447.
[5] 國家藥品監督管理局. 國家藥品監督管理局綜合和規劃財務司關于公開征求《古代經典名方關鍵信息表(25首方劑) (征求意見稿)》意見的通知[EB/OL]. (2022-08-01). [2022-12-18]. https://www.nmpa.gov.cn/directory/web/ nmpa/xxgk/zhqyj/zhqyiyp/20220801171436142.html.
[6] 國家藥品監督管理局藥品審評中心. 《按古代經典名方目錄管理的中藥復方制劑藥學研究技術指導原則(試行)》[EB/OL]. (2021-08-31). [2022-12-18]. https://www. cde.org.cn/main/news/viewlnfoCommon/1c18dd163e7c9221786e5469889367d0.html.
[7] 劉昌孝, 陳士林, 肖小河, 等. 中藥質量標志物 (Q-Marker): 中藥產品質量控制的新概念 [J]. 中草藥, 2016, 47(9): 1443-1457.
[8] 王逸飛, 朱振宇, 吳志生,等. QbD理念的中藥緩控釋制劑的設計與研發研究 [J]. 中國中藥雜志, 2019, 44(20): 4317-4321.
[9] 徐男, 王平, 王淑玲, 等. 基于UPLC特征圖譜和Q-Marker量值傳遞評價經典名方半夏白術天麻湯顆粒劑的關鍵生產工藝 [J]. 中草藥, 2021, 52(24): 7455-7463.
[10] 代珊, 李帥, 張愛軍, 等. 基于基準關聯度和AHP-熵權法綜合評價經典名方小續命湯古今提取工藝 [J]. 中草藥, 2022, 53(3): 726-734.
[11] 中國藥典[S]. 一部. 2020: 8, 15, 23, 89, 123, 288, 316.
[12] 李銳華, 孫增濤, 王永香, 等. 運用AHP結合熵權法優化疏風定喘顆粒炙麻黃組的醇沉工藝 [J]. 中國實驗方劑學雜志, 2016, 22(20): 1-5.
[13] 陳梅, 王盼盼, 賈六金, 等. 黃連湯方義探析及臨床應用 [J]. 遼寧中醫藥大學學報, 2021, 23(5): 162-165.
[14] 國家藥品監督管理局. 國家藥監局藥審中心關于發布《中藥新藥質量研究技術指導原則(試行)》的通告(2021年第3號) [EB/OL]. (2021-01-14). [2022-12-18]. https:// www.cde.org.cn/zdyz/domesticinfopage?zdyzldCODE=b30261779e4848579b15cf34608a06e7.html.
[15] 王智民, 劉菊妍, 王德勤,等. 關于經典名方研發的一些重要關鍵信息和科學問題的幾點看法 [J]. 中國實驗方劑學雜志, 2022, 28(1): 212-217.
[16] 彭梅梅, 郭爽, 陳琪,等. 基于特征圖譜和網絡藥理學的經典名方黃連湯質量標志物 (Q-Marker) 預測分析 [J]. 中草藥, 2021, 52(18): 5514-5523.
[17] 彭梅梅, 郭爽, 王璐, 等. 經典名方黃連湯的物質基準量值傳遞分析 [J]. 中國中藥雜志, 2022, 47(2): 313-323.
Optimization of extraction process for classical prescription Huanglian Decoction based orthogonal test, standard relation and analytic hierarchy process combined with entropy method
WANG Xiao-li1, SHEN Zhe-yuan1, LI Li-ping1, MEI Xi1, HE Tian-yu1, ZHAO Xiao-li1, MAO Jing1, HOU Jin-cai1, GUO Yong2, MAO Chun-qin1, CUI En-zhong1, 3, LU Tu-lin1
1. School of Pharmacy, Nanjing University of Traditional Chinese Medicine, Nanjing 210023, China 2. Shenwei Pharmaceutical Group Co., Ltd., Shijiazhuang 051430, China 3. Department of Pharmaceutical Preparation, General Hospital of Easter Theater Command, Nanjing 210002, China
The extraction process of the classical prescription Huanglian Decoction (黃連湯) was optimized based on orthogonal test, standard relation and analytic hierarchy process combined with entropy method.With the contents of coptisine, palmatine, berberine, 6-gingerol, liquiritin, glycyrrhizic acid, fingerprint similarity, paste-forming rate as critical quality attributes (CQAs). The amount of water, soaking time and extraction time were used as the critical process parameters (CPPs). The single factor experiment design was used to determine the level of each factor, and the orthogonal test was used to optimize the process parameters. The standard relation between each samples and standard decoction of various indexes of different extraction parameters was calculated, while AHP-entropy method was applied to determine the weight of each index for comprehensive score.A process evaluation function model was established by using orthogonal test combined with standard relation and AHP-entropy method as follow: comprehensive score = SR,coptisine× 30% + SR,palmatine× 24% + SR,berberine× 28% + SR,6-gingerol× 5% + SR,liquiritin× 5% + SR,glycyrrhizic acid× 6% + SR,paste-forming rate× 2%. The function model was stable and reliable. The extraction process was to add six times of water to the whole decoction pieces, soak for 60 min and extract for 45 min. The average score of the validation test was 90.11, and the RSD was 1.09%, which met the requirements of the reference material standard, and the method was applicable.The modern extraction parameters of Huanglian Decoction screened by this method were feasible, which provided a theoretical basis for the development and utilization of other classic prescriptions.
classical prescription; Huanglian Decoction; extraction process; standard relation; analytic hierarchy process; orthogonal design; information entropy method; quality by design; critical quality attributes; critical process parameters; coptisine; palmatine; berberine; 6-gingerol; liquiritin; glycyrrhizic acid; fingerprint
R283.6
A
0253 - 2670(2023)15 - 4804 - 08
10.7501/j.issn.0253-2670.2023.15.005
2022-12-21
國家重點研發計劃項目(2018YFC1707000);江蘇省研究生科研創新計劃項目(KYCX23-2027)
王曉麗,碩士研究生,主要從事中藥炮制及中藥飲片質量標準研究。E-mail: 2667631348@qq.com
通信作者:陸兔林,教授,博士生導師,主要從事中藥炮制及中藥飲片質量標準研究。E-mail: ltl2021@njucm.edu.cn
崔恩忠,高級工程師。Tel: 15952001774
[責任編輯 鄭禮勝]

