走進合成生物學
劉虎虎 田云

隨著國家“十四五”規劃、“中國制造2025”以及“健康中國行動”等一系列政策和文件的出臺與實施,我國生物技術產業已經進入快速發展時期。其中新出現的合成生物學一詞經常出現在新聞頭條上,伴隨著人工合成微生物、人工合成酵母染色體、青蒿素的發酵生產以及人工合成淀粉、葡萄糖和脂肪酸的實現,合成生物學被喻為是“認識生命的鑰匙”(建物致知)和“改變未來的顛覆性技術”(建物致用)[1,2]。
合成生物學的誕生與發展
19世紀初,人們普遍認為有機物是與生命現象密切相關的,是生物體內一種特殊的、神秘的“生命力”作用下產生的,只能從生物體內得到,不能人工合成,這就是當時的“生命力”學說。1828年,德國化學家維勒(F. Wohler)使用無機物氰酸銨人工合成了有機物尿素,從而給“生命力”學說以沉重打擊。20世紀初,法國化學家勒杜克(S. Leduc)試圖通過物理的理論來解釋生命的現象。他通過溶質滲透和擴散方法模擬了人工合成細胞及其次生細胞群,揭示了無機營養與人工絲狀真菌發育的關系,并用礦物質模擬了生物的趨光性、趨化性和趨電性。這些研究結果揭示,生物學僅僅是流體物理學的一個分支,物質的物理學機制可能導致生命的出現。但是,因為當時知識和觀察能力的局限,這些研究只能停留于生命表型和流體物理表型相關的“合成”描述,距離真正認識和改造生命的科學研究還很遠。1913年,《自然》周刊系統評述了勒杜克的相關研究,合成生物學一詞首次正式在學術期刊出現。
1950—1960年代,DNA雙螺旋結構和胰島素一級結構等先后被確定,具有生物活性的核酸和蛋白質等也實現了人工合成。我國科學家在1965年和1981年分別首次人工合成了牛胰島素和酵母丙氨酸tRNA,證實蛋白質和核糖核酸都可以人工合成,從根本上推翻了所謂的“生命力”學說。20世紀70年代,隨著重組DNA技術的發展和日益成熟,“合成生物學”被再次提出。波蘭遺傳學家斯吉巴爾斯基(W. Szybalski)提出了合成生物學的愿景:“一直以來,人們都在做分子生物學描述性方面研究,但當我們進入合成生物學的階段,真正的挑戰才開始。我們會設計新的調控元素,并將新的核酸序列加入已存在的基因組內,甚至建構一個全新的基因組”,并認為“這將是一個擁有無限潛力的領域,幾乎沒有任何事能限制我們去做一個更好的控制回路。最終,將會有合成的有機生命體出現”。
1990年代后期,隨著人類基因組計劃的成功推進,各種“生物組學”以及生物信息學、系統生物學等交叉學科迅速發展,在世紀之交,研究者在“設計—建造—測試”的工程學理念基礎之上,成功實踐出利用生物元件構建成邏輯線路,如美國普林斯頓大學的伊洛維茲(M. B. Elowitz)等運用3個轉錄抑制系統相互抑制的關系,研制出新型基因振蕩器。鑒于此,在2000年的美國化學學會年會上,斯坦福大學的庫爾(E. Kool)重新定義了“合成生物學”概念,即基于系統生物學的遺傳工程和工程方法的人工生物系統研究,從基因片段、DNA分子、基因調控網絡與信號傳導路徑到細胞的人工設計與合成。這標志著合成生物學的正式出現,隨后迅速獲得廣泛關注,被認為是繼DNA雙螺旋結構發現和人類基因組計劃之后的“第三次生命科學技術革命”。
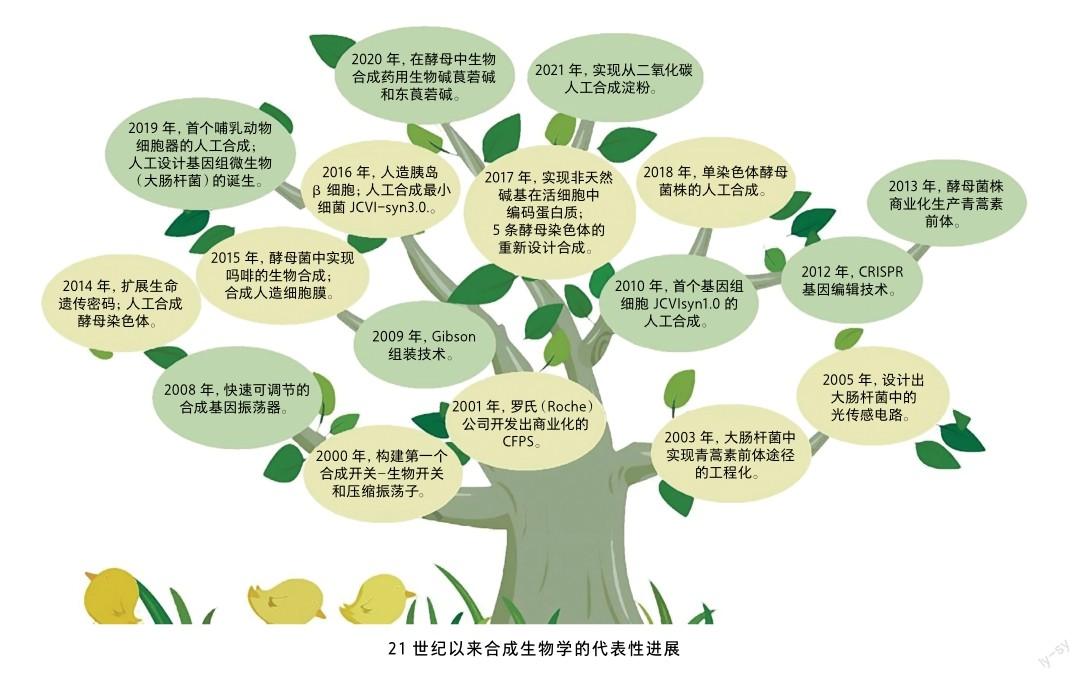
進入21世紀以來,合成生物學發展迅速,大致可以分為4個階段:①合成生物學的創建時期(2000—2003年),這個時期產生了許多具備領域特征的研究手段和理論,特別是基因線路工程的建立及在代謝工程中的成功運用;②摸索完善時期(2004—2007年),這個時期的重要特征是雖然領域有擴大趨勢,但工程技術進步比較緩慢;③快速創新和應用轉化時期(2008—2013年),這個時期涌現出了大量新技術和新工程手段,特別是人工合成基因組能力的提升,以及基因組編輯技術的突破等,從而使合成生物學的研究與應用領域大為拓展;④飛速發展新時期(2014年至今),該時期研究成果全面提升,特別是酵母染色體的人工合成等領域取得突破性成果,為人類實現“能力提升”的宏偉目標奠定了重要基礎。
合成生物學的應用
作為21世紀生物學領域催動原創突破和學科交叉融合的前沿代表,合成生物學不僅推動人類實現從“認識生命”到“設計生命”的偉大跨越,也將在一定程度上對生命科學研究范式進行改寫,即通過設計、改造和創造生命體系來理解生命,從而探尋是否具有支配生命復雜體系的自然法則。此外,合成生物學通過基因網絡工程,形成多學科交叉融合,其研究領域、研究內容和產業化應用等方面將迎來新的突破,也將為解決人類社會相關的全球性重大問題提供重要途徑。
合成生物學與人工合成生命
2010年,美國文特爾(J. C. Venter)研究團隊設計、合成和組裝了1.08 Mb長的蕈狀支原體基因組,并把它移植到已經剔除遺傳信息的山羊支原體受體細胞中,創造了世界上第一個僅由人工化學合成染色體控制的、具有自我復制能力的新細胞“Synthia”;2016年,研究人員在Synthia的基礎之上,不斷嘗試刪除基因組中的不必要基因,最終把901個基因刪除到只剩下473個基因,制造出最簡單的人造合成細胞——Syn 3.0合成細胞[3],文特爾也因此被譽為“人造生命之父”。2019年,英國劍橋大學泰真(J. W. Chin)研究組通過將大腸桿菌4 Mb長的基因組全部替換為合成基因組,創造出只使用61種密碼子的人造基因組大腸桿菌Syn61,打破了傳統生命體中共有64個密碼子編碼蛋白質的認知,這是迄今為止完成的最大人工合成基因組[4]。
2011年,中國、美國、英國等多國研究機構聯合開始實施第一個真核生物基因組合成計劃——合成酵母基因組計劃(Sc2.0),旨在對釀酒酵母的整個基因組進行重新設計、改造與人工合成。2014年,安娜盧儒(N. Annaluru)等報道了首條完整的合成型真核生物染色體——合成型釀酒酵母3號染色體(synⅢ)。2017年,Sc2.0團隊完成了釀酒酵母synⅡ、synⅤ、synⅥ、synⅩ和synⅫ共5條合成型染色體的從頭設計與合成,宣布有關合成型酵母基因組1/3的工作已經完成。其中,中國科學家領銜完成了其中的4條:天津大學元英進教授團隊完成了5號、10號釀酒酵母染色體的化學合成[5,6];清華大學戴俊彪研究員團隊完成了當前已合成釀酒酵母染色體中最長的12號染色體的全合成[7];深圳華大基因研究院團隊聯合英國愛丁堡大學團隊完成了釀酒酵母2號染色體的設計與合成[8]。2018年,美國博克(J. D. Boeke)團隊利用基因編輯技術將釀酒酵母的16條染色體融合在一起,構建出只含有2條染色體的“16合2”染色體新酵母菌株。與此同時,我國科學家通過15輪的染色體融合將釀酒酵母天然的16條染色體逐一融合,人工創建了只含有單條線型染色體的“16合1”染色體酵母細胞SY14 [9]。
單條染色體雖然在三維結構上有極大的改變,但是單染色體的酵母具有與野生型菌株相似的轉錄組和表型組,并且單染色體的酵母還保持了減數分裂的能力,說明單染色體的釀酒酵母可以具有正常的細胞功能,顛覆了染色體三維結構決定基因時空表達的傳統觀念,揭示了染色體三維結構與實現細胞生命功能的全新關系。
合成生物學與綠色生物制造
合成生物學通過設計和構建細胞工廠,能夠使細胞以淀粉、纖維素、CO2等可再生碳為原料,生產重要的化工產品、天然藥物、食品、生物能源以及生物材料等產品,具有清潔、高效、可再生等優點,開創了傳統石化產品、天然藥物等產品的全新生產模式。
青蒿素是一種應用非常廣泛的抗瘧藥物,目前市售的青蒿素主要是從植物黃花蒿中進行提取,由于植物中青蒿素的含量稀少且青蒿素需求廣泛,從而導致青蒿素供應不穩定。為了有效解決青蒿素的來源問題,迫切需要建立一種環境友好、廉價的青蒿素生產方法。
2004年,美國加州大學伯克利分校的基斯林(J. D. Keasling)課題組和生物技術公司Amyris合作開展半合成青蒿素項目。首先,研究人員根據植物中部分已知的青蒿素合成途徑,設計青蒿素如何在微生物中進行合成。然后探討青蒿素的合成途徑在不同的微生物底盤細胞中是否適配。通過在大腸桿菌中異源表達不同來源的甲羥戊酸途徑以及黃花蒿來源的紫穗槐—4,11—二烯合酶基因,成功合成了紫穗槐—4,11—二烯,產量達到27克/升,進一步將催化紫穗槐—4,11—二烯轉化為青蒿酸的植物源P450氧化酶CYP71AV1組裝到大腸桿菌中,最終獲得了能夠生產1克/升青蒿酸的重組大腸桿菌,但仍不能滿足生產的需求。
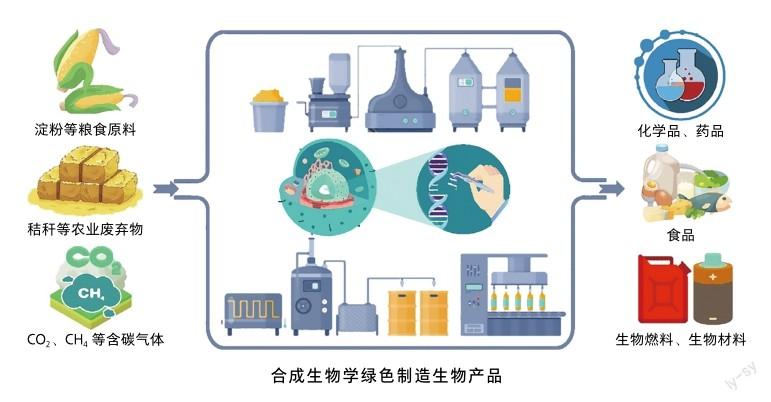
因此,項目組嘗試改用釀酒酵母來生產青蒿酸。首先,通過對酵母MVA途徑中代謝調控關系的調整、關鍵酶基因表達量優化、前體物法尼基焦磷酸代謝支路的削弱,結合氧化酶CYP71AV1的表達,成功構建能夠生產100毫克/升青蒿酸的酵母菌株;然后,研究人員進一步通過基因挖掘、體系優化等系列措施,最終獲得了能夠生產25克/升青蒿酸的重組酵母菌株及其生產工藝,在此基礎上,研究人員開發了從青蒿酸到青蒿素的化學合成方法,整個轉化過程的收率為40%~45%。至此,項目組耗時10年完成了青蒿素的半合成工藝(微生物合成加化學合成)[10]。
2013年4月,法國制藥業巨頭賽諾菲(Sanofi)公司宣布開始應用Amyris開發的青蒿素生產工藝工業化生產青蒿素。2013年5月,世界衛生組織批準微生物合成的青蒿素作為臨床藥物使用。2014年,賽諾菲公司生產的青蒿素正式上市出售。青蒿素微生物發酵生產商業化的成功成為了合成生物技術的重大應用典范。此外,筆者實驗室以FDA認證安全的解脂耶氏酵母為底盤細胞,通過“錦上添花”“移花接木”等方式設計合成途徑,構建細胞工廠,實現了角鯊烯、前列腺素、二十二碳二烯酸以及蟲草素等高附加值產品的綠色生物制造。這些事例證明了合成生物系統在生物產品綠色制造上具有巨大的潛力。
合成生物學與倫理
合成生物學對生命現象的探討從認知轉向合成,研究對象從自然生命轉向合成生命,其發展也非常迅猛,具有廣闊的應用前景,也引發了大量相關倫理問題與爭論,其主要表現在以下幾個方面。
首先,設計新生命帶來的倫理困境。人類是否具有構造新生命,打破自然約束和超越自然界限的權力?設計新生命的依據與重構的標準是什么?在多元文化交織的時代背景下,人類應該賦予新生命怎樣的道德地位?人工新生命所帶來的影響甚或危害該由誰來負責?另外,人的意志和文化將通過新生命的設計嵌入生命的進化當中,不僅將挑戰以生物進化自然法則為基礎的生命倫理,還將使人類進化的方向和前途面臨更大的不確定性。
其次,合成生物學涉及的安全風險包括生物安全和生物安保兩個方面。生物安全主要是指由于合成生物的功能以及進化的不確定性,所以導致其研究從設計、制備、存儲到運輸、應用與環境釋放等各環節都存在一定的安全風險;生物安保的重點是防止生物制劑和技術被某些群體濫用。例如,生物劑是檢測、鑒定、預防和治療等方面的基礎資源,但細菌、病毒、真菌、毒素等生物劑也可通過生物學誘導、基因改構與合成等技術被制造成生物武器。