急性腦梗死患者腸內營養喂養不耐受相關因素分析
楊婷,李玉
(中國科學技術大學附屬第一醫院,安徽 合肥 230031)
急性腦梗死(ACI)又稱急性缺血性腦卒中,是指腦血供中斷導致的腦組織壞死,多因腦動脈狹窄、堵塞所致,發病突然,具有高致殘率和高致死率[1-2]。ACI患者一般表現為半身不遂、口角歪斜、言語含糊不清等臨床癥狀,伴隨吞咽困難和意識障礙,常因難以正常進食引發營養不良,從而導致肺部感染、肌肉萎縮等一系列并發癥[3]。腸內營養(EN)是治療ACI患者營養不良的重要手段,但部分ACI患者會出現腸內喂養不耐受(EFI)[4-5]。據報道[6],30%以上接受EN支持的重癥患者會出現EFI,EFI的發生使患者達不到目標喂養量,增加敗血癥及多器官衰竭風險,影響預后。目前如何確保EN的順利實施是臨床急需解決的難題,尋找EFI發生的危險因素可以為ACI患者臨床診療提供幫助[7]。本研究回顧性分析了ACI患者的臨床資料,探討ACI患者發生EFI的可能危險因素,報告如下。
1 資料與方法
1.1 一般資料
選擇2019年6月—2021年6月收治的符合納入和排除標準的ACI患者120 例。納入標準:患者起病急,局灶或全面神經功能缺損,影像學可見責任病灶,符合ACI診斷標準[8];年齡≥18 歲;接受EN,預計EN時間≥7 d;患者臨床資料完整。排除標準:合并消化道出血、腸梗阻、嚴重器質性疾病等;胃腸道疾病史、手術史;因其他原因終止EN者;7 d內死亡者;急、慢性感染病患者。共納入120 例ACI患者,EN期間,58 例發生EFI(EFI發生組),62 例未發生EFI(EFI未發生組)。EFI診斷標準[9]:有胃腸道癥狀與體征(如嘔吐和腹脹等),EN因各種原因中斷,24 h胃殘留量(GRV)≥500 mL。本研究符合《赫爾辛基》宣言。
1.2 研究方法
收集患者電子病歷,采集以下資料。基本資料:性別、年齡、文化程度、并發癥、拉斯哥昏迷評分法(GCS)評分、急性生理與慢性健康(APACHE-Ⅱ)評分、序貫器官功能衰竭(SOFA)評分;EN監測記錄:腸鳴音、腹內壓(IAP)、乳酸、GRV、EN開始時間、營養液滲透濃度、首次營養液輸液量、達到目標喂養量時間、是否鼻飼;治療記錄:抗菌藥物、促胃動力藥、鎮靜藥、血管活性藥、益生菌、谷氨酰胺的使用以及添加膳食纖維、機械通氣、亞低溫療法。
1.3 統計學方法

2 結 果
2.1 兩組患者臨床資料比較
兩組患者年齡、并發低蛋白血癥、APACHE-Ⅱ評分、SOFA評分和凋亡抑制蛋白及EN開始時間、營養液滲透濃度、鼻飼情況比較,差異有統計學意義(P<0.05)(見表1)。
2.2 兩組患者治療相關因素比較
兩組患者抗菌藥物使用、鎮靜藥使用、血管活性藥使用、添加膳食纖維、機械通氣、亞低溫療法比較,差異有統計學意義(P<0.05)(見表2)。
2.3 ACI患者接受EN支持后發生EFI的多因素分析
以年齡>60 歲(是=1、否=0)、并發低蛋白血癥(是=1、否=0)、高APACHE-Ⅱ評分(連續變量,原值)、高SOFA評分(連續變量,原值)、IAP[>15 mmHg(1 mmHg≈0.133 kPa)=1、≤15 mmHg=0)]、EN開始時間(≥72 h=1、<72 h=0)、營養液滲透濃度(≥330 mmol/L=1、<330 mmol/L=0)、鼻飼(是=1、否=0)、抗菌藥物使用(是=1、否=0)、鎮靜藥使用(是=1、否=0)、血管活性藥使用(是=1、否=0)、添加膳食纖維(是=1、否=0)、機械通氣(是=1、否=0)為協變量,EFI(是=1、否=0)為因變量,行Logistic回歸分析,結果顯示,年齡>60 歲、高APACHE-Ⅱ評分、營養液滲透濃度≥330 mmol/L、機械通氣是ACI患者接受EN發生EFI的獨立危險因素,方差膨脹系數(VIF)<3(見表3)。
3 討 論
ACI是臨床常見的腦血管疾病,據報道我國腦梗死發病率和病死率高居世界第一,嚴重威脅到我國居民的生命健康。ACI患者會出現吞咽障礙和意識障礙,機體難以獲得充足營養,導致ACI患者營養不良,影響患者胃腸、免疫功能等,甚至并發肺部感染、心腎功能不全等疾患[10-11]。研究報道[12]早期EN對ACI患者的營養支持十分關鍵,可以提高患者免疫功能,促進患者神經功能恢復。EFI是ACI患者EN過程中的重要并發癥,是導致ACI患者暫停或終止EN的主要原因之一,會影響ACI患者臨床預后。既往文獻報道[13],重癥患者EFI發生率為30.5%~65.7%,本研究ACI患者EFI發生率為48.33%(58/120),與既往研究相符,但高于EFI平均發病率,可能與各研究EFI界定不同有關。本研究ACI患者EFI多發生在1~3 d內,該階段患者處于神經系統重創初期,機體應激反應較劇烈,更易發生EFI,因此ACI發病后3 d是防控EFI的重要階段。
本研究發現年齡>60 歲是ACI患者發生EFI的獨立危險因素。高齡患者食道括約肌松弛,易引發胃食管反流癥狀,加上高齡患者身體機能衰退,胃腸道功能減弱,腸道蠕動功能差,不利于EN攝入和胃排空。對于年齡>60 歲的ACI患者,醫護人員應盡早監測患者胃腸功能及胃腸道動力學,對有EFI先兆的患者及時調整EN途徑,保障EN順利實施。本研究結果表明,高APACHE-Ⅱ評分是ACI患者發生EFI的獨立危險因素。APACHE-Ⅱ評分反映患者病情嚴重程度,劉華等[14]報道APACHE-Ⅱ評分越高,患者越容易發生EFI。高APACHE-Ⅱ評分患者病情更嚴重,機體應激反應強烈,胃腸功能及耐受性下降,患者對營養液難以耐受,更易發生EFI。對于高APACHE-Ⅱ評分ACI患者,醫護人員同樣應該加強監測,及時評估有無EFI發生風險,避免EFI發生。本研究發現營養液滲透濃度≥330 mmol/L是ACI患者發生EFI的獨立危險因素。吳超等[15]發現接受EN支持的患者應用低滲透濃度的營養液治療效果及耐受性都更理想。營養液滲透濃度過高會刺激消化道腺體,引起強烈肌肉活動,加上為了使ACI患者盡早達到目標喂養量,短期內營養液的大量輸入超過腸道吸收極限,導致患者出現EFI。對于營養液滲透濃度過高的患者,可以在營養液中加入生理鹽水降低滲透濃度,利于腸道吸收,還可以根據患者GRV調整輸注速率。本研究結果表明,機械通氣是ACI患者發生EFI的獨立危險因素。ACI患者換氣功能較差,多數ACI患者需要進行機械通氣,而機械通氣會導致患者胸腔內壓力升高,影響心輸出量,胃腸道供血不足,從而影響患者胃腸道功能,同時機械通氣還會損傷患者食管括約肌功能,導致胃食管反流,繼而出現EFI。對于接受機械通氣治療的患者,不僅要及時評估胃腸功能,還要監測呼吸功能,對可以進行自主呼吸的患者盡早停止機械通氣,減少EFI發生。張偉等[16]對危重癥患者EFI危險因素進行分析,發現年齡>60 歲、高APACHE-Ⅱ評分、機械通氣是危重癥患者EFI危險因素,與本研究相符。但本研究另外發現營養液滲透濃度≥330 mmol/L也是EFI危險因素,曹金鳳等[17]在早期也發現高營養液濃度會導致EFI發生。由于研究樣本有限,來源單一,需進一步對結果進行驗證。
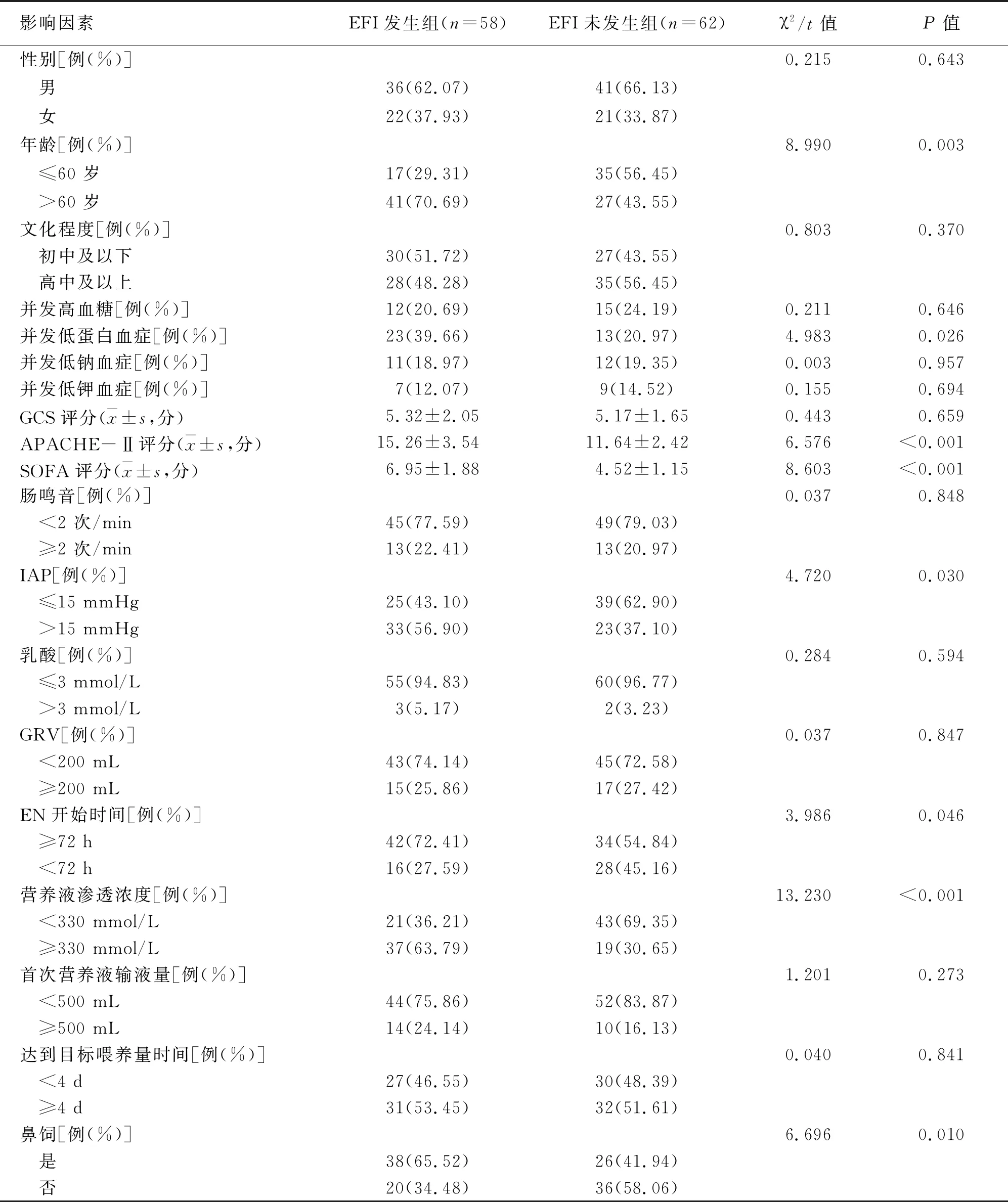
表1 兩組患者臨床資料比較
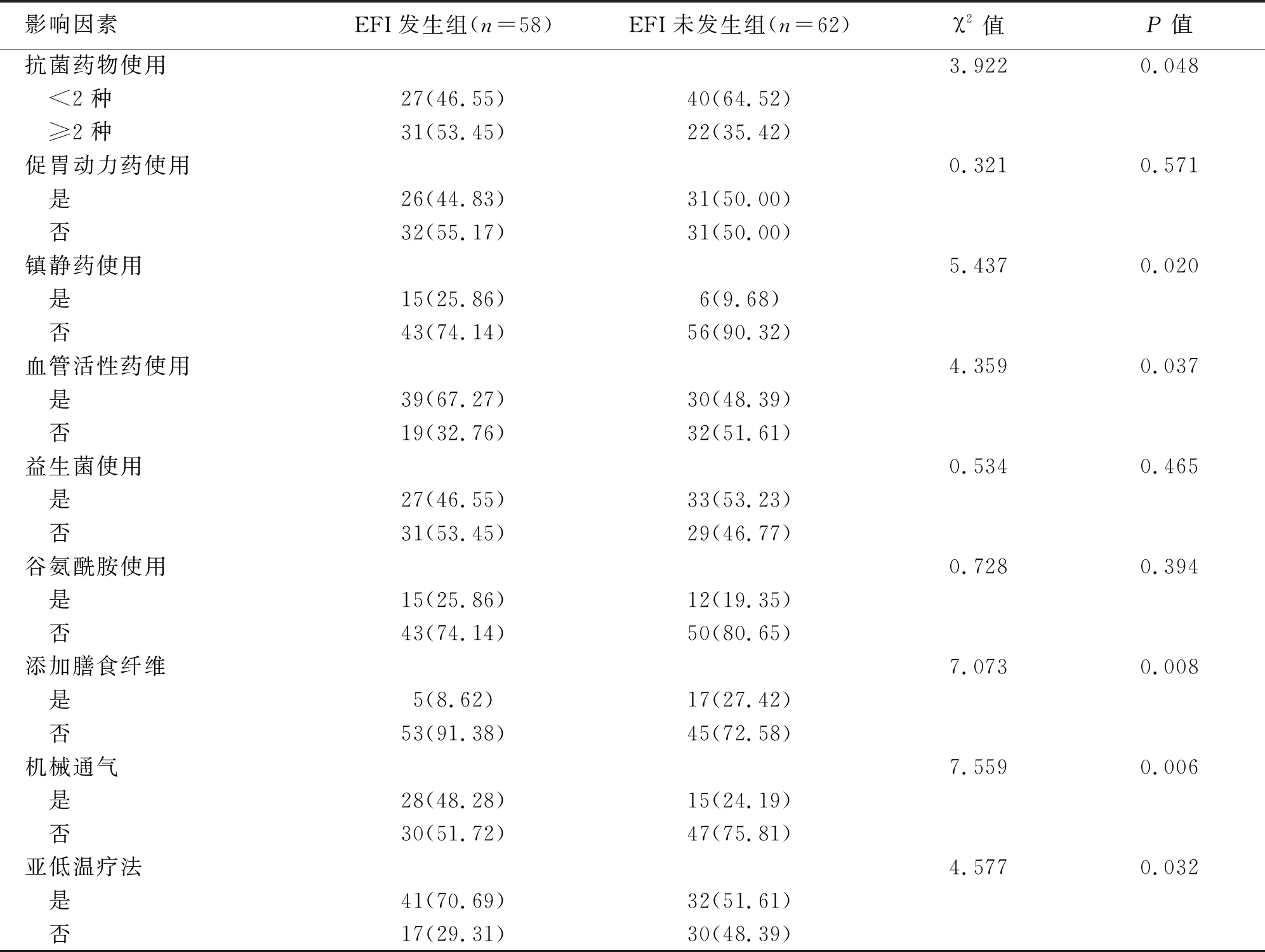
表2 兩組患者治療相關因素比較 單位:例(%)
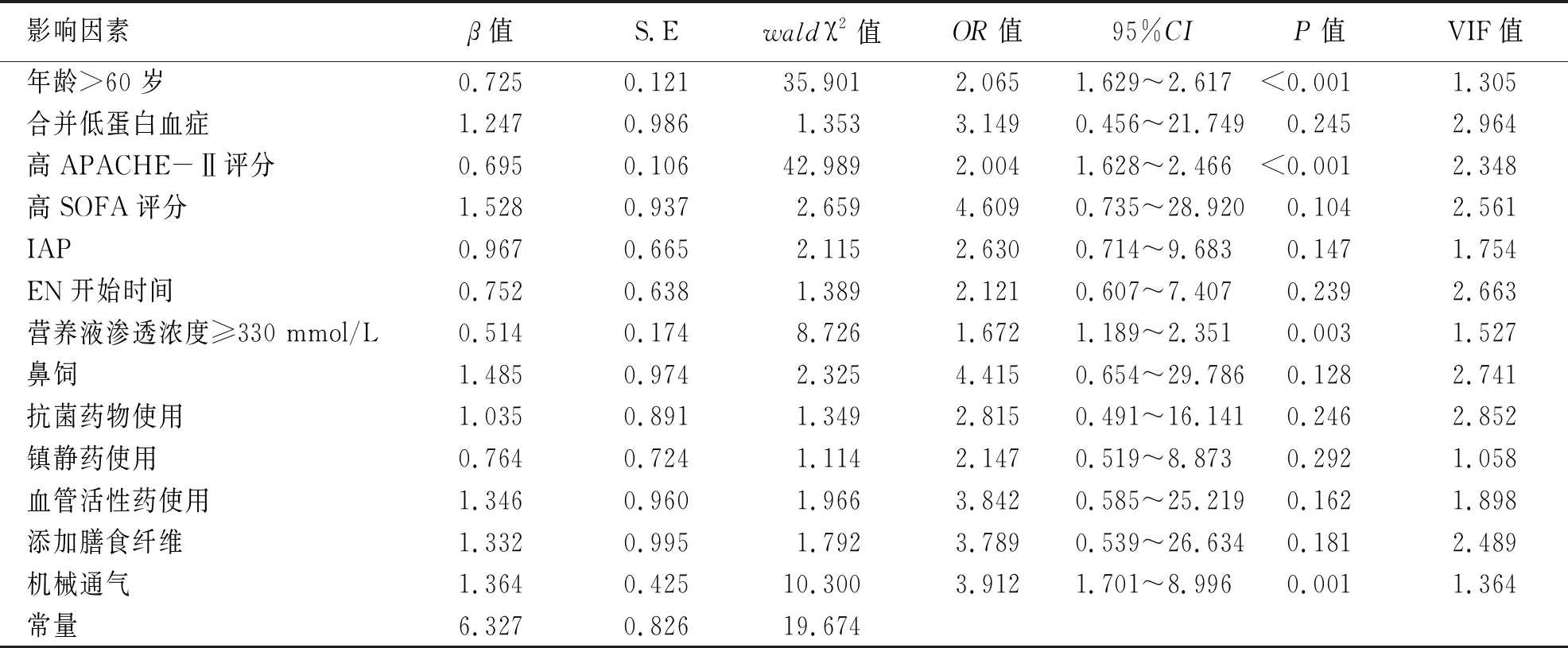
表3 ACI患者接受EN支持后發生EFI的多因素分析
綜上所述,ACI患者采取EN支持措施易發生EFI,年齡>60 歲、高APACHEⅡ評分、營養液滲透濃度≥330 mmol/L及機械通氣是ACI患者EFI的獨立危險因素,對可控危險因素采取合理護理可以降低EFI發生率。

