用于超級電容器的二硫化鉬納米片制備及電化學性能研究
張 蕊,王幼琪,沈培智,2
(1.湖北汽車工業學院材料科學與工程學院,十堰 442002;2.儲能與動力電池湖北省重點實驗室,十堰 442002)
0 引 言
隨著環境污染與能源枯竭問題逐漸凸顯,綠色能源的開發與存儲備受人們關注。超級電容器具有充放電速度快、工作溫度范圍寬和壽命長的優點,被認為是最具發展潛力的能量儲存和轉換裝置之一[1-2]。電極材料作為超級電容器的重要組成部分,對電容器的儲能能力起著決定性作用[3]。近年來,層狀過渡金屬硫化物由于獨特的結構和性能,成為電極材料研究熱點之一[4]。
鑒于目前納米MoS2制備方法普遍存在產率低、成本高、不易規模化生產的問題,本文采取高溫固相燒結-球磨法制備MoS2納米片并用于超級電容器活性材料。本方法工藝簡單、成本低、樣品性能穩定,具有一定的研究和應用前景。
1 實 驗
1.1 納米MoS2制備
以Na2MoO4·2H2O和(NH2)2CS為鉬源及硫源,按不同鉬硫比(摩爾比1∶10、1∶15、1∶30)混合后,當爐溫升至燒結溫度(700~900 ℃),將盛有原料粉末的瓷舟逆著氮氣保護氣方向推入管式爐,保溫2 h后隨爐冷卻至室溫,得到燒結產物。稱取一定質量燒結粉末以及直徑3 mm的氧化鋯磨球(球料質量比為50∶1)置于瑪瑙罐中,在行星球磨機中于不同轉速下(300~700 r·min-1)球磨10 h,制得納米MoS2。本實驗所用原料以及市售MoS2對比樣(上海麥克林生化有限公司)均為分析純。
1.2 電極片及超級電容器的制備
將活性物MoS2、導電石墨和摩爾分數5%的聚偏氟乙烯(PVDF)按質量比8∶1∶1混合,滴入適量N-甲基吡咯烷酮(NMP)攪拌至均勻糊狀。將糊狀物均勻刮涂在泡沫鎳片(1 cm×1 cm)上并于120 ℃干燥5 h后,在壓片機中以10 MPa壓力壓制成電極片,其中活性物質量控制在0.001~0.002 g。使用定性濾紙作為隔膜,0.1 mol·L-1KOH作為電解質溶液,組裝成對稱型超級電容器。
1.3 樣品表征及電化學測試
利用SDT-Q600型熱重-差示掃描量熱儀(TG-DSC,賽默飛世爾科技有限公司)、DX-2700型X射線衍射儀(XRD,丹東浩圓儀器有限公司)、JSM-7900F型掃描電子顯微鏡(SEM,日本電子株式會社)對樣品的熱穩定性、物相和微觀形貌進行表征。
根據樣品XRD衍射峰的強度計算MoS2的層數[22],如公式(1)所示:
(1)
式中:L為層數;I100和I103分別為(100)和(103)衍射峰的強度。
采用CHI660D電化學工作站(上海辰華儀器有限公司)對電極材料及組裝的超級電容器進行循環伏安(cyclic voltammetry, CV)、恒電流充放電(galvanostatic charge/discharge cycling, GCD)、電化學阻抗(electrochemical impedance spectroscopy, EIS)測試。交流阻抗測試頻率為10-2~105Hz。三電極測試體系中的工作電極、對電極和參比電極分別是待測電極片、鉑電極和飽和甘汞電極(SCE),電解質溶液為0.1 mol·L-1KOH溶液,測試均在室溫下進行。
根據CV和GCD曲線,分別由公式(2)和(3)計算樣品的比電容:
(2)
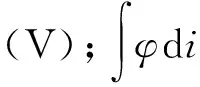
(3)
式中:I為恒電流(A);Δt為放電時間(s);ΔU為電勢差(V)。
2 結果與討論
2.1 高溫固相燒結制備MoS2
為確定燒結溫度區間,在氮氣氣氛中分別對(NH2)2CS以及Na2MoO4·2H2O和(NH2)2CS的混合物(摩爾比1∶15)進行TG-DSC測試,結果如圖1所示。本文將(NH2)2CS熱分解過程分成四個階段:① 室溫~180 ℃溫區,TG曲線保持穩定,DSC曲線也未觀察到明顯的吸熱或放熱峰。② 180~200 ℃溫區,TG曲線無明顯變化,DSC曲線出現明顯的吸熱峰,主要歸結為(NH2)2CS(熔點為176~178 ℃)熔化吸熱。③ 200~300 ℃溫區,(NH2)2CS樣品的失重率達到89.7%,DSC曲線也出現明顯的吸熱峰,主要是由于(NH2)2CS發生分解,生成NH2CS和硫化氫氣體(H2S),反應機理如式(4)所示。④ 300 ℃以上溫區,(NH2)2CS異構化反應生成的NH4SCN會和分解產物NH2CS發生反應生成硫氫酸胍(見式(5)和(6))并逐漸分解。
(4)
(NH2)2CS?NH4SCN
(5)
(6)
圖1(b)為Na2MoO4·2H2O和(NH2)2CS混合物(摩爾比為1∶15)的熱重分析曲線。在90 ℃附近,樣品出現微量失重,DSC曲線對應出現小吸熱峰,這主要歸因于原料的脫水;180 ℃附近DSC曲線上的吸熱峰主要是由(NH2)2CS熔融吸熱所引起。在200~650 ℃溫區,樣品失重率達82.3%,在此階段(NH2)2CS熱分解產生的H2S氣體(見式(5))與Na2MoO4反應生成MoS2,見式(7)所示;當溫度高于650 ℃,TG曲線無失重,表明燒結反應完成。
(7)
由以上分析可知,在氮氣氣氛中(NH2)2CS的熱分解溫區(180~300 ℃)與(NH2)2CS和Na2MoO4·2H2O生成MoS2的反應完成溫度(650 ℃)存在較大差異,因此本文采用氮氣為保護氣的到溫進料燒結方式。
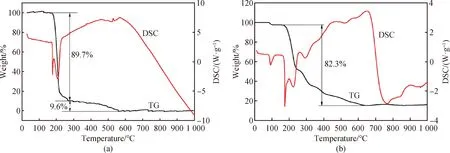
圖1 硫脲(a)、硫脲和鉬酸鈉混合物(b)的熱重-差示掃描量熱圖Fig.1 TG-DSC diagrams of thiourea (a), mixture of thiourea and sodium molybdate (b)
圖2是不同條件下制得樣品的XRD圖譜。經分析可知,當原料中鉬硫比大于等于1∶15,經750 ℃燒結2 h制備樣品(見圖2(a)),以及鉬硫比為1∶15,在不同燒結溫度(700~900 ℃)下制備樣品(見圖2(b))的XRD圖譜衍射峰與標準卡PDF 65-0160的衍射峰相吻合,且無雜峰出現,表明鉬硫比高于1∶15原料粉末,在氮氣氣氛中700~900 ℃燒結2 h可制得2H-MoS2。
圖3(a)~(f)為市售MoS2與700~900 ℃燒結制備MoS2的SEM照片。市售MoS2的形貌(見圖3(a))為1~10 μm的塊狀顆粒。700 ℃燒結樣品(見圖3(b))由亞微米至數微米厚薄不等的片狀顆粒相互堆疊構成;750 ℃燒結樣品形貌(見圖3(c))呈片狀,厚度較為均勻且堆疊現象較700 ℃制備樣品明顯減少;800 ℃燒結樣品形貌(見圖3(d))也為片層狀,但層厚比750 ℃樣品薄且出現相互交疊團聚;850 ℃燒結樣品(見圖3(e))呈現的片層狀顆粒邊緣圓滑并團聚成十幾微米大小的不規則二次顆粒;900 ℃燒結樣品形貌(見圖3(f))呈現類球狀顆粒的團聚體。
圖3(g)為不同燒結溫度下制備樣品的形貌變化示意圖。根據上述各項測試,解釋如下:在700 ℃,Na2MoO4·2H2O和(NH2)2CS混合物生成片層狀相互間堆疊的MoS2。當燒結溫度提高至750 ℃,硫源分解速率加快,生成的大量H2S氣體可將堆疊顆粒剝離,因此樣品呈現出高分散片層狀形貌。溫度進一步升至800 ℃,硫源的分解速率更快,單位時間內H2S濃度進一步增加,進而提高了產物形核數目,導致片層顆粒狀數量增大、厚度變薄。此外,為了降低顆粒表面的表面能,片狀微粒之間出現團聚現象。燒結溫度達到850 ℃,高溫下樣品表面揮發速度增大,導致片層狀顆粒邊緣變得圓滑,同樣也進一步導致900 ℃燒結樣品的形貌從片層狀顆粒的團聚體轉變為類球形顆粒的團聚體。
2.2 高溫固相燒結-球磨法制備納米MoS2
將750 ℃燒結制備MoS2粉末在球磨機中于不同轉速下球磨10 h,粉末經過水洗,離心分離,用激光筆照射離心分離上層清液可觀測到清晰的丁達爾現象,如圖4(a)~(c)所示。隨著球磨速度的提高(500/600/700 r·min-1),離心分離上清液的顏色逐漸加深,溶液中激光光路亮度不斷提升,該現象表明球磨轉速的增加有助于獲得粒徑小、難沉降的粉體顆粒。
圖4(d)~(f)分別是在500、600、700 r·min-1轉速下球磨10 h后制得粉末的SEM照片。由圖4(d)可看出,在500 r·min-1轉速下球磨10 h獲得的樣品是亞微米顆粒團聚成二次粉末的聚集體;當球磨轉速提高至600和700 r·min-1時,從圖4(e)和4(f)中可清晰觀察到片層狀的顆粒形貌,以及由于外力作用發生剝離而產生的裂紋。

圖4 不同球磨轉速下制得樣品的清液中的丁達爾現象(a)~(c)及其SEM照片(d)~(e)。(a)、(d)500 r·min-1;(b)、(e)600 r·min-1;(c)、(f)700 r·min-1Fig.4 Tydall phenomenon photos in solution and SEM images of the samples obtained by ball milling at different speeds. (a), (d) 500 r·min-1; (b), (e) 600 r·min-1; (c), (f) 700 r·min-1
圖5為不同球磨轉速下制備樣品的XRD圖譜。從圖中可以看出,各樣品的衍射峰均與標準卡PDF 65-0160完全對應,確定為MoS2。隨著球磨轉速逐漸增大,樣品衍射峰的強度逐漸降低并且峰寬逐漸增加。這表明隨著轉速增大,粉末的晶粒尺寸變小,該結果與樣品的微觀形貌變化趨勢相吻合。采用公式(1)計算出的球磨前以及300、400、500、600和700 r·min-1球磨轉速下得到的樣品層數分別為156以及109、102、96、91和88層。
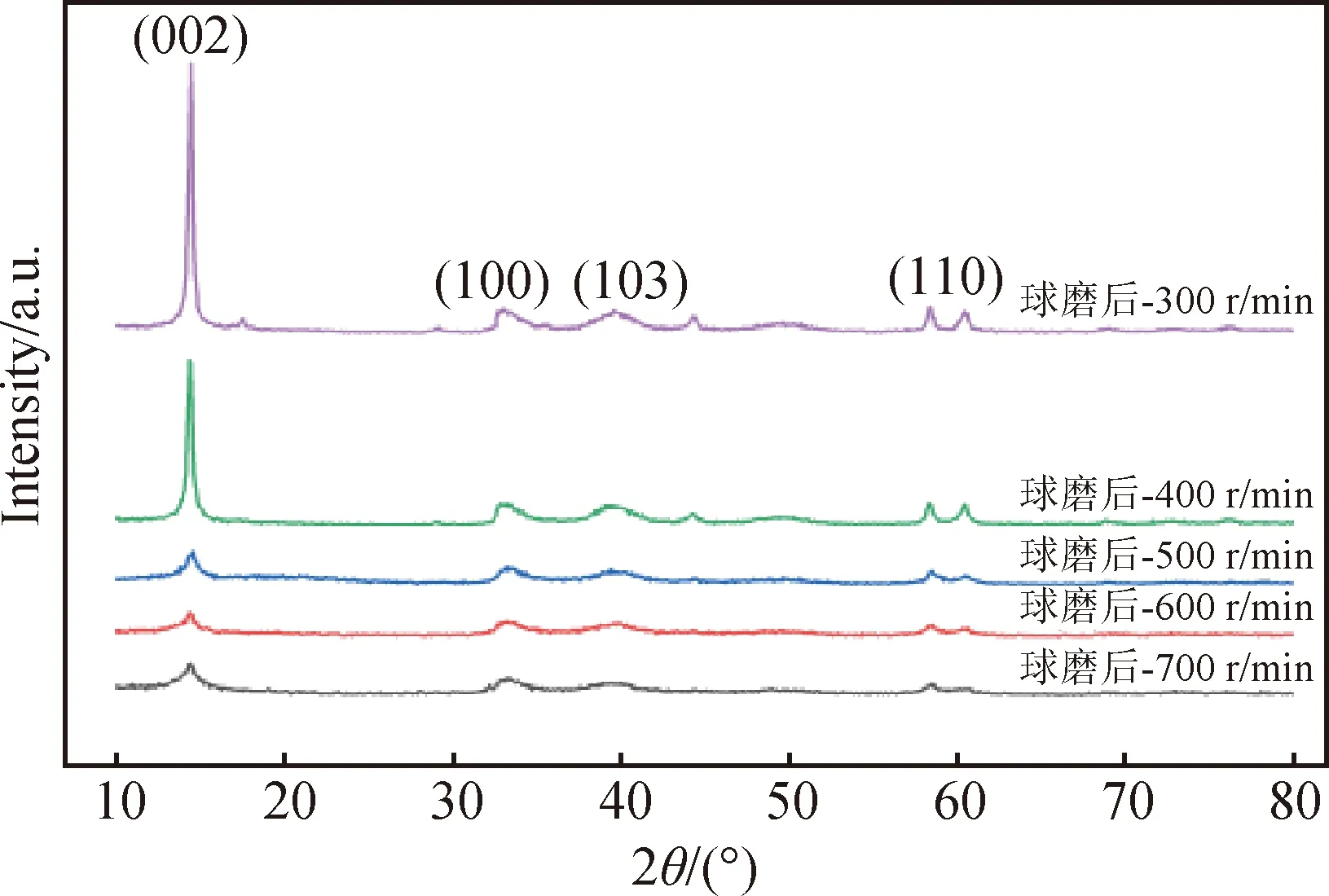
圖5 不同球磨轉速下制備樣品的XRD圖譜Fig.5 XRD patterns of samples prepared by ball milling at different speeds
2.3 樣品的電化學性能
圖6(a)為市售MoS2以及不同溫度燒結制備MoS2在掃速5 mV·s-1時的CV圖。圖6(a)中對稱的矩形圖上出現了明顯的氧化還原峰,表明該MoS2在充放電過程中表現出明顯贗電容特征,這是由于片狀MoS2的邊緣具有不飽和鍵,可以結合與釋放電子,從而造成充放電過程中氧化還原的發生[23-24]。此外,750 ℃燒結制備樣品的CV曲線所包含的面積最大,而市售MoS2的最小,表明750 ℃制備樣品的比電容優于其他溫度制備樣品以及商業化MoS2的比電容。圖6(b)為750 ℃燒結制備MoS2在不同轉速下球磨10 h制備樣品的CV曲線。從圖6(b)可以看出,CV曲線呈向右下方微傾斜的類矩形,對稱性較好,但未觀察到明顯的氧化還原峰。由于高能球磨過程中粉末在機械力強烈作用下被粉碎,顆粒斷裂面會產生新的不飽和鍵和帶電的結構單元。這種處于不穩定高能狀態的粉碎顆粒易團聚且會和粉末表面所吸附的氣體(如O2)發生反應,導致顆粒中的不飽和鍵破壞,這可能是干法球磨樣品CV曲線中未出現氧化還原峰的重要原因。隨著球磨轉速由300 r·min-1增至700 r·min-1,樣品CV曲線包圍的面積也隨之增加,根據公式(2)計算得到球磨轉速為600、700 r·min-1時樣品的比電容分別為78.4、82.6 F·g-1,高于球磨前樣品的55 F·g-1及市售MoS2的5.6 F·g-1。
分別用750 ℃燒結的未球磨和700 r·min-1球磨10 h的MoS2樣品作為電極活性材料組裝成對稱型超級電容器器件測試材料的電化學性能。圖7(a)和7(b)分別是由球磨前后樣品在不同充放電電流密度下的恒流充放電曲線。對比圖7(a)和7(b)可知,恒流充放電曲線整體呈類三角形,在相同電流密度下球磨后樣品的充電和放電時間(見圖7(b))均大于球磨前樣品的對應值。根據公式(3)計算出在電流密度為0.5、1和2 A·g-1時,未球磨樣品比電容分別為54.6、38.4和24.6 F·g-1,相應的球磨樣品比電容則分別為82.4、69.7和62.9 F·g-1(比電容較球磨前分別提高51%、81.5%和155%)。
圖7(c)為在0.5和1 A·g-1的充放電電流密度下,球磨前后MoS2樣品的比電容與循環次數關系曲線。在電流密度為0.5 A·g-1下循環2 000圈,未球磨樣品比電容由初始54.6 F·g-1降低至39.5 F·g-1(比電容保持率為72.3%),而球磨后樣品的比電容則是由初始82.4 F·g-1降低至76.1 F·g-1(比電容保持率為92.4%)。將電流密度提高至1 A·g-1繼續循環2 000圈,未球磨樣品比電容由24.0 F·g-1降低至17.3 F·g-1(比電容保持率為71.9%),球磨后樣品的比電容則由60.9 F·g-1降低至55.4 F·g-1(比電容保持率為91.7%),實驗結果表明球磨后MoS2的比電容和電容保持率都遠優于未球磨樣品的相應值。圖7(d)為球磨前后樣品的交流阻抗譜。與未球磨樣品阻抗圖對比,球磨后樣品阻抗圖中高頻區圓弧半徑明顯減小,低頻區斜線的斜率增大,表明經過球磨制得MoS2樣品的電阻、樣品與電解液間的電阻均有明顯減低。

圖7 球磨前后樣品的電化學性能。未球磨(a)與球磨后(b)樣品在不同電流密度下的恒電流充放電曲線;(c)球磨前后樣品的比電容-循環次數關系圖;(d)球磨前后樣品的交流阻抗圖Fig.7 Electrochemical properties of samples before and after ball milling. CV curves of unmilled samples (a) and ball milled samples (b) at different current densities; (c) specific capacitance-cycle number relationship plots of unmilled and ball milled samples; (d) AC impedance plot of unmilled and ball milled samples
3 結 論
本文以鉬酸鈉和硫脲為原材料,采用高溫固相燒結結合球磨法制備MoS2納米片。當鉬硫比為1∶15,采用到溫進料方式在氮氣保護氣中于750 ℃燒結2 h所制備MoS2的微觀形貌呈均勻薄片狀,繼續在700 r·min-1下球磨10 h,樣品片層數由156層減少至88層。電化學性能測試發現,CV曲線和GCD曲線分別呈現對稱性良好的類矩形和類三角形。將樣品組裝成對稱型超級電容器,在0.5 A·g-1和1 A·g-1的電流密度下,球磨前(后)的MoS2比電容分別為54.6 F·g-1(82.4 F·g-1)和24.0 F·g-1(60.9 F·g-1),依次經過各2 000圈充放電循環,球磨前后電容保持率分別達72.3%和92.4%。高溫固相燒結結合球磨法所制備的MoS2納米片具有較好的綜合電化學性能,具有一定的研究和應用前景。

