1 例異基因造血干細胞移植后繼發腸道急性移植物抗宿主病患兒腸外營養治療藥學監護實踐*
吳石威,寧麗娟,劉 湘△
(1. 湖南省湘潭市中心醫院,湖南 湘潭 411100; 2. 中國科學技術大學附屬第一醫院,安徽 合肥 230061)
近年來,隨著供體和受體選擇、移植前處理、感染、移植物抗宿主病(GVHD)等并發癥防治方法的不斷改善,患者移植后存活率升高。異基因造血干細胞移植(allo-HSCT)成為各種血液、腫瘤和先天性疾病的重要治療方法[1-2]。根據國際血液和骨髓移植研究中心的提供數據,行造血干細胞移值(HSCT)術患者每年超60 000例[3]。來自供體的免疫細胞攻擊健康的受體組織如胃腸道、肝臟、皮膚和肺,導致GVHD,表現為急、慢性,是主要的致死性并發癥之一,極大地限制了HSCT的有效性[4]。急性GVHD(aGVHD)的發病率因若干臨床變量而存在差異,HSCT 受者累計發病率為40%~80%,其中胃腸道aGVHD 的累計發病率為60%[5]。除嚴重腹瀉和嘔吐外,臨床癥狀還包括腹痛、痙攣、惡心、胃腸道出血和吞咽困難,可導致營養吸收不良、脫水、嚴重的電解質損失和體質量減輕[6]。使用免疫抑制劑產生的營養相關不良反應,嚴重惡化HSCT 受者的營養狀況,影響存活[7-8]。故營養治療對改善HSCT 患者的預后至關重要。本研究中分析了臨床藥師參與1 例allo -HSCT 后繼發腸道aGVHD 患兒營養治療的藥學監護實踐。現報道如下。
1 臨床資料
1.1 病例資料
患兒,6 歲,身高112 cm,體質量18.2 kg,體質量指數14.51 kg/ m2。因“急性粒細胞性白血病部分分化型(M2型)化療后1.5年,擬行臍血移植”于2019年4月19日入院。入院予“氟達拉濱+ 白消安+ 環磷酰胺”強化清髓預處理后,4月27日行臍帶血移植,移植后出現重度植入前綜合征(PES),給予糖皮質激素等治療后好轉,中性粒細胞植入(簡稱粒系植入)后仍有重度胃腸道aGVHD,表現為惡心嘔吐、反復腹瀉、消化道出血、腸梗阻等。6月8日,患兒粒系植入可,經對癥治療后皮疹、腹瀉、消化道出血等癥狀均較前好轉,遂轉出HSCT 病房行下一階段治療。轉出時,體格檢查示,患兒目前仍有不全性腸梗阻及消化道出血,持續胃腸減壓中,神志清,精神一般,全身皮膚未見可見陳舊性皮疹,咽部無充血,雙肺聽診呼吸音清,未聞及明顯干濕羅音,腹部無壓痛。轉入診斷:急性粒細胞性白血病;臍血移植術后;急性移植物抗宿主病;消化道出血;巨細胞病毒感染;腸梗阻。
1.2 治療經過
患兒入駐HSCT 病房期間,臨床醫師制訂腸外營養配方1,對患兒進行全腸外營養支持。其中,總能量625 kcal(1 kcal ≈4.184 kJ),氨基酸21.25 g,糖脂比63∶37,總液量607 mL,輸注方式為單瓶輸注(表1)。6月8日,轉入普通病房,患兒體質量16.3 kg、較前下降,白蛋白32.6 g/L,前白蛋白165 mg/L,低于正常值。針對患兒營養不良等問題,6月10日。臨床醫師請臨床藥師會診,臨床藥師對患兒進行綜合評估后,予調整腸外營養支持配方2。其中,總能量927 kcal,氨基酸29.25 g,糖脂比63∶37,總液量797 mL,輸注方式為全合一輸注(表1)。臨床醫師采納。在腸外營養治療過程中,臨床藥師定期對患兒的營養治療情況進行監護,關注營養相關監測指標(表2)。7月14日,患兒經營養支持、免疫抑制、抗感染、止血、輸血小板、調節腸道菌群、止吐護胃等對癥治療后,腹瀉、消化道出血較前明顯好轉,胃腸道功能逐步恢復。復測體質量17.5 kg,較前升高,白蛋白較前恢復(34.5 g/L)、前白蛋白正常(215 mg/L)。表明經臨床藥師給予營養干預后,患兒營養狀況改善,且未發生營養相關不良反應,指標較前改善,開始由腸外營養向腸內營養過渡。HSCT患兒營養治療時間軸見圖1。
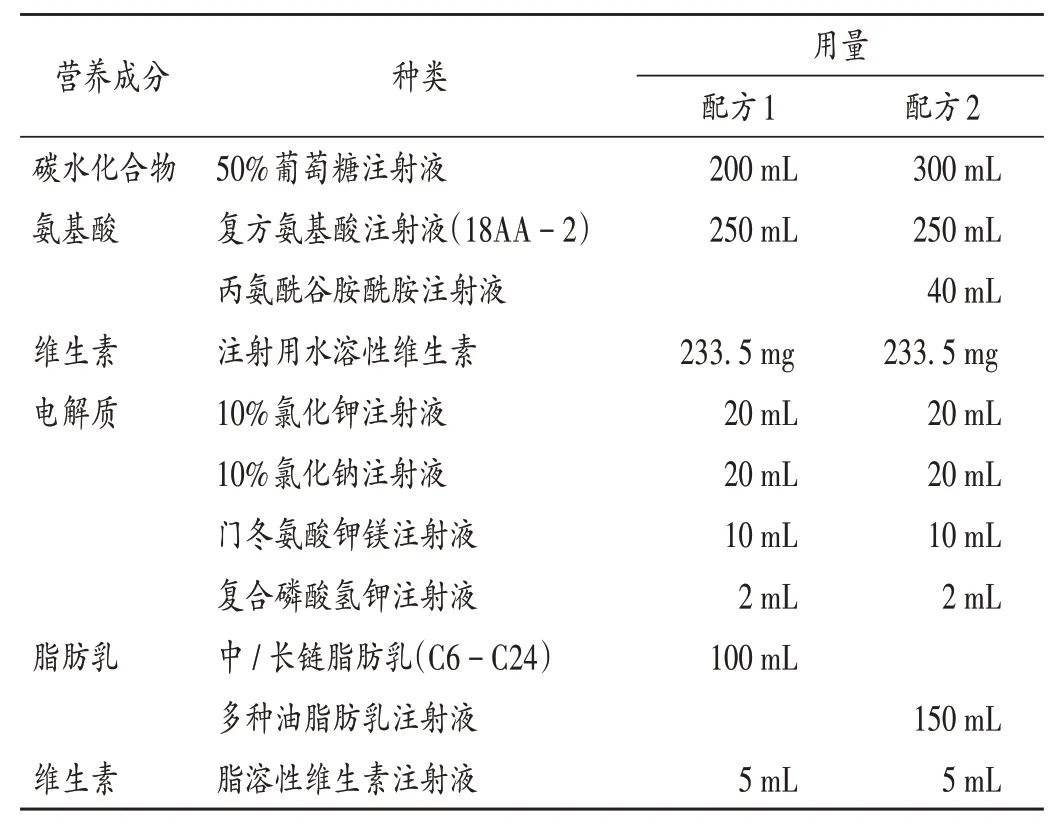
表1 患兒腸外營養支持方案Tab.1 Parenteral nutrition support plan for the child

表2 HSCT患兒腸外營養治療時監測指標Tab.2 Monitoring indicators of parenteral nutrition in the child with HSCT
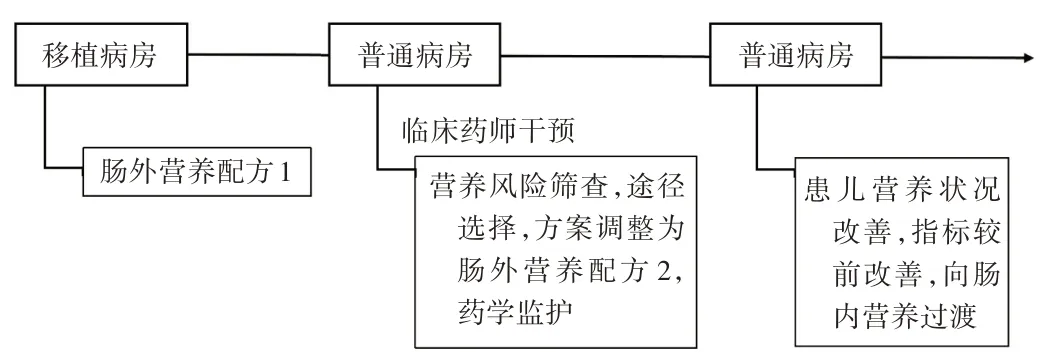
圖1 HSCT患兒營養治療時間軸Fig.1 Timeline of nutritional therapy for the child with HSCT
2 討論
2.1 HSCT 患兒的營養風險篩查
HSCT 患兒常需接受高劑量化學治療(簡稱化療),化療引起的系列不良反應(如惡心、嘔吐、黏膜炎、腹瀉、感染等)會影響患兒的營養攝入,導致臨床不良結局。《腫瘤患者營養支持指南》指出,HSCT 患者入院時應行營養篩查,入院后每周監測營養狀況、營養攝取及消耗情況,保證每日充分的營養素攝入,對營養不足患者應及時給予營養支持,避免體質量進一步丟失[9]。對于成年患者,如營養風險篩查2022(NRS2002)工具在成年患者臨床應用中效果良好,獲得美國腸內腸外營養學會(ASPEN)、歐洲腸內腸外營養學會(ESPEN)、中華醫學會腸外腸內營養學分會(CSPEN)等多個權威機構認可。考慮兒童生長發育的動態評價等問題,目前尚無世界公認的兒童營養風險篩查工具[10]。歐洲兒科胃腸肝病及營養學會于2010年推出重癥兒童營養調查(STAMP)量表[11-12],以評估住院兒童是否存在營養不良風險,目前臨床應用較為廣泛。因此,臨床藥師首先采用STAMP 量表對患兒進行營養風險篩查,結果評分>4分,提示患兒轉入普通病房時仍為營養不良高風險,仍需繼續進行積極的人工營養干預,以改善臨床結局。
2.2 初始腸外營養治療方案的分析
2.2.1 營養治療途徑選擇
營養支持治療時,在腸道功能基本正常情況下,應優先考慮口服營養補充(ONS)或腸內營養。越來越多的證據表明,腸內營養在兒童HSCT 期間是可行的,較腸外營養更能降低GVHD 發病率、住院時間、血小板計數恢復時間,產生更多臨床獲益[9,13-14]。但ESPEN 指南指出,對于HSCT 患者,當有嚴重的黏膜炎、頑固性嘔吐、腸梗阻、嚴重吸收不良、長期腹瀉或有癥狀的GVHD時,可選擇腸外營養,且allo-HSCT 患者可能需要更頻繁和更長時間的腸外營養治療[14]。一項隨機對照和對照試驗表明,與標準腸外營養支持相比,由藥師參與調控的個體化腸外營養方案在體質量增加和縮短住院時間方面具有優勢[14]。本例患兒存在嚴重急性腸道GVHD、消化道出血、不完全性腸梗阻、反復腹瀉,故選用全腸外營養支持(TPN)途徑進行營養治療。轉入普通病房后,臨床藥師綜合評估患兒的臨床狀況,選擇繼續進行個體化的全腸外營養支持,同時調整營養支持配方。
2.2.2 給予全合一方式腸外營養
全合一方式給予腸外營養是指將人體需要的碳水化合物、氨基酸、脂肪乳、電解質、微量元素、維生素等營養素按一定比例配制于輸液袋中成為全營養混合液(TNA),經腸外途徑用于患者。較單瓶輸注或多瓶串輸更有利于營養管理,可減少代謝并發癥,降低感染風險,提高營養物質的利用,同時可整合靜脈用藥,有助于液體管控[15]。本例患兒轉入普通病房前腸外營養支持方案將脂肪乳、脂溶性維生素與其他營養素分開輸注,不利于營養素的有效利用,且易增加不良風險;臨床藥師詢問患兒前期腸外營養用藥史,結合近期實驗室營養相關檢查指標(如血糖、血脂、肝腎功能、電解質等)無明顯異常,判斷患兒近段時間腸外營養治療耐受可,故將營養方案調整為全營養混合液,經中心靜脈以全合一的方式滴注。臨床醫師采納。
2.2.3 能量和氨基酸目標需要量分析
少量證據顯示,腸道GVHD 患者的能量消耗有所增加[8]。但指南推薦,對于allo-HSCT 患兒接受腸外營養支持時的目標能量需要量少,大多針對成年患者。ASPEN 在兒科重癥患者的營養支持指南中建議,通過間接量熱法(IC)確定能量需求,并指導每日能量目標的處方,若IC 不能實施,則建議使用Schofield 方程式來估算能量消耗。但多項隊列研究表明,大多數公布的預測方程都不準確,可能導致意外的過度喂食或喂食不足[16]。《中國兒科腸內腸外營養支持臨床應用指南》(以下簡稱《兒科指南》)指出,對于6歲兒童,每日能量推薦用量為40~60 kcal/(kg·d),脂肪用量為1~2 g/(kg·d),建議使用20%脂肪乳劑,選擇中長鏈脂肪乳劑,如有條件,也可選擇橄欖油/大豆油混合制劑),碳水化合物8~10 g/(kg·d),且葡萄糖攝入應占非蛋白熱卡的60%~75%,同時注意電解質、維生素等微量營養素的補充[17]。該患兒轉入時體質量16.3 kg,初始營養方案提供的能量為625 kcal/(kg·d),已不能滿足患兒的能量需要,需調整配方。
根據《兒科指南》,6 歲兒童氨基酸每日用量為1~2 g/(kg·d),可使用成人平衡型氨基酸[17]。文獻[8]指出,腸道GVHD 患者的蛋白質需求可能增加,如長期使用大劑量的糖皮質激素可導致增加對蛋白質的需求,以及由于黏膜表面損害或發炎可造成黏膜滲出而失去蛋白質,建議存在營養不良和嚴重并發癥(如GVHD)的患者蛋白質目標需要量為1.8~2.5 g/(kg·d);癥狀輕微、無嚴重營養不良則為1.5~1.8 g/(kg·d)。腸外營養配方1 中氨基酸供應量為21.25 g,對于存在嚴重腸道GVHD、低蛋白血癥的患兒,氨基酸供應量可能不足。
2.3 腸外營養治療方案調整
轉入普通病房后,臨床藥師會診協助,調整腸外營養支持方案,臨床醫師采納會診意見。腸外營養配方2提供的能量為927 kcal,氨基酸為29.25 g,葡萄糖用量為9 g/(kg·d),脂肪用量為1.8 g/(kg·d),葡萄糖提供的熱量占非蛋白熱卡的63%,同時繼續補充電解質、維生素等微量營養素,能滿足患兒需要[17]。
多種油脂肪乳是由大豆油、中鏈脂肪乳、橄欖油、魚油(ω-3多不飽和脂肪酸)和維生素E 物理混合成的脂肪乳劑,通過添加ω-3多不飽和脂肪酸調整ω-3與ω -6 脂肪的比例。研究表明,ω -3 多不飽和脂肪酸可作為免疫調節因子,通過抑制炎性細胞因子和血管內皮損傷的產生及通過改善總體免疫功能來下調炎性反應,減輕細胞因子風暴,有助于降低HSCT 后并發癥的發生率。因此,對于allo - HSCT 患者使用ω - 3 脂肪酸可能在減少嚴重GVHD方面獲益。此外,添加ω-3脂肪酸還可能有助于維持脂質攝入熱量的比例和三酰甘油的最佳水平,維持肝功能,減少感染并發癥等[8,18]。因此,臨床藥師將原方案中的脂肪乳替換成添加了含ω - 3多不飽和脂肪酸的多種油脂肪乳,使患兒獲益。
盡管ESPEN 指南中指出,缺乏充分且一致的臨床數據來提出使用谷氨酰胺改善HSCT 腫瘤患者臨床結局的建議[14]。但已有研究證明,補充谷氨酰胺可恢復胃腸黏膜的完整性并減少腫瘤治療期間的細菌移位,調節免疫系統在消化道中的功能,還可促進腸道愈合,并減輕GVHD的嚴重程度[8]。對于本例存在腸道aGVHD的患兒,補充谷氨酰胺可能有助于促進其腸道黏膜修復,減少腸道蛋白丟失,改善消化道出血。因此,臨床藥師在調整腸外營養配方時加入丙氨酰谷胺酰胺注射液,由于丙氨酰谷氨酰胺提供的氨基酸量不應超過全部氨基酸供給量的20%。最終加入40 mL丙氨酰谷胺酰胺。
患兒的微量營養素供給可參考《兒科指南》。存在腸道GVHD 的患者由于經歷營養和代謝紊亂,對微量營養素的需求和代謝可能會改變,HSCT 中尚未確定微量營養素的最佳劑量,應根據監測結果個體化調整。對于allo-HSCT 受者,尤其需要關注維生素C、維生素D、維生素B12、鋅、鎂和鐵的缺乏情況[8,18]。
2.4 營養治療中的藥學監護要點
臨床藥師在營養支持中應對患兒進行積極的藥學監護。監護要求:評估疾病狀態、生理狀態的變化;核實營養液的配比合理性、安全性及具體使用情況;關注患兒的耐受性及潛在不良反應,做好用藥教育和心理疏導,避免營養相關導管和代謝相關并發癥的發生。HSCT患者腸外營養的常規監測指標至少應包括能量和蛋白質攝入、液體平衡、體質量、電解質、血糖、三酰甘油、肝腎功能等[19]。
2.5 小結
經過調整腸外營養治療方案,本例患兒體質量、前白蛋白、白蛋白等營養指標較前明顯改善,且未發生相關藥品不良反應。目前,患兒allo - HSCT 后繼發腸道aGVHD 后營養治療的相關案例報道較少,未見相關臨床指南。陸姍姍等[20]采用全腸外營養對1 例HSCT 后繼發腸道GVHD 的2歲患兒行腸外營養治療,營養狀況改善。本例患兒的營養治療藥學監護不同之處在于,臨床藥師綜合分析相關文獻,首先選擇STAMP 量表對患兒進行營養篩查,制訂個體化腸外營養方案,同時選擇具有調節炎癥作用的含ω - 3 多不飽和脂肪酸的多種油脂肪乳、谷氨酰胺配方,以及維生素、電解質、微量元素等微量營養素,以全合一的方式給予,最大限度地保證了營養用藥的合理化與規范化,有助于營養素的吸收利用,減輕不良風險,提高患兒獲益。但存在一定局限和不足,未對后續腸內營養進行全程營養管理,仍需多樣本、多中心研究數據進行論證,以及添加特殊營養配方對此類患兒的獲益程度,缺乏從藥物經濟學角度對此類患兒的營養治療進行成本-效益分析等。

