Logistic回歸聯(lián)合ROC曲線評價CT增強定量值在術前預測胸腺瘤危險度中的診斷價值
章婷婷,宋 文,黃國權,余永強
胸腺瘤是成人前縱隔最常見的腫瘤,約占所有胸腺上皮腫瘤的80%[1],我國胸腺上皮腫瘤發(fā)病率略高于歐美國家,約為4.09/100萬[2]。2021年WHO將胸腺瘤主要分為A型、AB型、B1型、B2型和B3型[2];根據(jù)不同預后,A型、AB型和B1型統(tǒng)一歸為低危組,B2型和B3型統(tǒng)一歸為高危組[3]。因此,術前無創(chuàng)準確預測胸腺瘤危險度,對臨床醫(yī)師選擇精準的治療方案及判斷患者預后具有重要價值。
增強電子計算機斷層掃描(computed tomography, CT)具有較高空間和時間分辨率,且成像方便迅速,是胸腺腫瘤治療前的首選檢查手段。以往研究[4-8]主要集中CT影像表現(xiàn)與WHO組織學分型之間的關系,然而這些研究僅基于CT影像特征組間差異的比較,并沒有評估這些特征對胸腺瘤危險度的預測效果。該研究旨在篩選出有助于預測胸腺瘤危險度的臨床、CT定性特征及定量值,構建單因素和多因素 Logistic回歸模型,探討有預測意義的因素對胸腺瘤危險度的預測效能。
1 材料與方法
1.1 一般資料回顧性分析2018年1月—2022年1月安徽醫(yī)科大學第一附屬醫(yī)院經(jīng)病理證實的81例胸腺瘤患者臨床、病理及CT資料。采集所有患者基本信息,包括性別、年齡、有無重癥肌無力等。
1.2 CT檢查81例胸腺瘤患者采用 GE Revolution CT進行胸部平掃和雙期增強(動脈期和靜脈期)。掃描范圍自胸廓入口到膈肌水平。掃描參數(shù)為管電壓120 kV,自動mAs技術,矩陣512 × 512,旋轉時間0.5 s,掃描層厚 5 mm,圖像層厚1.25 mm,縱隔窗參數(shù)設置為:窗寬350 HU,窗位40 HU。增強掃描采用的是300 g/L的非離子對比劑碘海醇,劑量為1.1~1.5 ml/kg,增強掃描是經(jīng)肘靜脈按2.5~3.0 ml/s的速度高壓注射器團注碘海醇。動脈期采集時間點是胸部動脈感興趣區(qū)(region of interest, ROI)內CT值達150 HU觸發(fā)閾值后5.9 s,靜脈期采集時間點是動脈期掃描結束后25 s。
1.3 圖像分析由兩名具有5年以上診斷經(jīng)驗的影像科醫(yī)師在ADW 4.7工作站上對CT數(shù)據(jù)進行分析,事先觀察者并不知道腫瘤的具體病理分型。評估CT特征從定性和定量兩方面來分析,定性特征包括:① 位置,包括胸骨左后方、胸骨正后方或胸骨右后方;② 形態(tài),包括規(guī)則或不規(guī)則;③ 邊界,包括清楚或不清楚;④ 有無鈣化;⑤ 有無囊變壞死;⑥ 平掃均勻:是腫塊的最大密度和最小密度相差10 HU以下;⑦ 強化均勻:增強后腫瘤最大密度和最小密度相差10 HU以下;⑧ 其內有無強化血管;⑨ 鄰近脂肪浸潤;⑩ 鄰近結構受累;縱隔淋巴結腫大:縱隔淋巴結最短徑大于10 mm;胸腔積液;心包腔積液;定量特征包括:① 最長徑:橫軸位圖像上腫瘤最大截面的最長徑;② 短徑:橫軸位圖像上腫瘤最大截面最長徑的垂直徑;③ 短徑/最長徑:短徑與最長徑之比;④ 接觸面長度:腫瘤與鄰近結構接觸的曲面長度;⑤ 平掃CT值和最大增強CT值:將ROI置于橫軸位圖像病灶面積最大處,避開囊變壞死、強化血管、鈣化和部分容積效應區(qū),取連續(xù)三個層面的平均值為最終值,增強CT值選取強化程度最大的一期測量;⑥ 增強前后CT最大差值:CT增強值減去平掃值,連續(xù)三個層面差值的平均值。
病理標本由高年資病理科醫(yī)師根據(jù)2021年WHO胸腺上皮腫瘤組織學分型,將胸腺瘤分為5個亞型(A型、AB型、B1型、B2型和B3型),并將A、AB和B1三個亞型歸為低危組,B2和B3 兩個亞型歸為高危組。
1.4 統(tǒng)計學處理正態(tài)連續(xù)性變量采用平均值±標準差描述,非正態(tài)連續(xù)性變量采用中位數(shù)(第一四分位數(shù),第三四分位數(shù))描述,分類變量采用頻數(shù)(百分比,%)描述。符合正態(tài)分布的采用雙樣本t檢驗,非正態(tài)分布的采用非參數(shù)檢驗的曼-惠特尼U檢驗;四格表中所有的理論數(shù)均≥1采用χ2檢驗,至少一個理論數(shù)<1時采用Fisher確切概率法。使用 SPSS 23.0統(tǒng)計軟件進行數(shù)據(jù)分析。
以病理結果為金標準,使用單因素和多因素Logistic回歸分析,以期尋找對胸腺瘤危險度有預測意義的影像學和臨床因素。將單因素Logistic回歸分析中P<0.2的變量納入多因素Logistic回歸分析中。采用SPSS 23.0統(tǒng)計軟件進行分析。
繪制受試者工作特征曲線(receiver operating characteristic curve, ROC曲線)分析最大增強CT值和增強前后CT最大差值在預測胸腺瘤危險度方面的效能,獲得曲線下面積(area under curve, AUC)判斷預測因素的優(yōu)劣。AUC在實踐中可以很好地反映指標的預測價值,一般取值范圍在0.5~1之間,AUC越接近1,則該指標預測性能越好。P<0.05表示差異有統(tǒng)計學意義。采用軟件Medcalc進行統(tǒng)計學分析。
2 結果
2.1 低危組和高危組胸腺瘤患者臨床特征、CT定性特征和定量值的組間比較81例胸腺瘤包括低危組62例和高危組19例。年齡、性別、重癥肌無力、位置、形態(tài)、邊界、鈣化、囊變壞死、最長徑、短徑、短徑/最長徑、接觸面長度、平掃均勻、強化均勻、其內見強化血管、平掃CT值、縱隔脂肪浸潤、鄰近結構受累、縱隔淋巴結腫大、胸腔積液、心包腔積液在亞組之間差異無統(tǒng)計學意義(P>0.05),最大增強CT值、增強前后CT最大差值在各亞組之間差異有統(tǒng)計學意義(P<0.001),高危組最大增強CT值和增強前后CT最大差值明顯小于低危組。見表1和圖1~5。

表1 兩組患者臨床和影像特征比較
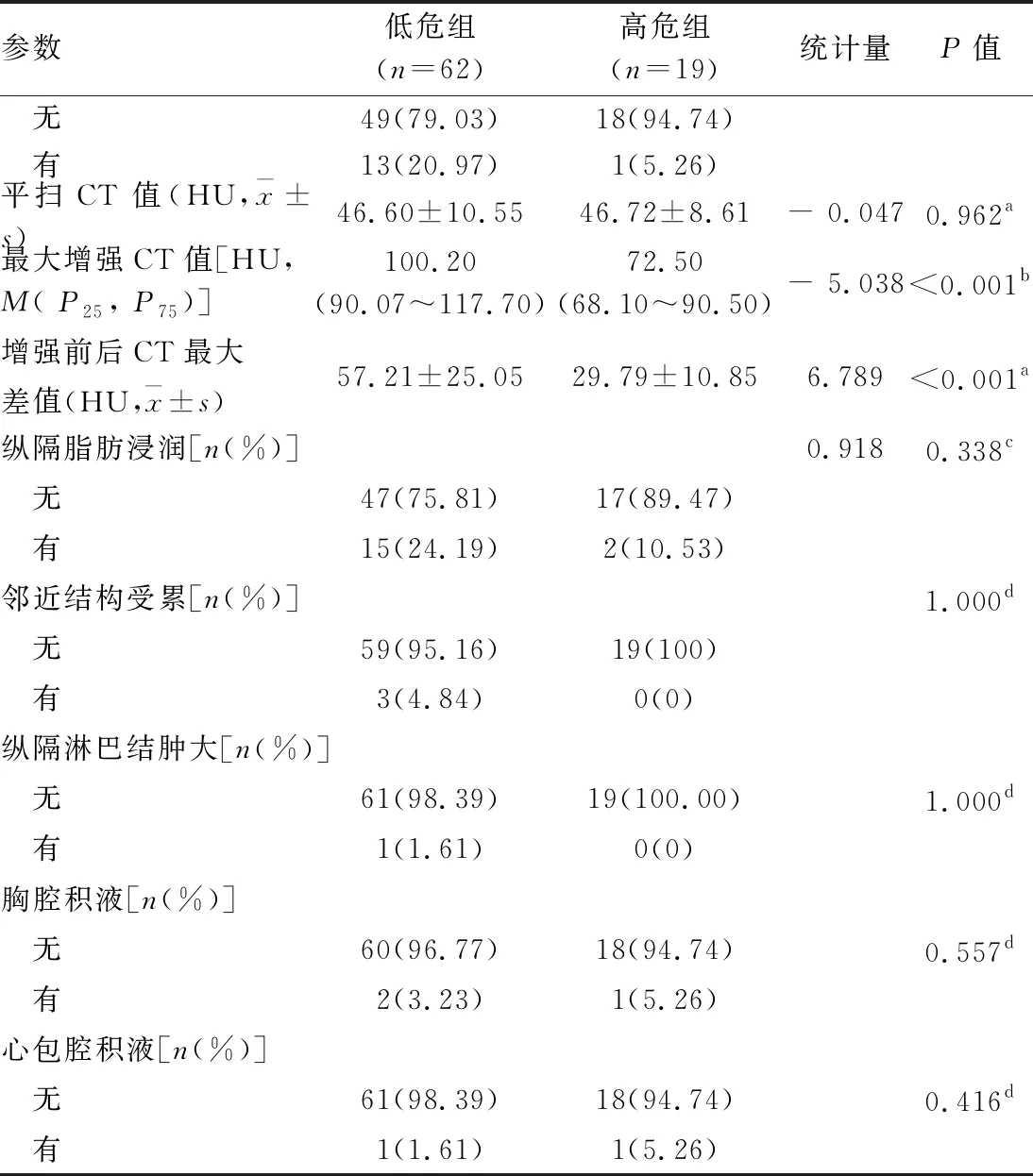
表1(續(xù))
2.2 預測胸腺瘤危險度的Logistic回歸分析單因素Logistic回歸分析顯示,性別、其內見強化血管、最大增強CT值、增強前后CT最大差值與胸腺瘤危險度相關(P<0.2)。見表2。
由于最大增強CT值和增強前后CT最大差值在信息上存在重疊,未將它們同時輸入同一多因素Logistic回歸分析中。多因素Logistic回歸分析顯示,最大增強CT值、增強前后CT最大差值仍然是胸腺瘤危險度的獨立預測因子(P<0.001)。見表3。
2.3 最大增強CT值和增強前后CT最大差值在預測胸腺瘤危險度中的診斷價值在ROC曲線分析中,最大增強CT值 AUC為0.884(P<0.001),最佳截斷值為77.9 HU,預測胸腺瘤危險度的敏感性和特異性分別為68.4%和96.8%,見表4和圖6。
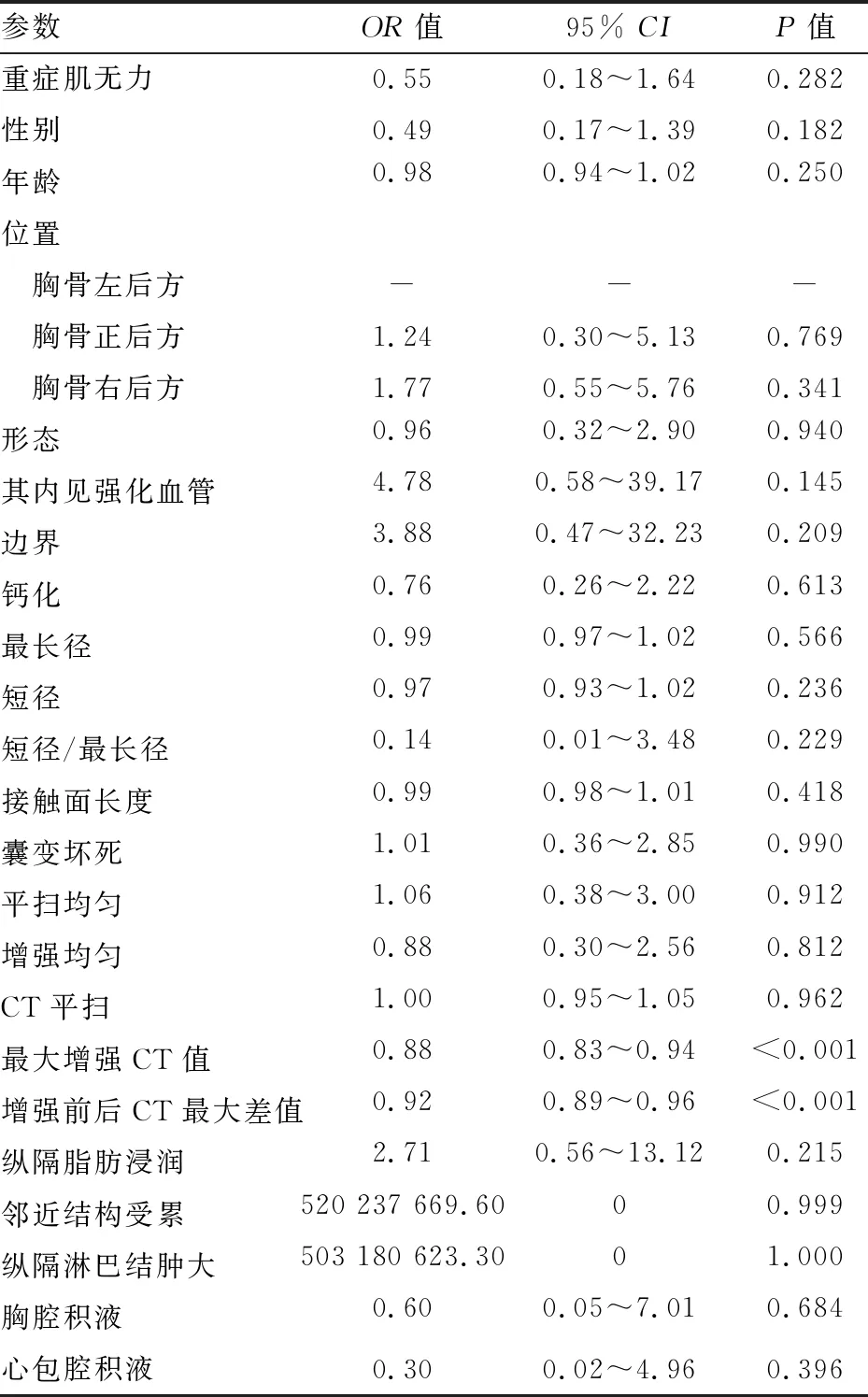
表2 單因素的二分類Logistic回歸分析預測胸腺瘤危險度的相關因素
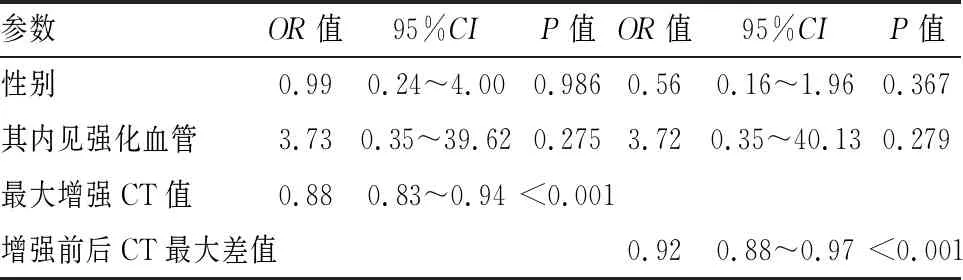
表3 多因素的二分類Logistic回歸分析預測胸腺瘤危險度的相關因素
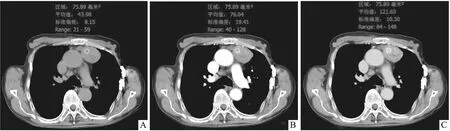
圖1 81歲男性A型胸腺瘤患者
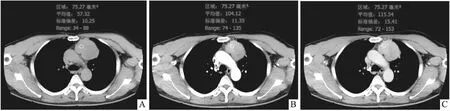
圖2 53歲男性AB型胸腺瘤患者
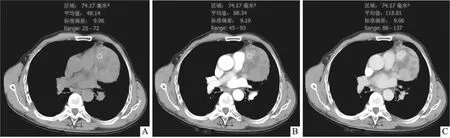
圖3 67歲男性B1型胸腺瘤患者
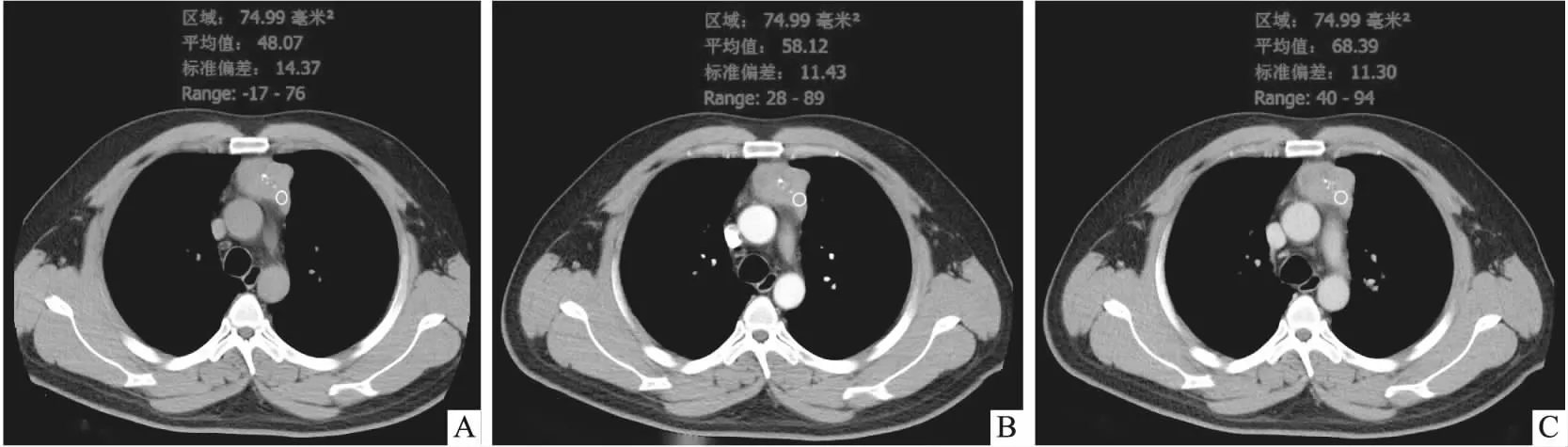
圖4 33歲男性B2型胸腺瘤患者
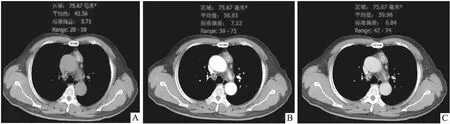
圖5 54歲男性B3型胸腺瘤患者
在ROC曲線分析中,增強前后CT最大差值AUC為0.833(P<0.001),最佳截斷值為39.2 HU,預測胸腺瘤危險度的敏感性和特異性分別為89.5%和72.6%,見表4和圖6。
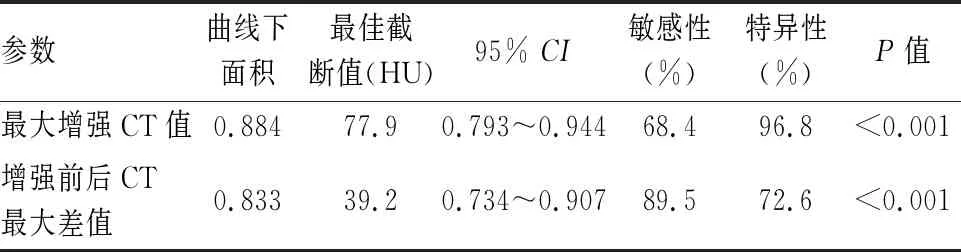
表4 最大增強CT值和增強前后CT最大差值在預測胸腺瘤危險度中的診斷價值
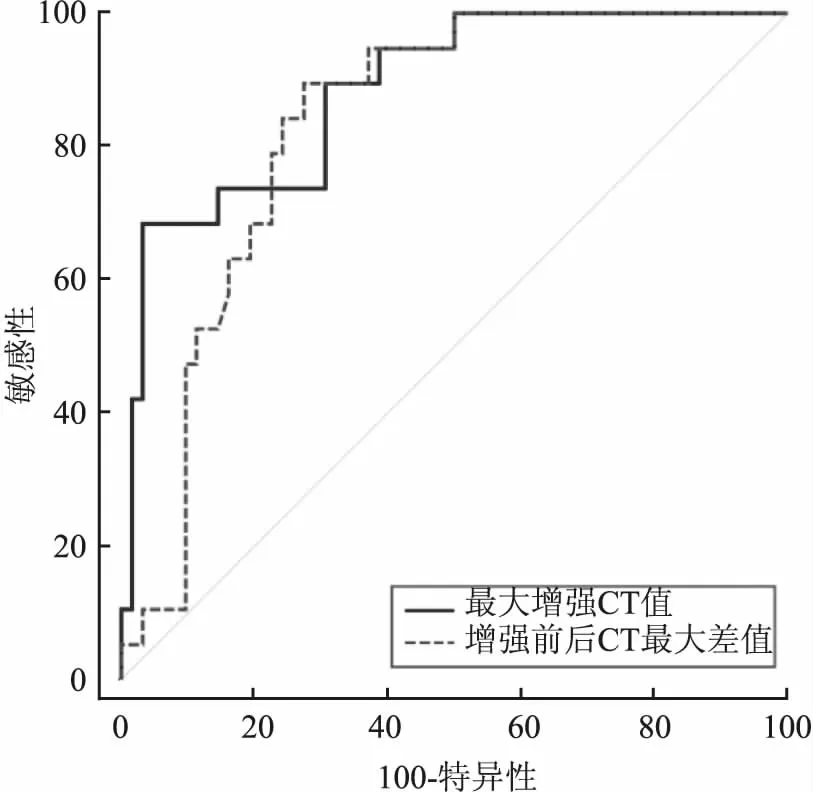
圖6 增強前后CT最大差值、最大增強CT值的ROC曲線
3 討論
胸腺瘤是前縱隔最常見的腫瘤,低危胸腺瘤通常手術完全切除就足夠了,而高危胸腺瘤需要外科手術和放化療聯(lián)合治療。因此,術前無創(chuàng)性準確預測胸腺瘤的危險度,對臨床醫(yī)師為患者制定精準的治療方案及判斷患者預后有非常重要的價值。
增強CT是胸腺瘤治療前的首選檢查手段,其可以精準評估胸腺腫瘤的位置、形態(tài)、邊界、邊緣、大小、密度、強化程度以及與相鄰結構的關系[9]。已有學者利用CT特征的機器學習來預測胸腺瘤的危險度[10],但這需要后期復雜繁瑣的分析和處理,在臨床實際工作中的應用受到極大限制。CT值是影像科醫(yī)師在日常臨床工作中最常用的定量參數(shù),具有執(zhí)行速度快、可用性廣、客觀等特點。增強后CT值、平掃和增強后CT值之間的差值是影像科醫(yī)師量化病變強化程度的最常用的定量指標,可以反映病變血供情況。
本研究結果顯示,高危組胸腺瘤患者的最大增強CT值和增強前后CT最大差值均明顯小于低危組,組間差異有統(tǒng)計學意義(P<0.001);最大增強CT值高危組和低危組分別為[72.50(68.10~90.50)] HU、[100.20(90.07~117.70)] HU;增強前后CT最大差值在高危組和低危組分別為(29.79±10.85)HU、(57.21±25.05)HU;這與之前學者關于胸腺瘤不同危險度的CT強化程度研究[11-13]結果一致。Hu et al[12]研究認為CT最大強化差值可幫助鑒別胸腺瘤的WHO病理分型。金晶 等[13]等應用單因素方差分析研究發(fā)現(xiàn),低危胸腺瘤的CT強化幅度高于高危者,分別為(33.44±10.60)HU、(23.62±6.73)HU,兩個亞組的強化趨勢與本研究結果一致,但各亞組的測量值均低于本研究結果,可能是由于增強掃描采集時間點和樣本量選取不同所致。本研究除了發(fā)現(xiàn)CT強化程度在兩亞組間差異有統(tǒng)計學意義外,最大增強CT值組間差異亦有統(tǒng)計學意義,這更加驗證了低危組胸腺瘤的血供高于高危組。
血管內皮完整性的破壞和血管生長隨著腫瘤進展更加明顯[14],CT增強程度可以反映腫瘤的血液供應及腫瘤血管內皮完整性,因此腫瘤CT增強程度可以反映其進展;然而,本研究結果提示低危組CT強化程度明顯高于高危組,這與上述的理論不一致。Pan et al[15]研究發(fā)現(xiàn)A型胸腺瘤的腫瘤細胞呈梭形或紡錘形,AB型胸腺瘤由梭形上皮細胞和淋巴細胞混合組成,A型和AB型的梭形細胞通常排列為血管外皮瘤樣或微囊樣,這可以解釋低危組的胸腺瘤最大增強CT值和增強前后CT最大差值較高危組更大的原因。
Logistic回歸模型是一種概率模型,具有尋找危險因素、預測和判別等功能。以前學者僅僅探究胸腺瘤低危組和高危組之間差異有統(tǒng)計學意義的因素,并沒有進行預測胸腺瘤危險度的Logistic回歸分析和ROC預測價值的探討。因此,結合本研究中最大增強CT值和增強前后CT最大差值組間差異有統(tǒng)計學意義的因素,再聯(lián)合Logistic回歸分析和ROC分析探究胸腺瘤危險度的預測因素。筆者發(fā)現(xiàn)最大增強CT值和增強前后CT最大差值為胸腺瘤危險度的獨立預測因子;最大增強CT值、增強前后CT最大差值的AUC均高于0.800,前者較后者的預測效能高。這再次佐證了低危組胸腺瘤和高危組胸腺瘤的血供和腫瘤血管內皮完整性存在差別,其可作為預測腫瘤危險度的一種簡便、實用、客觀的指標。
本研究尚有一些局限性。首先,該研究是單中心的回顧性分析,這可能存在選擇偏差;其次,樣本量不夠大,需要一個更大、多中心的樣本量來驗證這些結果。
綜上所述,CT增強定量值可以作為術前胸腺瘤風險分級的預測因子,最大增強CT值的預測效能高于增強前后CT最大差值,可作為評價胸腺瘤危險度的一種客觀影像學標志物。

