油相結構化對大豆蛋白藻油納米乳液氧化穩定性的影響
楊韻儀,曹沐曦,陳文榮,萬芝力,*,方素瓊,*,楊曉泉
(1.華南理工大學食品科學與工程學院,食物蛋白與膠體研究中心,廣東省天然產物綠色加工與產品安全重點實驗室,廣東 廣州 510641;2.仙樂健康科技股份有限公司,廣東 汕頭 515041)
提取自海洋藻類的藻油中二十二碳六烯酸(docosahexaenoic acid,DHA)含量高、安全可持續,然而藻油不溶于水,且DHA極易氧化變質產生酸、醛、酮等氧化物,影響風味、口感的同時也帶來健康風險[1-2]。目前,食品工業常將其密封于軟膠囊中以隔絕外界的氧化因子,但是存在食用不便、應用形式單一等缺陷,無法滿足人們對多樣化藻油產品日益增長的需求。研究團隊已成功利用小分子甜菊糖(stevioside,STE)改善大豆分離蛋白(soy protein isolate,SPI)的乳化特性,構建出高穩態的納米乳液體系[3-5]。此外,SPI-STE復合體系已被證明能作為優良載體用于包埋多種天然活性成分[3,5-6],可用于開發藻油納米乳液,滿足嬰幼兒、老人等特殊人群的日常補充需求的同時,對拓展藻油在運動營養、特醫食品等新興領域中的應用具有重要意義。
然而,O/W納米乳液含有豐富的水相以及比表面積極大的油水界面,會導致脂質快速氧化,這將嚴重限制該技術在藻油開發中的應用[7-8]。傳統的抗氧化劑技術無法穩定高度不穩定的脂質(胡蘿卜素、不飽和脂肪酸等),目前正在開發新技術以改變乳液的物理性質,從而抑制脂質氧化反應,如填充型水凝膠和油相結構化乳液[9-11]。其中,油相結構化策略通過將脂質捕獲在凝膠網絡中,從而降低其與水相氧化因子的接觸,有效提高乳液的抗氧化性[7-9]。蜂蠟是一種常用的天然蠟,具有安全無毒、凝膠性優異、可塑性強、穩定性高等優良特性,已被美國食品藥品監督管理局的食品添加劑標準允許使用,且沒有進行添加量的限制[12]。近年來,蜂蠟作為脂質結構化助劑已被成功用于制備各種尺度的乳液[13-14],在脂質抗氧化方面的研究仍停留在微米尺度。Wei Feilong等[15]比較了蜂蠟和單甘脂作為油相結構劑對乳液氧化的影響,結果表明蜂蠟能形成更致密的油凝膠網絡,從而賦予乳液更好的氧化穩定性,延緩氧化效果并隨蜂蠟添加量的增加而增強,然而蜂蠟結構化策略能否在納米乳液中展現出優異的抗氧化效果還有待考究。
為探究蜂蠟結構化對藻油納米乳液穩定性的影響,本研究首先研究蜂蠟對藻油的結構化行為,然后以SPI-STE復合體系作為乳化劑制備藻油納米乳液,評估蜂蠟結構化對藻油納米乳液形成及物化穩定性的影響,并嘗試通過調控油相結構化構建高穩定性的藻油納米乳液體系。
1 材料與方法
1.1 材料與試劑
藻油(DHA含量≥40%) 內蒙古金達威藥業有限公司;蜂蠟(酸值17.5 mg/g,皂化值89.1 mg/g,碘值9.3 mg/g,均以KOH計算) 北京麗康偉業科技有限公司;低溫脫脂豆粕 山東禹王實業有限公司;STE(純度>90%) 山東海根生物技術有限公司;實驗用其他化學試劑均為國產分析純;實驗用水為Million-Q超純水。
1.2 儀器與設備
Axioskop 40 Pol偏振光顯微鏡 德國Zeiss公司;U-HGLGPS多功能光學顯微鏡 日本Olympus公司;RS600HAKKE流變儀 美國賽默飛世爾科技公司;TGA/DSC1差示掃描量熱儀(differential scanning calorimeter,DSC) 瑞士梅特勒-托利多公司;T25 digital ULTRA TURRAX高速剪切機 德國IKA公司;M-110-EH-30高壓微射流納米均質機 美國MFIC公司;DELTA冷凍干燥機 德國Christ公司;Multimode SPMBX51原子力顯微鏡 美國維易科精密儀器有限公司;Nano-ZS90納米粒度及Zeta電位分析儀 英國馬爾文儀器有限公司;7890B氣相色譜儀 美國安捷倫科技公司;NanoPhotometer C40 Touch紫外分光光度計德國Implen公司;EC-TL01B紫外燈 廣東省佛山益辰電子科技有限公司;TANKPE060純水機 法國密理博公司。
1.3 方法
1.3.1 藻油凝膠的制備
取不同質量的蜂蠟至藻油中,于80 ℃水浴鍋中攪拌加熱 3 min后蜂蠟完全溶解,自然冷卻至室溫,放置24 h,得到含不同質量分數(0%、2%、3%、4%、6%、8%)蜂蠟的藻油凝膠。
1.3.2 藻油納米乳液及油粉的制備
以SPI-STE復合體系為乳化劑制備藻油納米乳液[5]。參考萬芝力[3]的堿溶酸沉方法制備SPI,經杜馬斯燃燒定氮法測得SPI凍干粉蛋白含量為(97.18±0.56)%。將SPI分散于10 mmol/L磷酸鹽緩沖液(pH 7.0),攪拌2 h后置于4 ℃水化過夜。取一定量的STE粉末至10 mmol/L磷酸鹽緩沖液(pH 7.0)中,攪拌至澄清。使用NaOH或HCl溶液調節SPI和STE溶液至pH 7.0,隨后將兩者混合并攪拌30 min,獲得SPI-STE復合體系。
將藻油凝膠80 ℃水浴加熱3 min,按油相與水相質量比1∶9加入處于相同溫度(80 ℃)的SPI-STE復合體系中,攪拌獲得油水混合液。將混合液先進行高速剪切機預均質(5000 r/min,2 min),隨后立即進行高壓均質處理(50 MPa,2 次),制得納米乳液。乳液制備過程中樣品溫度始終保持在80 ℃。最終乳液中含有質量分數為10%的油相、1% SPI和0.5% STE。向乳液中加入0.04%疊氮鈉防止染菌。
油粉由新鮮乳液冷凍干燥得到。
1.3.3 藻油凝膠微觀結構觀察
利用放大倍數為1000 倍的明場和偏光顯微鏡觀察藻油凝膠的微觀結構。將樣品80 ℃水浴加熱3 min,趁熱將5 μL融化樣品滴在預熱的載玻片上,并用預熱的蓋玻片輕輕覆蓋,室溫下靜置24 h后觀察樣品。
1.3.4 藻油凝膠熱力學性質測定
采用DSC測量藻油凝膠融化和結晶的相變行為。取適量樣品放入坩堝,以空坩堝作為對照。加熱樣品,2 ℃/min速率從20 ℃加熱到85 ℃,保溫10 min,以相同速率冷卻至初始溫度。
1.3.5 藻油凝膠流變學性質測定[16]
振蕩測試:分別在應力0.1~1000 Pa、頻率1 Hz和頻率0.1~50 Hz、應力1 Pa條件下進行應力掃描和頻率掃描,測定藻油凝膠樣品的儲能模量(G’)和損耗模量(G’’)。
流動測試:在剪切速率0.01~100 s-1條件下記錄樣品表觀黏度的變化。選用直徑35 mm平板,間隙1 mm,測試溫度25 ℃。
1.3.6 藻油包封率測定[17]
取0.5 mL乳液至離心管中,稱量乳液(m1)與離心管質量(m2)。加入1 mL己烷,5000 r/min離心10 min分離乳液與己烷。用針管將下層乳液全部吸出,加入離心管,用己烷潤洗針管,加入離心管。將離心管敞口放置在通風櫥內使己烷完全揮發,稱量離心管終質量(m3)。按下式計算藻油包封率:
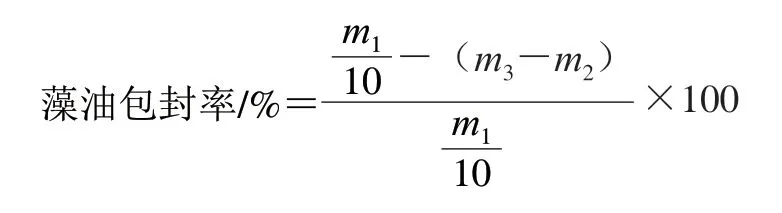
1.3.7 乳液粒度和Zeta電位測定
將乳液用pH 7.010 mmol/L磷酸緩沖液適當稀釋后,用Nano-ZS納米粒度及Zeta電位分析儀測定乳液的平均粒徑、多分散性指數(polydispersity index,PDI)和Zeta電位。參數設置:分散相(藻油)折射率1.503,吸收率0.002;連續相折射率1.333;測試溫度25 ℃。
1.3.8 乳液貯存穩定性測定
將乳液于25 ℃貯存30 d后,按1.3.7節步驟測定乳液的粒度變化。
1.3.9 脂質氧化穩定性測定
熱促氧化條件:將新鮮乳液放入40 ℃恒溫箱中貯存30 d;光促氧化條件:用紫外燈照射新鮮乳液8 h,紫外線波長為254 nm,光輻照度為6.9 mW/cm2。根據杜振亞[18]的方法分別在熱促氧化和光促氧化條件下測定乳液脂質氧化產物含量。
1.3.9.1 一級氧化產物脂質氫過氧化物含量測定
取200 μL乳液,加入1.5 mL異辛烷-異丙醇溶液(3∶1,V/V),渦旋振蕩3 次,每次持續10 s,5000 r/min離心5 min。取200 μL上清液,加入2.8 mL甲醇-正丁醇溶液(2∶1,V/V),依次加入15 μL 3.94 mol/L硫氰酸銨溶液和15 μL二價鐵離子溶液(等體積混合0.132 mol/L氯化鋇和0.144 mol/L硫酸亞鐵),混勻,密封靜置20 min后于510 nm波長處測定吸光度。使用30%過氧化氫溶液制備系列標準溶液(50、100、200、300、400、500 μmol/L)繪制標準曲線。
1.3.9.2 二級氧化產物含量測定
采用硫代巴比妥酸法測定二級氧化產物丙二醛的含量。取200 μL乳液,加入1.8 mL去離子水,混勻,加入4 mL硫代巴比妥酸試劑,漩渦振蕩3 次,每次持續10 s,隨后沸水浴15 min。冷卻至室溫后6000 r/min離心20 min,取上清液,于535 nm波長處測定吸光度。使用1,1,3,3-四乙氧基丙烷制備系列標準溶液(2、5、10、20、30、40 μmol/L)繪制標準曲線。
采用動態頂空法檢測揮發性二級氧化物己醛的含量。取10 mL新鮮乳液于頂空瓶中,40 ℃避光靜置30 d后使用氣相色譜儀測定己醛含量。色譜條件:HP-5毛細管柱(30 m×0.25 mm,0.25 μm);升溫程序:以4 ℃/min從40 ℃上升到50 ℃,隨后立即以5 ℃/min上升到100 ℃,再以8 ℃/min上升到230 ℃;進樣口和火焰離子化檢測器溫度均為250 ℃。載氣為氮氣,流速1.0 mL/min,分流比1∶1。
1.4 數據處理
利用SPSS 13.0軟件進行單因素方差分析,采用Duncan檢驗進行多組樣品間差異顯著性分析,采用Origin 2018軟件繪圖。
2 結果與分析
2.1 藻油凝膠的理化性質研究
2.1.1 藻油凝膠的外觀及微觀結構
油凝膠的臨界凝膠濃度與其凝膠能力相關[19-22]。圖1A中樣品外觀顯示,將藻油凝膠倒置后,含2%蜂蠟的藻油凝膠在宏觀上不能凝固,含3%蜂蠟的藻油凝膠呈半凝固狀態,而含4%~8%蜂蠟的藻油凝膠能形成穩定的凝膠。進一步通過顯微鏡觀察其晶體微觀形貌(圖1B、C),純蜂蠟的網絡結構致密,晶體較為細膩且分布均勻。從含2%和3%蜂蠟的藻油凝膠中可觀察到晶體呈團簇花瓣狀均勻地分散于凝膠體系中,晶體形貌、結構清晰可見,直徑約為15 μm,與Ashok等[19]觀察到的蜂蠟凝膠簇群結構相似。此外,視野中含3%蜂蠟的藻油凝膠的晶體數量比2%更多,但是單個晶體的堆積不能使含3%蜂蠟的藻油凝膠維持穩定的凝膠狀態。當蜂蠟質量分數達到4%時,蜂蠟晶體較多從而發生聚集并進一步互連,形成3D網絡結構,單個晶體微粒幾乎不可見,與純蜂蠟的微觀結構相似,表明藻油已完全凝膠化[22]。隨著蜂蠟質量分數進一步增加(6%~8%),晶體網絡更致密,與Winkler-Moser等[23]的報道一致。
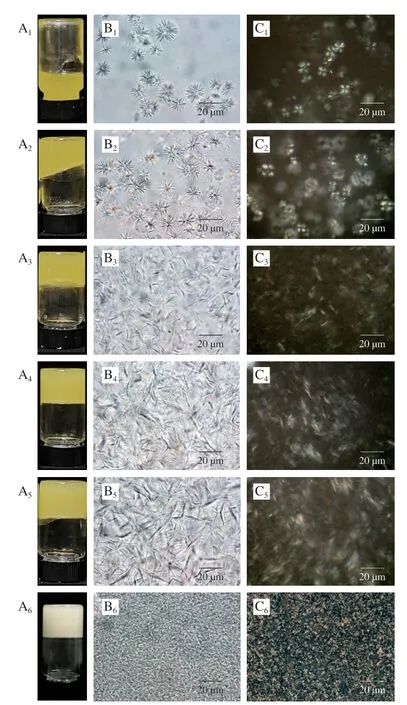
圖1 含不同質量分數蜂蠟的藻油凝膠及純蜂蠟的倒置外觀圖(A)、明場顯微鏡圖(B)和偏振光顯微鏡圖(C)Fig.1 Visual appearance (A),bright (B) and polarized light microscopic (C) images of algal oil-based oleogels with different amounts of beeswax added
2.1.2 藻油凝膠的DSC分析
由圖2可知,純蜂蠟在加熱過程中,于66.5 ℃處出現一個強吸熱峰,即熔融溫度[23-25];在冷卻過程中,存在兩個放熱峰(峰1為50.2 ℃,峰2為55.6 ℃),即蜂蠟在峰2時開始結晶,在峰1處發生晶型轉變(β型變為α型)[23,25-26]。而藻油在20~85 ℃的溫度變化范圍內無明顯的結晶峰和熔融峰。藻油凝膠在加熱過程中,蜂蠟質量分數2%的藻油凝膠在45.7 ℃出現吸熱峰,但峰面積較小;隨著蜂蠟含量逐漸增大,藻油凝膠的吸熱峰逐漸后移且峰面積增大,呈現向純蜂蠟樣品靠攏的趨勢;當蜂蠟質量分數增至8%時,吸熱峰為54.1 ℃,輪廓明顯。而在冷卻時,含2%蜂蠟的藻油凝膠在34.5 ℃處出現結晶峰(峰2),晶型轉變峰(峰1)不明顯;隨著蜂蠟含量逐漸增大,峰1逐漸可觀測到,兩個放熱峰呈現位置后移、面積增大的趨勢;蜂蠟質量分數8%的藻油凝膠中,放熱峰出現在35.2 ℃和46.7 ℃處。上述結果表明,藻油凝膠的熔融溫度低于60 ℃,結晶溫度高于30 ℃,可適應大多數食品的加工和貯存條件,符合工業化生產的要求[27]。
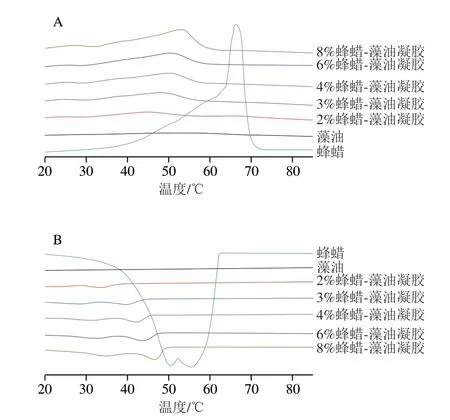
圖2 蜂蠟、藻油及含不同質量分數蜂蠟的藻油凝膠的加熱(A)和冷卻(B)曲線Fig.2 Comparative heating (A) and cooling (B) curves of pure beeswax,algae oil and algal oil-based oleogels with different amounts of beeswax added
2.1.3 藻油凝膠的流變學特性
藻油凝膠的微觀結構與其機械性質密切相關,通過測定樣品的流變學特性進一步了解藻油凝膠的結構性質。由圖3A可知,在線性黏彈區內,所有樣品的G’均顯著高于G”,說明所有樣品均表現出類彈性固體性質[18,28]。隨著蜂蠟質量分數增加,藻油凝膠的G’和G”、屈服應力值及線性黏彈區均增大,說明油凝膠具有更強的機械性能和抵抗外力破壞的能力[16,19,28-29]。如圖3B所示,2%蜂蠟質量分數的藻油凝膠在0.1~50 Hz范圍內表現出較強的頻率依賴性,這是因為此時樣品的黏彈性較弱,容易受到頻率的擾動而導致結構被破壞;3%~8%蜂蠟質量分數的藻油凝膠表現出較低的頻率依賴性,表明樣品的振蕩性質受所施加應力的影響較小,顯示出較好的黏彈性[28-29]。
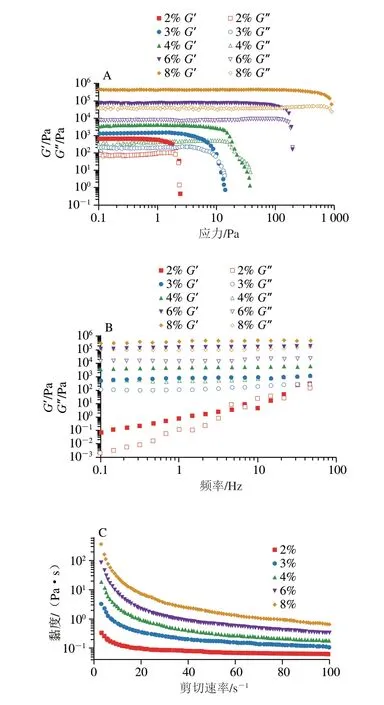
圖3 含不同質量分數蜂蠟的藻油凝膠的應力掃描(A)、頻率掃描(B)及黏度曲線(C)Fig.3 G’ and G” versus stress (A),G’ and G” versus frequency (B)and viscosity versus shear rate curves (C) of algal oil-based oleogels with different amounts of beeswax added
藻油凝膠黏度反映樣品的流動特性[27-28]。由圖3C可知,所有藻油凝膠均表現出強烈的剪切變稀行為,且樣品的表觀黏度隨著蜂蠟質量分數的增加而提高,表明形成了強度更大的凝膠結構[28-29],與黏彈性測試結果一致。
2.2 藻油納米乳液的性質分析
如表1 所示,油相中不含蜂蠟時,藻油納米乳液的平均粒徑為178.40 nm,PDI值為0.15,Zeta電位為-29.25 mV,與課題組前期研究結果[5-6]一致。以蜂蠟結構化的藻油凝膠為油相,得到的藻油納米乳液平均粒徑為184.18~204.03 nm,PDI值均小于0.30,Zeta電位處于-29~-27 mV間,表明蜂蠟的添加對藻油納米乳液(約200 nm)的形成無明顯影響。相較于對照樣品,蜂蠟的添加增大了乳液的平均粒徑;當蜂蠟添加量為2%~4%時,乳液的平均粒徑隨蜂蠟質量分數的增加而增大;當蜂蠟質量分數進一步增加時(6%~8%),乳液的平均粒徑變化不顯著,但值得注意的是,蜂蠟質量分數8%的樣品PDI值達到0.27,說明該乳液中存在不均一的聚集體[3]。這可能是由于此時較高的蜂蠟添加量構筑出剛性較強的凝膠網絡,乳液自然冷卻過程中,晶體的生長速率過快以及局部不平衡性(一旦膠凝劑在特定位置形成晶核便會繼續生長)導致界面被刺破,從而引起乳液液滴局部失穩并黏結[9,15]。藻油包封率結果顯示,蜂蠟的添加對藻油包封率有輕微改善作用,但改善幅度較小(2.23%~4.22%)。
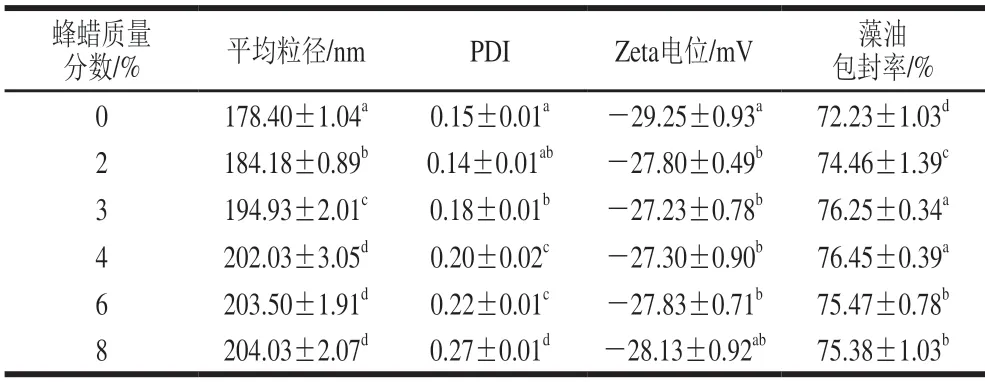
表1 藻油納米乳液的平均粒徑、PDI值、Zeta電位及藻油包封率Table 1 Mean particle diameter,PDI,zeta-potential and encapsulation efficiency of algal oil-based nanoemulsions
2.3 藻油納米乳液及油粉的貯存穩定性
如圖4A所示,藻油納米乳液在25 ℃貯存30 d,所有樣品仍呈現正常的乳白色,質地均勻,無明顯的乳析或相分離現象,樣品間無明顯的外觀差異。如圖4B所示,貯存期內所有樣品的粒徑變化均小于60 nm,表明乳液均具有良好的長期穩定性[7,19]。其中,對照樣品和8%樣品的平均粒徑變化最大(分別增大52 nm和51 nm),表明適量的蜂蠟添加量(2%~6%)利于乳液的長期穩定。
如圖4C所示,未油相結構化(0%)和含2%蜂蠟的油粉均呈淡黃色,有輕微的油析現象,這可能是因為快速的溶劑蒸發對界面膜的強擾動破壞[30-31];貯存30 d后,黃色加深,表明油析程度加重。含3%~6%蜂蠟的樣品呈乳白色,無明顯的油析現象;貯存30 d后,顏色、狀態均無明顯變化,說明藻油凝膠機械強度的增強賦予了乳液更穩定的熱力學性質,即使經歷了相對苛刻的凍干過程,其界面結構仍保持相對完整[31-32]。而含8%蜂蠟的樣品呈乳白色,貯存30 d后變為深黃色,出現嚴重的油析現象,表明該樣品貯存穩定性較差,可能是此時結構化的油相剛性較強,影響了界面層的穩定性,與粒徑測定結果一致。由于藻油被凝膠網絡捕獲,新鮮狀態下油脂沒有明顯的溢漏,但隨著時間的推移,未被完全包封的油脂快速氧化,導致粉末變色、凝結。這些結果表明添加3%~6%蜂蠟能明顯增強藻油納米乳液和油粉的物理穩定性。
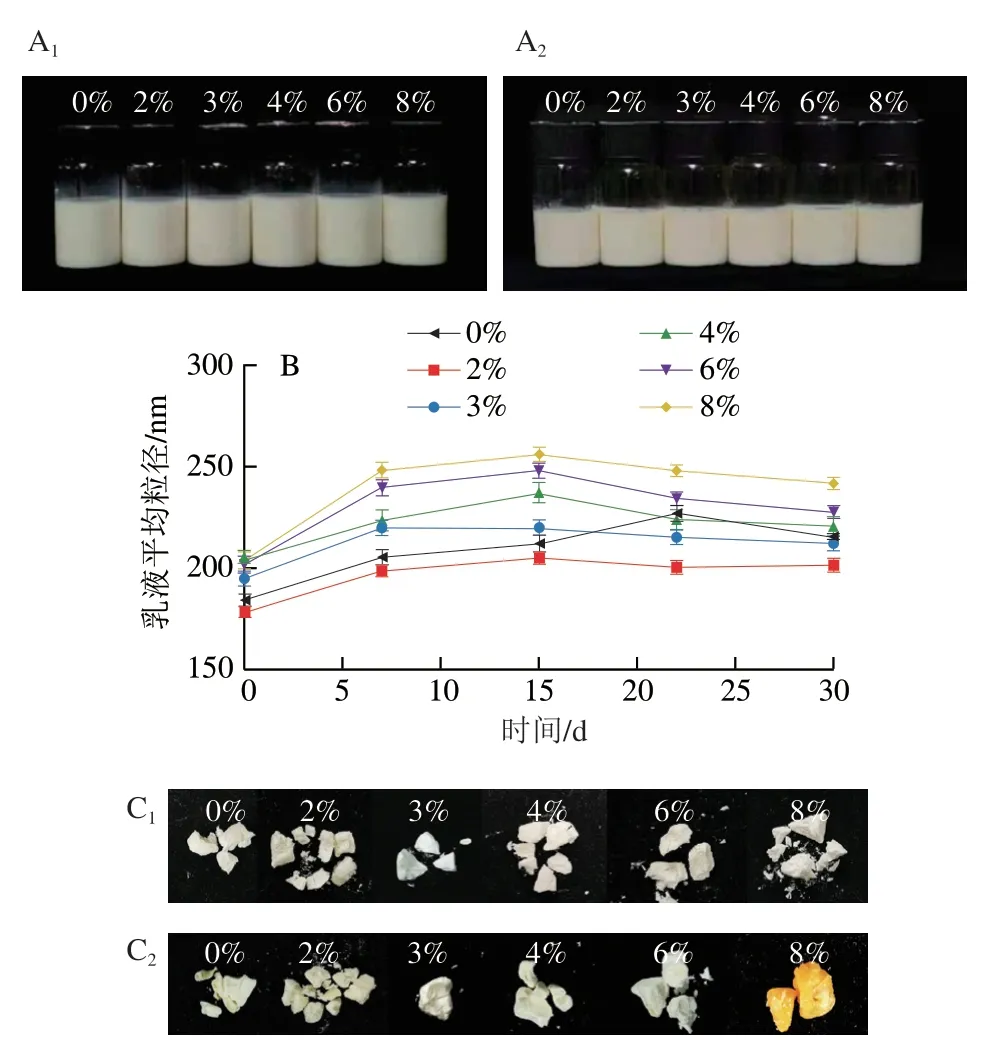
圖4 含不同質量分數的藻油納米乳液外觀(A)、平均粒徑(B)及其油粉外觀(C)Fig.4 Appearance (A),mean particle diameter (B) of algae oil-based nanoemulsions containing different amounts of beeswax,and appearance of powders prepared from each of them (C)
2.4 藻油納米乳液的氧化穩定性
2.4.1 熱促氧化
油脂氧化為鏈式反應,初級反應產物氫過氧化物可用于評估乳液氧化的起始速率[3,31]。如圖5A所示,熱促氧化過程中,貯存第18天時,所有藻油納米乳液的脂質氫過氧化物含量均達到峰值,對照組的氫過氧化物含量(44.63 mmol/(L·kg))遠高于其他樣品。隨著蜂蠟添加量的增大(2%~6%),樣品的氫過氧化物含量逐漸降低至22.23 mmol/(L·kg);當蜂蠟質量分數為8%時,樣品的氫過氧化物含量略微增大(23.41 mmol/(L·kg))。氧化穩定性的提升可能是因為蜂蠟對油相的固化,抑制促氧化金屬離子以及自由基對多不飽和脂肪酸不飽和鍵的攻擊[2,9]。因此,隨著蜂蠟含量的增加,油相凝膠網絡增強,物理屏蔽作用的提高有效提升乳液的氧化穩定性;但是蜂蠟含量過高時,乳液中存在部分絮凝體影響了乳液的氧化穩定性。圖5B為乳液經30 d貯存后產生的揮發性物質的頂空分析結果,其中己醛是藻油中主要的次級氧化產物之一[3,31,33]。結果顯示,對照樣品的己醛峰面積最大,其次為含2%、3%、4%、8%、6%蜂蠟樣品,與初級氧化物的變化趨勢一致。熱促氧化的綜合數據表明,藻油中添加6%蜂蠟對乳液的氧化穩定性改善效果最顯著。
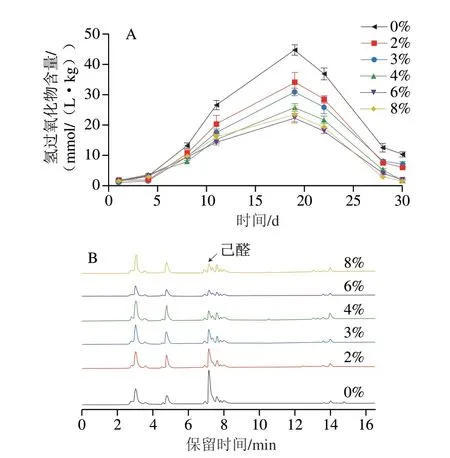
圖5 藻油納米乳液在熱促氧化下脂質氫過氧化物的含量變化(A)和己醛含量分析(B)Fig.5 Changes in lipid hydroperoxides (A) and hexanal (B) contents of algal oil-based nanoemulsions under thermal treatment
2.4.2 光促氧化
如圖6A所示,對照樣品和含2%蜂蠟藻油納米乳液的初始氧化速率較快,在2 h左右氫過氧化物含量已達到峰值;含3%、4%和8%蜂蠟藻油納米乳液在4 h左右出現峰值;含6%蜂蠟藻油納米乳液的初級氧化速率最慢,在6 h左右出現峰值。由圖6B可知,曝光8 h后,含0%、2%、3%、4%、8%、6%蜂蠟的樣品中的次級氧化物丙二醛含量依次減小,與對照樣品相比氧化值分別降低了17.67%、28.74%、36.13%、37.23%、77.48%,表明油相中添加蜂蠟能顯著延緩乳液的光促氧化進程[3,31,33],其中6%蜂蠟添加量效果最佳。光促氧化的研究結果與熱促氧化相符。
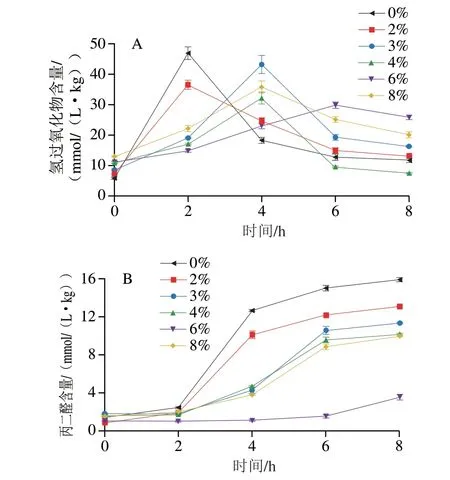
圖6 藻油納米乳液在光促氧化下脂質氫過氧化物的含量變化(A)和丙二醛含量分析(B)Fig.6 Changes in lipid hydroperoxides (A) and malondialdehyde (B)contents of algal oil-based nanoemulsion upon light exposure
3 結論
以蜂蠟為天然油相凝膠劑、SPI-STE復合體系為天然乳化劑,構建出具有高貯存穩定性與氧化穩定性的藻油納米乳液載體,實現對藻油的保護,拓展其在食品加工中的應用。結果表明,蜂蠟添加量達到4%時,大量晶體聯結成穩固的網絡結構,從而構筑出穩定的油凝膠。蜂蠟對藻油的結構化對納米乳液(約200 nm)的形成沒有明顯影響,所有樣品的平均粒徑、Zeta電位及藻油包封率相近。乳液穩定性結果表明,蜂蠟的固化作用使乳液具有更好的貯存穩定性,但是凝膠強度過大(8%蜂蠟添加量)會影響界面穩定性,導致乳液物理穩定性變差。乳液的熱促氧化和光促氧化研究表明,油相中添加蜂蠟的樣品均表現出明顯提升的氧化穩定性;其中,蜂蠟添加量為6%時延緩藻油乳液氧化的效果最明顯。本研究結果表明,經蜂蠟油相結構化的大豆蛋白基納米乳液體系可作為藻油的高穩態載體應用于食品工業。

