原發性高血壓患者血壓變異性及Lp-PLA2、sdLDL-C與頸動脈硬化程度的相關性*
梁營營 張娟 秦瑞丹
原發性高血壓(primary hypertension,PH)是以體循環動脈壓升高為主要臨床表現的循環系統疾病,可引起多個靶器官損害,對人類的生命健康構成巨大威脅,加重社會經濟負擔[1]。相關研究表明,血壓變異性(blood pressure vari-ability,BPV)是心血管事件和死亡的可靠獨立預測因子,高BPV 進一步加重靶器官損傷[2]。動脈血管壁改變是高血壓最重要和致命的并發癥之一[3]。研究報道顯示,動脈硬化是一種慢性炎癥性疾病,脂質代謝異常加速動脈內膜增厚或斑塊形成的進程[4]。脂蛋白相關磷脂酶A2(lipoprotein-associated phospholipase A2,Lp-PLA2)由巨噬細胞高度表達,被認為可能是血管炎癥的特異性標記物,與斑塊的形成和發展密切相關[5]。小而密低密度脂蛋白膽固醇(small and dense low density lipoprotein cholesterol,sdLDL-C)是低密度脂蛋白膽固醇(low density lipoprotein cholesterol,LDL-C)的亞組分之一,有研究證明sdLDL-C 比LDL-C 更容易致動脈硬化,與冠心病嚴重程度相關[6]。綜合以上背景,本研究分析了原發性高血壓患者BPV、Lp-PLA2、sdLDL-C 與頸動脈硬化的關系,旨在為高血壓患者早期臨床干預提供更多的依據。
1 資料與方法
1.1 一般資料 回顧性分析2021 年1 月-2022 年5 月鄭州大學第二附屬醫院收治的151 例高血壓患者的臨床資料為高血壓組,根據頸動脈內膜中層厚度(IMT)將高血壓組分為單純高血壓組54 例、高血壓頸動脈硬化組97 例兩個亞組;另隨機選擇同期體檢的64 例健康人為對照組。納入標準:(1)年齡≥18歲,臨床資料完整;(2)觀察組符合文獻[1]《中國高血壓防治指南(2018 年修訂版)》中PH 診斷標準:①在未使用降壓藥物的情況下,非同日3 次測量診室血壓(OBPM),收縮壓(SBP)≥140 mmHg(1 mmHg=0.133 kPa)和/或舒張壓(DBP)≥90 mmHg;②SBP≥140 mmHg和DBP<90 mmHg 為單純收縮期高血壓;既往有高血壓史,目前正在使用降壓藥物,血壓雖然低于140/90 mmHg,仍應診斷為高血壓;③動態血壓監測(ABPM)的高血壓診斷標準為平均24 h SBP/DBP≥130/80 mmHg;白天≥135/85 mmHg;夜間≥120/70 mmHg;④家庭血壓監測(HBPM)的高血壓診斷標準為≥135/85 mmHg,與OBPM 的140/90 mmHg 相對應。排除標準:(1)合并急慢性感染、嚴重心肝腎功能受損;血液系統疾病、自身免疫病、罹患惡性腫瘤或腫瘤待排;(2)處于妊娠期或哺乳期婦女。高血壓組男90例,女61例,年齡35~87歲,平均(63.15±9.61)歲。對照組男38例,女26例,年齡42~85歲,平均(61.34±9.90)歲。本研究經本院倫理委員會審核通過,入組者均簽署知情同意書。
1.2 方法
1.2.1 臨床資料采集 入組對象完善姓名、性別、年齡、身高、體重、體重指數(BMI)、吸煙史等基本資料;所有對象空腹至少8 h 采集肘靜脈血3 mL,利用全自動生化分析儀測定空腹血糖(FPG)、糖化血紅蛋白(HbA1c)、甘油三酯(TG)、總膽固醇(TC)、高密度脂蛋白膽固醇(HDL-C)、低密度脂蛋白膽固醇(LDL-C)、尿酸(UA)、同型半胱氨酸(Hcy)、肌酐(Scr)等生化指標。
1.2.2 血漿Lp-PLA2、sdLDL-C 水平檢測 利用全自動生化分析儀測定sdLDL-C 水平。另采集3 mL靜脈血采用ELISA 檢測循環Lp-PLA2 水平。
1.2.3 24 h 動態血壓監測 入選患者均佩帶24 h 美高儀動態血壓儀(MGY-ABPL 型)監測動態血壓,監測期間禁煙酒,設定6:00~22:00 為白天,每30 min 自動充氣測量并記錄血壓1 次;22:00~次日6:00 為夜間,每60 min 自動充氣測量并記錄血壓1 次。并囑患者當測量血壓時保持袖帶綁定側上肢靜止。24 h 血壓監測期間每小時至少有1 次血壓讀數,確保有效讀數應占總讀數次數的70%以上[1]。記錄24 h 平均收縮壓(24 h systolic blood pressure,24 h SBP)、24 h 平均舒張壓(24 h diastolic blood pressure,24 h DBP)、白天平均收縮壓(daytime systolic blood pressure,dSBP)、白天平均舒張壓(daytime diastolic blood pressure,dDBP)、夜間平均收縮壓(nighttime systolic blood pressure,nSBP)、夜間舒張壓均值(nighttime diastolic blood pressure,nDBP)、24 h 收縮壓標準差(the standard deviation of 24 h systolic blood pressure,24 h SSD)、24 h 舒張壓標準差(the standard deviation of 24 h diastolic blood pressure,24 h DSD)、白天收縮壓標準差(the standard deviation of daytime systolic blood pressure,dSSD)、白天舒張壓標準差(the standard deviation of daytime diastolic blood pressure,dDSD)、夜間收縮壓標準差(the standard deviation of nighttime systolic blood pressure,nSSD)、夜間舒張壓標準差(the standard deviation of nighttime diastolic blood pressure,nDSD)等指標。
1.2.4 頸動脈超聲檢查 由本院彩超室同一有經驗的醫師應用三MOODEL-WS80A 超聲診斷儀檢查入組對象頸動脈粥樣硬化情況,探頭的頻率為8~12 MHz,取頸總動脈遠端即分叉前2、1.0~1.5 cm范圍內觀察頸總動脈,測量頸動脈內膜中層厚度(IMT),記錄IMT 最厚處;頸動脈分叉IMT 亦選取分叉處前、后壁IMT 最厚處;在舒張末期測定IMT值,記錄3 個心動周期取平均值。IMT<1.0 mm 為正常;IMT 在1.0~1.5 mm 為增厚;IMT>1.5 mm 表示斑塊形成,IMT 增厚和斑塊形成標記為頸動脈硬化[1]。
1.3 統計學處理 使用統計軟件SPSS 26.0 進行所有數據的統計分析,呈正態分布或近似正態分布的計量資料以()表示,組間比較采用單因素方差分析,若方差齊,兩兩間采用LSD 法;若方差不齊,則采用Tamhane’s 法;呈偏態分布的計量資料則以M(P25,P75)表示,組間比較采用秩和檢驗;而計數資料用率(%)表示,組間比較采用χ2檢驗;高血壓患者頸動脈IMT 的影響因素采用Spearman相關分析和二元logistic 回歸分析。以P<0.05 表示差異有統計學意義。
2 結果
2.1 三組一般資料比較 三組年齡、性別、吸煙史、TG、HDL-C、FPG、UA、BMI、Hcy、Scr、HbA1c比較,差異均無統計學意義(P>0.05)。高血壓頸動脈硬化組TC、LDL-C 均高于對照組和單純高血壓組(P<0.05)。單純高血壓組和對照組的TC、LDL-C 比較,差異均無統計學意義(P>0.05)。見表1。
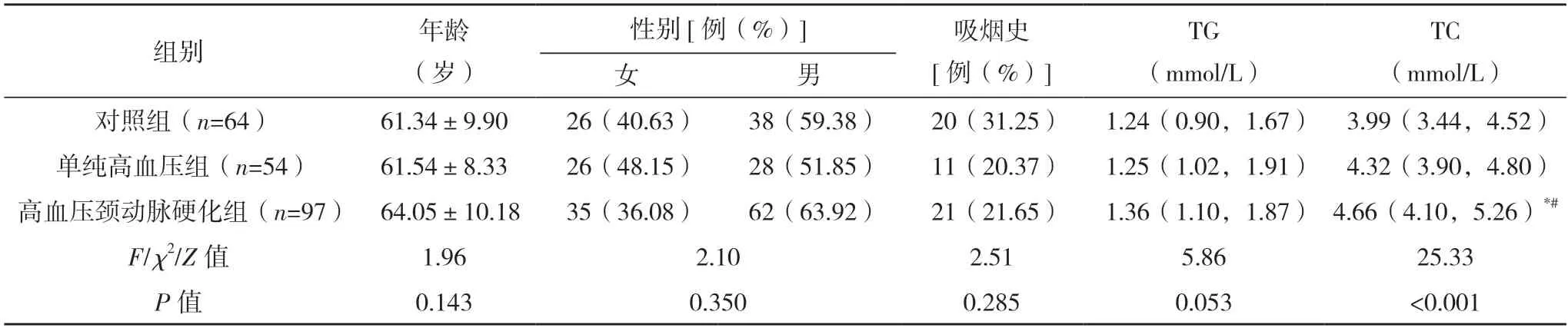
表1 三組一般資料比較
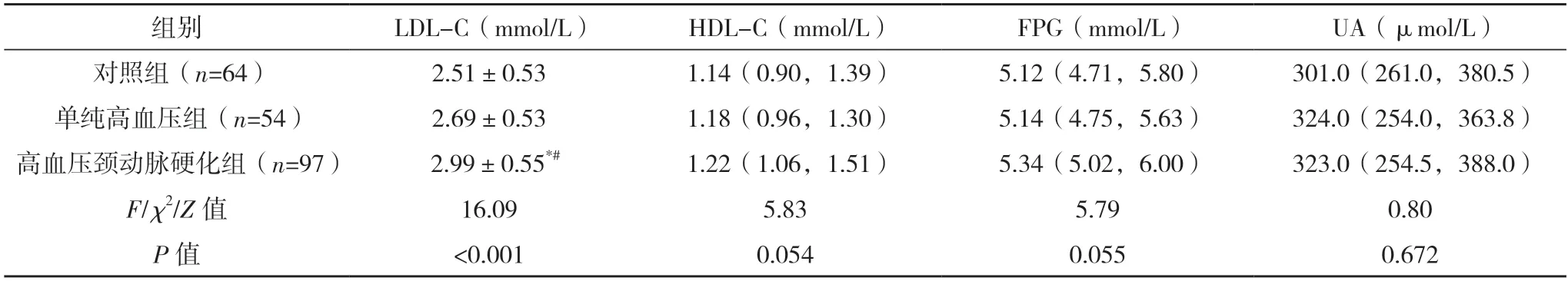
表1(續)
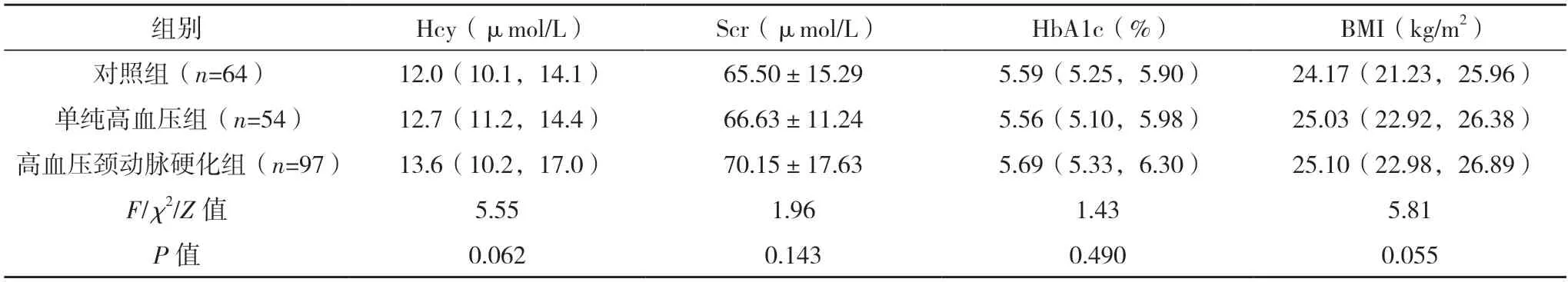
表1(續)
2.2 三組動態血壓水平比較 單純高血壓組和高血壓頸動脈硬化 組24 h SBP、24 h DBP、dSBP、dDBP、nSBP、nDBP 均高于對照組,差異均有統計學意義(P<0.05)。高血壓頸動脈硬化組24 h SBP、dSBP、nSBP 水平均高于單純高血壓組,差異均有統計學意義(P<0.05)。見表2。
表2 三組動態血壓水平比較[mmHg,()]
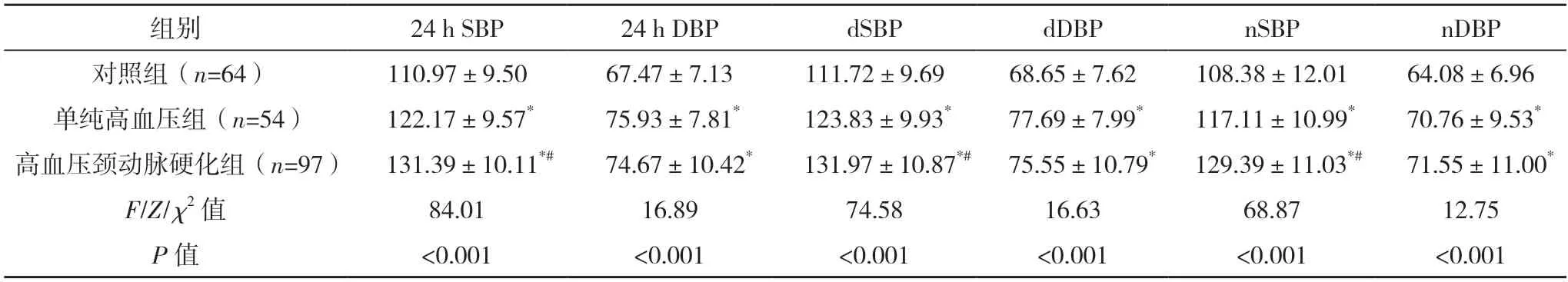
表2 三組動態血壓水平比較[mmHg,()]
*與對照組比較,P<0.05;#與單純高血壓組比較,P<0.05。
2.3 三組血壓變異性指標比較 高血壓頸動脈硬化組24 h SSD、24 h DSD、dSSD、nSSD、nDSD 均高于對照組,差異均有統計學意義(P<0.05)。高血壓頸動脈硬化組24 h SSD、dSSD、nSSD 均高于單純高血壓組,差異均有統計學意義(P<0.05)。見表3。
表3 三組血壓變異性指標比較[mmHg,()]
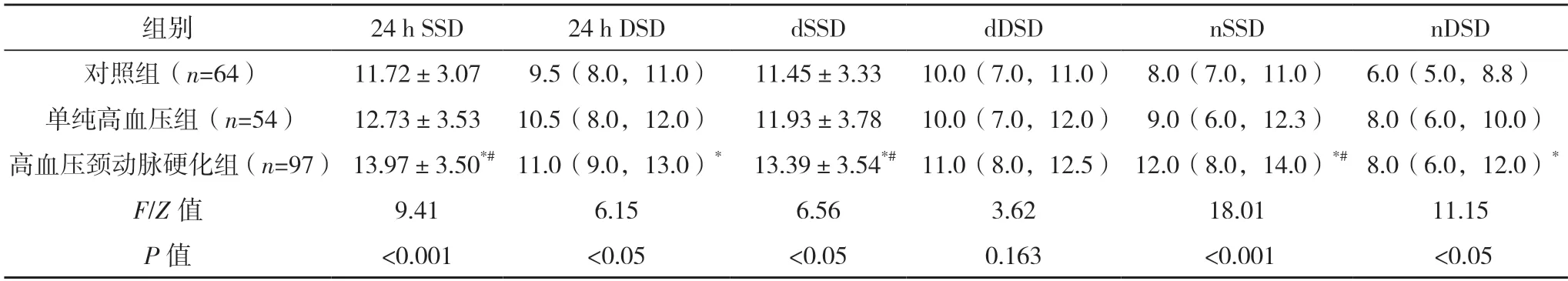
表3 三組血壓變異性指標比較[mmHg,()]
*與對照組比較,P<0.05;#與單純高血壓組比較,P<0.05。
2.4 三組Lp-PLA2、sdLDL-C 水平比較 高血壓頸動脈硬化組Lp-PLA2、sdLDL-C 水平均高于對照組和單純高血壓組,且單純高血壓組均高于對照組,差異均有統計學意義(P<0.05),見表4。
表4 三組Lp-PLA2、sdLDL-C水平比較()
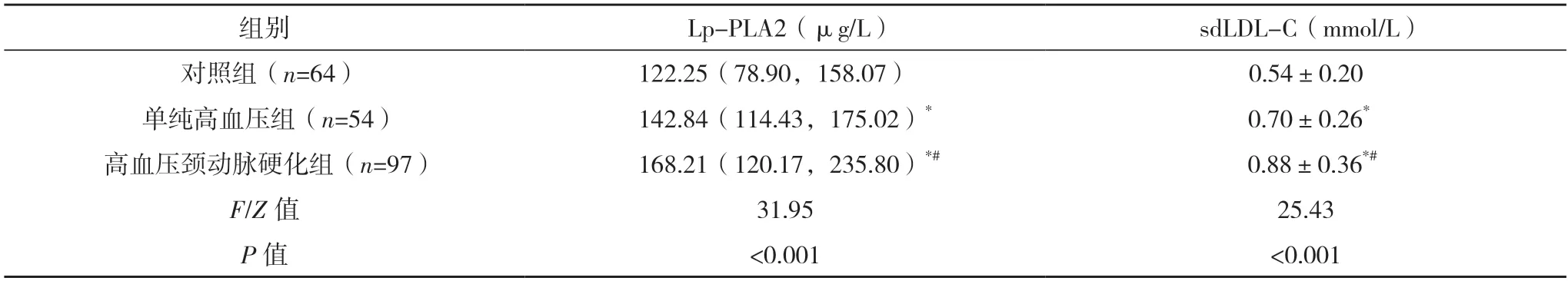
表4 三組Lp-PLA2、sdLDL-C水平比較()
*與對照組比較,P<0.05;#與單純高血壓組比較,P<0.05。
2.5 高血壓組頸動脈硬化程度與Lp-PLA2、sdLDL-C、動態血壓及BPV 參數的相關性分析 Spearman 相關分析可得,高血壓組患者的頸動脈硬化程度與Lp-PLA2、sdLDL-C、24 h SBP、dSBP、nSBP、24 h SSD、dSSD、nSSD 均呈正相關(P<0.05),見表5。
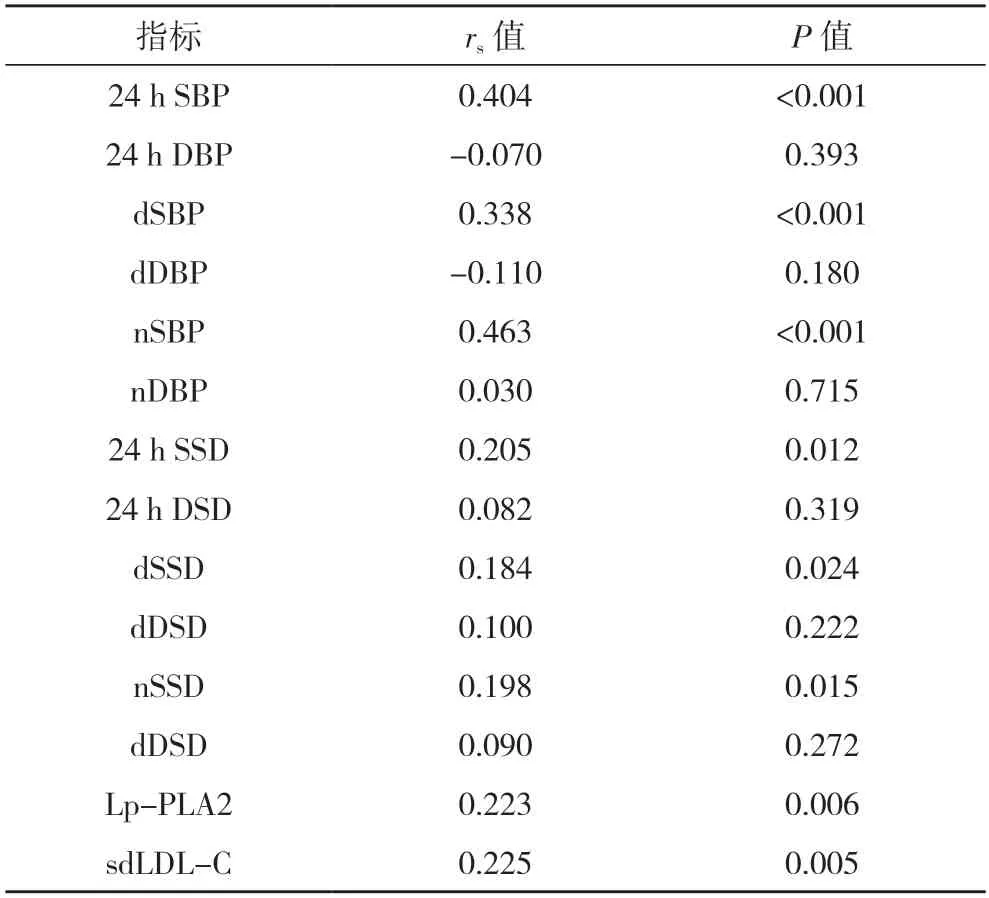
表5 頸動脈硬化程度與Lp-PLA2、sdLDL-C、動態血壓及BPV相關性分析
2.6 Lp-PLA2、sdLDL-C、動態血壓及BPV 對高血壓患者IMT 影響的logistic 回歸分析 高血壓組以是否動脈粥樣硬化為應變量,以Lp-PLA2、sdLDL-C、BPV 及動態血壓的各個指標為協變量,依次進行二元logistic 回歸分析,結果顯示:β 值為2.752,P值為0.022,OR值為15.672,95%CI(1.487,165.179),提示sdLDL-C 是高血壓患者頸動脈硬化的獨立危險因素(P<0.05)。
3 討論
研究發現頸動脈硬化程度可間接反映冠脈、腦等全身大、中血管動脈粥樣硬化的程度,被認為是心腦血管事件的獨立危險因素[7],臨床上經常通過超聲測量IMT 以早期發現動脈血管硬化情況[3]。高血壓、糖尿病、高脂血癥、吸煙等易引發動脈粥樣硬化,具體機制如下:脂質浸潤學說、損傷反應學說、炎癥學說、神經體液調節。這些學說的基礎主要源于血管內皮損傷,血壓增高導致血流速度和沖擊力增加,造成了血管壁的機械性損傷,使脂質、血小板等血管內物質易于沉積在動脈內膜[8-9],從而導致了動脈硬化的發生。目前,高血壓患者BPV與Lp-PLA2、sdLDL-C 及頸動脈硬化的關系鮮有報道。本研究將高血壓患者作為研究對象,根據彩超結果將高血壓患者分為單純高血壓組、高血壓頸動脈硬化組,擬探尋高血壓患者BPV 與Lp-PLA2、sdLDL-C 及頸動脈硬化的關系。
正常人24 h 血壓節律呈“雙峰雙谷”或“雙峰一谷”的曲線變化。在一定時間內血壓變異的程度稱為BPV,可以用動態血壓標準差(SD)和變異系數(CV)表示。本研究通過對151 例高血壓患者和64 例正常人進行分析發現:與單純高血壓組比較,高血壓頸動脈硬化組在24 h SBP、dSBP、nSBP、24 h SSD、dSSD、nSSD 水平升高,而在舒張壓水平則無明顯差異,提示收縮壓及收縮壓變異性可能在老年高血壓人群頸動脈硬化過程中發揮了更重要的作用。相關性分析顯示頸動脈硬化程度與24 h SSD、dSSD、nSSD、24 h SBP、dSBP、nSBP 均呈正相關,由此推測收縮壓及收縮壓變異性可能與高血壓患者靶器官損傷的關系更為密切,與國內外研究基本一致[10]。BPV 對動脈粥樣硬化的影響主要表現在血壓晝夜節律改變加大了對血管壁的壓力,導致了血管內皮損傷,另一方面也可以直接誘發炎癥反應。Li 等[11]觀察了80 例高血壓患者24 h SBPV 與靶器官損害的關系,結果亦發現高血壓組患者24 h SBPV和dSBPV 明顯高于對照組,高BPV 組的冠心病、動脈粥樣硬化斑塊、IMT 等發生率均高于低BPV 組。因此在老年患者降壓過程中,不僅要根據血壓變化特點合理選擇降壓藥將血壓控制在合適的水平,而且要盡量保持正常血壓節律,以減少靶器官損傷。
Lp-PLA2 又稱血小板活化因子乙酰水解酶(PAF-AH),是磷脂酶A2 家族的一個50 kD、Ca2+獨立成員,血液中大約80%的Lp-PLA2 與LDL-C結合,只有約20%與HDL-C 或其他循環脂蛋白結合,其分解氧化低密度脂蛋白(ox-LDL)產生溶血磷脂酰膽堿和氧化自由脂肪酸等物質可促進動脈粥樣硬化的形成[12],被認為是一種新出現的與動脈粥樣硬化相關的炎癥生物標志物[13]。地里夏提·吾斯曼等[14]認為隨著高血壓的分級增高,Lp-PLA2 水平較對照組明顯升高,差異具有統計學意義。一項關于頑固性高血壓患者的研究顯示,高血壓病情越重,血漿Lp-PLA2 水平越高[15]。本研究發現高血壓組血漿Lp-PLA2 水平均明顯高于對照組,高血壓亞組分析時高血壓頸動脈硬化組Lp-PLA2 水平高于單純高血壓組,Spearman 相關性分析顯示Lp-PLA2與頸動脈硬化程度正相關。分析其原因可能為Lp-PLA2 的水平越高,氧化及誘導炎癥反應的能力越強,促進了動脈硬化的形成;而隨著動脈硬化程度的加重,機體通過復雜的生物反應刺激大量Lp-PLA2 的產生,進一步加重了血管內皮的損傷,從而加速了動脈硬化的進展,二者互為因果關系。但回歸分析尚未發現Lp-PLA2 與頸動脈硬化的關系,原因可能是少量患者應用了調脂藥物,會對結果產生影響,未來需大樣本研究進一步證實Lp-PLA2 是否是高血壓頸動脈硬化的獨立危險因素。
研究顯示根據LDL-C 顆粒的異質性、脂蛋白直徑、密度和氧化等特點,可將其分為兩大類,其中LDL-3-7 顆粒較小,稱為sdLDL-C[16-17]。指南中指出LDL-C 在動脈粥樣硬化性心血管疾病(ASCVD)中起著關鍵性作用,LDL-C 水平降低是ASCVD 一級和二級預防的主要治療目標[18]。但在臨床工作中,發現許多LDL-C 水平正常或低于正常范圍的患者仍可檢出動脈粥樣硬化斑塊[16],提示亞組分可能影響動脈粥樣硬化的進展。一項關于sdLDL-C與冠心病風險的前瞻性、大樣本的研究顯示:血清sdLDL-C 水平是未來冠心病發展的相關生物標志物,它提供了除血清LDL-C 水平之外的益處[19]。Hanlu 等[20]臨床研究結果表明,sdLDL-C 是高危卒中患者心腦血管事件的危險因素,與心腦血管事件呈正相關。但在高血壓患者的研究中目前相對較少,有部分小樣本研究顯示:與對照組相比,sdLDL-C水平在高血壓患者中更高[21-22]。本研究發現,高血壓組sdLDL-C 水平高于對照組,差異有統計學意義(P<0.05);進一步對高血壓組分析,高血壓頸動脈硬化組sdLDL-C 水平高于單純高血壓組,差異仍有統計學意義(P<0.05),說明sdLDL-C 可能致高血壓患者頸動脈硬化形成的能力更強,在高血壓治療過程中,降低sdLDL-C 水平有望成為新的方向;logistic 回歸分析表明sdLDL-C 是高血壓患者頸動脈硬化的獨立危險因素。這一觀點可解釋為:(1)sdLDL 顆粒較小,與肝臟LDL 受體的親和力較低,清除緩慢,在血液中滯留時間長;(2)sdLDL 增加氧化修飾,抗氧化能力減低;(3)sdLDL 對動脈蛋白多糖氧化親和力和敏感性增加等[21,23]。
本研究的局限性:為小樣本、單中心,未來需完善大樣本、多中心研究;其次影響動脈硬化的因素眾多,尚未對混雜因素校正。
綜上所述,本文明確了Lp-PLA2、sdLDL-C、BPV 對高血壓患者頸動脈硬化的影響,有助于在臨床上早期識別危險因素,從而早期干預,使高血壓患早期臨床獲益,對預防高血壓患者心腦血管疾病具有重要意義。

