基于穩定同位素的葡萄酒摻糖鑒別技術研究進展
李信萍,劉亞新,齊鵬宇,康天浩,譚丹,馬雯,張昂*
(1. 寧夏大學食品與葡萄酒學院,寧夏銀川 750021;2. 河北省葡萄酒質量安全檢測重點實驗室,河北秦皇島 066000;3. 秦皇島海關技術中心,河北秦皇島 066000)
葡萄酒作為一種營養豐富的低酒精度飲料酒,適量飲用可以養顏益壽,防治心血管等疾病,深受消費者的青睞。隨著我國葡萄酒市場日漸繁榮,葡萄酒的消費量呈快速增長趨勢[1]。在經濟利益驅動下,市場上葡萄酒摻假現象時常發生,一些不法生產商在葡萄酒釀造過程中,通過摻外源糖、外源水等手段來調整酒精度[2]。這些行為不僅侵犯了消費者的權益,擾亂葡萄酒市場的秩序,同時也損害了葡萄酒行業的形象[3]。目前國內外針對葡萄酒摻偽鑒別的方法多種多樣,其中最行之有效的當屬利用各種穩定同位素建立的鑒別技術。王廣浩[4]利用乙醇同位素分析-同位素比質譜法(Ethanol Isotope Measurement-Isotope Ratio Mass Spectrometry, EIMIRMS)和點特異性天然同位素分餾核磁共振(Specific Natural Isotope Fractionation of Nuclear Magnetic Resonance, SNIF-NMR)測定葡萄酒樣品中δ2H值來鑒別葡萄酒中外源糖的添加,發現葡萄酒樣品中乙醇不可交換位點δ2H值被用來鑒別摻糖葡萄酒。譚夢茹等[5]采用元素分析-同位素質譜儀(Elementary Analyzer-Isotope Ratio Mass Spectrometers,EA-IRMS)對不同種類純正葡萄汁的糖、有機酸δ13C值進行測定,初步建立了純正葡萄汁中δ13C值的數據庫,根據糖和有機酸δ13C值間的差異鑒別葡萄汁中C4植物糖的摻假。王道兵等[6]建立了連續流穩定同位素比質譜儀(Gas BenchⅡ-Isotope Ratio Mass Spectrometers,Gas BenchⅡ-IRMS)測定葡萄酒水中氧同位素組成的在線分析方法來鑒別摻水葡萄酒。本文綜述了穩定同位素技術在葡萄酒摻糖鑒別中的研究進展,比較了穩定同位素技術在葡萄酒摻糖鑒別中的優缺點,重點闡述了碳、氫穩定同位素在葡萄酒摻糖鑒別中的應用,旨在為我國葡萄酒真實性鑒別建立數據庫提供參考,以期促進葡萄酒真實性鑒別的深入研究。
1 穩定同位素技術概述
同位素是指含有相同質子數、不同中子數的一類元素,分為C、H、O、N等輕同位素和Pb、Sr等重同位素[7]。自然界中,生物體會不斷與外界環境進行物質交換,穩定同位素會在物理、化學、生化反應過程中發生同位素分餾。外界環境條件不同、自身代謝模式的差異,都會導致不同來源的生物體內穩定同位素的自然豐度存在差異,這種差異可以作為鑒別食品真實性的有效指標[8-9]。
目前,穩定同位素技術是國內外應用于食品真實性鑒別研究較多的技術,其中主要用來鑒別葡萄酒摻糖的穩定同位素聯用技術,見表1。
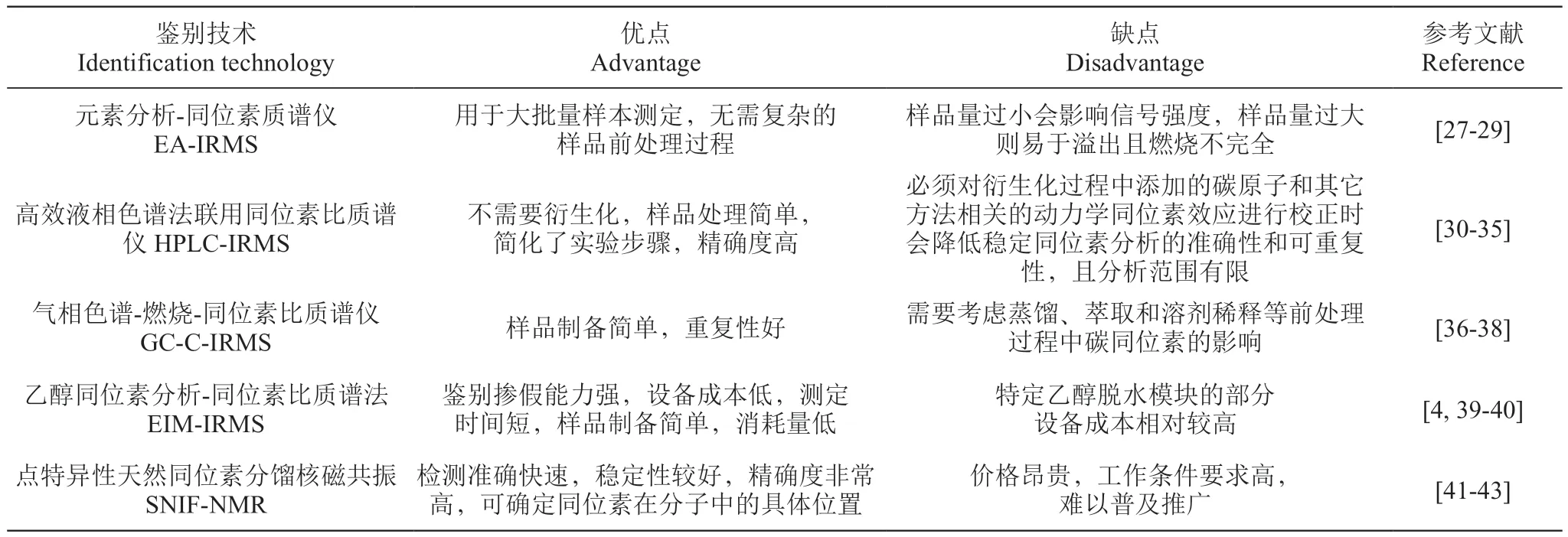
表1 穩定同位素聯用技術的原理及優缺點Table 1 Principle and advantages and disadvantages of stable isotope combination technology
C、H、O是最常用的幾種穩定同位素,也是組成生物體含量的主要元素,屬于原子水平信息,不會隨著外源物的添加而改變,也不可進行人為更改[10-11]。外界環境(氣候條件、地理位置、土壤來源等)條件和自身代謝模式的差異,都會使不同來源生物體內穩定同位素自然豐度存在差異[12-16]。C同位素作為最重要的生命元素,自然界中以12C和13C兩種形式存在,其組成與光合碳代謝途徑息息相關[17-18]。溫度、降水量和CO2濃度都是影響C同位素豐度的主要因素[19-20]。除此以外,壓力、光照、大氣壓等其它因素也會影響C同位素豐度[21]。H、O同位素以單質和化合物的形式遍布全球。H同位素主要有1H、2H、3H三種,其中1H、2H常被用于食品的真實性分析[4]。由于H同位素質量小,在化學反應中更容易發生分餾,溫度、降水、溫度、離海距離等都會影響它的豐度[22]。O同位素主要有16O、17O、18O三種,地下水、植物組織自身的蒸騰作用、生產過程中的濃縮都會影響O同位素豐度改變[23-24]。植物體中穩定C、H、O同位素因質量不同,在一些環境因素作用下產生分餾,使不同來源植源性食品的同位素自然豐度產生差異,這種差異可用來鑒別食品的真實性[25-26]。
2 穩定同位素技術在葡萄酒摻糖鑒別中的應用
隨著消費者對食品安全要求的與日俱增,葡萄酒作為食品中的重要組成部分,真實性問題也逐漸進入消費者視野[44]。在葡萄酒真實性領域中,穩定同位素技術是目前國內外應用于葡萄酒摻糖鑒別研究較多的技術手段之一[10]。其中,C、H穩定同位素是最常用于葡萄酒真實性鑒別的兩種同位素,目前已在葡萄酒真實性鑒別中得到了廣泛的研究和應用,見表2。
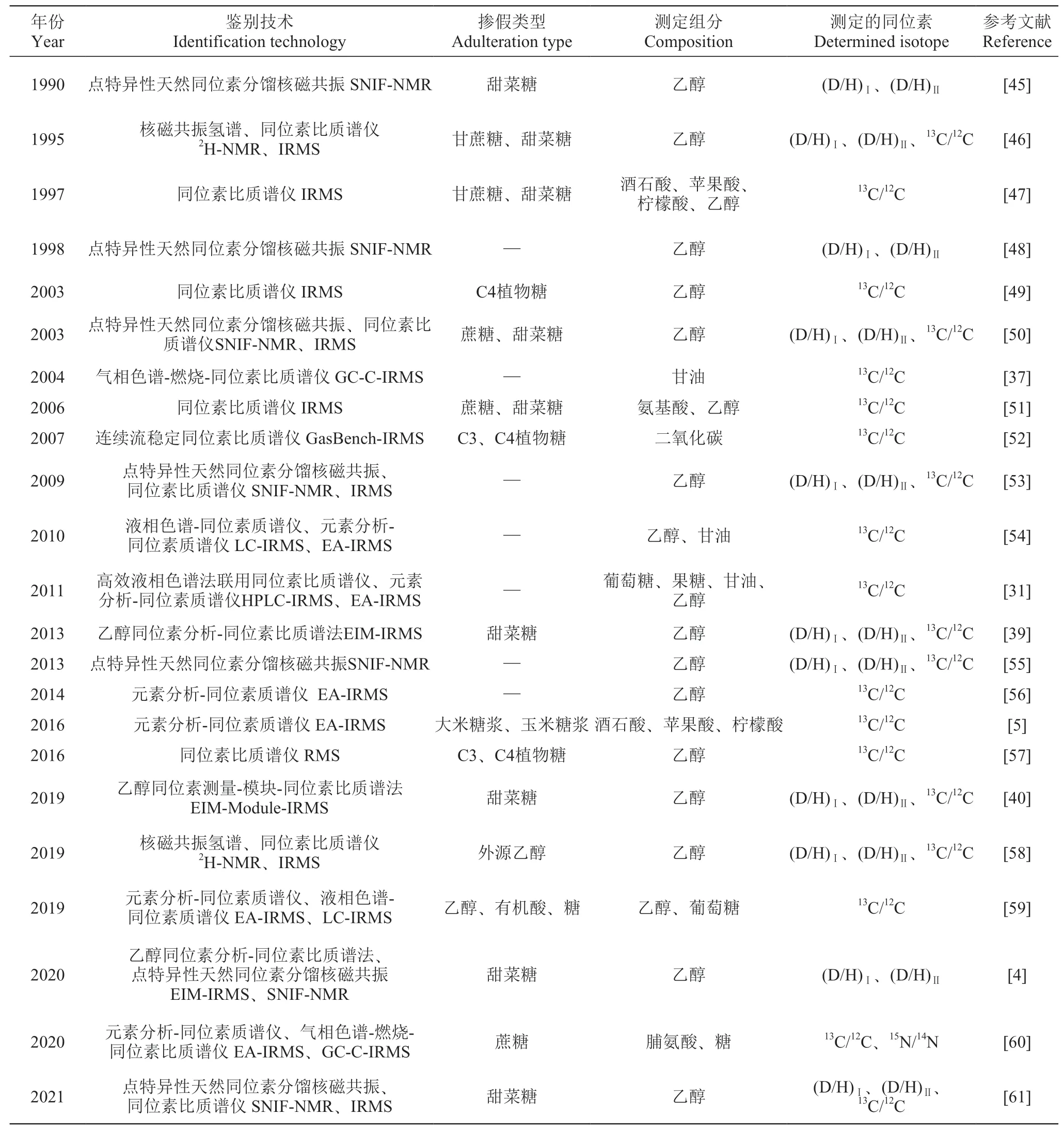
表2 C、H穩定同位素在葡萄酒摻糖鑒別中的應用Table 2 Application of C and H stable isotopes in wine sugar identification
2.1 碳同位素在葡萄酒摻糖鑒別中的應用
目前穩定同位素用于鑒別葡萄酒摻糖已成為研究熱點[14,62]。其中,C穩定同位素被用于葡萄酒摻糖鑒別的依據是C4和C3兩種不同植物光合作用代謝途徑所得產物δ13C值的差異[5]。但由于δ13C值不同的外源糖較多,建立數據庫工作量較大,需要利用葡萄酒發酵過程中產生的副產物δ13C值間的差異進行判定,如甘油、有機酸、氨基酸等與乙醇結合鑒別葡萄酒發酵過程中外源糖的添加[63]。這些不同來源的碳是否被混合,可通過比較同位素δ13C值之間的差異來鑒別[64]。
2.1.1 乙醇
葡萄酒中的乙醇是由果實中糖分在無氧條件下,酵母菌通過對糖的不完全分解而產生的,故乙醇δ13C值與糖組分中δ13C值具有同源性,但由于各種因素的作用,每個產地葡萄果實中糖分含量不同,其發酵產生的乙醇δ13C值也有差異[65-66]。在葡萄汁發酵過程中添加外源糖,會引起乙醇δ13C值改變,因此,乙醇δ13C值可用于追溯葡萄汁發酵時有無外源糖的摻入[67]。
Martinelli等[49]采用IRMS技術測定了巴西和美國起泡葡萄酒乙醇δ13C值來鑒別葡萄酒的摻糖情況,該技術僅鑒別出了部分葡萄酒樣添加了C4植物糖,但對于混合類型的植物糖仍需結合其它化學方法來進行鑒別。李學民等[56]采用EA-IRMS和LC-IRMS技術測定國內外40款葡萄酒樣品中乙醇δ13C值,發現這兩種技術的檢測結果差值具有很強的相關性,且采用EA-IRMS技術測定葡萄酒乙醇δ13C值,具有較好的精密度和準確度,為葡萄酒摻假鑒別研究奠定了基礎。相比之下,Cabanero等[68]利用HPLC-IRMS和GC-IRMS技術,通過優化葡萄酒基質中分離乙醇的柱溫度、流動相、流量和注入方式等參數,分析了23個不同來源的葡萄酒樣品乙醇δ13C值。研究發現,優化儀器參數后能夠改進現有的葡萄酒摻假檢測方法,并克服了樣品制備的困難。此外,與傳統方法相比,HPLC-IRMS技術耗時少、操作簡單、重復性好、無同位素分餾,可用于葡萄酒中乙醇δ13C值的高精度測量,被認為是一種快速、準確、簡單的葡萄酒摻糖檢測方法。
2.1.2 甘油
甘油是葡萄酒發酵過程中的主要副產物[69]。在酒精發酵開始時,參加3-磷酸甘油醛轉化為3-磷酸甘油酸這一反應所需的輔酶Ⅰ(NAD),是通過磷酸二羧丙酮的氧化作用來提供的,甘油伴隨著這一氧化作用產生。
葡萄酒數據庫的建立需要大量數據,這些數據的收集需要投入大量的人力和時間。為此,Cabanero等[54]利用HPLC-co-IRMS技術分析葡萄酒中乙醇和甘油δ13C值之間的差異來鑒別葡萄酒的真實性。結果表明,該技術簡單、快速,用乙醇和甘油δ13C值之間的差異可以作為鑒別葡萄酒真實性的依據,但兩者之間的差異也會因產地和葡萄酒類型有所不同。Calderone等[37]采用GC-CIRMS技術對歐盟數據庫中170種葡萄酒樣品中甘油δ13C值進行分析,認為該技術成功地解決了在大量葡萄酒樣品中添加甘油的問題,且樣品制備簡單,重復性好。但不足之處是難以將葡萄酒中的甘油從其它濃縮的成分中完全分離出來,需要考慮蒸餾、萃取和溶劑稀釋等前處理過程中C同位素的影響[37-38]。李學民等[70]采用LC-IRMS技術測定葡萄酒中甘油和乙醇δ13C值鑒別葡萄酒摻假問題,結果表明,該方法的精密度可達0.015%~0.026%,有較好的重現性,是可以同時測定葡萄酒中甘油和乙醇δ13C值的首選方法,既克服了樣品處理技術的困難,同時提高了檢測速度,達到了鑒別葡萄酒真實性的目的。
2.1.3 有機酸
蘋果酸、酒石酸、乳酸、檸檬酸等作為葡萄酒中主要的有機酸,對葡萄酒品質的優劣起著重要作用[71-72]。其中酒石酸是葡萄酒中特有的有機酸,占葡萄酒總酸的四分之一,也是酸度最高的有機酸,對葡萄成熟和葡萄酒發酵起著重要作用;蘋果酸是葡萄酒發酵的重要中間產物,是生物體代謝三羧酸循環及其支路乙醛酸循環的中間產物,具有巨大的生物學作用;檸檬酸存在于葡萄原料中;葡萄酒釀造過程中的蘋果酸-乳酸發酵會產生另一種重要的有機酸——乳酸,乳酸會影響葡萄酒的成熟,至葡萄酒發酵結束[73]。
Weber等[47]采用IRMS技術對57種來自萊茵普法爾茲地區不同年份葡萄酒中的乙醇、L-戊二酸、L-酒石酸和檸檬酸的δ13C值進行測定,建立有機酸與糖、乙醇之間的同位素相關性,鑒別葡萄酒摻假。結果表明:糖δ13C值與乙醇δ13C值之間存在良好的相關性,并發現葡萄酒中乙醇和檸檬酸δ13C值有緊密相關性,可以將葡萄酒中的有機酸作為內標物質結合乙醇、糖δ13C值來鑒別葡萄酒中外源糖的摻入。譚夢茹等[5]采用EA-IRMS技術對152個不同產區純正葡萄汁的糖和有機酸δ13C值進行測定,初步建立了純正葡萄汁的同位素數據庫,分析了純正葡萄汁應滿足糖和有機酸δ13C值的限定要求。依據這個限定條件,對市售葡萄汁、自制摻入外源糖、有機酸的葡萄汁中糖和有機酸δ13C值進行測定,分析兩者δ13C值的差異。結果表明,采用該技術檢出了摻入C4植物糖和有機酸的樣品,且在摻假鑒別的靈敏度方面顯示了很大優勢,有較好的應用前景。
2.1.4 氨基酸
葡萄汁發酵過程中,氨基酸由酵母菌自溶而形成,是酒精發酵結束后乳酸菌的營養物質。有研究表明,采用GC-C-IRMS測定葡萄酒中脯氨酸和糖組分的δ13C值是一種新的分析工具,可以支持和改進葡萄酒中添加外源糖的檢測[60]。
Perini等[60]開發了一種能夠鑒別葡萄酒摻糖和確定加糖量的新方法,采用EA-IRMS技術分析了葡萄汁發酵過程中提取的糖δ13C值,采用GC-C-IRMS技術分析了萃取和衍生化后脯氨酸的δ13C值。結果表明,葡萄酒中糖和氨基酸的同位素組成之間存在相關性,在葡萄汁發酵過程中添加外源糖,只能改變糖組分的δ13C值,而不改變脯氨酸的δ13C值。因此,糖組分和脯氨酸δ13C值的相關性分析可以被認為是一個可靠的內部標準,來鑒別外源糖的添加。
2.1.5 葡萄糖、果糖
葡萄糖和果糖作為葡萄酒中的重要組成成分,是由蔗糖預先經酵母菌本身分泌的轉化酶或葡萄果實中的轉化酶水解而產生。
Guyon等[31]通過HPLC-co-IRMS技術測定了20款來自法國的葡萄酒樣品中的葡萄糖、果糖、甘油和乙醇δ13C值,鑒別半甜型葡萄酒中糖的真實性。結果表明:該技術實現了葡萄糖、果糖、甘油和乙醇的完全分離和δ13C值測定,外源葡萄糖、果糖或甘油的添加均會使δ13C值發生變化,且該方法對添加物的檢出限低至2.5 g·L-1,具有良好的再現性和重復性。通過比較δ13C值之間的差異發現,該技術可以鑒別葡萄酒中C4植物糖的添加,對C3植物糖和葡萄酒中一些有機酸的鑒別也提供了寶貴信息。
2.2 氫同位素在葡萄酒摻糖鑒別中的應用
葡萄酒中的同位素以2H/1H、13C/12C、18O/16O為主,在葡萄汁發酵前,添加外源糖進行發酵,會影響發酵后酒精中氘(D)的分布,氘同位素會在甲基位(CH2DCH2OH)、次甲基(CH3CHDOH)、羥基位(CH3CH2OD)和水分子(HOD)4個位點重新分布,這種分布特點被稱為點特異性同位素分布[74]。有研究表明,葡萄酒乙醇分子中甲基位(D/H)Ⅰ含量很大程度上取決于發酵糖的氘含量,它代表著糖的植物來源[64]。
在葡萄酒真實性鑒別中,SNIF-NMR是第一個被歐盟委員會用于分析葡萄酒乙醇分子中δ2H值差異的技術,是推進葡萄酒真實性鑒別的一個里程碑,為鑒別葡萄酒的真實性做出了重大貢獻[42,44]。Martin等[75]在上世紀80年代采用該技術分析乙醇中δ2H對谷物酒和果酒的摻糖進行鑒別,Markus采用SNIF-NMR在葡萄酒發酵前加入不同類型外源糖,通過測定乙醇中(D/H)Ⅰ、(D/H)Ⅱ含量,根據含量變化有效鑒別出摻入單一外源糖的類型,但對于混合植物類型的外源糖卻無法鑒別。相比之下,Kosir等[76]同時采用IRMS技術和SNIF-NMR結合主成分分析(Principal Components Analysis,PCA)、聚類分析(Cluster Analysis,CA)等化學計量學方法測定斯洛文尼亞3個產區中葡萄酒中乙醇δ13C值和δ2H值,有效鑒別了葡萄酒發酵過程中不同類型外源糖的摻入。2008年,蔣露等[43]首次采用SNIF-NMR測定葡萄酒乙醇(D/H)Ⅰ、(D/H)Ⅱ。結果表明,乙醇分子中不同位點H含量可用來鑒別葡萄酒在釀造過程中是否進行了加糖操作。Smajlovi等[39]2013年采用EIM-Module-IRMS測定摻糖葡萄汁發酵蒸餾樣品與真實葡萄汁發酵蒸餾樣品乙醇δ2H值來鑒別外源糖的摻入,結果表明,該方法與SNIF-NMR相比,能夠以更高的準確性來鑒別葡萄酒中外源糖的添加,并能檢測出無指定來源葡萄酒的非法生產行為。2019年,采用EIM-Module-IRMS對42個摻假葡萄酒樣品中乙醇δDn值、水δ18O值和乙醇δ13C值進行測定,結果表明,使用葡萄酒乙醇中δDn值分析參數可以有效鑒別非法葡萄酒生產實踐中外源糖的摻入和乙醇的來源[40]。王廣浩等[4]模擬真假葡萄酒樣,蒸餾后采用EIM-Module-IRMS和SNIF-NMR分析酒樣中乙醇不可交換δ2H值和(D/H)Ⅰ含量,鑒別葡萄酒中外源糖的添加。結果證明,兩種方法都能夠實現葡萄酒中外源糖的鑒別,但在現有蒸餾系統的條件下EIM-Module-IRMS比SNIF-NMR更適合鑒別葡萄酒中外源糖的摻入,且該技術具有鑒別能力高、對儀器要求低、測定時間短、測定步驟簡單、樣品消耗量少等優點。
穩定同位素聯用技術與其它化學計量法聯合使用對同位素進行分析,能夠有效降低葡萄酒摻糖判定誤差,提高葡萄酒摻糖的鑒別效率,已成為解決葡萄酒摻糖的強有力手段。這些聯用技術對實現我國葡萄酒市場的有效監管、促進葡萄酒市場向規范化發展具有極其重要的指導意義[64]。
3 結語
GB/T 15037—2006《葡萄酒》作為葡萄酒行業最重要、最基礎的標準,但與真實性相關的水、糖、乙醇等添加方面沒有明確的要求。鑒于此,在葡萄酒真實性領域中,國家制定了與葡萄酒質量相關的標準并拓展了鑒別摻假的技術,其中,穩定同位素聯用技術在葡萄酒摻糖鑒別中展現出獨特的優勢。針對葡萄酒中不同類型外源糖的添加,穩定同位素聯用技術穩定性相對較好,能有效提高鑒別準確率,能準確快速對樣品δ13C值進行測定,對鑒別葡萄酒摻假做出了巨大貢獻。針對摻入單一類型的C4植物糖能夠進行有效鑒別,但對于摻入與葡萄光合原理相同的C3植物糖,因為兩者的δ13C值相近,沒有明顯的差異,不能有效地進行鑒別,可借助SNIFNMR測定葡萄酒中乙醇不同位點H的含量來鑒別。
穩定同位素技術結合尖端、高效的化學方法鑒別葡萄酒真實性已在國際上認定為非常有效的分析工具并在實際應用中取得了一些效果。但對于形成完整、行之有效的鑒別技術目前仍存在以下幾方面的問題:(1)同位素值不同的外源糖類型較多、摻假的方式多樣性、摻假物質的復雜性逐漸增加,導致使用單一穩定同位素技術對葡萄酒摻糖進行鑒別存在一定的難度和局限性;(2)當葡萄酒中摻入外源糖的穩定同位素值與葡萄酒的穩定同位素值特別接近時,單獨使用該方法進行鑒別存在一定的困難,需借助其他的鑒別方法加以輔助;(3)同位素質譜儀設備和標準品價格昂貴限制了該技術在葡萄酒摻糖鑒別中的發展和應用,所以不斷開發儀器的應用,降低檢測成本,才能在葡萄酒真實性鑒別中得到更廣泛的應用。
未來,隨著摻假物質的復雜化,摻假手段的多樣化,采用單一技術很難對葡萄酒摻糖進行全面準確地鑒別。因此,為了提高穩定同位素技術在葡萄酒摻假鑒別方面的準確性和有效性,采用多技術聯用,并在此基礎上結合一些化學計量學方法,建立覆蓋面更全的葡萄酒鑒別模型數據庫,是發展穩定同位素技術在葡萄酒真實性分析領域應用的必然趨勢,也將為我國葡萄酒市場乃至全世界葡萄酒市場健康發展提供有力保障。

