外源性脈沖電磁場干擾下的心臟起搏器“窗口效應”及防護
盧 武, 丁苒苒, 趙文彬, 黃 冬, 王哲銘
(1. 上海電力大學 電氣工程學院,上海 200090; 2. 上海交通大學附屬第六人民醫院 心內科,上海 200233)
工業、醫療、電信或無線領域中的數據傳輸大多具有脈沖性質,外源性脈沖電磁場(Pulsed Electromagnetic Field, PEMF)廣泛存在于人們生產生活的各個角落[1-2].特定職業環境、醫療場景及日常生活的PEMF產生的電磁干擾(Electromagnetic Interference, EMI)安全防護問題應得到關注.大功率PEMF對普通人的健康尚不構成威脅,但對植入式電子設備如心臟起搏器佩戴者的健康可能造成一定影響.目前我國35歲以上人群的心衰率高達1.3%,心臟起搏器植入人數呈直線上升的趨勢,預計到2022年起搏器滲透率將達到0.118%,且植入人群逐漸低齡化和普遍化[3].在此情況下,大功率脈沖電磁場對起搏器佩戴者健康的潛在威脅更需要得到關注.
雖然引入了包括鈦合金外殼、饋通濾波器和雙極引線在內的先進電磁屏蔽技術來降低起搏器的電磁敏感性,但自1970年以來,電磁波引起的起搏器電磁干擾事件頻發[4-5].一旦發生嚴重的電磁干擾,可能會導致起搏器發生脈沖被抑制、起搏器誤動作、起搏器電子電路永久性損壞甚至導致患者心室顫動和死亡等嚴重后果[3, 6-8].起搏器電磁干擾產生的主要原因是起搏器脈沖發生電路與外源性電磁場發生電磁耦合[6].大量在體與離體實驗表明外源性工頻電磁場對起搏器有實質影響[9-13].如文獻[9]中發現在50 Hz或60 Hz工頻電磁輻射中,當接觸電流達到25~300 μA(對應場強約3~24 kV/m)時,將發生起搏器過感知事件.電網職業環境、醫療環境和日常生活中低頻(kHz級)瞬態電場磁場較為常見[14].但目前對低頻瞬態電磁場引發的起搏器電磁干擾研究較少.低頻瞬態電磁場與工頻電磁場中的電磁干擾發生機制不同,低頻瞬態電磁場引起的起搏器電磁干擾主要取決于傳輸信號中的非周期性分量,即PEMF,其中醫療場景和電網職業場景中的PEMF對起搏器佩戴者影響較大,但這些干擾源對心臟起搏器佩戴者的影響機制尚不明確[14].因此,亟需解析生物組織的脈沖電流空間耦合場效應現象的明確機制,幫助推動心臟起搏器佩戴者在脈沖磁場中電磁安全防護標準的制定.
本文通過離體實驗,在傳輸線中注入快波前特性電流(1~5 kA幅值,μs級脈沖寬度)模擬常見醫療和電網職業場景產生頻率為kHz、磁場強度為幾千A/m的典型PEMF對起搏器佩戴者的影響,包括由PEMF觸發的典型起搏器故障,以及短路電流功率與起搏器電磁干擾嚴重程度之間的關系.并且通過改變囊袋中起搏器導線的纏繞術形,探究PEMF與起搏器的電磁耦合窗口.基于實驗結果,提出模擬人體胸腔解剖學結構的傳輸線等效模型,并對PEMF在固/液態組織界面上的傳播和衰減特性進行分析.此外,利用有限元(Finite Element Method,FEM)仿真軟件構建心臟植入電子裝置與組織結合的參數化暫態生物電磁模型,以確認在PEMF作用下的起搏器回路電磁耦合窗口效應,并在此仿真模型上建立基于窗口效應的防護措施.
1 典型脈沖電磁場特征
典型脈沖電磁場特性可以用磁場強度進行表征.文獻[15]指出發生短路的電氣設備可以等效為圓柱體模型.在低頻電磁場的情況下,以圓柱體模型的底面圓心為中心建立圓柱坐標系,則發生短路的電氣設備周圍空間中任意點的磁場強度可以通過如下方程組推算,即
(1)
式中:E為任意點的電場強度;H為該點處磁場強度;B為該點處磁感應強度;J為傳導電流密度;D為位移電流;A為磁矢位;μ為空氣磁導率;ε為處于脈沖電磁場傳播頻率下的組織介電常數;t為時間.由于本文所研究內容均處于低頻段,所以位移電流可以忽略.用文獻[15-25]中不同情形下給定的電流除以設備的等效橫截面積,可以推導出傳導電流密度,將傳導電流密度代入式(1)可得出磁場強度.根據文獻[15-25]所描述的暫態電流推算出典型場景磁場強度,如表1所示.表中:IA為電流幅值;D1為操作距離.當磁場強度高于 150 A/m 時,起搏器EMI水平需要評估[21].表1統計數據和文獻[14]研究表明,電網職業暴露環境和醫療環境中更易形成速波前時間(μs級)和較高電磁輻射(kA/m 級)的PEMF,這類脈沖電磁場的磁場強度遠高于 150 A/m,將會對起搏器佩戴者造成嚴重影響.因此本文主要研究電網暫態過程和低頻醫療設備使用過程產生的脈沖電磁場對起搏器佩戴者的影響.
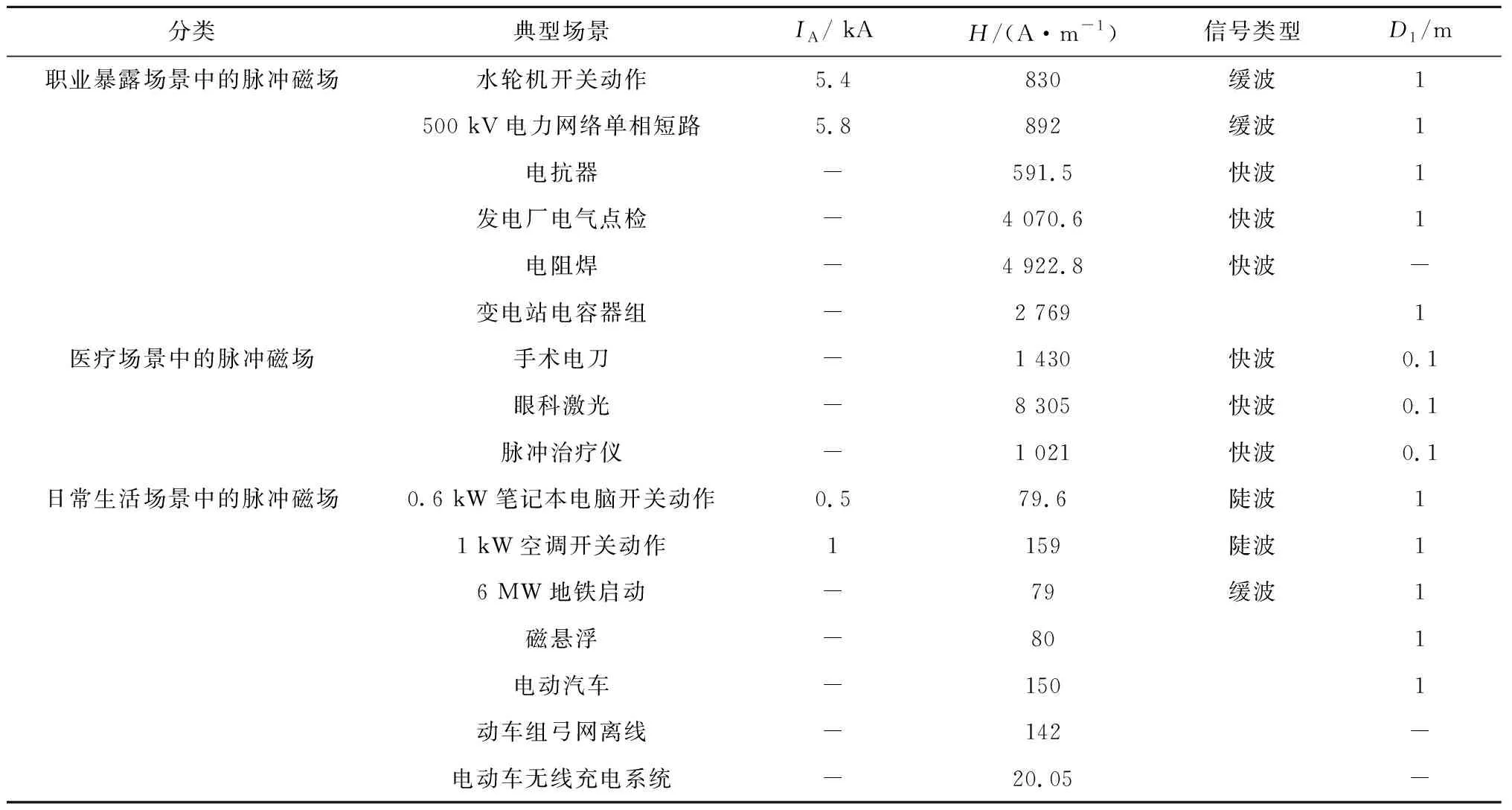
表1 典型脈沖電磁場的固有特性Tab.1 Inherent characteristics of typical PEMFs
一般來說,脈沖電磁場低頻周期分量的輻射功率較低[10-11],不會對附近電氣設備造成電磁干擾.因此,由瞬態電磁場引起的起搏器EMI主要取決于傳輸信號中持續時間為ns~μs級的非周期性分量,即PEMF.由于電網短路信號、合閘信號以及低頻醫療設備使用時產生的電磁場均具有波前持續時間短(μs級及以下)的特性,所以這些信號產生的瞬態電磁場均可以視為PEMF.根據IEC TR 60071-4—2004[25],實際的PEMF可以描述為緩波前、快波前和陡波前暫態電磁場.相較其他兩種信號,快波前功率較大,對電力系統影響范圍較廣,同時在醫療環境也較為常見[14, 26].因此,下一節中描述的起搏器電磁干擾測試采用幅值在kA級的標準快波前脈沖電流源以模擬常見電力設備投切過程和常見醫療設備產生的PEMF(頻率為kHz級,磁場強度為kA/m級)對起搏器佩戴者的影響.
2 PEMF對心臟起搏器電磁干擾效應研究
2.1 實驗平臺
為了最大限度還原真實場景中PEMF產生的EMI對心臟起搏器佩戴者的影響,構建如圖1所示的離體實驗系統.整個離體實驗測試系統由電磁干擾輻射源、人體胸腔等效模型、可植入式電磁干擾監測裝置組成.其中,電磁干擾輻射源由脈沖電流發生器、放電球隙器,以及一根直徑為4 mm的圓柱形通電銅線組成.信號通過5 kV·A電源激勵和 220 V/5 kV 升壓變壓器,經過100 kV/1 A整流器進行調制產生直流電壓,并將直流電壓注入由1 μF電容器組成的能量存儲單元中完成充電.充電完成后,利用球隙發出開關信號來產生幅值為1~5 kA的脈沖電流.操作距離為銅線到人體胸腔等效模型皮膚表面的距離.注入銅線的脈沖電流是由開關信號和RLC串聯電路中的阻尼振蕩共同形成的快波前信號,波型如圖2所示,其中上升時間約為5 μs,持續時間約為30 μs.由于PEMF中的磁場分量分布在與傳播方向垂直的橫平面內,這與通電導線周圍的磁場分布相同,所以可以將脈沖電流注入銅線以模擬電氣設備投切過程和低頻脈沖治療儀等醫療設備產生的μs級衰減震蕩電流.本文將1~5 kA電流注入通電銅線,并將通電銅線與人體胸腔模型之間的距離設置為150 mm.根據式(1)計算可得,此電流下產生的磁場強度,與實際情形下典型的PEMF在人體周圍產生的磁場強度數量級一致.
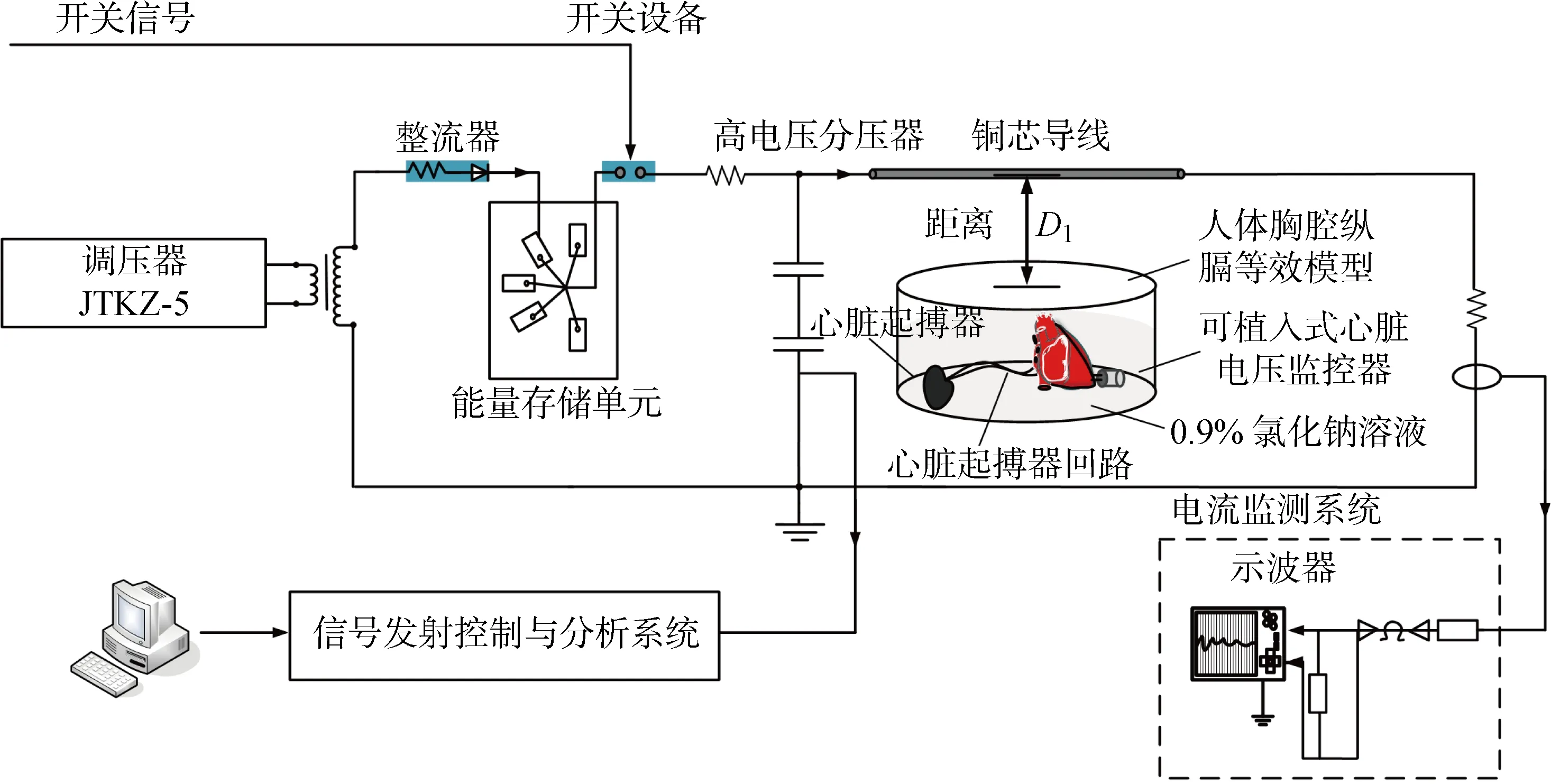
圖1 用于模擬起搏器受脈沖電磁場干擾的實驗系統構成圖Fig.1 Configuration of test system for pacemaker EMI generated from PEMFs
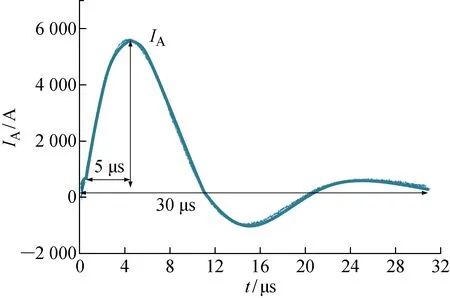
圖2 快波前脈沖電流典型波型Fig.2 Typical waveform of fast-front impulse current
本文使用的人體胸腔等效模型包括豬肉、豬心、豬肋骨和帶有雙極引線的起搏器,如圖3所示.圖中:Φ為直徑.文獻[27-29]表明,精確的離體實驗應使用0.9%氯化鈉溶液模擬人體電解質,因此本文在高 400 mm、直徑600 mm圓柱形亞克力筒中注滿含質量濃度為 0.9 g/L的氯化鈉溶液用以模擬體液環境.該亞克力筒的尺寸可以較好地匹配成人患者胸部的典型解剖尺寸[18].實驗過程中,人體胸腔等效模型被完全浸入0.9%氯化鈉溶液中,且豬肋排完全于覆蓋豬心臟上方,并整體放置于亞克力支架上,以模擬真實人體結構中心臟與胸部外層組織結構的相對位置.
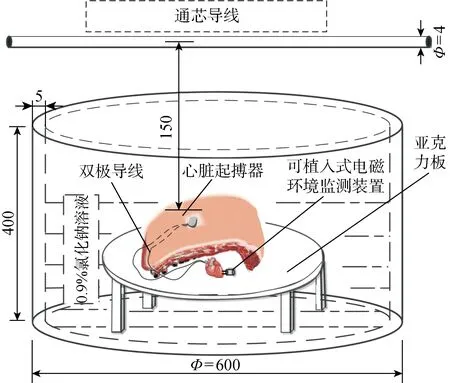
圖3 用于植入式起搏器的人體胸腔等效模型(mm)Fig.3 Human torso phantom for implantable pacemakers (mm)
以國內市場滲透率最高的St. Jude AccentDR PM2112、Medtronic Relia RED01、Vitatron E50D E50A1這3種雙腔起搏器為測試對象,分別記為起搏器A,B和C.起搏器系統的典型尺寸如圖4所示.在實驗中,起搏器P波和R波的感知閾值分別為2.5 mV和 0.5 mV.起搏采用DDD模式,脈沖以 60次/min 作為基本起搏速率,且脈沖幅值設置為 2.5 V,脈沖寬度設置為0.5 ms.實驗中使用主動固定雙極起搏導線(心房導線為Medtronic 5076,長度為52 cm;心室導線為Medtronic 5076,長度為58 cm)連接起搏器和豬心臟.實驗操作嚴格按照人體心臟起搏器植入術式進行,脈沖發生器植入由皮下組織從胸大肌分離形成的囊袋中.與脈沖發生器相連的兩根起搏器導線通過鎖骨穿刺手術,經靜脈分別導入右心房與右心室中,具體操作過程如圖5所示.
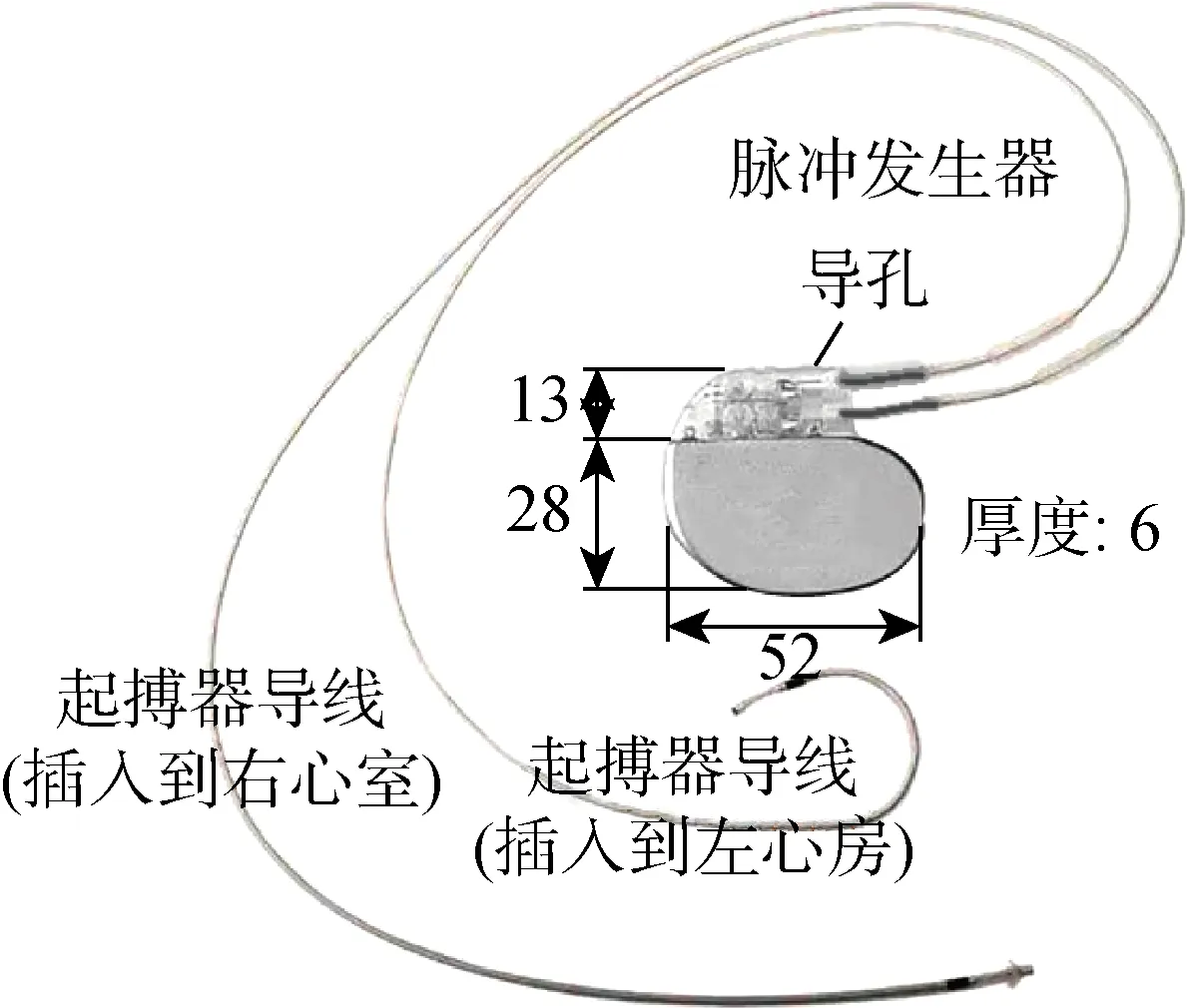
圖4 電磁干擾測試中使用的起搏器尺寸(mm)Fig.4 Dimensions of pacemaker used in EMI test (mm)
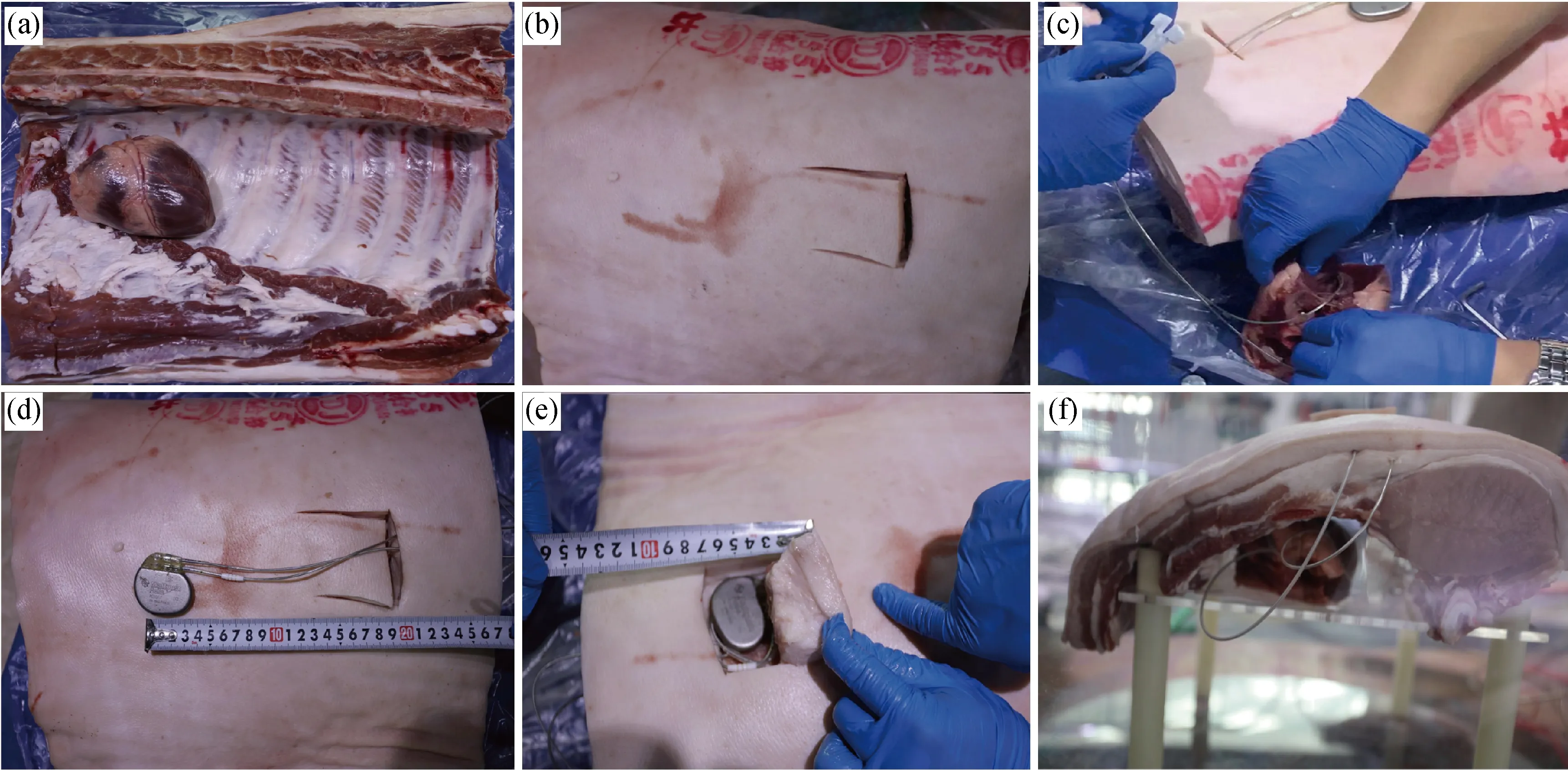
圖5 模擬人體起搏器植入術的心臟起搏器植入過程Fig.5 Pacemaker implantation process following heart surgery
實際情形中,脈沖電磁場的非周期性分量可能會在起搏回路中引起頻率遠高于1 kHz的電磁干擾,這些高頻信號無法被臨床中使用的起搏器程控儀有效檢測[29].為解決上述問題,設計一款基于無線通信傳播的可植入式電磁干擾監測裝置,其結構與工作原理如圖6所示.圖中:I/O、IIC表示接口;DC表示直流;AC表示交流.實驗中,植入式裝置嵌入豬心臟表面,利用其頂部探針對心肌表面心電信號進行監測.探針記錄的信號經過集成電阻網絡和高通濾波器后,在高靈敏度低噪聲的運算放大器TLV9152中放大.放大的心電圖(Electrocardiogram, ECG)信號經過16位逐次逼近寄存器型(Successive Approximation Register, SAR)模數轉換器(Analog to Digital Converter, ADC)轉為數字信號,隨后傳送至中央處理單元(Central Processing Unit, CPU)MSP432P4011RGCR中,CPU使用幀結構打包ADC輸出數據.記錄的數據存儲在 1 GB 的串行外接口(Serial Peripheral Interface, SPI)閃存中,并通過節能藍牙發射器無線傳輸到上位機.本裝置由3.7 V的鋰電池供電,前期測試表明在4 m通信距離內本裝置工作穩定能實現數據的高效傳輸且本裝置具有高達1 MHz的采樣率.
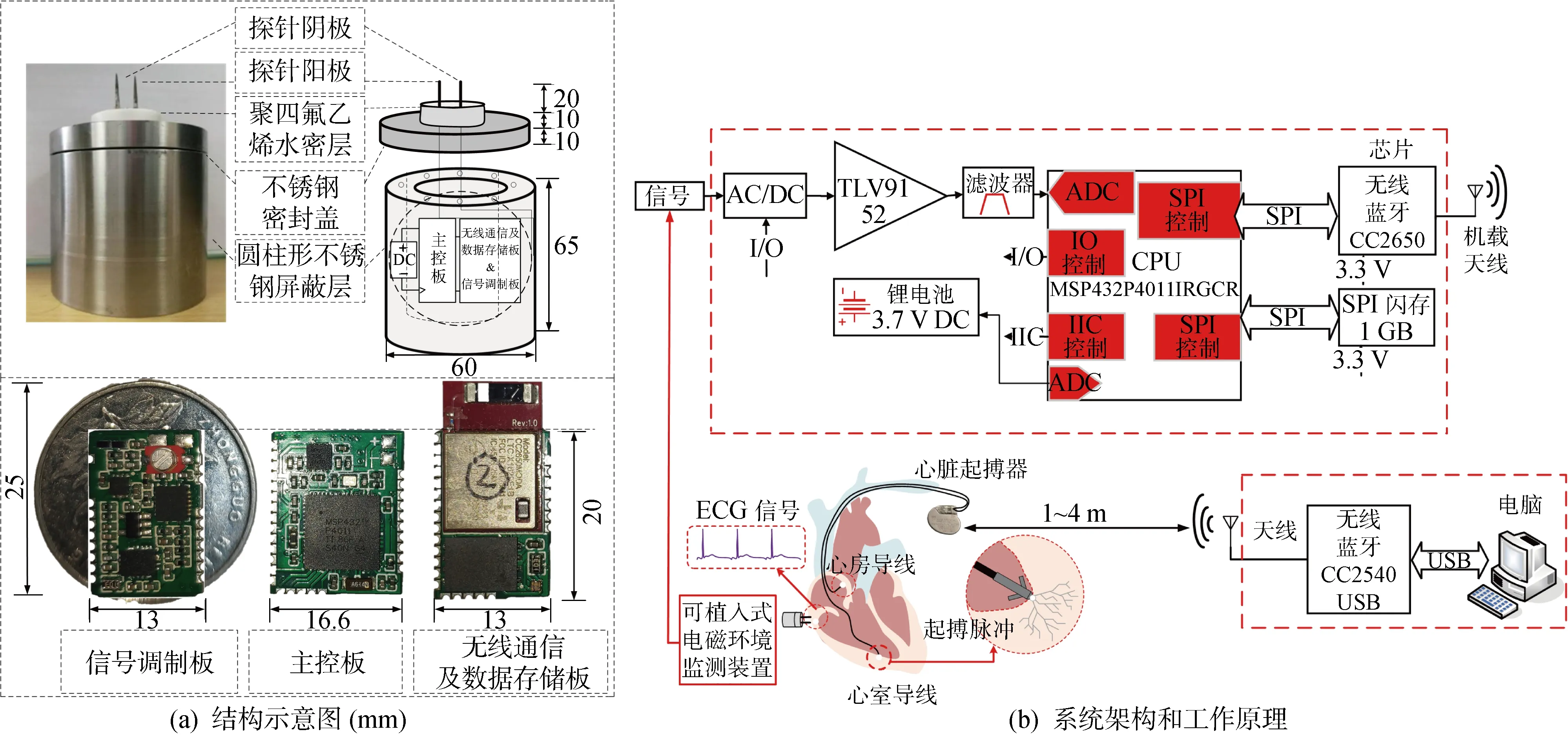
圖6 可植入式電磁環境監測裝置系統Fig.6 System overview of bio-integrated electromagnetic environment monitoring detector
2.2 實驗方法
起搏器電磁干擾離體實驗在上海電力大學高電壓技術實驗室完成.實驗中以1 kA為步長,將快波前脈沖電流源的數值從1 kA增至5 kA.使用示波器記錄輸入脈沖電流波型,同時利用植入式電磁環境監測裝置實時采集與心臟起搏器導線相連的心肌表面電壓信號.由于橫平面電磁波包括折反射和衰減,很難直接用磁通強度測量起搏回路中感應的EMI水平,所以本文選起搏回路中心肌上感應電壓的幅值作為電磁干擾強度的參考.每個脈沖電流等級下完成10組測量,取感應電壓平均值作為該條件下EMI強度.
2.3 實驗結果
2.3.1脈沖電磁干擾對起搏器的危害 當電磁干擾源處于關閉狀態時,起搏器發出起搏脈沖刺激豬心臟,心肌上將檢測到幅值約為50~60 mV的正常心電信號,如圖7所示.圖中:UA為電壓幅值.由于體外試驗使用的豬心臟不跳動,所以不會發生形成P波的心房去極化過程[30].起搏器輸出信號僅表示心室去極化過程的QRS波群,即實驗采集的正常起搏脈沖幀代表實際中正常的QRS波群波型.當電磁干擾源工作時,在離體測試期間可觀察到兩類起搏器故障,即脈沖發出高尖P波信號和起搏器過感知.如圖8所示,當起搏器暴露于PEMF時,心電圖上會出現持續時間為幾十微秒、幅值遠大于 2.5 mV 的電磁干擾信號,可以被認為是異常的P波.起搏器EMI引起的高尖P波心電信號,與實際中具有肺型P波(PH)的真實心電波型相似,這意味著當起搏器在日常和臨床場景中短期暴露于具有快波前的PEMF時,可能會出現類似短期PH造成的心絞痛和胸痛[31].而當患者在電網職業場景中長期暴露于快波前PEMF時,可能會出現類似長期PH導致的勞力性呼吸困難和疲憊感[31].
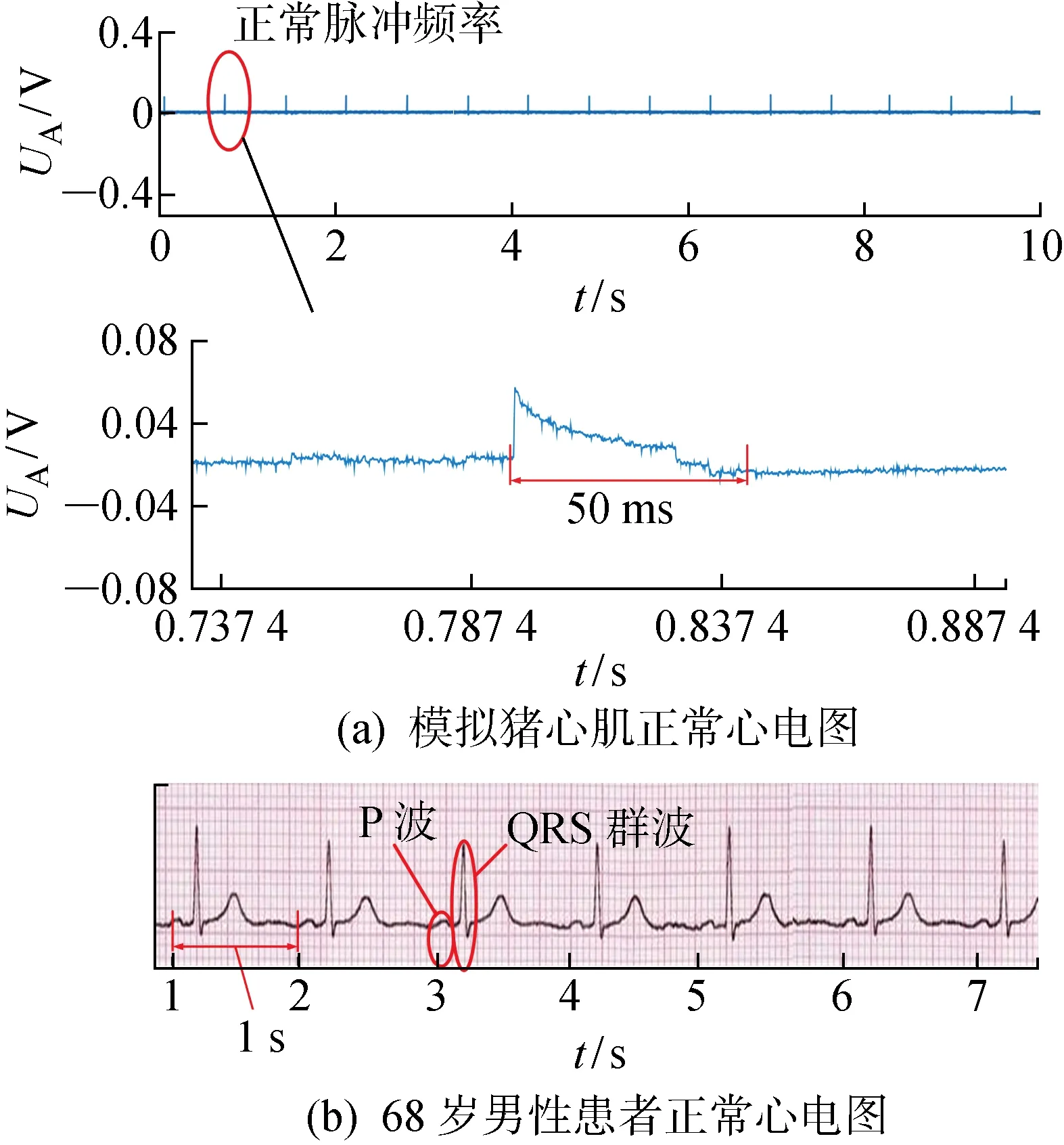
圖7 模擬和真實情況下的正常心電圖對比Fig.7 Simulated and real normal ECG waveforms
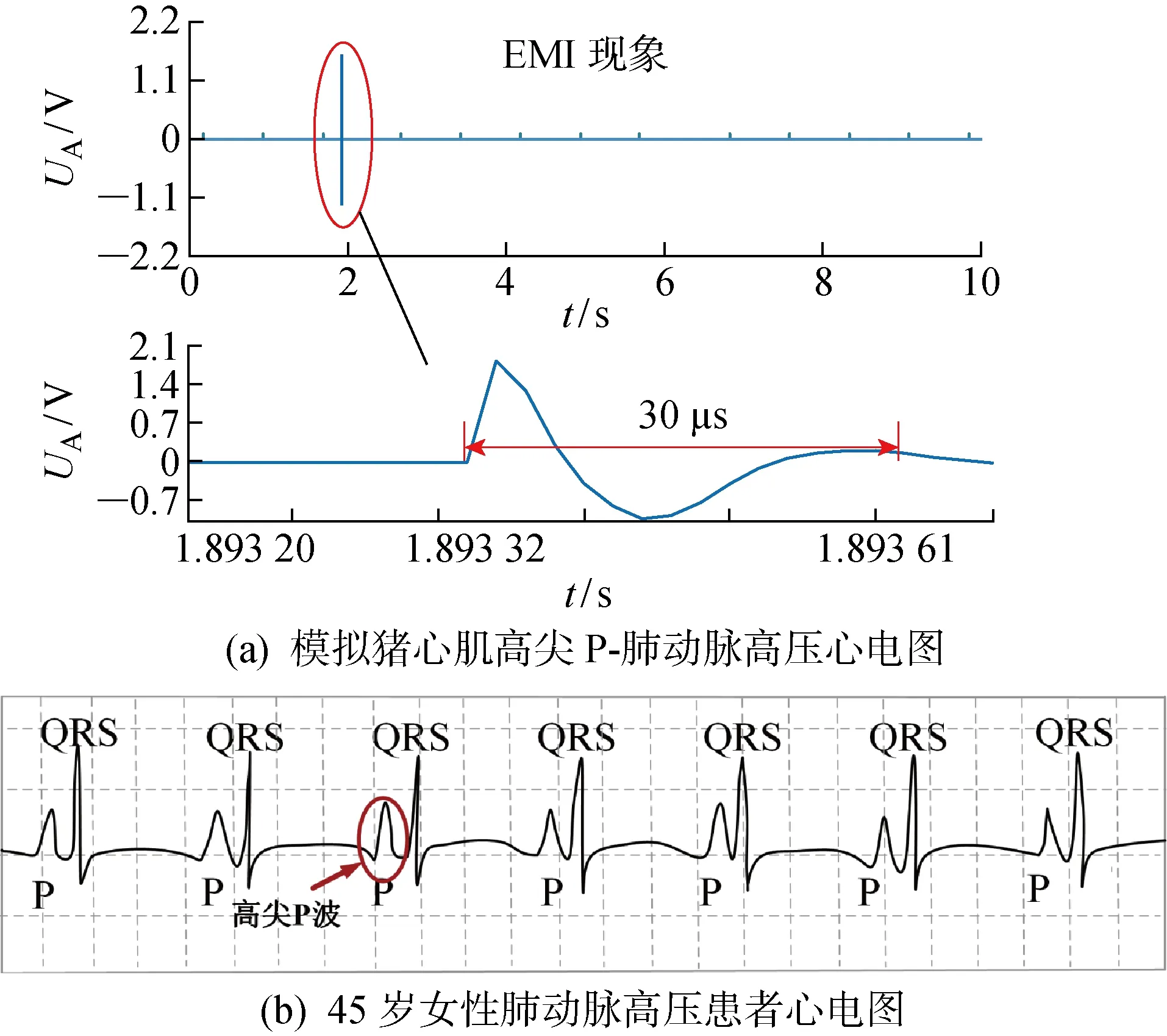
圖8 模擬和真實情況下的高尖P波心電圖波型Fig.8 Simulated and real P-pulmonale ECG waveforms
此外,當脈沖電磁干擾導致的異常心電信號出現在起搏器正常脈沖周期時,由于異常心電信號的幅值遠高于起搏器的靈敏度,起搏器可能會將其誤認為豬心臟產生的正常心電信號.這會導致來自起搏器的正常起搏脈沖被阻斷,出現起搏器過感知故障,即兩個正常起搏脈沖之間的時間間隔超過 1 000 ms.起搏器電磁干擾引起的起搏過感知心電信號典型波型如圖9所示,其與實際中具有呼吸性竇性心律失常(Respiratory Sinus Arrhythmia, RSA)的真實心電圖波型相似.這意味著在日常和臨床中,起搏器暴露于快波前PEMF時,可能會使起搏器出現過感知問題,這會導致患者出現類似呼吸性竇性心律失常造成的頭暈感,長期職業暴露更可能導致患者出現心悸和胸悶的癥狀[32].
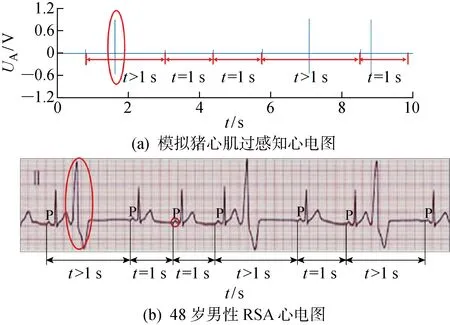
圖9 模擬和真實情況下的過感知心電圖波型Fig.9 Simulated and real over-sensing ECG waveforms
圖10和圖11分別描述了3種起搏器的起搏回路中感應電壓幅值和起搏器過感知發生概率隨著脈沖電流增加的變化趨勢.圖中:P為過感知發生概率,其結果以同一電壓等級下3種起搏器過感知概率的平均值作為參考.結果表明,起搏器電磁干擾強度和起搏器過感知發生概率隨著沖擊電流幅值的增加而增大.在5 kA沖擊電流下的電磁干擾強度比 1 kA 沖擊電流下的EMI強度高約2~3倍,同時起搏器過感知概率高約1.7倍.
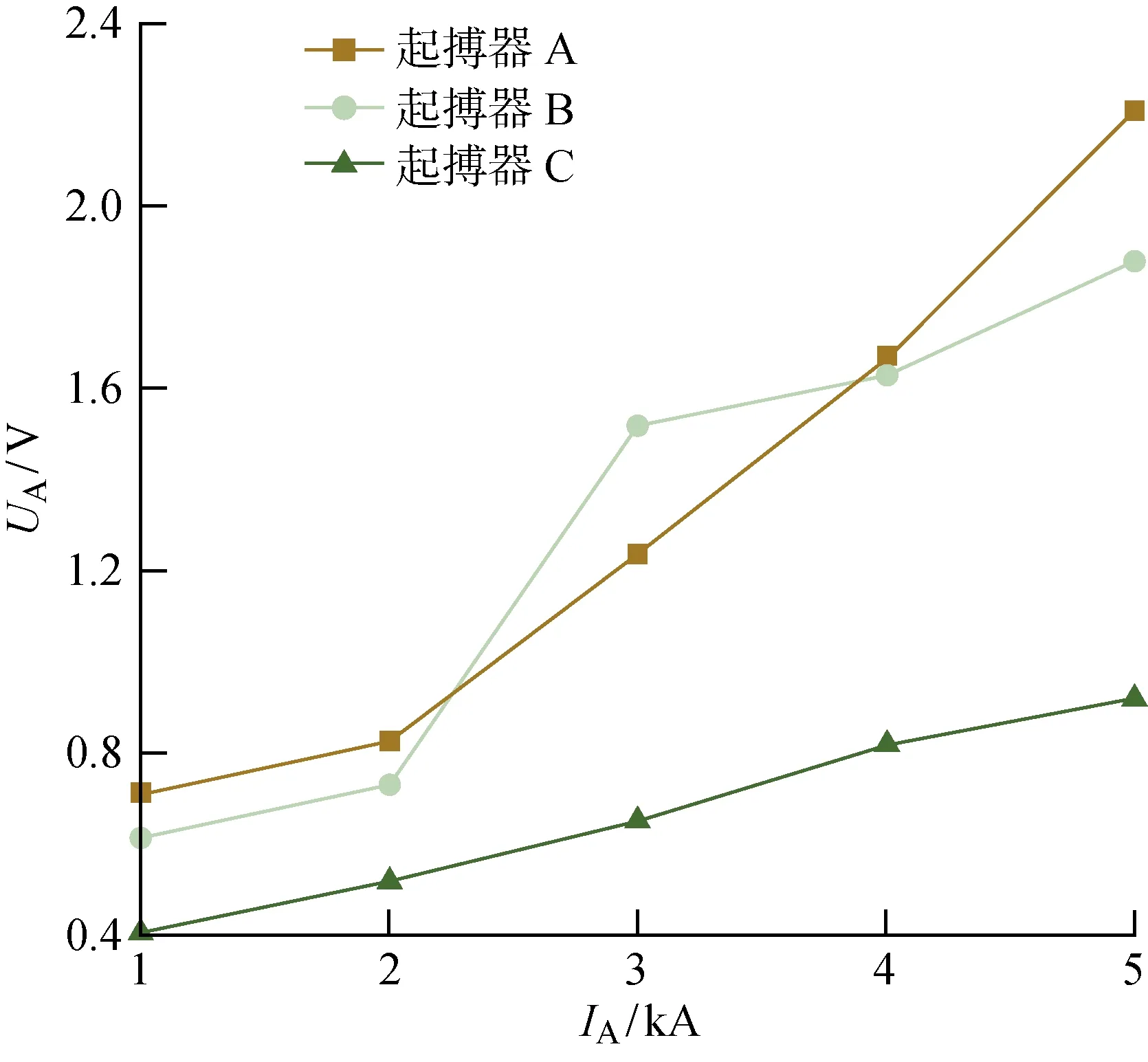
圖10 電磁干擾強度與脈沖磁場幅度的關系Fig.10 EMI intensity versus PEMFs magnitude
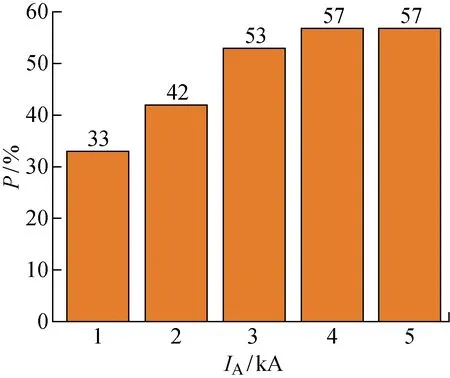
圖11 起搏過感知發生率與脈沖電磁場幅度的關系Fig.11 Incidence of pacing inhibition versus PEMF magnitude
2.3.2脈沖電磁干擾下囊袋回路的“窗口效應” 目前臨床上往往采用醫療風險管理的方式,即通過管控心臟起搏器從生產到使用全過程的安全性檢測來保證用械安全,但該方法無法做到從源頭減小乃至消除起搏器EMI[33].已有研究發現在外源性電磁波作用下,起搏器導線端部產生的感應電壓與起搏器回路在人體中形成的回路面積密切相關[6].而通信中常用的非屏蔽雙絞線模型正是通過改變導線回路面積改善EMI現象.因此本文參考非屏蔽雙絞線模型,對起搏器導線進行優化纏繞,以減小起搏器導線回路產生的EMI,如圖12所示.起搏器導線電極閉環分為埋入皮下組織與胸肌層剝離后所形成囊袋中的外部回路以及浸入胸肌和胸骨血管中的內部回路.由于血管中的面積無法改變,所以本文只通過優化囊袋中導線的纏繞方式以降低導線回路面積.以起搏器A為例,術形改變的實驗結果如圖13所示,可見囊袋中起搏器回路面積與電磁干擾強度成線性正相關.當囊袋中回路面積減小85%時,電磁干擾降低至常規術式的1/10,即降低22 dB, 這表明囊袋中回路面積對體內電磁干擾起決定作用,即囊袋中外部回路為脈沖電磁場與起搏器的電磁耦合窗口.
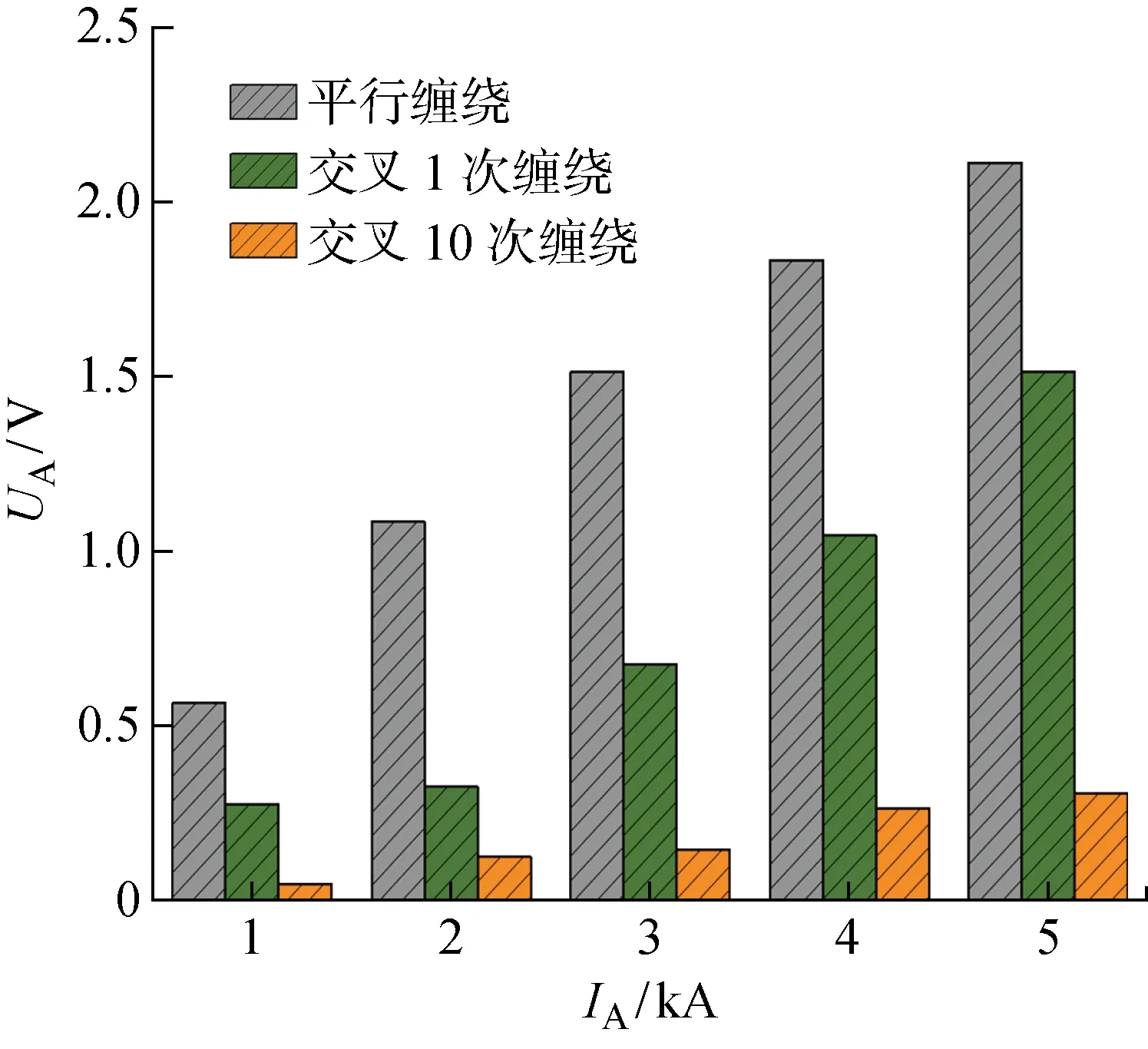
圖13 術形改變后電磁干擾強度與脈沖磁場幅度的關系Fig.13 EMI intensity versus PEMFs magnitude after twisting the excess leads for several turns
3 脈沖電磁場與起搏器的電磁耦合窗口形成機理
3.1 人體胸腔結構的脈沖形成線模型
根據2.3.2節實驗結果可知,僅減小囊袋中起搏器外部回路面積便可以有效降低PEMF對起搏器的電磁干擾強度.然而根據解剖結構,埋入囊袋中的起搏器外部回路面積占整體起搏回路面積的比例較小,由此可以初步得出囊袋組織內起搏器外回路對電磁易感,同時浸入血管的起搏器內回路對暫態電磁波具有很強的電磁屏蔽效應.外回路包含多組織界面,其高電磁敏感性可以通過多層組織的傳輸線模型來解釋.如圖14所示,脈沖電磁場通過多個組織間界面的傳播可視為在單脈沖形成線(Pulse Forming Line, PFL)網絡中進行[34].PFL的電路模型由電感和電容元件級聯的一系列T拓撲電路結構組成.每個T拓撲電路結構代表脈沖電磁場經過空氣-皮膚、皮膚-脂肪、脂肪-肌肉分界面的電路模型,圖中R,G,L,C分別為PFL模型單位長度的電阻、電導、電感和電容;下角標從0~4分別代表空氣、皮膚、脂肪、肌肉和血液層的特征阻抗,K0~K4分別代表單脈沖形成線電路模型中的開關;Zlead為線路阻抗.電流發生器接通的瞬間,脈沖電磁場波前時間內的躍遷能量被存儲于傳輸線的電容中,而傳輸線的電感則用于存儲脈沖電磁場波尾時間的躍遷能量,兩者共同作用,使具有一定能量的電磁波由外及內向下一級組織分界面傳播.同時,在單脈沖形成線中多次折反射引起的電磁波傳播延遲將導致脈沖電磁場的波型在通過組織分界面時發生波型壓縮[34-35].對于單脈沖形成線,脈沖電磁場在通過某一級組織的脈沖持續時間可以計算為
(2)
式中:l為組織層厚度;σ為處于脈沖電磁場傳播頻率下的組織電導率;v為自由空間中電磁波的速度.由于人體各組織層的厚度僅為約2~10 mm,而本文使用的快波前PEMF可視為具有單一頻率的脈沖波型,其頻率可計算為f=0.45/Tf=9×104Hz,其中波前時間Tf為5 μs.在此頻率下,可以推算出PEMF的脈沖持續時間在通過空氣/皮膚界面后被壓縮到只有幾納秒,此時PEMF在人體組織中的傳播過程可視為平面電磁波在遠場區域傳播.同時由于組織間界面的厚度可以忽略不計,界面處幾乎沒有電磁波能量的吸收和耗散,通過將每個組織層簡化為均勻介質,電磁波傳播特性可以估計為
α=
(3)
β=
(4)
式中:α為衰減常數;β為相位常數;Rx,Lx,Cx為單脈沖形成線模型單位長度的電阻、電感和電容;ω為電磁波的角頻率.當電磁波在單脈沖形成線中傳播會逐級產生波型壓縮,因此脈沖電磁場逐級穿過組織時,電磁波角頻率會不斷增加.當脈沖電磁波到達肌肉和血液層時,α值已經變得極高.因此,脈沖電磁場極難穿透肌肉/血液界面,與內部回路相互作用,即只有外部起搏回路可以作為脈沖電磁場與起搏器的生物電磁相互作用窗口.
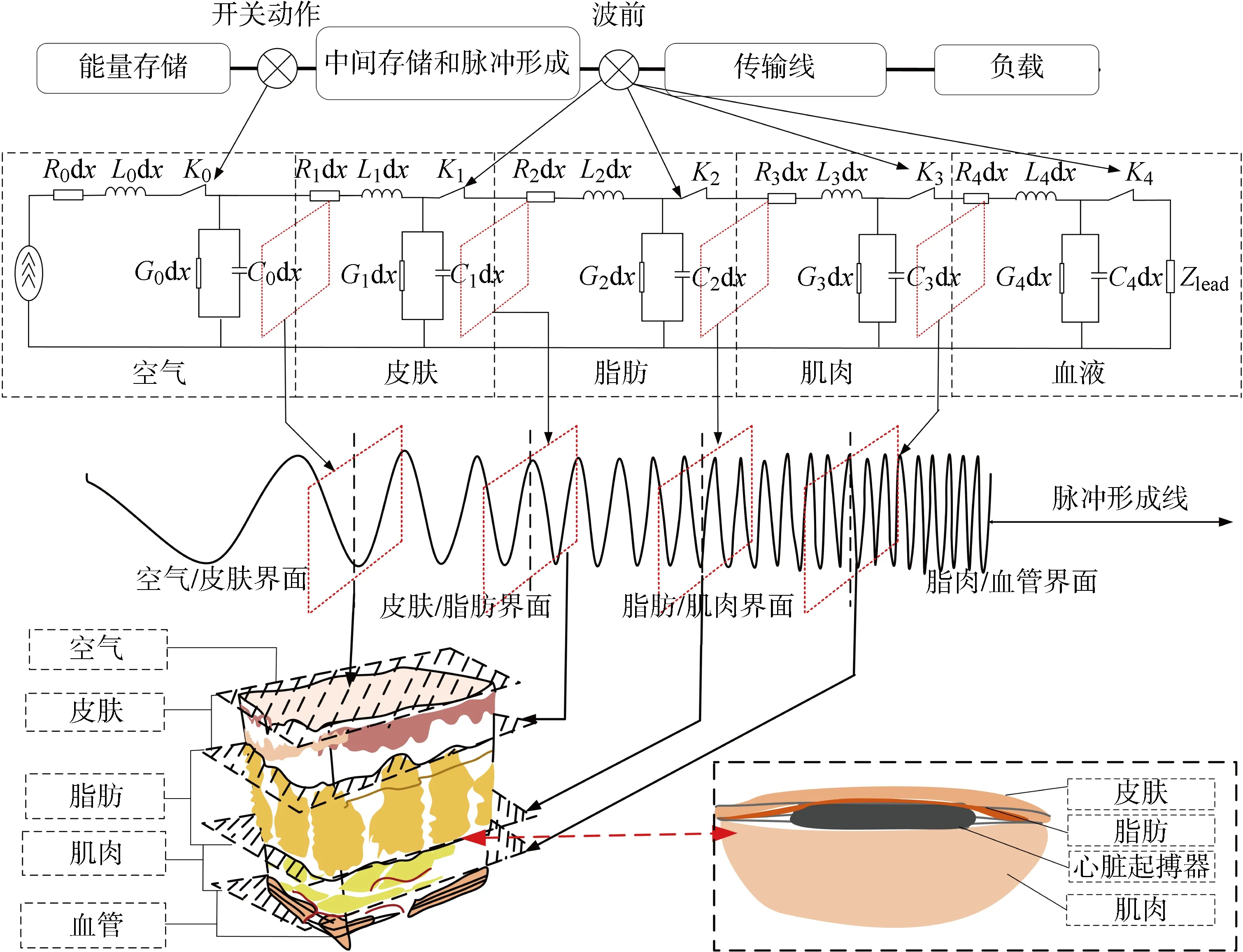
圖14 電磁波在人體組織內傳播的脈沖形成線模型Fig.14 Pulse forming of EM wave through multiple tissue-to-tissue interfaces
3.2 基于FEM仿真的參數化生物電磁暫態模型
為了確認電磁耦合路徑與胸腔解剖結構之間的空間映射關系,明確生物電磁相互作用的窗口,本文利用FEM軟件建立了植入心臟起搏器的人體胸部解剖模型,如圖15所示.圖中:I(t)為脈沖電流源;h為高度;a為寬度;b為長度.仿真模型的構建完全仿照實驗布置,并充分展示分層結構.銅芯線由直徑為4 mm的圓柱形表示.整個胸腔靜置于由電解質材料參數填充的直徑為600 mm,高400 mm的圓柱形中.用直徑480 mm,高120 mm的圓柱體模擬胸腔.胸腔上表面與銅芯線的垂直距離為150 mm.胸腔結構分為3層,由外到內依次定義為皮膚、脂肪和肌肉層.其中皮膚層厚度為5 mm,脂肪層的厚度設定為3 mm,剩下部分為肌肉層.將體積為41 mm×52 mm×6 mm的鈦鎳合金長方體定義為起搏器脈沖發生器,與皮膚表面的距離設置為6 mm.脈沖發生器與橢圓形交叉回路相連.長、短半徑分別為56、16 mm的橢圓形交叉外回路埋藏于肌肉與脂肪層間,用于模擬囊袋中的起搏器外部回路,這部分距離皮膚表面7 mm;長、短半徑分別為60、16 mm的橢圓形交叉外回路穿過肌肉到達直徑和高度分別為100、50 mm的圓柱形心臟,用于模擬血管中的起搏器內部回路.其中心臟組織距離皮膚表面65 mm.仿真中使用的人體組織和起搏器導線的相對磁導率(μr)、相對介電常數(εr)和電導率等參數均根據文獻[36]中 90 kHz 頻率下的參考數據進行設置,具體數值如表2所示.
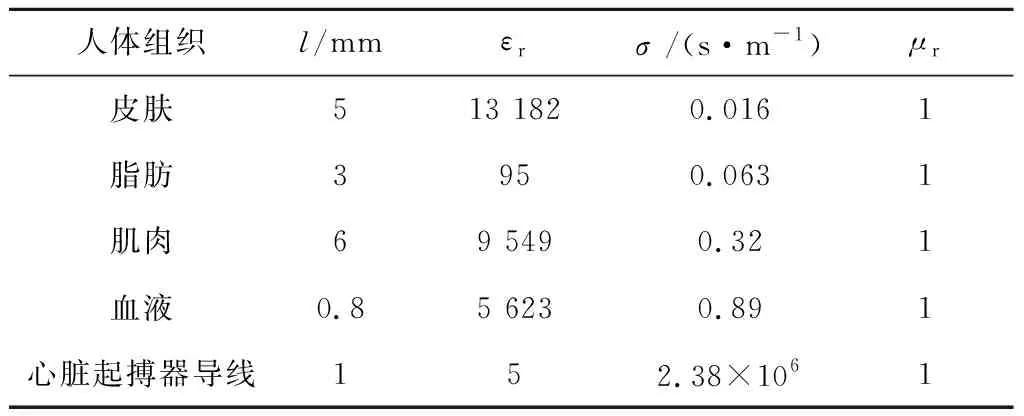
表2 90 kHz下組織和心臟起搏器導線的電導率、相對介電常數和相對磁導率設置值
仿真中通過向直徑為4 mm的圓柱形銅線施加脈沖電流來模擬脈沖電磁場輻射源.脈沖電流的波型由雙指數方程定義為
I=0.349K(1-e10-6(t+0.1))×
(1-e10-7t/160)cos 50 000πt
(5)
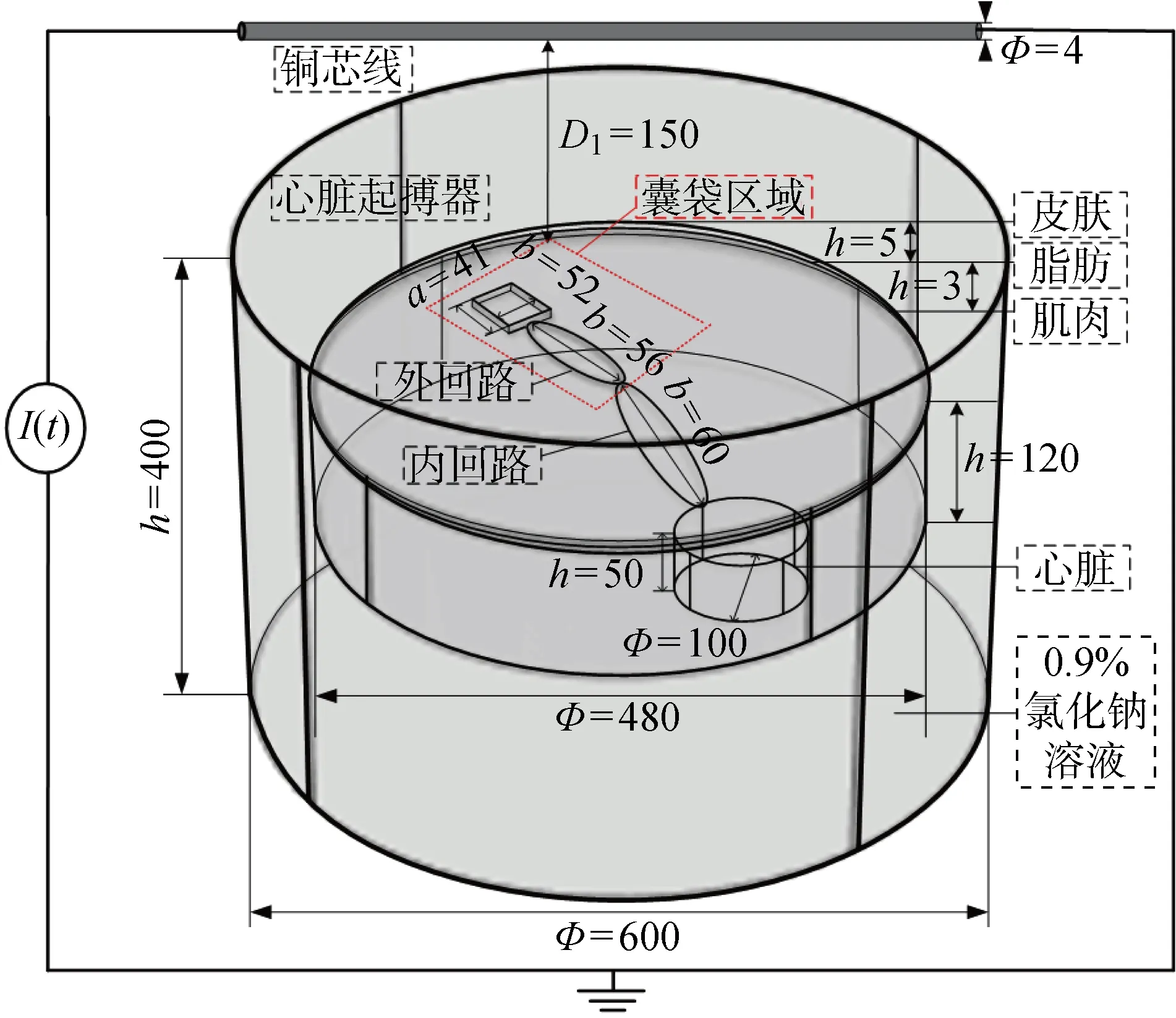
圖15 用于探究起搏器EMI的人體胸腔結構仿真模型(mm)Fig.15 Human chest geometry used for pacemaker EMI modelling (mm)
式中:K為常數,在1~5 kA變化;t在10~50 μs變化.仿真和實驗條件下起搏器的電磁干擾輸入和輸出信號對比結果分別如圖16和圖17所示.其中輸出信號均為內回路導線與心肌連接點的感應電壓.實驗和仿真條件下電磁干擾輸入和輸出信號波型高度擬合證實了本文數值建模方法精確可靠.
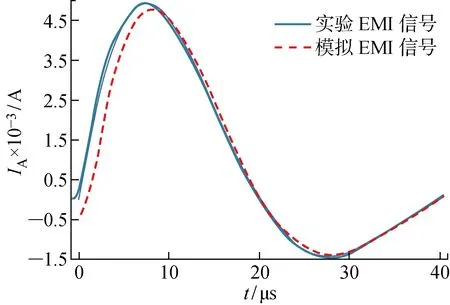
圖16 仿真與實際情況下起搏器電磁干擾輸入信號波型對比Fig.16 Waveforms of pacemaker EMI input signals in simulation and actual situation
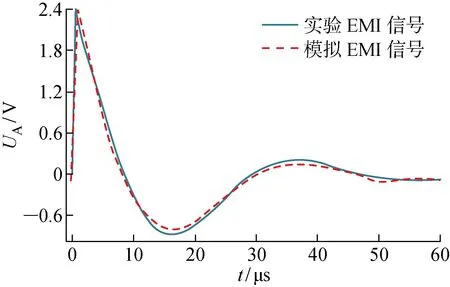
圖17 仿真與實際情況下起搏器電磁干擾輸出信號波型對比Fig.17 Waveforms of pacemaker EMI output signals in simulation and actual situation
圖18是將最外部代表電解質溶液的圓柱體部分做幾何隱藏后所描述的電場分布.該圖分別從整體和僅展示內回路與心臟接觸點的所在平面,描述在脈沖電流為5 kA時胸腔電場強度的分布情況.由圖可見,起搏器內部回路中的電場強度遠小于外部回路.起搏器外回路最大平均場強約為 5 V/m,幾乎是起搏器內回路的3倍.同時起搏器內回路與心肌接觸點的感應電壓為2.4 V.結果表明,人體組織的皮膚和脂肪層無法很好地屏蔽電磁干擾,但血管使瞬態電磁場減到很小的值.簡言之,囊袋中的起搏器外部回路確實是脈沖電磁場與起搏器發生電磁耦合的窗口.
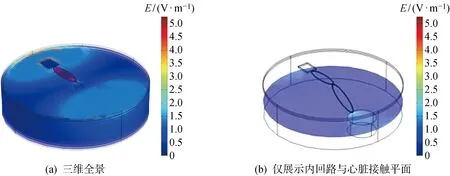
圖18 脈沖電磁場作用下電場分布Fig.18 Electric field distribution under PEMF
3.3 基于電磁窗口效應的脈沖電磁干擾防護策略
3.3.1電磁窗口屏蔽層防護 2.3.2節中證明將窗口中電極導線進行優化纏繞可以有效屏蔽來自PEMF的電磁干擾.但實際手術過程中,導線交叉纏繞方法仍存在一些局限性.研究表明彎曲會破壞絞型纏繞方式的平衡特性[37].在實際手術時,導線不可避免要彎曲.當導線彎曲時,相鄰絞節將疏密不同,抵消電磁干擾及電磁輻射的能力將下降.同時由于個體體脂率存在一定差異,無法保證采用“導線交叉纏繞”術式對所有患者都達到理想的電磁干擾屏蔽效果.為了提高起搏器佩戴者處于極端電磁暫態環境的安全性,本文為職業暴露人群提出通過復合材料結構進行“窗口”屏蔽的防護策略.
目前,常見的人體電磁屏蔽防護服均基于整體防護策略設計,但是現有電磁防護服材料往往不具有親膚性,長時間佩戴可能會使個體出現肌膚過敏等不良反應.佩戴整體性的電磁屏蔽防護服對于長期處于脈沖電磁污染的職業工作者不適用.對此,本文擬在起搏器囊袋電磁窗口處配置一款1.3 mm厚度的、由Ti3C2TxMXene涂層的聚對苯二甲酸乙二醇酯(Polyethylene Terephthalate,PET)織物構成的護心鏡,以減小屏蔽材料與人體的接觸面積.該復合材料具有良好的電磁屏蔽效應和親膚性,是新型柔性可穿戴式電磁屏蔽設備的優良選擇.本文基于FEM軟件中的參數化生物電磁模型對護心鏡的屏蔽效果進行驗證.在皮膚組織上方加入厚度為 1.3 mm、面積為58 cm2的由Ti3C2TxMXene涂層的PET織物構成的屏蔽層,平行覆蓋于內回路囊袋上方.圖19分別從整體和僅展示內回路與心臟接觸點所在平面的角度對護心鏡的防護效果進行了展示,結果表明,僅通過采用復合屏蔽材料覆蓋電磁耦合窗口的方式外源性脈沖電磁場在心臟表面上產生的感應電場強度便降低了80 dB,初步印證了該防護措施的理論可行性.
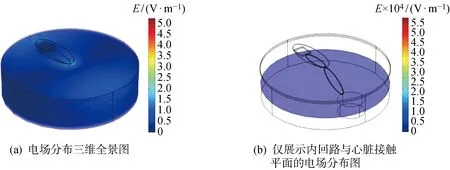
圖19 添加由Ti3C2TxMXene涂層的PET織物構成的屏蔽鏡后電場分布Fig.19 Electric field distribution under EM shielding made by PET coated with Ti3C2TxMXene
3.3.2典型場景安全凈距 除上述兩種防護,起搏器佩戴者在職業和醫療環境中還可以增大與電力源的安全距離降低體內起搏器工作狀態所受脈沖電磁場的影響.脈沖電磁場下起搏器環路感應電壓[38]為
(6)
式中:n為外回路的寬度;m為外回路的長度;d1,w為回路至身體邊緣的距離;d1,r為外回路至頭頂的平均距離;kH為形狀系數,取0.01;t1為注入電流波前時間.參數相對位置如圖20所示.當感應電壓低于人體心臟正常跳動幅值(60 mV),感應電壓將不再對人體產生威脅.令式(6)中Emax=60 mV,即可求得起搏器佩戴者在所處環境中的安全凈距,這將給起搏器佩戴者有效提示,其計算結果如表3所示.
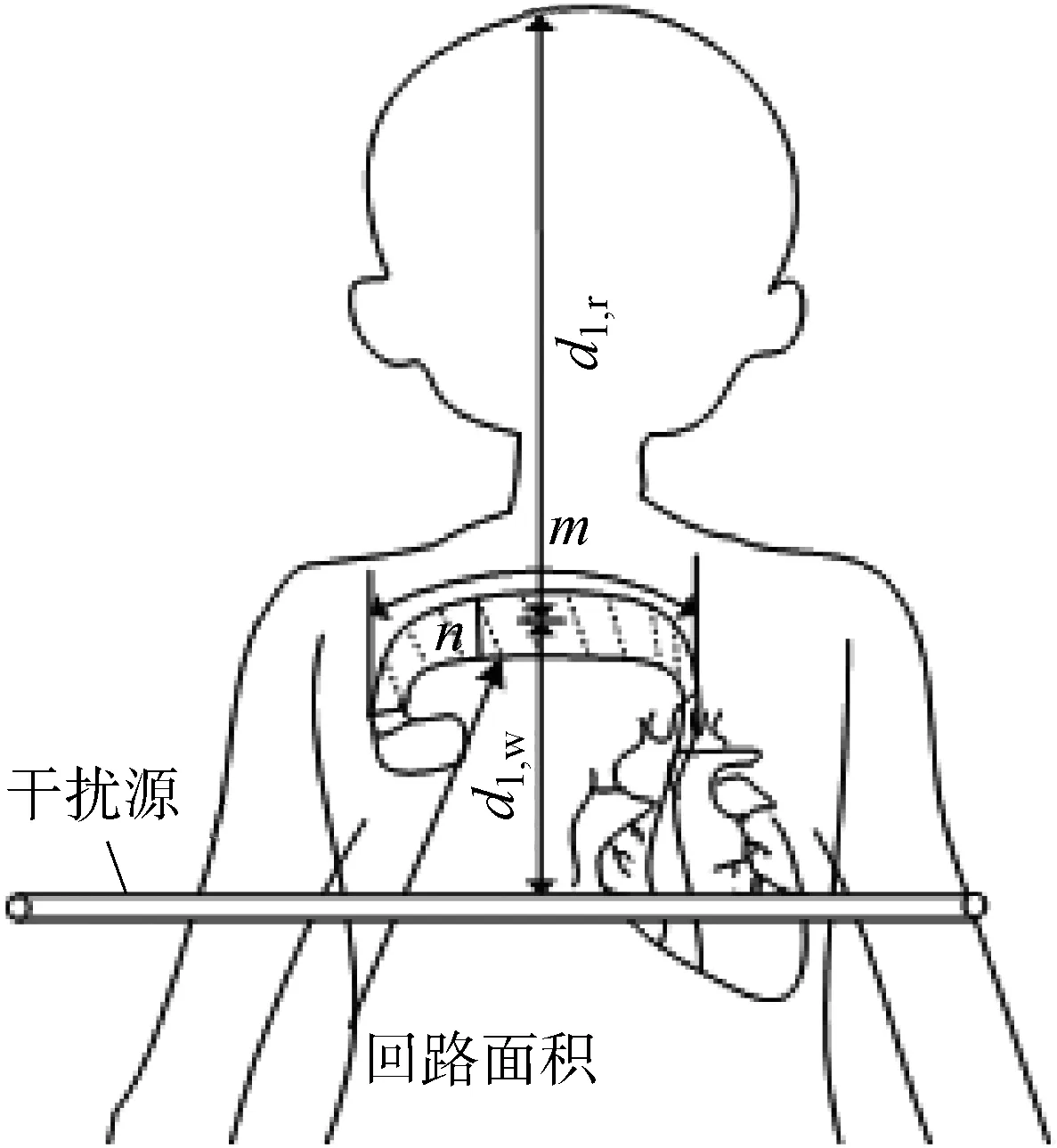
圖20 人體心臟起搏器回路位置示意圖Fig.20 Position of pacemaker loop
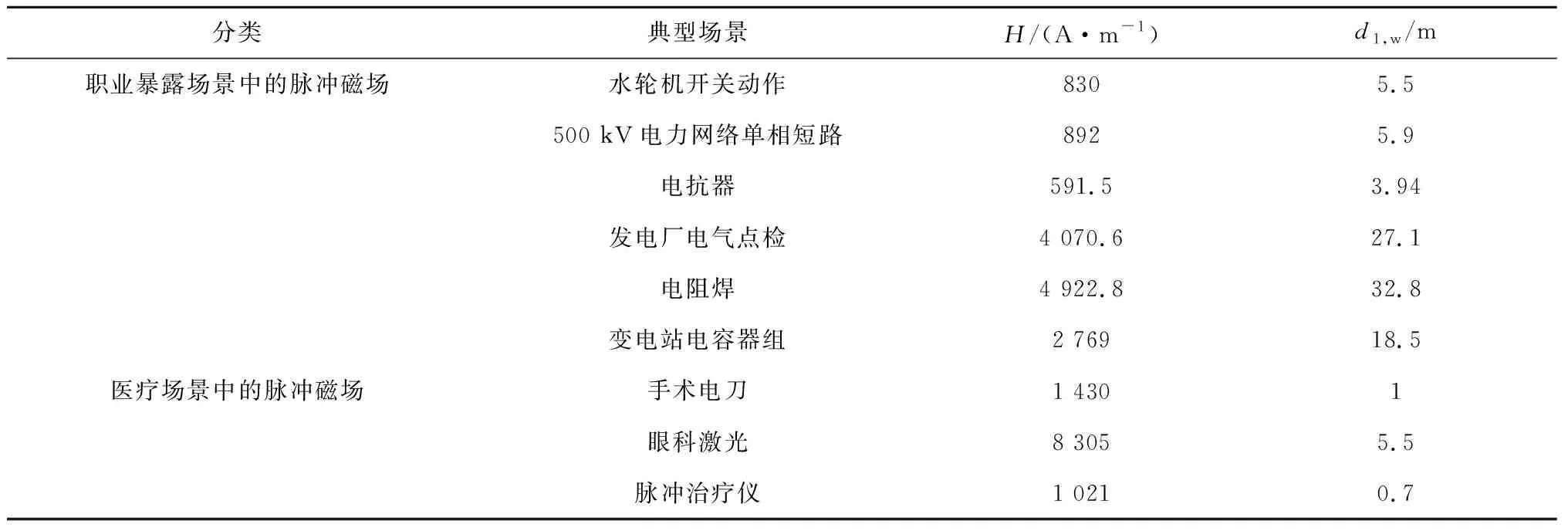
表3 典型脈沖電磁場安全距離Tab.3 Safe distances of typical PEMF
4 結論
從電力系統安全防護的角度出發,針對脈沖電磁波對心臟起搏器的干擾現象展開相應研究,所得結論如下:
(1) 通過將豬肉組織浸入0.9%氯化鈉溶液構筑了起搏器術后人體等效離體場景,同時對直徑為4 mm的標準銅線中通以短路電流信號來模擬典型的快波前沿脈沖電磁場.以此搭建了脈沖電磁波對人體胸腔內起搏器干擾的模擬實驗平臺,最后通過自主研發的可植入式電磁環境監測裝置進行實驗過程中的電磁監測.實驗結果表明,起搏器電磁干擾取決于傳輸信號的平均功率.同時來自PEMF的輻射會導致包括過感知和脈沖發出高尖P波的起搏器故障.兩種類型的起搏器故障都會威脅患者健康.
(2) 通過實驗結果推測PEMF輻射對起搏器的干擾可能是由囊袋外回路引起,即脈沖電磁波對起搏器的影響可能存在“窗口效應”.
(3) 通過FEM仿真軟件搭建了胸腔解剖幾何結構模型,并在電磁耦合物理場下進行了仿真研究,結合仿真結果和平面波傳播理論分析可知,在PEMF下外部起搏回路的感應電場強度遠高于內部起搏回路.人體組織的皮膚和脂肪層無法屏蔽起搏器電磁干擾,即驗證了“窗口”效應的存在.
(4) 依據“窗口效應”,提出一種針對性防護措施,即采用復合型屏蔽材料制成的護心鏡對囊袋進行覆蓋.并通過仿真初步驗證了該防護策略的理論可行性.

