運動促進免疫抵御COVID-19 的機制—基于肥胖與低體力活動人群視角
白新玥,陳佩杰,石 慧,李 斐,石 月
(1.上海體育學院 運動健康學院,上海 200438;2.上海交通大學附屬瑞金醫院 風濕免疫科,上海 200025;3.上海體育學院 競技運動學院,上海 200438)
由新型嚴重急性呼吸系統綜合征冠狀病毒-2(severe acute respiratory syndrome coronavirus 2,SARSCoV-2)引起的新型冠狀病毒肺炎(coronavirus disease-19,COVID-19)大流行已成為全球公共衛生問題[1]。據Worldometer 網站統計數據,截至世界標準時間2022 年3 月28 日20 點,全球累計COVID-19 患者達4.82 億人,死亡人數達614 萬人。2020 年2 月11 日,國際病毒分類委員會冠狀病毒研究小組將新冠病毒正式命名為“SARS-CoV-2”;同日,世界衛生組織宣布將新冠病毒感染引起的疾病正式命名為“COVID-19”[2]。SARS-CoV-2 是一種高度傳播的病毒,主要通過空氣中的飛沫進行傳播[3]。根據臨床觀察和尸檢數據,該病毒對全身血管組織有很強的攻擊性,易造成缺血性損傷和炎癥反應,破壞細胞功能和組織完整性[4]。此外,該病毒還會導致直接的組織損傷,引起機體免疫系統的“過激反應”,從而引發對機體破壞極大的“細胞因子風暴”[5]。COVID-19 在不同人群中存在普遍的易感性,其中,老年人、孕婦、兒童、患有基礎疾病人群、缺乏體力活動免疫力低下人群及肥胖人群尤為易感(圖1)。
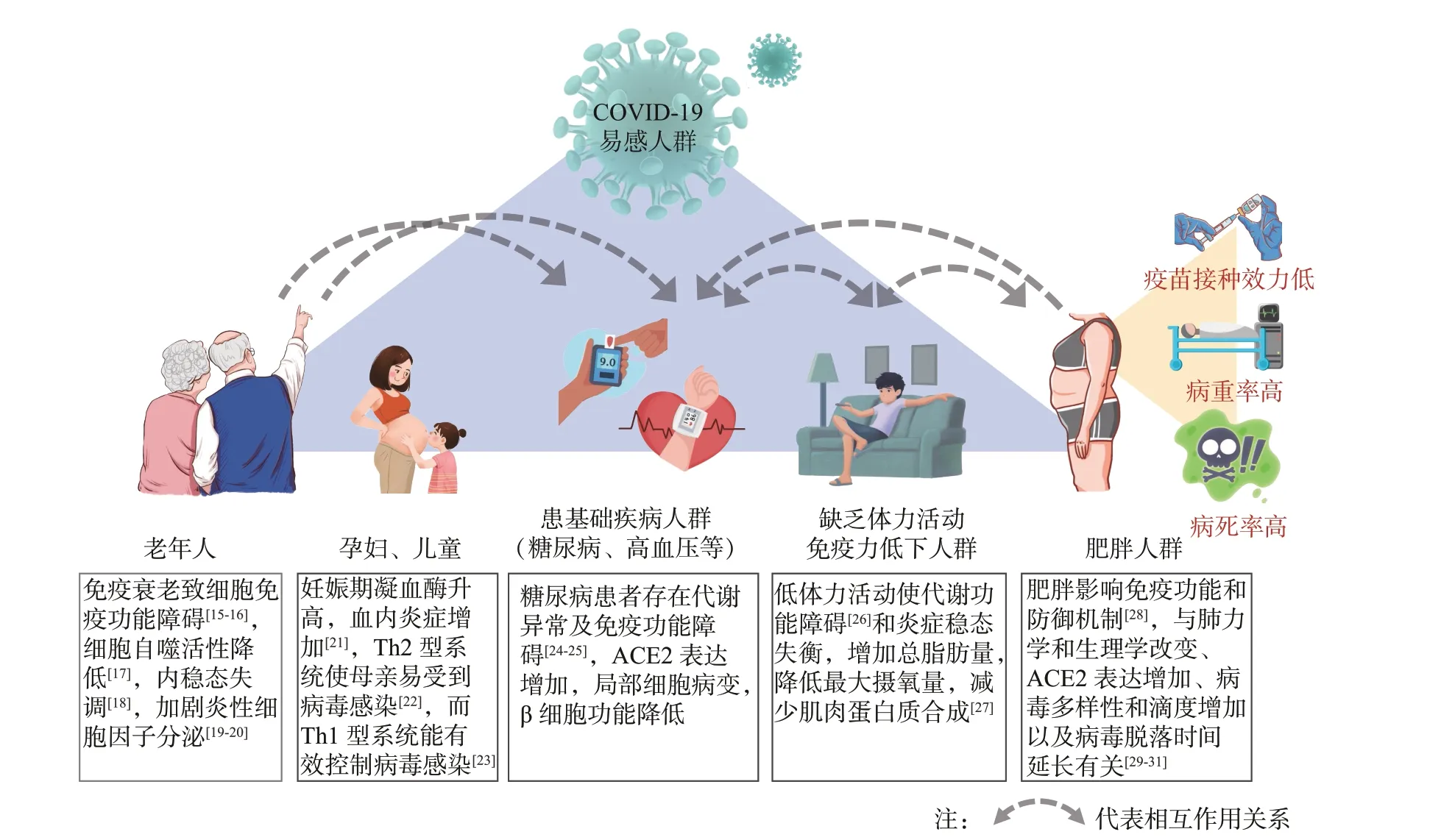
圖1 COVID-19 易感人群及易感機制Figure 1 Vulnerable population to COVID-19 and the mechanism
報道COVID-19 住院患者特征的首批研究[6-7]數據表明,高血壓、糖尿病、心血管疾病、慢性肺病、慢性腎臟疾病、癌癥和慢性肝病是COVID-19 最常見的合并癥。在中國,感染COVID-19 患者的相關合并癥中,心血管疾病的死亡率最高(10.5%),其次是糖尿病(7.3%)、慢性呼吸道疾病(6.3%)、高血壓(6.0%)、癌癥(5.6%)[7]。肥胖作為心血管疾病、2 型糖尿病和高血壓的獨立危險因素,與病毒性疾病過程的直接代謝和內分泌機制有重要聯系[8]。高身體質量指數(Body Mass Index,BMI)可能是患者病情惡化的重要影響因素,與肺炎風險增加有關[9-10]。至2020 年4 月中旬,肥胖也被證實是COVID-19 患者重要的合并癥[11-12]。體力活動缺乏及不健康的飲食是超重和肥胖的重要危險因素,合理運動和良好的生活方式干預能夠使2 型糖尿病的患病風險降低約60%[13]。同樣,規律運動作為提升機體整體免疫水平的“良藥”,已被流行病學研究指出與COVID-19 感染低風險相關[14]。
1 肥胖與COVID-19 易感性緊密相關
肥胖被世界衛生組織列為威脅人類健康的十大疾病之一,其發病率在世界范圍內不斷提升[32-33]。肥胖是各種感染、感染后并發癥和嚴重感染死亡的關鍵風險因素,也是非傳染性疾病的主要風險因素之一,這些非傳染性疾病的風險隨著BMI 的提升而增加[34]。在社會高速發展和科技不斷進步的環境下,久坐不動的工作模式、身體活動的不斷減少及不健康的飲食方式是導致全球肥胖流行的關鍵因素[34]。
1.1 肥胖者的COVID-19 感染率和重癥率高
肥胖已被證明以多種方式影響肺功能,肥胖者更易出現呼吸系統癥狀并發展為呼吸衰竭[35]。COVID-19在極端情況下會引發急性呼吸窘迫綜合征,其發生率在肥胖患者中顯著增高[36]。據統計,肥胖者是繼老年人后最易感染COVID-19 的人群,肥胖患者需要機械通氣的比例和死亡率高于非肥胖患者[12,37]。
來自中國和美國的病例數據證實了BMI 對新冠患者病情的影響。在深圳的383 例COVID-19 患者中,超重者發展為重癥的概率是體質量正常患者的1.84 倍,而肥胖者發展為重癥的概率是體質量正常患者的3.40 倍[38]。來自美國6 個不同地區重癥監護病房的265 例COVID-19 患者信息顯示,年齡和BMI 之間存在顯著的負相關,入院的年輕個體更可能是肥胖人士;此外,入院患者BMI 的中位數達到29.3,并有25%的人BMI 超過了34.7[39]。在紐約的5 700 例COVID-19 患者中,41.7%是肥胖患者,而紐約肥胖人群的平均患病率為22%[36,40]。肥胖人群患COVID-19的風險超過46%,住院率高達113%,ICU 入院率達74%,死亡人數較正常人群增加了48%[36]。此外,新的研究[41]結果表明,內臟肥胖和代謝健康受損相關疾病,如高血糖、高血壓和亞臨床炎癥與COVID-19 的高風險有關。
1.2 肥胖者易感COVID-19 的機制
研究表明,SARS-CoV-2 棘突蛋白使用人類血管緊張素轉化酶2(angiotensin-converting enzyme-2,ACE2)作為進入宿主細胞的主要受體[42],SARS-CoV-2 與ACE2 結合的親和力比ACE2 與SARS-CoV 結合的親和力高10~20 倍[43],這使得ACE2 成為SARS-CoV-2入侵的特定靶位。ACE2 在心臟和肺中高度表達,而脂肪組織的ACE2 表達高于肺組織,是SARS-CoV2 感染的主要靶組織[44]。肥胖受試者表達ACE2 的細胞數量增加,因此,肥胖患者的脂肪組織可能作為更廣泛的病毒傳播的儲存庫,導致免疫激活和細胞因子擴增[45]。在病毒感染下,研究人員發現肥胖與疾病嚴重程度加劇、病毒脫落時間延長、呼氣中病毒滴度升高以及病毒多樣性增加有關[29-31]。過量脂肪與補體系統的過度激活有關[46],補體系統已被證實是SARS-CoV 誘導疾病加重的重要介質[47],可誘發炎癥級聯反應,最終發展為“細胞因子風暴”[5]。此外,肥胖還可能導致肺力學和生理學改變,增加氣道阻力、損傷氣體交換并引起呼吸道慢性炎癥,共同影響肺損傷的預后,增加COVID-19急性呼吸衰竭甚至多器官衰竭的風險[48]。
此外,在病毒感染的情況下,肥胖患者可能比瘦型患者更具傳染性。①在延長病毒脫落時間上,有癥狀的肥胖患者比非肥胖患者釋放病毒的時間長約42%[31]。②人類和動物研究均發現,肥胖狀態機體產生干擾素的能力延遲[29,49],這種延遲使病毒RNA 復制增加,從而提高出現新的、更具毒性的病毒株的風險[29]。③BMI 與呼出空氣中的傳染性病毒水平呈正相關[50]。這些發現均支持肥胖人群更加易感COVID-19的假設并闡明了感染COVID-19 的肥胖患者病情發展的原因。
1.3 肥胖者與COVID-19 患者機體的免疫特征
肥胖是一種由體質量增加合并適應性免疫系統功能失調引發的機體慢性炎癥狀態[51-52],肥胖癥患者的免疫細胞生理功能出現障礙,表現為血漿炎癥標志物升高、淋巴細胞結構和完整性發生改變、白細胞群向炎癥表型轉移、免疫異常激活等[33]。肥胖引起的免疫系統紊亂會降低機體免疫力,削弱對病原體的控制和清除,引發代謝功能紊亂和慢性病,從而引起機體免疫系統整體的功能失調,即代謝綜合征[34,48]。在肥胖患者中,脂肪組織內的髓系和淋巴系反應存在失衡,并伴有相關的細胞因子譜失調[53],與此伴隨的是內分泌和代謝紊亂,包括胰島素抵抗、脂肪因子失調以及功能失調的脂質和脂肪酸代謝[54]。肥胖患者異常的代謝系統與免疫系統之間相互影響,會降低免疫系統效應細胞的激活,抑制免疫功能和宿主防御,導致感染并發癥和疫苗失效率提升[28,48]。一項對248 名醫護人員進行第二劑BNT162b2 疫苗接種后7 d 監測抗體滴度的研究[55]顯示,與男性、超重及老年人群相比,女性、體質量正常及偏瘦和年輕人群產生的體液反應能力更高,這為為肥胖人群制定針對性COVID-19 接種策略提供了依據。
COVID-19 患者的肺炎范圍從輕度炎癥到急性呼吸窘迫綜合征及多器官衰竭[56]。大多數患者血漿中的白細胞、中性粒細胞、單核細胞計數在正常范圍內,淋巴細胞減少[57],而危重患者的自然殺傷細胞(natural killer cell,NK)、B 細胞、T 細胞、單核細胞、嗜酸性粒細胞和嗜堿性粒細胞數量減少,導致病毒清除延遲[58-59]。患者淋巴細胞減少表明COVID-19 可能導致CD4+T 和CD8+T 細胞的耗竭[60],因此,淋巴細胞數量可作為指標判定患者患病嚴重程度[61]。此外,COVID-19還是一種高炎癥綜合征,是由先天免疫激活引起的不同促炎細胞因子水平升高,所謂的“細胞因子釋放綜合征”(Cytokines Release Storm,CRS)可能是該疾病不良發展的原因[5,62]。在臨床上,重病患者和死亡患者均表現出CRS,即體內白細胞介素2(Interleukin-2,IL-2)、IL-6、IL-7、IL-18、IL-33、IL-1β、粒細胞刺激因子、干擾素-γ、誘導蛋白10、單核細胞趨化蛋白1、巨噬細胞炎性蛋白1α 和腫瘤壞死因子-α 增加[59,63]。入住ICU 和未入住ICU 的患者在實驗室檢查結果上同樣存在差異,包括ICU 患者血液中較高的白細胞和中性粒細胞計數、血漿中增高的多種炎性細胞因子水平等[57,63-64]。以上研究均表明,COVID-19 患者存在先天免疫和適應性免疫異常的情況,并且異常的程度與疾病的嚴重程度密切相關。肥胖造成機體免疫系統功能紊亂并引發機體的慢性低度炎癥狀態使得在面臨COVID-19 感染的風險時,機體承受的不只是疊加免疫應答反應,而是席卷全身各臟器的免疫風暴;肥胖導致的各臟器功能減弱也將使其無力抵抗病毒侵襲,進而引發臟器功能衰竭甚至死亡。
2 低體力活動與COVID-19 交錯影響
2.1 COVID-19 流行下全球低體力活動現狀
隨著電子辦公及電子娛樂形式的普及、交通格局的改變和職業類型的轉變[65],兒童、青少年以及成年人的日常行為模式受到深刻的影響,體力活動大幅削減。全球各國尤其是發達國家和部分發展中國家國民超重流行率迅速增加,不良飲食行為、體力活動減少和久坐時間增加是促成該趨勢的重要因素[65]。低體力活動已被證實是許多非傳染性疾病(心臟病、中風、2 型糖尿病、乳腺癌和結腸癌)發展的關鍵風險因素[66-67]。現今,越來越多的研究證明低體力活動也成為感染性疾病的高風險因素[26-27]。
在COVID-19 流行期間,低體力活動狀況進一步增加,青少年體力活動時間顯著減少。中國上海2 426名兒童和青少年(男孩占51.2%,女孩占48.8%)在COVID-19 流行期間,體力活動時間大幅減少,從540 min/周(COVID-19 流行前)減少到105 min/周(COVID-19 流行期間),平均減少435 min。同時,不參加體育活動的學生的患病率從21.3%上升到65.6%,總屏幕時間大幅增加(平均每周增加1 730 min)[68]。低體力活動與全因死亡率相關,對于年輕健康男性,每日體力活動減少僅維持2 周就會導致肌肉質量的損傷和內臟脂肪量的增加,以及胰島素抵抗和血漿甘油三酯水平的升高[69]。長時間久坐所帶來的風險只有通過有計劃的中等強度或高強度體力活動(60~75 min/d)才能消除[70]。除了引起過早死亡和增加多種疾病發病率外,低體力活動也帶來巨大的經濟負擔。《柳葉刀》于2016 年評估了142 個國家(占世界人口的93%)低體力活動造成的經濟負擔狀況,報告顯示僅2013 年,國際醫療系統公司在世界范圍內低體力活動的總成本為675 億美元,包括直接成本(醫療成本)和間接成本(與低體力活動相關的死亡導致生產力損失)。低體力活動導致全球1 340 萬傷殘調整生命年(disabilityadjusted life-years,DALYs)[67],DALYs 是指目前人群的健康狀態和無人受疾病傷殘困擾、長壽的理想健康狀態之間的差距,換言之就是疾病負擔程度。
2.2 低體力活動加劇COVID-19 感染的潛在機理
COVID-19 疫情下,持續的封控及社交隔離導致的低體力活動狀態將對機體骨骼肌系統、呼吸循環系統及免疫系統的正常運轉造成極大的威脅,機體免疫系統的強弱直接影響其被感染的風險。此外,已有明確證據證實了體力活動與感染之間存在劑量-反應關系,高體力活動的成年人有著較低的感染風險,低體力活動的成年人則有著最高的感染風險[71]。
低體力活動加劇COVID-19 感染的生物學機理可能在于ACE2-Ang(1-7)-Mas 軸的失平衡[72]。在機體未感染狀態下,廣泛分布于肺臟、消化道、心臟及血管的ACE2 蛋白可將血管緊張素Ⅱ(AngⅡ)水解為Ang(1-7),Ang(1-7)進而結合Mas 受體形成ACE2-Ang(1-7)-Mas軸,該軸在機體內起到重要的調節血管收縮、水電解質平衡、抗炎及抗纖維化的作用[73]。在機體遭受SARSCoV-2 入侵時,SARS-CoV-2 與ACE2 的大量結合消耗了肺上皮和肺血管內皮細胞上的ACE2 受體,進而致使ACE2-Ang(1-7)-Mas 軸調節功能受損;相反,激活了與該軸呈反向作用的ACE-AngⅡ-AT1R 通路,而該通路的過度激活造成肺毛細血管通透性增加、炎癥反應加劇,進而引發肺損傷[74-76]。研究[77-79]顯示,體力活動和運動訓練可以增強ACE2-Ang(1-7)-Mas 軸效應并抑制ACE-AngⅡ-AT1R 通路的激活。此外,脂肪組織中ACE-AngⅡ-AT1R 通路激活程度較高,并可促進脂肪細胞增殖、增加脂質存儲,從而加劇機體慢性炎癥狀態[72,80]。據此,高水平的體力活動對于調節ACE2-Ang(1-7)-Mas 軸及ACE-AngⅡ-AT1R 通路間的平衡顯得尤為重要,也可作為降低COVID-19 易感風險及病重率的有效預防手段。
3 運動對于感染性疾病的積極作用
肥胖可以通過日常行為的改變來有效控制,包括減少能量攝入和增加能量消耗。經常從事體力活動和參加規律的體育鍛煉有助于減少體脂、降低體質量,更重要的是提高免疫力、降低感染性疾病風險及恢復機體代謝健康[32,81]。不同形式的運動對于常見慢性疾病的預防和輔助治療作用已廣泛得到公眾的認可和實踐的檢驗。然而,運動對于感染性疾病的預防和康復治療中發揮的益處鮮為人知,對近10 年來有關運動對多種感染性疾病(急性呼吸道感染、肺炎、肝炎等)干預治療情況的研究進行歸納匯總(表1),得出結論:規律有氧運動可以對感染性疾病患者免疫系統產生積極的調節作用,有效改善患者的運動能力,提高其生活質量,降低發病風險;藥物與運動相結合的治療方式逐漸興起,但運動強度、運動頻率應因人而異,制定適合患者的個性化方案更有利于患者康復。
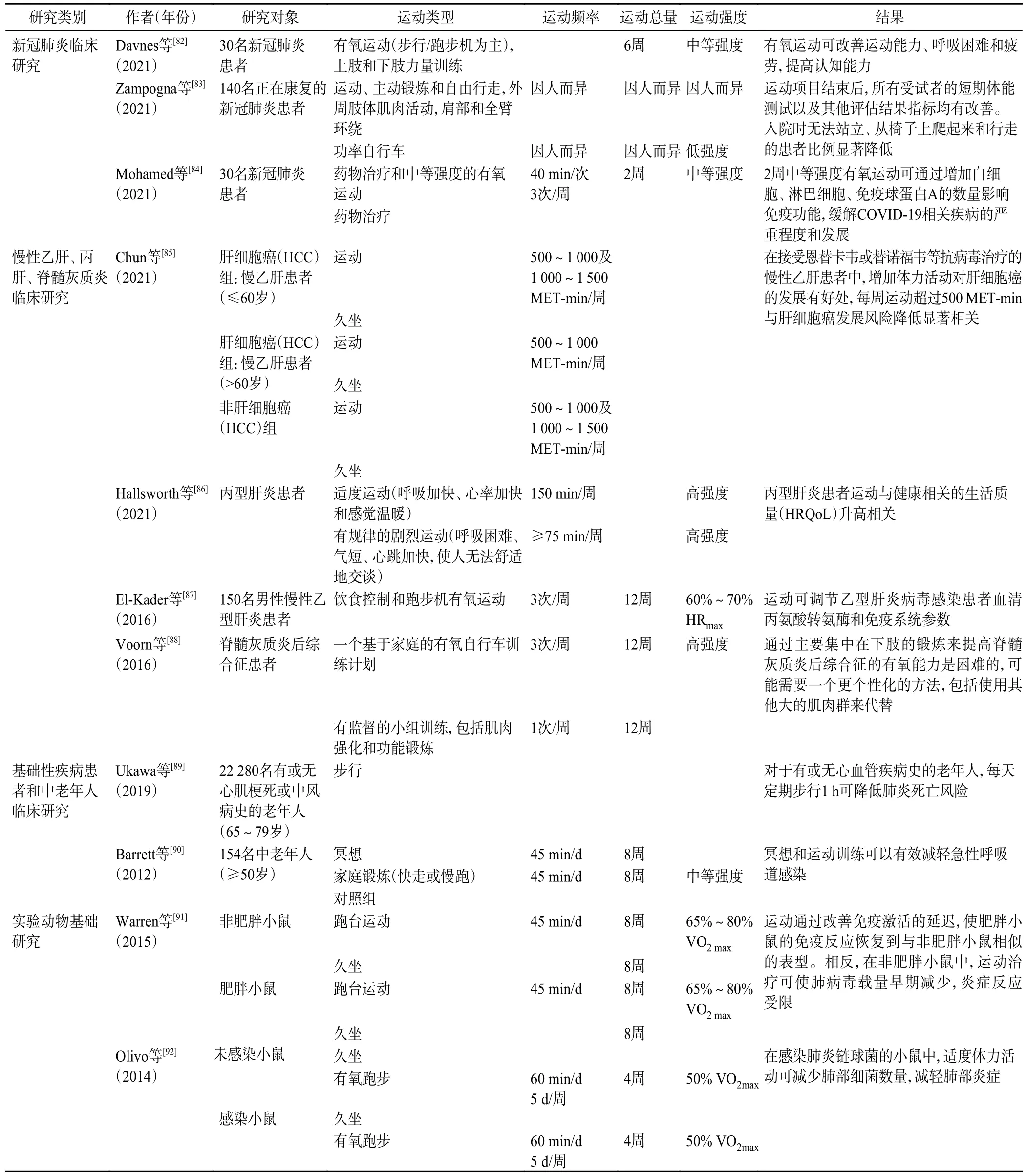
表1 運動干預促進多種感染性疾病(肺炎、肝炎、脊髓灰質炎及普通呼吸道感染)恢復相關臨床及動物研究一覽Table 1 Clinical and animal studies related to exercise intervention promoting recovery from multiple infectious diseases(pneumonia,hepatitis,poliomyelitis,and common respiratory tract infections)
4 運動提升機體免疫力抵抗疾病的機制
在COVID-19 大流行下,除了做好外在必要的防護措施及保持社交距離外,還需要尋求能夠提升內在機體免疫力以抵抗感染的途徑,而進行體力活動及體育鍛煉是可以控制的、最經濟的方式。體力活動不僅可以減輕肥胖癥、2 型糖尿病和高血壓等代謝性疾病的癥狀[81],還可以改善免疫監視,并有可能在3 個預防層級上對抗COVID-19 感染:在第一預防層級上,已有證據證明規律的運動與COVID-19 感染的風險呈負性相關,這種相關性在其他多種呼吸道感染中已被廣泛證實;在第二預防層級上,基于其他類型傳染性疾病(如流感)的調查數據,規律的運動在提高COVID-19疫苗的接種效力上具有潛在正向作用;在第三預防層級上,人們逐漸認識到COVID-19 感染會導致部分患者持續發病,并在康復后依然存在多種后遺癥,而運動可直接提高身體綜合素質、改善身體健康水平,從而提升生活質量[14]。急性(單次)及規律(長期)適度運動改善機體免疫力的機制總結(圖2)如下。
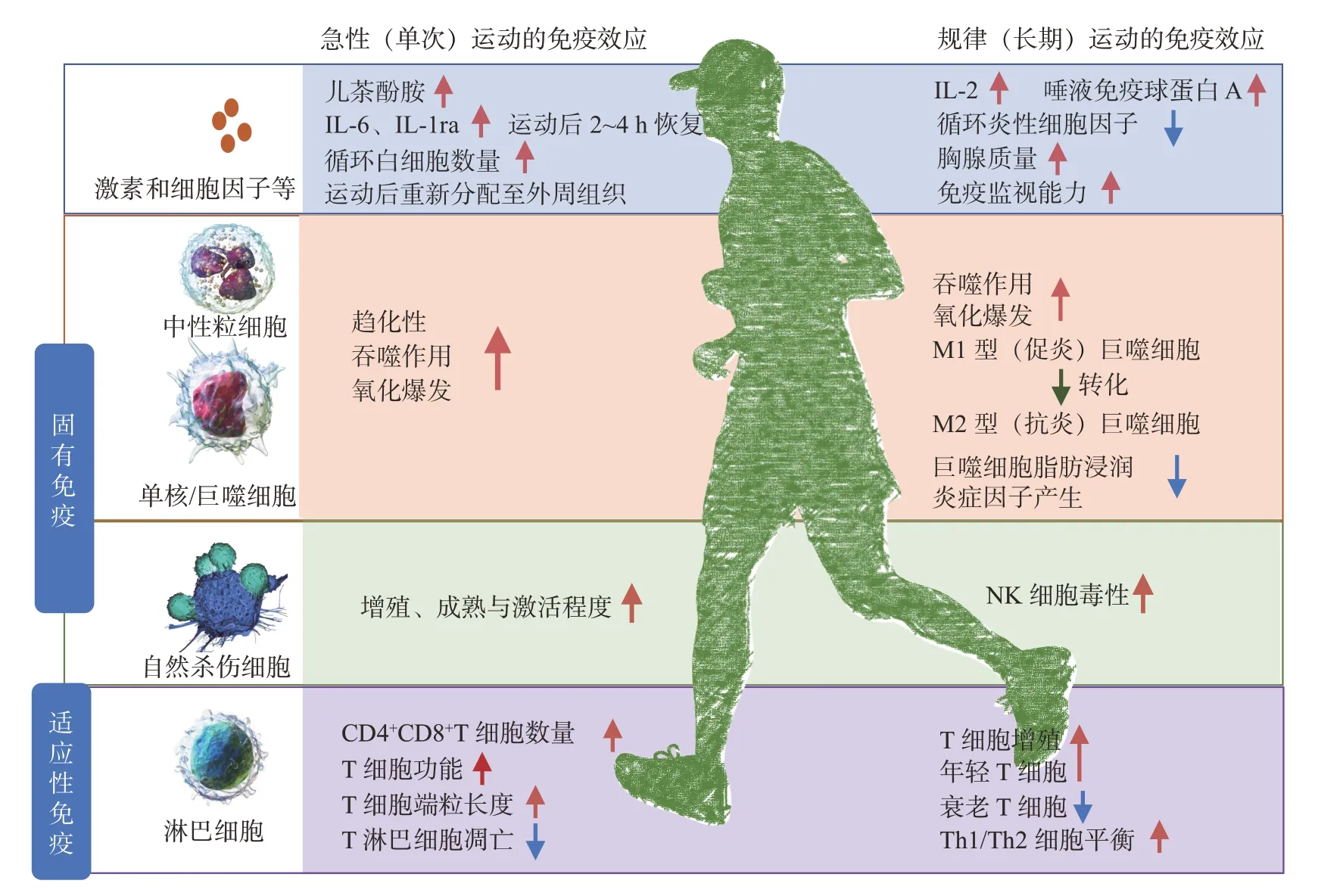
圖2 急性(單次)和規律(長期)運動提升機體免疫力效應Figure 2 The effect of acute (single) and regular (long-term) exercise on improving immunity
4.1 急性(單次)運動和固有免疫
急性運動通常指一次性的單次運動,重點在于觀察特定的運動形式、強度和持續時間對于機體免疫系統造成的短期影響。急性運動會影響循環白細胞的總數和組成,以及白細胞的趨化性。運動通過釋放的兒茶酚胺與白細胞上的β-腎上腺素能受體結合,促進白細胞動員進入循環重新部署,刺激血液循環和組織之間白細胞的持續交換[95-98]。
在中等強度運動期間和運動后,許多具有強大效應功能的免疫細胞被重新分配到外周組織[99]。早期的研究[95,100]報道,急性中等強度運動可增強中性粒細胞趨化性及吞噬能力。50%VO2max運動增強中性粒細胞氧化爆發。運動干預可使循環單核細胞數量增加[97],其吞噬功能已被證明在進行2.5 h 75% VO2max的運動后增強。巨噬細胞的功能隨運動強度而改變,中等急性運動增強巨噬細胞的許多功能(黏附、趨化、吞噬、殺微生物活性),可能與皮質醇的作用有關[101]。NK 細胞是對運動刺激最為敏感的免疫細胞,因為肌肉衍生的運動因子可以調節NK 細胞的增殖、成熟和激活,在體力消耗時表現出循環NK 細胞的急性動員[102],在耐力訓練30 min 內達到最大程度的細胞動員,之后繼續運動不會導致NK 細胞數量的進一步增加。在整個耐力訓練過程中的最初動員后,NK 細胞水平的升高維持了長達3 h;運動停止后,循環中的NK 細胞數量減少,可能是由于動員的NK 細胞重新分布到周圍組織中了[102]。
4.2 急性(單次)運動和適應性免疫
T 淋巴細胞在免疫應答的協調中起著關鍵作用[103]。有報道稱,與運動前相比,T 淋巴細胞以及較小的B 淋巴細胞數量增加[100],急性運動后T 細胞功能的變化與運動強度和運動時間成正比[95]。中等強度訓練可產生更多的中央記憶CD4+T 細胞、效應記憶CD8+T 細胞,且對CD4+終末效應記憶細胞(terminal effector,TEMRA)的影響比CD8+TEMRA細胞更明顯。中等強度訓練后,CD8+T 和CD4+T 細胞的端粒長度均有輕微增加;此外,通過caspase-3 和Bcl-2 的表達觀察到靜息T 細胞凋亡減少[104]。以上均提示急性中等強度運動對于維持T 淋巴細胞的年輕狀態起到正向作用。目前,有新的觀點認為,運動后12 h 的短暫性淋巴細胞減少癥并非抑制免疫能力,而是有利于免疫監測和調節[99,105]。
運動在誘導炎癥標志物的急性變化方面較為顯著。一次運動可以增加促炎細胞因子IL-6 的表達[106],在較短時間的運動過程中可以觀察到局部組織IL-6升高,而循環IL-6 的增加通常只在較長時間的運動下才能觀察到[107]。由于延遲反應的存在,大多數抗炎指標(如IL-1ra 和IL-10)的最大變化出現在運動后2 h,許多指標在運動后4 h 恢復到基線水平[97]。
4.3 規律(長期)運動和固有免疫
規律的中等強度運動訓練對免疫功能有益。越來越多的研究表明,經常參加規律運動可以作為一種佐劑來刺激免疫系統[99]。經常運動可因其抗炎作用而降低患病風險,然而過度訓練會削弱免疫系統的功能[100]。規律適度運動改善免疫功能可能是由于適度強度的運動可減少炎癥、維持胸腺質量、改變“衰老”和“年輕”免疫細胞組成、增強免疫監視或緩解心理壓力等[95]。規律中等強度運動與疫苗反應增強、衰老T 細胞數量減少、T 細胞增殖增加、循環炎性細胞因子水平降低、中性粒細胞吞噬活性增加、對細菌挑戰的炎癥反應降低、NK 細胞細胞毒性和IL-2 的產生增加及細胞自噬水平升高有關[95,108]。
中等強度連續訓練可以提高VO2peak,改善中性粒細胞吞噬和氧化爆發及單核細胞吞噬和產生氧化爆發的百分比,降低瘦素水平,從而減少感染風險。訓練后CD14+單核細胞上CD16、TLR2 和TLR4 的表達減少,但中性粒細胞CD16、TLR2 和TLR4 的表達無明顯差異,提示規律運動對單核細胞的吞噬能力似乎沒有改善,但能清除系統中功能失調的中性粒細胞,從而改善剩余的中性粒細胞的功能,提高機體免疫能力[109]。規律適度運動可促進M1 型炎性巨噬細胞向抗炎M2 型轉變,減少巨噬細胞向脂肪組織的浸潤,導致炎性細胞因子產生減少[110]。所有這些研究都表明,規律中等強度運動能夠改善并維持整個生命周期的免疫功能[95]。
4.4 規律(長期)運動和適應性免疫
運動可以增強人們對抗原挑戰的免疫反應[99]。積極的身體活動通常與比例較低的記憶T 細胞及比例較高的幼稚T 細胞有關,記憶T 細胞在規律運動中經常被動員到血液及外周組織中。有規律的結構化鍛煉可以增加休息時循環幼稚T 細胞的數量[99]。幼稚T 細胞的數量增加,作為控制免疫系統中幼稚和記憶細胞數量的負反饋機制的一部分,受益于運動誘導的胸腺生成和胸腺外T 細胞發展的作用[111-112]。Th1 和Th2 反應之間的平衡對于維持正常免疫系統至關重要。其中,IFN-γ 和IL-4 分別作為Th1 和Th2 細胞產生的主要效應細胞因子[113]。由于IFN-γ 和IL-4 在Th1/Th2 系統的啟動、發展和調節中發揮作用,所以IFN-γ/IL-4 比例過高或過低被認為是自身免疫和過敏反應的指標[114]。規律中等強度運動后,有絲分裂刺激的外周血單核細胞中IFN-γ 和IL-12 顯著增加,IFN-γ/IL-4 比率也顯著升高。這表明,中等強度運動可能通過IFN-γ 的作用,將免疫系統中的平衡轉移到Th1 類應答反應,這解釋了運動誘導的暫時性促炎反應有關的分子機制[115]。
上述總結的均是運動的良性效應機制,然而,并非所有形式的體育活動均對機體健康有益。當前,在運動免疫學研究領域已基本達成共識,即:規律適度運動提高機體免疫機能,而過度運動致機體暫時性免疫抑制。這也是經典的“J 型曲線理論”和“窗口期假說”的核心觀點。對于高度活躍的個體和競技運動員而言,值得關注的問題是SARS-CoV-2 可能導致心臟損傷。在COVID-19 住院患者中有很大比例會出現急性心臟損傷和心肌炎的并發癥[116-117],運動可能加速病毒的復制和心臟損傷。因此,如何做好運動員群體的環境控制,降低病毒暴露風險并嚴格監控隊員機能狀況是運動隊管理者面臨的挑戰。
此外,規律適度運動就不同身體素質和健康狀況的個體而言,其涉及運動方案中的核心要素(運動強度、運動頻率和運動形式等)也不可一概而論,需予以區別對待。對于久坐不動、運動背景薄弱及患有慢性疾病的人群而言,即使單次中低強度的體力活動也有一定的健康益處;關鍵在于讓未意識到運動益處的人群形成鍛煉意識,讓意識到運動益處的人群有足夠動機“邁出第一步”,讓已經“動起來”的人群科學、持續地開展鍛煉。
5 應對策略
COVID-19 大流行本身給人類造成了前所未有的健康危機,而因疫情導致的身體活動限制及體力活動不足所引發的骨骼肌肉系統、心肺系統及免疫系統的退化和損害則可能對全人類造成“二次健康危機”。為應對上述惡性循環急需創新鍛煉思維,在不違反公共衛生安全和社區管理規定的前提下,在有限的活動空間和條件下保持適度的體力活動量,維持良好的身體機能,以更好地應對潛在的感染風險。COVID-19在全球范圍內流行已持續3 年多的時間,我們無法準確判SARS-CoV-2 是否會像流感一樣呈現季節性的變化或是全年持續的威脅,我們能做的是將COVID-19視為擴大和推廣整體人群規律性進行身體活動的契機,并針對個人的情況創新生活行為和體育鍛煉方式,克服疫情對于團體和社交活動的障礙與限制,優化身體、心理和情感的整體健康狀況。
2020 年8 月,美國運動醫學會在行動呼吁聲明中指明了COVID-19 大流行下個體從事運動和體育鍛煉的注意事項[118]:①鼓勵身體健康的人開始或繼續適度的體力活動,運動總時長為每周150~300 min,即使達不到上述鍛煉時長,參加一定量的體力活動依然具有健康效益。②每周參加150~300 min 中等強度或75~150 min 高強度的運動,并保持體質量達到推薦水平,從而保持免疫健康。③在家中或室外進行中高強度運動時,與他人保持適當的物理距離,在需要時使用面罩以最大程度地減少飛沫傳播。④暴露于SARSCoV-2 高風險的個人應避免劇烈運動、過度鍛煉和過度訓練[4]。⑤對于確診COVID-19 感染的輕癥患者,建議休息,2 周內不運動。目前的臨床數據表明,輕癥COVID-19 感染患者從發病到臨床康復的中位時間約為2 周,在這2 周時間內建議休息,停止運動直至癥狀消失。在身體康復后剛開始體力活動或運動時,應當在幾天甚至幾周內減少運動強度和持續時間。個體對于病毒感染的反應與恢復不盡相同,需要以身體狀況和醫生的建議為導向決定重返鍛煉的時間[116-117]。在完全恢復之前,貿然達到感染之前的日常鍛煉強度和時間運動會增加疾病傷害的風險[119]。
此外,在COVID-19 大流行期間尋求創新策略以促進體力活動。就創新體力活動形式而言:合理布局居家空間,創造“家庭鍛煉區”,使用阻力帶、負重水瓶等簡易工具增加體力活動的強度;開展室內球類活動或親子體育游戲,增加運動樂趣和互動性,帶動家人共同參與運動;注重科學訓練監控,使用運動手表或智能手機App 監測能量消耗和體力活動情況;依托互聯網平臺開展居家健身行為,通過新穎的互聯網+健身產品,開展如健身魔鏡、在線運動視頻課程等多元化體育活動[120-121]。對于代謝健康受損的肥胖人群,除改善生活方式及增加體力活動外,還要關注合理的飲食方案以減少脂肪組織質量,降低患心臟代謝疾病的風險。
當前,無論對于個人、學校、社區、企業主還是政府而言,都應比以往任何時候更注重體力活動對于健康的益處,鼓勵并努力實施促進體力活動的規劃和政策迫在眉睫。學校和社區需在COVID-19 流行期間嚴格做好體育活動和身體鍛煉的安全防護措施。政府應加大對學校和體育活動組織機構的政策扶持力度,提供激勵措施以促進人們形成積極的生活方式,對于低收入群體體育設施和衛生保健資源的獲得需要給予更多關注和保障。在臨床與科學研究領域,有待更多的流行病學數據證明良好運動習慣對COVID-19 易感風險和患病程度的直接益處;此外,運動在慢性疾病和感染性疾病中的作用機制和關鍵分子有待多學科領域研究者共同協作探究。
作者貢獻聲明:
白新玥:整理統計相關文獻,撰寫論文;
陳佩杰:調整論文結構布局,審核修改論文;
石 慧:調研文獻,修改論文;
李 斐:調研文獻,核實數據,撰寫部分內容;
石 月:提出論文主題,設計論文框架,撰寫論文。

