蚌埠及周邊地區血脂異常患者SLCO1B1與APOE基因多態性分析及臨床意義*
孫思雨,李 楠,丁海虎
(1.蚌埠醫學院第二附屬醫院藥劑科,安徽 蚌埠 233040;2.蚌埠醫學院基礎醫學部,安徽 蚌埠 233000)
作為羥甲基戊二酰輔酶A(HMG-CoA)還原酶抑制劑的他汀類藥物(statins),是臨床降脂的首選藥物,也是預防心腦血管疾病的重要藥物之一[1]。然而,他汀類藥物的使用存在較大個體差異,部分患者會出現神經毒性、肝毒性、肌肉毒性、肝毒性及胃腸道反應等不良反應[2],因此為臨床醫生選擇個體化用藥和預后評估等方面帶來了很大的困擾。研究發現,他汀類藥物不良反應與遺傳因素相關,尤其與有機陰離子轉運多肽(OATP1B1)編碼基因SLCO1B1及載脂蛋白E(APOE)基因的單核苷酸多態性(SNP)密切相關,SLCO1B1與APOE的不同基因型對藥物的療效及不良反應差異較大[3]。進行SLCO1B1與APOE基因檢測能夠幫助臨床醫生對患者實施個體化用藥指導,因此具有重要的診斷意義,并能提示他汀類藥物不良反應發生風險。本研究對蚌埠醫學院第二附屬醫院收治的血脂異常患者進行SLCO1B1和APOE基因多態性位點分析,采用聚合酶鏈反應(PCR)-熒光探針法,以分子水平分析蚌埠及周邊地區SLCO1B1和APOE基因多態性分布,可以防止心腦血管疾病的發生,為個體化治療奠定基礎。
1 資料與方法
1.1一般資料 選取2020年7—12月在蚌埠醫學院第二附屬醫院就診的血脂異常患者為研究對象。入組標準:(1)年齡大于18歲患者;(2)患者血脂指標:血清總膽固醇(TC)≥5.2 mmol/L,即大于200 mg/dL;或低密度脂蛋白膽固醇(LDL-C)≥3.4 mmol/L,即大于130 mg/dL;或高密度脂蛋白膽固醇小于1.0 mmol/L,即小于40 mg/dL;或甘油三酯大于或等于1.7 mmol/L,即大于200 mg/dL。(3)經蚌埠醫學院第二附屬醫院醫學倫理專業委員會審查通過,患者簽署知情同意書。(4)長期服用他汀類藥物的患者。排除標準:合并有嚴重心腦血管疾病和嚴重肝腎疾病的患者。經篩選后共選取符合要求患者1 530例,采用PCR-探針法對SLCO1B1和 APOE基因進行多態性位點分析。患者年齡30~95歲,其中男1 002例,女528例,平均年齡(67±16)歲。
1.2方法
1.2.1儀器和試劑 SLCO1B1和APOE基因多態性檢測試劑盒(PCR-熒光探針法)購自武漢友芝友醫療科技有限公司;核酸提取純化試劑盒購自蘇州曠遠生物分子技術有限公司;全自動醫用PCR分析系統(型號:SLAN-48P)購自上海宏石醫療科技公司;全自動核酸提取儀(型號:NP968-C)購自西安天隆科技公司;超凈工作臺(型號:SW-CJ-1D)購自上海蘇凈公司;高速離心機(型號:TGL-16G)購自江蘇新康醫療公司。
1.2.2核酸提取 收集1~2 mL紫色乙二胺四乙酸抗凝全血(無須空腹,可正常飲食,2~4 ℃冰箱保存,72 h內處理)。按照核酸提取說明書進行操作,提取核酸:在96孔預裝板的第1列和第7列先加入核酸釋放劑60 μL及蛋白酶K 16 μL,之后在第1列和第7列加入全血樣本200 μL,選擇全自動核酸提取儀按照提取操作程序進行核酸提取,運行時間為48 min。運行結束后,相應第6列和第12列為對應標本DNA,用100 μL移液槍吸取75 μL核酸至1.5 mL EP管中。所提取的核酸用微量紫外分光光度計進行檢測,核酸 A260/ A280在1.8~2.0,A260/A230>2。推薦定量濃度稀釋為5~15 ng/μL,要求核酸原液-20 ℃保存。
1.2.3PCR擴增 SLCO1B1和APOE反應體系:根據標本數準備好八聯管,先加入提取好的核酸2.4~2.6 μL,之后加入ApoE2、ApoE4、SLCO1B1*1b、SLCO1B1*5反應液各21 μL,每個標本加4個孔,同時做弱陽性對照和空白對照,蓋上PCR反管蓋,同時做好標記,排除管內多余氣泡并進行渦旋混勻。先打開全自動醫用PCR分析系統并檢查是否正常運行,擴增程序設置為40個循環:37 ℃ 10 min、95 ℃ 5 min、95 ℃ 15 s、60 ℃ 45 s。將數據采集定在60 ℃,熒光信號收集為VIC通道(SLCO1B1*1b388G、SLCO1B1*5521C、ApoE2526T和ApoE4 388C)、FAM通道(SLCO1B1*1b388A、SLCO1B1*5521T、 ApoE2526 、ApoE4388T)和ROX通道(內標基因)。
1.2.4結果判斷 (1)樣本有效性的判定:內標基因(ROX通道)的Ct<38,擴增曲線有明顯指數增長期。(2)樣本基因多態性判定:相應通道的Ct<38,擴增曲線有明顯指數增長期,則該通道代表的基因型為陽性。若Ct≥38或無Ct值,則該通道代表的基因型為陰性。(3)試劑盒有效性判定:①弱陽性對照,FAM、VIC、ROX通道Ct≤32,擴增曲線有明顯指數增長期;②空白對照,FAM、VIC、ROX通道擴增曲線為輕微斜線或直線,或無擴增曲線,無明顯指數增長期,Ct≥38或無Ct值。(4)基因類型判定:若僅ROX通道Ct<38,FAM通道無Ct值或Ct≥38,則判斷為純和突變型;若僅 FAM通道Ct<38,ROX通道無Ct 值或Ct≥38,則判斷為純和野生型;若ROX通道和FAM通道的Ct值均小于38,則判斷為雜合型。
1.3統計學處理 采用SPSS22.0統計軟件對數據進行分析,計數資料以例數表示,進行Hardy-Weinberg遺傳平衡檢驗,然后分別計算基因型及基因頻率。基因型及等位基因頻率與其他地區已報道數據進行比較,采用χ2檢驗,P<0.05為差異有統計學意義。
2 結 果
2.1蚌埠及周邊地區患者APOE基因多態性分布 他汀類用藥與APOE基因388T>C、526C>T 2個位點有關,APOE2和APOE4是APOE的檢測基點,可形成6種基因型及其所占比例分別為 0.52%(E2/E2)、14.12%(E2/E3)、1.96%(E2/E4)、67.12%(E3/E3)、15.10%(E3/E4)、1.18%(E4/E4)。其中APOE的療效正常基因型(E2/E4 、E3/E3)組合最多,占比為69.08%,見表1。

表1 蚌埠及周邊地區患者SLCO1B1和APOE基因多態性分布情況(n=1 530)
2.2蚌埠及周邊地區患者SLCO1B1基因多態性分布 他汀類用藥與SLCO1B1基因388A>G、521T>C兩個位點多態性有關,SLCO1B1*1b和SLCO1B1*5是SLCO1B1的檢測基點,可形成9種基因型,所占比例分別為4.90%(*1a/*1a)、30.13%(*1a/*1b)、36.60%(*1b/*1b)、0.59%(*1a/*5)、8.24%(*1a/*15)、17.32%(*1b/*15)、 0.26%(*5/*5)、 0.13%(*5/*15)、1.83%(*15/*15)。正常肌病風險患者占比為71.65%,中度肌病風險患者占比為26.15%,高度肌病風險患者占比2.22%,見表1。根據服用的藥物劑量與肌病的風險發生橫紋肌溶解癥可見,正常肌病風險基因型(*1a/*1a、*1a/*1b、*1b/*1b)組合最多,高度肌病風險患者肝臟攝取藥物能力較差,發生橫紋肌溶解癥,建議使用較低劑量他汀類藥物;對于中度肌病風險患者,建議使用中等劑量他汀類藥物。
2.3不同性別患者SLCO1B1基因多態性分布差異 男性患者的SLCO1B1各基因型所占比例分別為4.79%(*1a/*1a)、29.54%(*1a/*1b)、36.13%(*1b/*1b)、0.80%(*1a/*5)、8.68%(*1a/*15)、18.16%(*1b/*15)、0.30%(*5/*5)、0.20%(*5/*15)、1.40%(*15/*15)。正常肌病風險基因型占比為70.46%,占比最大;中度肌病風險占比為27.64%;高度肌病風險占比為1.90%。女性患者的SLCO1B1各基因型所占比例分別為5.11%(*1a/*1a)、30.87%(*1a/*1b)、37.88%(*1b/*1b)、0.19%(*1a/*5)、7.39%(*1a/*15)、15.72%(*1b/*15)、0.19%(*5/*5)、0(*5/*15)、2.65%(*15/*15)。正常肌病風險基因型占比為73.86%,占比最重;中度肌病風險占比為23.30%;高度肌病風險占比為2.84%。男女患者SLCO1B1各基因型占比比較,差異均無統計學意義(P>0.05),見圖1。
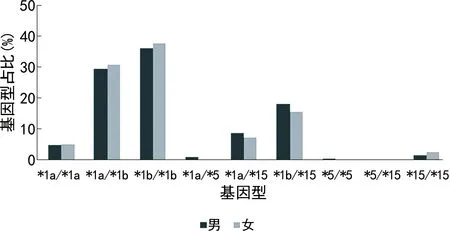
圖1 不同性別患者SLCO1B1基因多態性分布結果
2.4不同性別患者APOE基因多態性分布差異 男性患者APOE的各基因型所占比例分別為0.60%(E2/E2)、14.07%(E2/E3)、 2.10%(E2/E4)、66.96%(E3/E3)、15.07%(E3/E4)、1.20%(E4/E4)。療效正常基因型占比為69.06%,占比最大;療效較好基因型占比為14.67%;療效較差基因型占比為16.27%。女性患者APOE的各基因型所占比例分別為0.38%(E2/E2)、14.58%(E2/E3)、1.70%(E2/E4)、67.05%(E3/E3)、15.15%(E3/E4)、1.14%(E4/E4)。療效正常基因型占比為68.75%,占比最大;療效較好基因型占比為14.96%;療效較差基因型占比為16.29%。男女患者APOE各基因型占比比較,差異無統計學意義(P>0.05),見圖2。

圖2 不同性別患者SLCO1B1基因多態性分布結果
2.5蚌埠及周邊地區患者APOE基因型分布及等位基因頻率分布 1 530例患者中,APOE基因的388T>C位點檢測出野生型(TT)1 251例,純合突變型(CC)18例,雜合突變型(TC)261例,等位基因發生突變率為9.71%;APOE的526C>T位點共檢測出野生型(CC)1 276例,純合突變型(TT)8例,雜合突變型(CT)246例,等位基因發生突變率為8.56%。APOE的等位基因分布頻率與基因型見表2。

表2 蚌埠及周邊地區患者APOE基因型和等位基因分布頻率
2.6蚌埠及周邊地區患者SLCO1B1基因型分布及等位基因頻率分布 1 530例患者中,SLCO1B1基因的388A>G位點檢測出野生型(AA)88例,純合突變型(GG)853例,雜合突變型(AG)589例,等位基因發生突變率為75.00%;基因SLCO1B1的521T>C位點檢測出野生型(TT)1 096例,純合突變型(CC)34例,雜合突變型(TC)400例,等位基因突變發生率為15.29%。SLCO1B1的等位基因分布頻率與基因型見表3。

表3 蚌埠及周邊地區患者SLCO1B1基因型和等位基因分布頻率
采用χ2檢驗,將本研究中基因型及等位基因頻率與其他地區已報道數據進行比較,論證SLCO1B1及APOE基因的上述多態性位點突變頻率觀察值符合Hardy-wenberg遺傳平衡(P>0.05),具有群體代表性。
3 討 論
引起心腦血管疾病的主要原因是血脂異常,在我國人群中,因TC水平增高所導致的缺血性腦卒中事件發生率約為冠心病2倍以上,他汀類藥物就成為臨床使用最為廣泛的降脂藥[4],循證醫學證據顯示,他汀類藥物降低LDL-C有明顯的個體差異(10%~70%)[5],會引起相關不良反應,如肌肉毒性、肝毒性、糖尿病和認知功能改變等,因此基因多態性已成為影響他汀類藥物降脂效果及不良反應發生風險的重要因素之一。
APOE基因存在于人體第19號染色體長臂13區上[6]。機體脂質代謝的調節因子是APOE基因的388T>C、526C>T,是影響他汀類降脂療效的主要因素,也是動脈粥樣硬化性心腦血管病和高脂血癥的候選易感基因。APOE基因形成APOE2(388T-526T)、APOE3(388T-526C)、APOE4(388C-526C)3種單倍體和6種表型[7]。其中APOE3(388T-526C)為野生型,對機體正常生理功能發揮起重要作用。APOE2(388T-526T)為突變型,攜帶者血漿TC、LDL-C水平低于APOE3(388T-526C)型患者,他汀類藥物降脂效果相對其他2型最好。APOE4(388C-526C)為突變型,與阿爾茲海默病(AD)、心腦血管病、冠心病、抑郁癥的高發性相關[8],降脂療效往往不佳或無療效,TC、LDL-C水平均遠高于APOE3型。
人類的SLCO1B1基因存在于12號染色體上,SLCO1B1基因2種常見的單核苷酸多態性是388A>G、521T>C[9]。SLCO1B1基因可形成SLCO1B1*1a(388A-521T)、SLCO1B1*1b(388G-521T)、SLCO1B1*5(388A-521C)、SLCO1B1*15(388G-521C)4種單倍體和9種表型[10]。有機陰離子轉運多肽OATP1B1參與多種藥物的轉運,在他汀類藥物代謝中將血液中的藥物轉移至肝臟中,從而直接發揮藥效,是具有基因多態性的跨膜轉運蛋白[11],OATP1B1轉運蛋白活力減弱是由突變型SLCO1B1基因引起,會增加肝毒性,導致肝臟攝取藥物能力降低,造成他汀類藥物血藥濃度上升,加重橫紋肌溶解癥或肌病的風險。有研究表明,攜帶有*5位點與他汀性肌病的風險顯著相關,他汀類藥物相關肌病的發生為劑量依賴性,目前臨床上已有相關病例報道攜帶SLCO1B1* 5等位基因是發生橫紋肌溶解癥的主要原因[12-13]。
蚌埠及周邊地區患者中APOE基因的E3/E3型1 027例,占比最大,為67.12%,表明他汀治療療效正常;老年癡呆、冠心病、腦梗死風險正常。SLCO1B1基因的*1a/*1b和*1b/*1b共1 021例,占比最大,為66.73%,則可以考慮使用較大劑量他汀。另外,APOE基因和SLCO1B1基因的各表型占比在男女患者之間比較,差異均無統計學意義(P>0.05);不同性別的APOE與 SLCO1B1 基因型分布符合人群總體分布趨勢。
蚌埠及周邊地區人群中APOE的E3/E4和E4/E4基因型患者共246例,占比為16.08%;從降脂效果看,他汀類藥物療效較差,有增加冠心病、急性心肌梗死、腦梗死、老年癡呆風險。研究發現:攜帶1個E4基因患者的AD發病率為47%,而攜帶2個E4基因患者的AD發病率高達91%,并且,E4基因攜帶者的發病時間較非攜帶者提早10~20年[14]。所以,有AD家族史或記憶力已經明顯衰退的人群需進行APOE基因多態性檢測,因此要盡早干預高風險人群以延緩AD的發生,能更好地指導患者合理化用藥和健康生活。SLCO1B1基因的高度肌病風險患者共31例,占比為2.03%,此類患者需要注意藥物使用劑量,使用阿托伐他汀降脂效果更好[15]。因此應當重點關注心腦血管患者服用他汀類藥物后的反應,篩查APOE風險類及SLCO1B1高度風險基因型不僅可以更好地指導臨床醫生用藥,還可以讓患者避免不良反應和達到藥物治療的最大療效。
總之,SLCO1B1和APOE基因檢測能幫助臨床更合理地選擇藥物和劑量,制定個體化的降脂方案,最終使患者受益。

