泰拉霉素國家對照品的標定研究
戴 青,張秀英,楊秀玉,韓寧寧,王 軒, 季 璇,趙 暉
(中國獸醫(yī)藥品監(jiān)察所,北京 100081)
泰拉霉素是由美國輝瑞動物保健公司開發(fā)的動物專用新型大環(huán)內酯類抗生素,主要用于治療牛和豬呼吸系統感染性疾病[1-2],目前臨床上廣泛應用的制劑為泰拉霉素注射液。泰拉霉素由15元氮雜內酯環(huán)(泰拉霉素A)和13元氮雜內酯環(huán)(泰拉霉素B)兩種同分異構體組成[3],該兩種同分異構體均是泰拉霉素中的抗菌活性成分,原料藥中泰拉霉素B含量較少,但泰拉霉素A與泰拉霉素B這兩個異構體在溶液中易發(fā)生轉化,且處于平衡,需要以兩個異構體之和對含量進行控制。目前,各國藥典均未收載泰拉霉素原料藥及相關制劑的質量標準,均無泰拉霉素國家標準物質供應,調研發(fā)現,在企業(yè)內部質量控制過程中,多使用自制工作對照品。因此,為了更好地對產品進行質量控制,研制了泰拉霉素國家對照品,對于泰拉霉素原料及注射液的生產及質量控制具有重要意義。
1 儀器與試藥
1.1 儀 器 e2695型高效液相色譜儀(美國Waters公司);2489型紫外檢測器(美國Waters公司);2998型二極管陣列檢測器(美國Waters公司);AUTOPOL V型自動旋光儀(美國Rudolph公司);TENSOR 27型傅里葉變換紅外光譜儀(德國Bruker公司);7890A型氣相色譜儀(美國Agilent公司);AX205型電子天平(美國Mettler公司);701KF型水分測定儀(瑞士Metrohm公司); DSC Q200型差示掃描量熱儀(美國TA公司)。
1.2 試 藥 原始發(fā)明廠泰拉霉素工作對照品(含量99.0%,美國Zoetis公司);泰拉霉素原料由Zoetis公司生產;甲醇、乙腈(色譜純,德國Merk公司);磷酸二氫鉀(分析純,中國上海源葉公司);實驗用水為超純水。
2 方法與結果
2.1 樣品制備 將精制后的泰拉霉素原料分裝于棕色安瓿瓶中,每支100 mg,置于5 ℃冰箱儲存,作為待標品,經理化分析、標定含量后貼簽入庫,作為國家對照品發(fā)放。
2.2 比旋度 取待標品適量,用乙腈溶解制成40 mg/mL的溶液,采用鈉光譜D線(589 nm),測定待標品溶液旋光度,測定結果為-25°。
2.3 紅外光譜鑒別 分別取待標品與泰拉霉素工作對照品適量,用溴化鉀壓片,測定二者紅外光吸收圖譜,結果為二者紅外光吸收圖譜一致(圖1~圖2)。
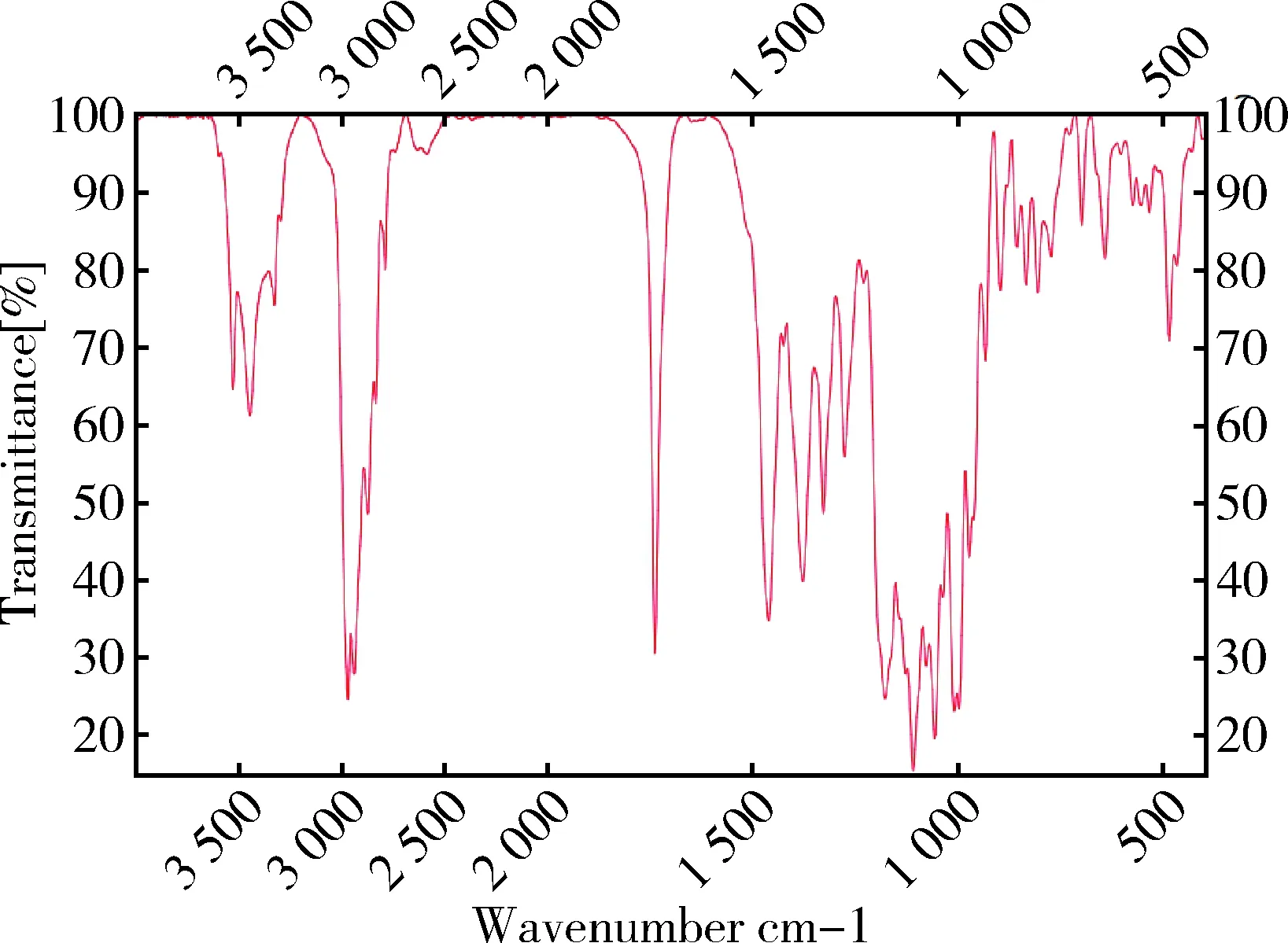
圖1 泰拉霉素工作對照品紅外光譜圖Fig. 1 Infrared spectrum of tulathromycin working reference substance
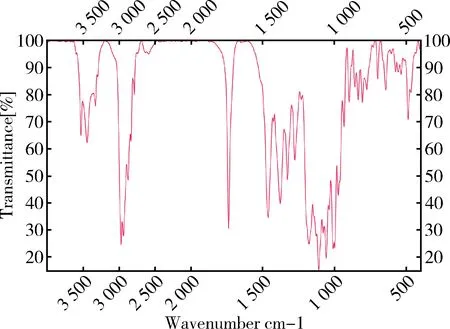
圖2 本批泰拉霉素對照品紅外光譜圖Fig 2 Infrared spectrum of this batch of tulathromycin reference substance
2.4 有關物質
2.4.1 液相色譜條件 色譜柱Kromasil C18(4.6 mm×150 mm,3.5 μm);以甲醇-乙腈-0.075 mol/L磷酸二氫鉀溶液(pH 7.0)(45∶25∶30)為流動相;流速1.0 mL/min;檢測波長205 nm;柱溫40 ℃。待標品溶液質量濃度為2 mg/mL,進樣體積為25 μL。采用自身對照法計算有關物質,測得總有關物質量為1.38%。
2.4.2 方法專屬性 按照上述方法,在待標品溶液中加入1 mol/L鹽酸溶液,室溫破壞2 h進行酸降解;在待標品溶液中加入1 mol/L氫氧化鈉溶液,室溫破壞2 h進行堿降解;在待標品溶液中加入3%雙氧水溶液,室溫破壞2 h進行氧化降解;將待標品在120 ℃放置8 h進行高溫降解;將待標品在5000 lx光照下放置8 h進行光照降解。分別測定各種破壞性試驗條件下待標品的有關物質,并采用二極管陣列檢測器,進行峰純度檢查。破壞性試驗結果見表1,結果表明,酸、堿、氧化降解均易增加雜質含量,提示樣品應避免接觸強酸、強堿、氧化劑等,以防止產生過量雜質。各條件下主峰均可與相鄰峰實現良好分離,且各雜質峰純度角度均小于閾值,為單一物質峰,降解產物不干擾主峰測定,表明方法專屬性良好。
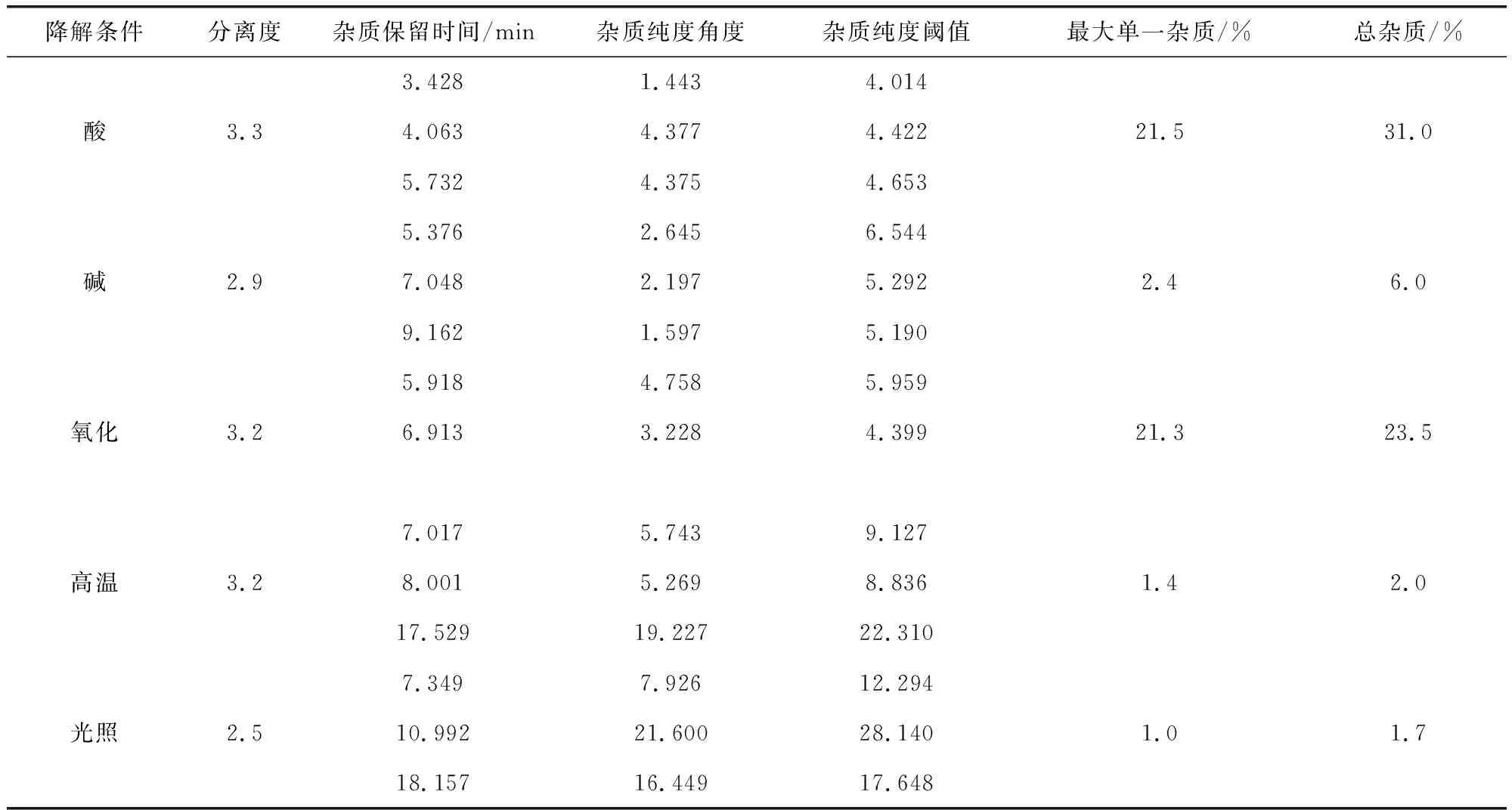
表1 破壞性試驗結果Tab 1 Results of destructive tests
2.4.3 檢測限 將2 mg/mL的溶液進一步稀釋為1 μg/mL的檢測限溶液,測定信噪比。檢測限溶液信噪比為3∶1,表明該方法泰拉霉素的檢測限為1 μg/mL。
2.4.4 線性與范圍 配制10 mg/mL的貯備液,經一系列精密稀釋,分別制成5000、2000、1000、400、100、10、2 μg/mL的溶液,采集色譜圖,以峰面積與濃度作圖,用最小二乘法進行線性回歸。峰面積與濃度線性方程為:y=3414.7x-5881.9,r=1。表明在2~5000 μg/mL范圍內濃度與峰面積具有良好的線性關系。
2.4.5 溶液穩(wěn)定性 將溶液于室溫放置12 h,期間不同時間進樣采集色譜圖,考察峰面積變化情況。溶液穩(wěn)定性結果見表2,峰面積12 h內RSD為1.6%,小于2.0%,表明該溶液室溫放置12 h穩(wěn)定性良好。
2.5 液相色譜鑒別 分別取待標品與泰拉霉素工作對照品適量,按照2.4.1項下色譜條件,測定二者主峰的保留時間,結果為樣品高效液相色譜圖主峰保留時間與泰拉霉素工作對照品的保留時間一致,且溶劑空白對泰拉霉素測定無干擾(圖3~圖5)。
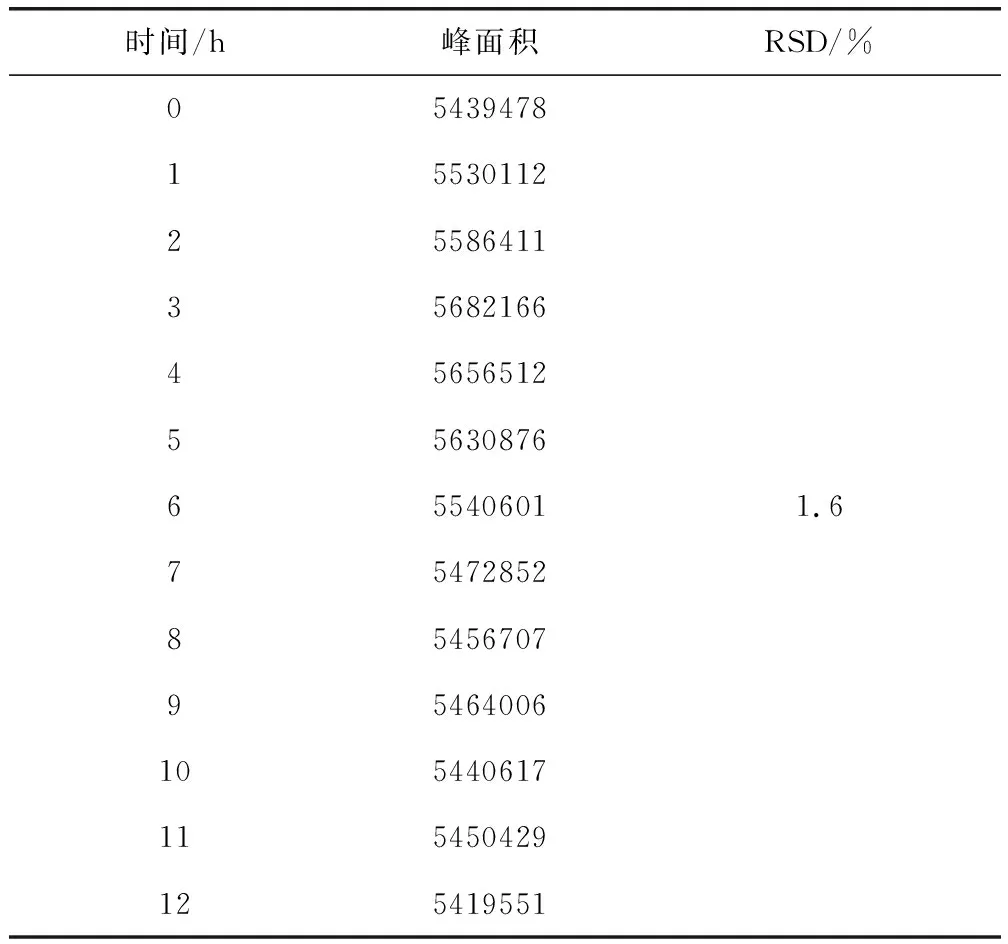
表2 溶液穩(wěn)定性結果Tab 2 Results of solution stability test
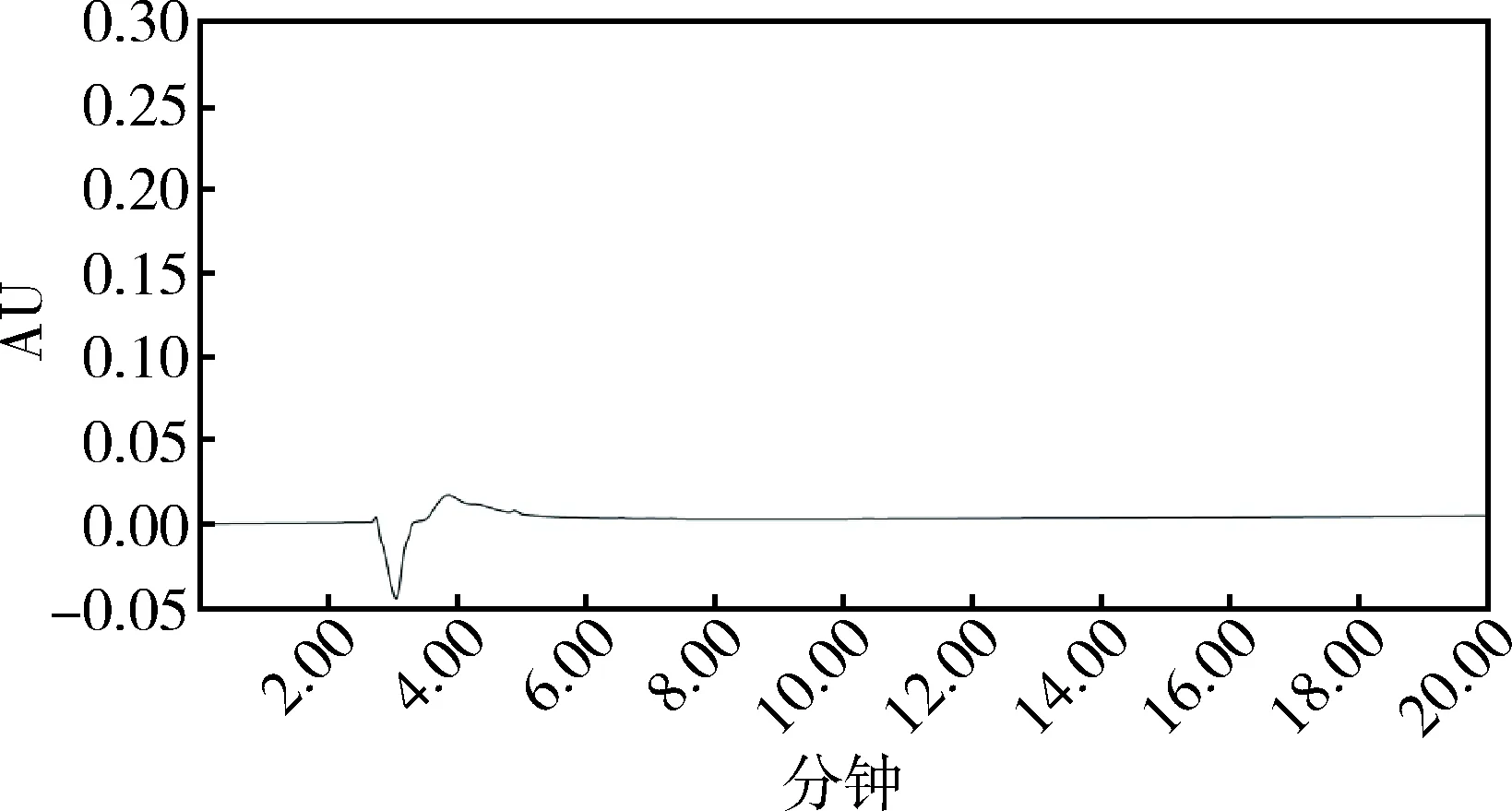
圖3 溶劑空白液相色譜圖Fig 3 Liquid chromatogram of solvent blank
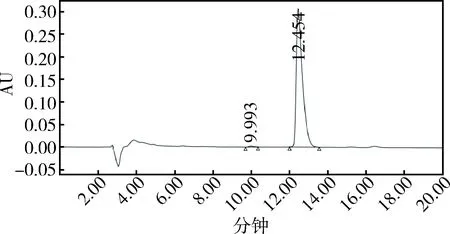
圖4 泰拉霉素工作對照品液相色譜圖Fig. 4 Liquid chromatogram of tulathromycin working reference substance

圖5 本批泰拉霉素對照品液相色譜圖Fig 5 Liquid chromatogram of this batch of tulathromycin reference substance
2.6 水分 按照《中國獸藥典》2020年版一部附錄0832費休氏法,取待標品3.0 g,精密稱定,置于水分測定儀中,測定水分含量,結果為0.19%。
2.7 熾灼殘渣 按照《中國獸藥典》2020年版一部附錄0841熾灼殘渣檢查法,精密稱取本品1.0 g,置坩堝中,于750 ℃下熾灼至恒重,計算遺留殘渣量,結果為0.09%。
2.8 殘留溶劑 采用氣相色譜法檢測待標品合成工藝中使用的有機溶劑(庚烷、二氯甲烷、異辛烷)殘留量。以 DB-624 毛細管柱(30 m×0.32 mm,1.8 μm) 為分離柱,以氮氣為載氣,柱溫采用程序升溫,起始溫度40 ℃,維持5 min,再以20 ℃/min的速率升溫至90 ℃,立刻以30 ℃/min的速率升溫至225 ℃,維持2 min。頂空進樣,平衡溫度105 ℃,頂空平衡時間60 min,供試品溶液的質量濃度為30 mg/mL。采用外標法以峰面積計算。樣品殘留溶劑中僅檢出異辛烷,殘留量0.01%(圖6~圖8)。
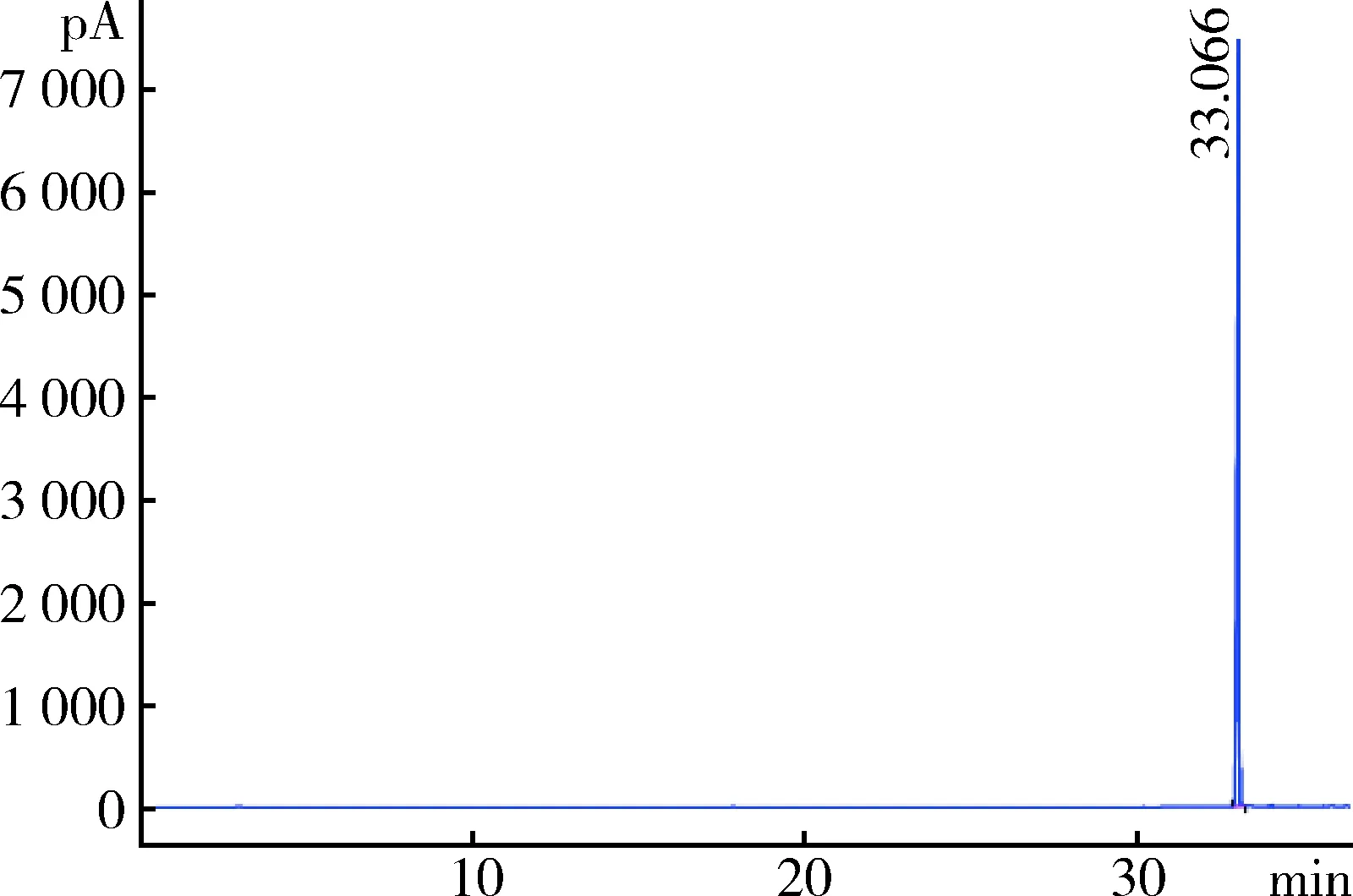
圖6 溶劑空白氣相色譜圖Fig 6 Gas chromatogram of solvent blank
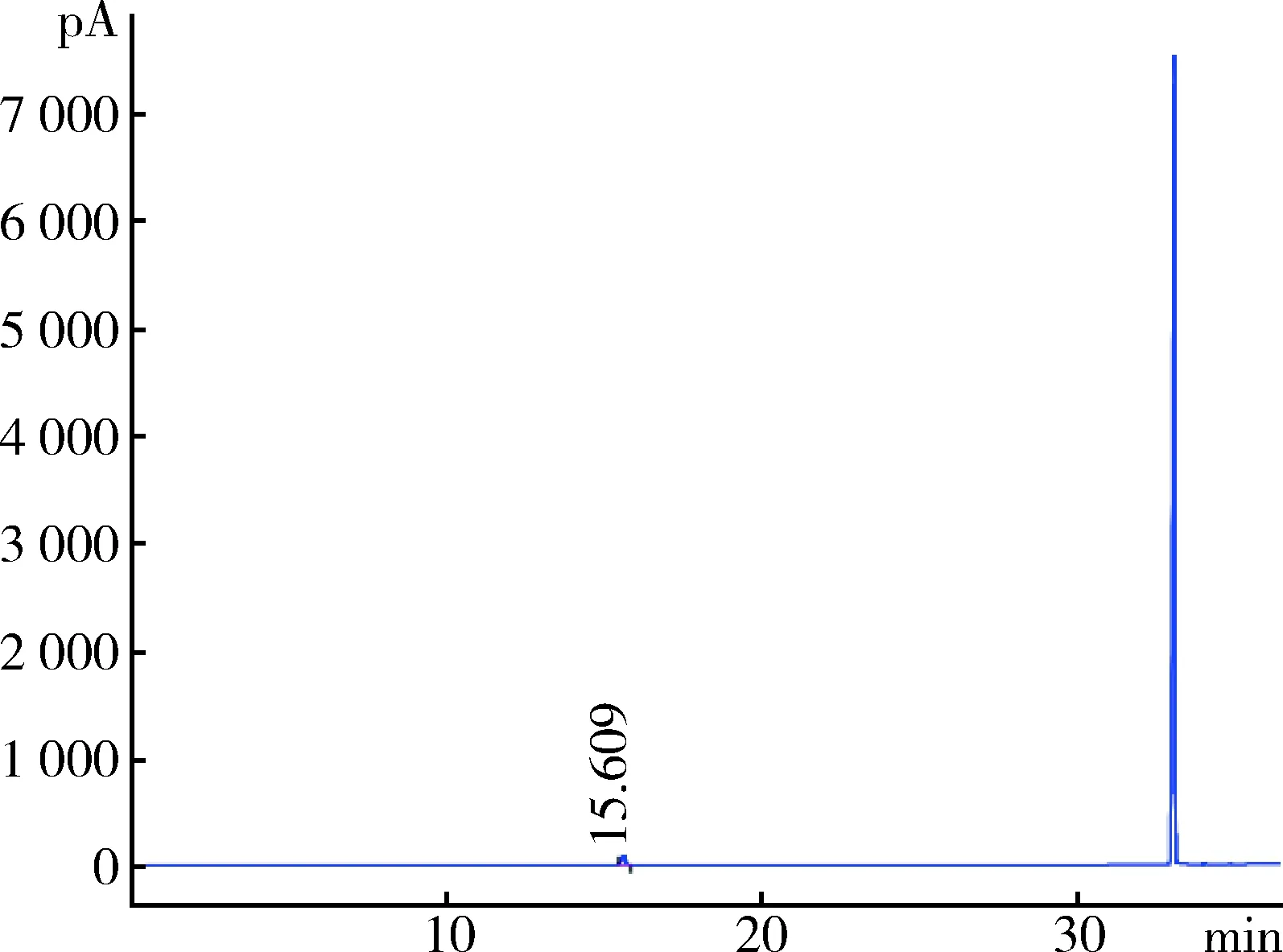
圖7 異辛烷氣相色譜圖Fig. 7 Gas chromatogram of isooctane
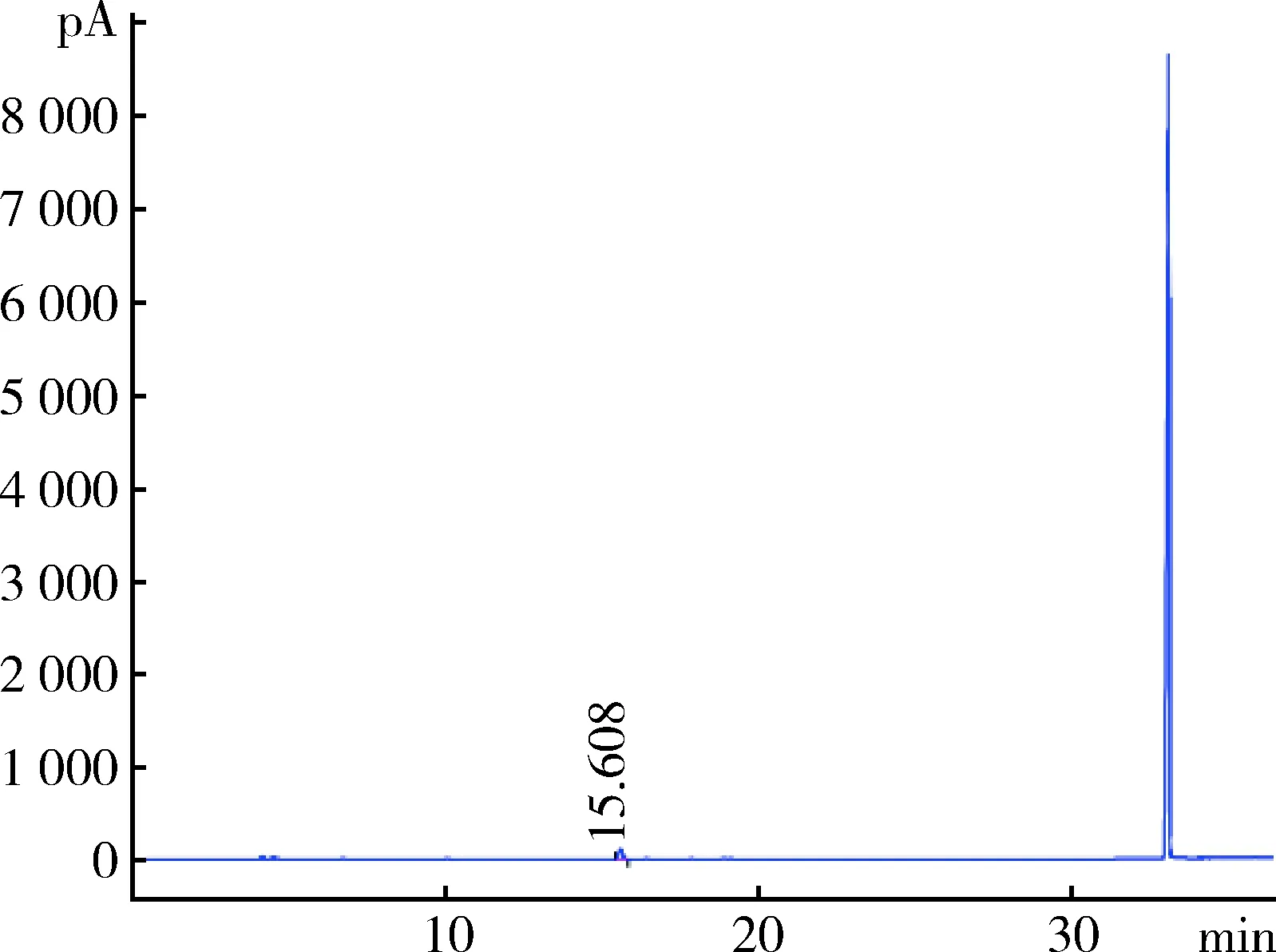
圖8 本批泰拉霉素對照品氣相色譜圖Fig 8 Gas chromatogram of this batch of tulathromycin reference substance
2.9 均勻性評估 隨機抽取待標品10支,每支取樣2次進行測定,采用高效液相色譜法,按照2.4.1項下色譜條件,取本品20 mg,精密稱定,制成質量濃度為2 mg/mL的溶液。以單位質量峰面積為結果,采用單因素方差分析法對測定結果進行均勻性評估。樣品間自由度為9,樣品內自由度為10,在約定自由度水平α=0.05的顯著水平下,計算臨界值F0.05(9,10),計算結果與查表得到的F臨界值3.02比較,若計算值小于3.02,則表明在α=0.05的顯著水平下,樣品是均勻的。計算得樣品均勻性單因素方差分析結果統計量F為2.60,小于3.02,表明研制的本批對照品均勻性良好,符合國家標準物質研制的要求。
2.10 含量測定
2.10.1 質量平衡法 根據質量平衡法的計算方法,采用以下公式計算泰拉霉素的含量:(1-有關物質)×(1-水分-殘留溶劑-熾灼殘渣)×100%。根據質量平衡法計算公式,計算得泰拉霉素含量為98.3%。
2.10.2 差示掃描量熱法 采用差示掃描量熱法對質量平衡法賦值結果進行驗證。以不同升溫速率,在175~210 ℃溫度范圍內測定待標品中泰拉霉素的含量,結果見表3,不同升溫速率對測定結果影響不大。DSC法升溫速率一般低于1 ℃/min時,體系接近平衡態(tài),但有時為了節(jié)省時間和避免分解,可以用更快的升溫速率,較快的升溫速率有利于將分解效應與熔融效應分離。考慮到1 ℃/min升溫速率圖譜基線不平衡,因此選取了2 ℃/min和5 ℃/min的升溫速率進行多次測定,泰拉霉素含量為98.5%,結果見表4,圖譜見圖9。
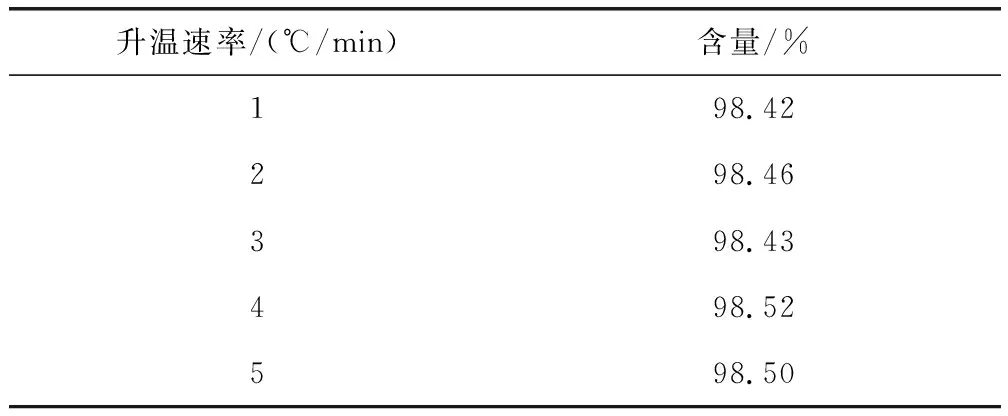
表3 不同升溫速率樣品含量Tab 3 Sample content at different heating rates
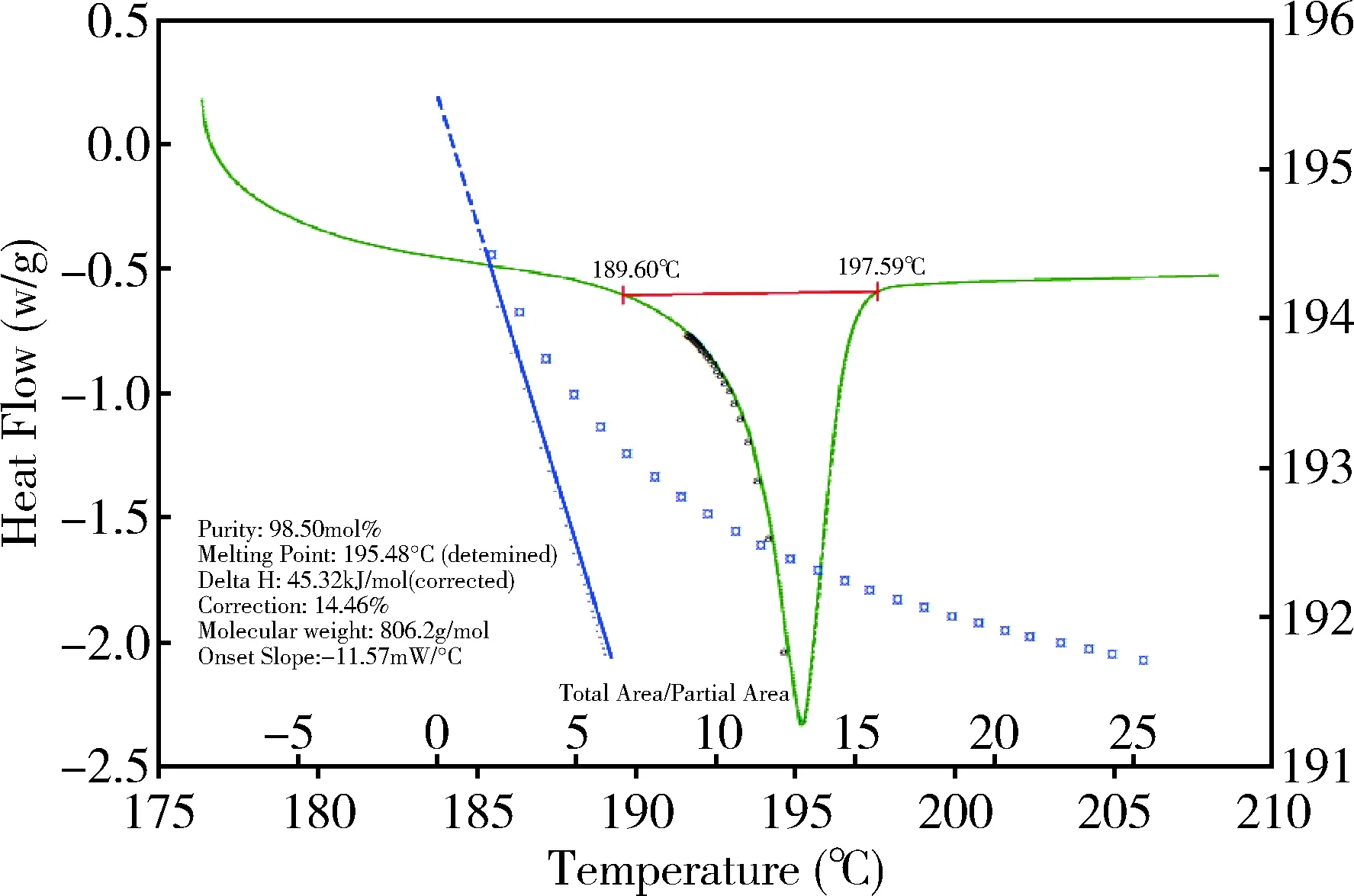
圖9 本批泰拉霉素對照品差示掃描量熱法圖譜Fig 9 DSC atlas of this batch of tulathromycin reference substance
3 討論與結論
化學標準物質的定值目前較為普遍的方法是質量平衡法,其能夠直接溯源到國際單位制中的質量單位,是國際上標準物質定值推薦的常用方法[4-5]。該方法賦值結果準確,但受影響因素較多,往往需要采用其他方法對質量平衡法的賦值結果進行驗證[6]。差示掃描量熱(DSC)法是研究應用最廣泛的熱分析技術之一,具備快速采集、操作簡便等特點,越來越廣泛地應用于標準物質的定值中[7-8]。本研究針對泰拉霉素樣品的特點,在標定國家獸藥標準物質的過程中,采用質量平衡法、差示掃描量熱法分別對泰拉霉素進行定值與驗證,確保定值結果的準確性。
本研究研制了泰拉霉素國家對照品,采用質量平衡法與差示掃描量熱法兩種不同原理的定值方法測定泰拉霉素含量,結果分別為98.3%和98.5%,兩種方法標定結果基本一致,相互驗證,可以保證定值的準確性。由于質量平衡法是世界衛(wèi)生組織推薦的藥品標準物質定值方法,能夠更準確地反映本品的真實含量,因此,以質量平衡法的結果進行賦值,可作為國家對照品用于泰拉霉素及其制劑的含量測定。

