覆膜金屬罐中PBT/PET環狀低聚物在食品中的遷移測試及基于膳食暴露量的風險評估
李倩云1, 吳剛2, 王亞2, 王曉龍2, 潘峰1, 張泓1, 邢航1, 李建文1*, 朱蕾1*
(1. 國家食品安全風險評估中心, 北京 100022;2. 中國食品發酵工業研究院, 北京 100015)
金屬覆膜是一種通過熱熔、淋膜或粘合的方法將塑料薄膜附著在金屬基板表面的技術[1]。常用的金屬基板包括鍍鉻鐵、馬口鐵、鋁板以及冷軋薄鋼板等, 其中鍍鉻鐵具有優異的耐腐蝕性能和涂覆性能, 且成本低、外觀獨特[2], 成為覆膜鐵的主要材料, 是食品罐、啤酒罐以及飲料罐首選的金屬基板[3]。金屬罐覆膜材料包括聚對苯二甲酸乙二醇酯(PET)、聚丙烯(PP)、聚乙烯(PE)、聚對苯二甲酸丁二醇酯(PBT)和聚對苯二甲酸己二酸丁二醇酯(PBAT)等, 其中PET的綜合性能最優, 具有成型易、可殺菌、硬度高、耐磨以及經特殊處理可印刷等特性[4]。與傳統的馬口鐵、涂料鐵相比, 覆膜鐵作為一種新型的復合材料, 具有優異的耐腐蝕性、耐加工性、防銹性、防潮性和阻隔性, 其生產工藝簡潔高效、低碳、低耗能、無廢液廢氣排放[5-6], 具有綠色環保、可減少碳排放以及可回收等特點。隨著國內外金屬罐類食品接觸材料需求的巨大增長, 以及全球資源可持續利用和綠色環保的發展理念, 覆膜金屬罐的市場占有率將日益上升, 在罐裝食品包裝方面的應用也會越來越廣泛。
然而, 用作食品金屬罐覆膜的主要為PET、PBT和PBAT等幾種物質的共聚產物, 這些熱塑性樹脂薄膜在聚合過程中由于溫度、氧氣等的作用, 會發生熱降解、氧化等副反應, 或在酯交換/酯化過程中由于反應不完全或聚合物的水解等生成PET和PBT環狀低聚物[7]等非有意添加物(NIAS), 并通過接觸遷移到食品中。目前國內外均無PET和PBT環狀低聚物毒理學的研究報道, 此類物質也不在GB 9685-2016[8]的添加劑列表和GB 4806. 6-2016[9]的特定遷移限量物質列表中, 目前僅通過食品接觸材料及制品通用安全要求[10]進行通用管理。因此, 對于覆膜金屬罐遷移到食品中的PET和PBT環狀低聚物的量及安全性應引起關注, 并亟需建立簡便有效的方法對我國居民通過與食品接觸的覆膜金屬罐中的PBT和PET環狀低聚物的膳食暴露量進行風險評估。
毒理學關注閾值(TTC)作為一種有效的風險評估工具, 其基本原理是認為所有化學物質均可確定一個普適的安全暴露閾值, 當人體暴露水平低于相應的閾值時, 不會對人體健康產生危害。目前, 對于PET和PBT環狀低聚物遷移量的檢測已有研究, 如徐彤彤等[11]首次采用超高效液相色譜-質譜聯用技術(UPLC-QTOF MS)對層壓鋼罐中的PET和PBT環狀低聚物進行定性和定量分析, 研究了6種低聚物在3種食品模擬物中的遷移量;Emmanouil等[12]采用TTC方法對寵物茶包中的PET低聚物進行了風險評估。但國內外很少有對覆膜金屬罐遷移到食品中的PET和PBT環狀低聚物進行風險評估的報道, 因此有必要根據我國消費者食物消費量的特點, 結合市場上覆膜金屬罐中PET和PBT環狀低聚物的遷移情況進行風險評估以評價其安全性。
本文結合金屬覆膜中可能遷移出的PET和PBT環狀低聚物的特點, 建立了食品中這兩種物質遷移量的檢測方法。基于遷移試驗結果、我國人群食物消費量調查、與食品接觸面積和食品單位質量/體積比(S/V)調查結果, 運用TTC定量風險評估方法, 對我國市售食品覆膜金屬罐包裝中遷移出的PET環狀二聚體、PET環狀三聚體、PET環狀四聚體、PET環狀五聚體和PBT環狀二聚體、PBT環狀三聚體6種低聚物(圖1)開展評估, 初步評估其健康風險。
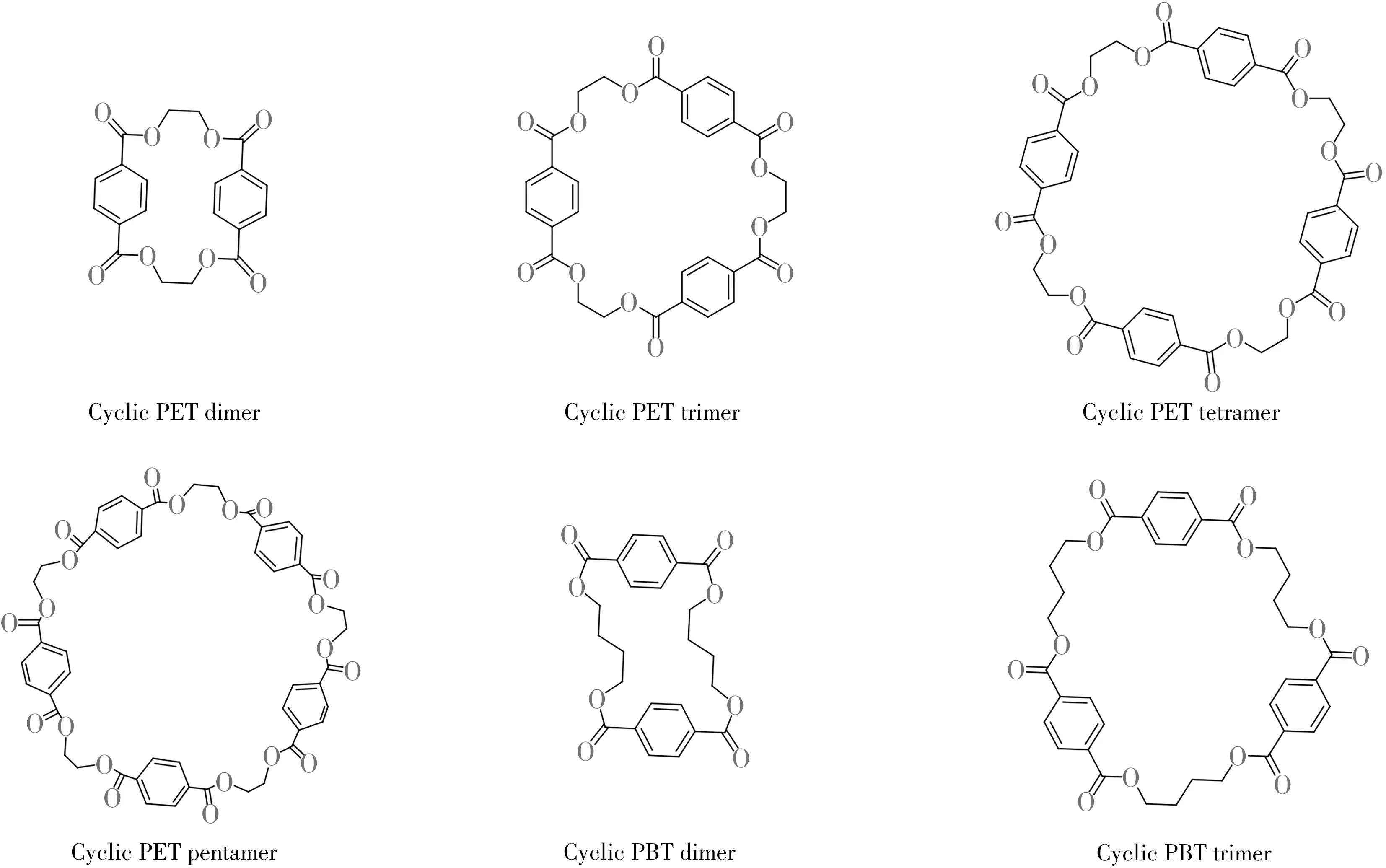
圖1 PET和PBT環狀低聚物分子結構圖Fig. 1 The chemical structures of cyclic PET and PBT oligomers
1 實驗部分
1.1 儀器、試劑與樣品
Agilent 1290 UPLC-Agilent 6546 UHD QTOF MS(美國安捷倫儀器公司);KQ-500DE超聲波清洗儀(中國江蘇昆山超聲波儀器有限公司);TG18K高速離心機(上海舜制儀器制造有限公司);VORTEX05渦旋混勻器(上海達姆實業有限公司);AB204-N分析天平(梅特勒-托利多儀器有限公司);UGC-45C圓形水浴氮吹儀(北京優晟聯合科技有限公司);QSE-12D固相萃取儀(上海比朗儀器制造有限公司)。
PET環狀低聚物標準品(北京匯科同創科學儀器有限公司);PBT環狀低聚物標準品(北京百靈威科技有限公司);乙腈、甲醇、甲酸、甲酸銨(質譜純, 上海霍尼韋爾貿易有限公司);二氯甲烷、正己烷、無水乙醇(色譜純, 德國Merck公司);2, 2, 2-三氟乙醇(色譜純, 西格瑪奧德里奇貿易有限公司);六氟異丙醇、N-丙基乙二胺固相吸附劑(PSA)、三氧化二鋁(色譜純, 上海安譜實驗科技股份有限公司);氯化鈉、無水硫酸鎂(色譜純, 中國醫藥上海化學試劑公司), 聚四氟乙烯(PTFE)濾膜(0. 22μm, 天津津騰實驗設備有限公司)。
檢測樣品為市面購買的水果罐頭、飲料、啤酒覆膜金屬罐, 并根據樣品的實際情況對最小(Min)、最大(Max)和平均(Mean)S/V結果進行統計。
1.2 標準溶液的配制
4種PET環狀低聚物標準儲備液(1 000 mg/L):分別準確稱取PET環狀低聚物標準品1 mg(精確至0. 01 mg)至棕色小瓶中, 加入1 mL六氟異丙醇(HFIP), 混勻。
PBT環狀二/三低聚物標準儲備液(1 000 mg/L):準確稱取PBT環狀二/三低聚物標準品1 mg(精確至0. 01 mg)至棕色小瓶中, 加入1 mL HFIP, 混勻。
混合標準工作液(10 mg/L):分別準確量取6種環狀低聚物標準儲備溶液(1 000 mg/L)0. 1 mL至10 mL容量瓶中, 以乙腈定容至刻度線, 混勻。系列混合標準工作液:分別精確量取0. 010、0. 025、0. 050、0. 100、0. 250、0. 500 mL混合標準工作液(10 mg/L)于5 mL容量瓶中, 用乙腈定容至刻度線, 得到質量濃度分別為20、50、100、200、500、1 000μg/L的混合標準工作液。
1.3 樣品制備及實驗方法
1.3.1 樣品固相萃取處理將食品樣品全部均質(約2 min), 取2 g樣品置于離心管中, 室溫下穩定15 min后進行樣品提取。向離心管中加入10 mL含0. 1%甲酸的乙腈溶液, 渦旋5 min。將處理后的樣品放入冰箱(4℃)儲存一夜。第二天將樣品從冰箱中取出并于4 000 r/min離心10 min, 吸取上清液在常溫下進行氮吹, 至溶液剩余約1 mL, 向溶液中加入5μL甲酸, 混勻。使用甲醇和含0. 1%甲酸的水對固相萃取柱(Agilent Bond Elut C18, 500 mg, 3 mL)進行預處理, 然后將上述混合溶液轉移入柱, 最后使用1 mL乙腈洗脫分析物, 將所得溶液過PTFE濾膜, 使用UPLC-QTOF MS分析。
1.3.2 樣品QuEChERS處理將食品樣品全部均質, 稱取2 g樣品置于50 mL離心管中, 加入8 mL六氟異丙醇-2, 2, 2-三氟乙醇-乙醇混合溶劑(體積比2∶2∶4)、3. 0 g無水MgSO4和0. 8 g NaCl, 將混合物渦旋2. 0 min后于6 000 r/min離心10 min。吸取上清液2 mL至15 mL離心管中, 加入100 mg無水MgSO4、20 mg PSA和200 mg Al2O3, 將混合物渦旋2 min后于6 000 r/min離心10 min。取1 mL上清液過PTFE濾膜, 使用UPLC-QTOF MS分析。
1.3.3 樣品液液萃取處理將樣品內容物全部均質, 稱取均質樣品2. 0 g, 置于10 mL離心管中。加入8 mL乙腈, 將混合物渦旋振蕩5 min, 隨后超聲20 min, 于4 000 r/min離心10 min。取上清液于常溫下氮吹至干, 再用1 mL乙腈復溶, 過PTFE濾膜, 使用UPLC-QTOF MS分析。
1.3.4 儀器條件對于PET及PBT低聚物, 采用UPLC-QTOF MS和質譜檢測器的信息相關采集(IDA)模式進行測試, 具體條件如下:流動相A為水(含0. 1%甲酸和2 mmol/L甲酸銨);B為甲醇(含0. 1%甲酸和2 mol/L甲酸銨), 流速為500μL/min;梯度洗脫程序為:0~0. 5 min, 20% B;0. 5~2 min, 20%~70%B;2~7 min, 70%B;7~17 min, 70%~100%B;17~17. 5 min, 100%B;17. 5~20 min, 100%~20%B;柱溫為35℃;注射體積為5μL;掃描模式為正模式的增強子離子(EPI)掃描, 離子源溫度為550℃, 噴射電壓為5 500 V, 質量范圍為m/z 80~1 500, 碰撞電壓為10 V, 氣簾氣壓力為241 kPa(35 psi), 碰撞氣壓力為48 kPa(7 psi);MS/MS收集質量范圍為m/z 50~1 500, 碰撞能量設置為(35±15)V。
1.4 風險評估
1.4.1 TTC評估方法本研究采用的TTC評估方法主要參考歐洲國際生命科學學會(ILSI)改進的TTC評估方法以及歐洲食品安全局(EFSA)推薦的TTC評估通用流程[13], 采用歐洲化學品局建立的Toxtree軟件[14]進行歸類, CramerⅠ、CramerⅡ、CramerⅢ三類物質的TTC安全閾值分別為30. 0、9. 0、1. 5μg/kg·BW/d。
1.4.2 膳食暴露評估方法目前國際上食品接觸材料的暴露評估方法共分為3種:傳統方法、雙因子法和接觸面積法。傳統方法易偏離實際膳食暴露水平;雙因子法的數據需要從行業企業調查中得到, 數據獲得性較差, 且得到的數據不夠準確、全面, 導致結果有很大的不確定性;接觸面積法獲得的是實際消費數據, 工作量相對較大, 但數據更加準確, 更能反映真實水平。因此本研究采用食品接觸面積法進行膳食暴露評估。
采用食品接觸面積法對食品接觸材料暴露進行評估需要獲得3個參數:(1)人群食物消費量數據(kg/kg·BW/d);(2)物質遷移量(mg/dm2);(3)與食品接觸面積和食品單位質量/體積比(S/V)(dm2/kg)。估計膳食暴露量(EDI)公式如下:
EDI(mg/kg)=與食品接觸面積(dm2)/食品質量或體積V(kg)×物質遷移量(mg/dm2)×食物消費量(kg/kg(食品))。
1.4.3 食物消費量調查方法借助我國食物消費量調查工作平臺, 選取山東省德州市的12個社區, 共計60戶181人作為調查對象, 采用回顧法、食物稱重法、記賬法和食物日記法等調查方法對被調查人群非連續2 d 24 h內攝入的全部預包裝食品種類、重量、品牌、包裝類型、包裝材質、包裝面積、規格、口味、消費量、消費頻率、包裝材質及其面積等信息進行收集整理。
1.4.4 與食品接觸面積和食品單位質量/體積比(S/V)的調查方法本研究通過行業調查、市場采樣和線上采購3種方式開展數據調查。調查內容包括食品類別、保質期、食品特性、規格、包裝類型、食品接觸材料材質和面積、樣品照片等27個項目, 對食品特性、所用包裝材質、食品質量、接觸面積等數據進行測量后匯總分析, 計算獲得S/V。材質采用目視法和紅外光譜法結合的分級確認方法[15]。GB 31604. 1-2015《食品安全國家標準 食品接觸材料及制品遷移試驗通則》[16]規定, 結果換算中S/V的選擇要反映實際的使用情形, 取可預見使用情形下的最大S/V, 當無法估算時, 一般采用6 dm2/L(液態食品密度以1 kg/L計)進行計算。
2 結果與討論
2.1 前處理方法的選擇
本實驗分別考察了采用固相萃取、QuEChERS和液液萃取3種方法對實驗樣品進行提取分析的效果。結果發現, 使用固相萃取和QuEChERS兩種方法處理后, 6種目標物的回收率均在80%以下, 可能是在樣品處理過程中損失較大所致。而當使用液液萃取進行樣品處理時, 目標物的回收率為80%~120%。因此, 本實驗選擇液液萃取對樣品進行處理。
2.2 提取溶劑的優化
2.2.1 提取溶劑種類的優化分別考察了乙腈、甲醇和二氯甲烷3種提取溶劑對樣品中6種目標物(空白樣品中加入低聚物標準溶液)提取效率的影響。由圖2可知, 甲醇為提取溶劑時, 6種目標物的回收率較低, 均在80%以下;二氯甲烷作為提取溶劑時, PET環狀二聚體和PBT環狀二聚體的回收率仍然低于80%。而乙腈作為提取溶劑時, 6種目標物的回收率均在80%~120%之間。因此, 采用乙腈作為PET和PBT環狀低聚物的提取溶劑。
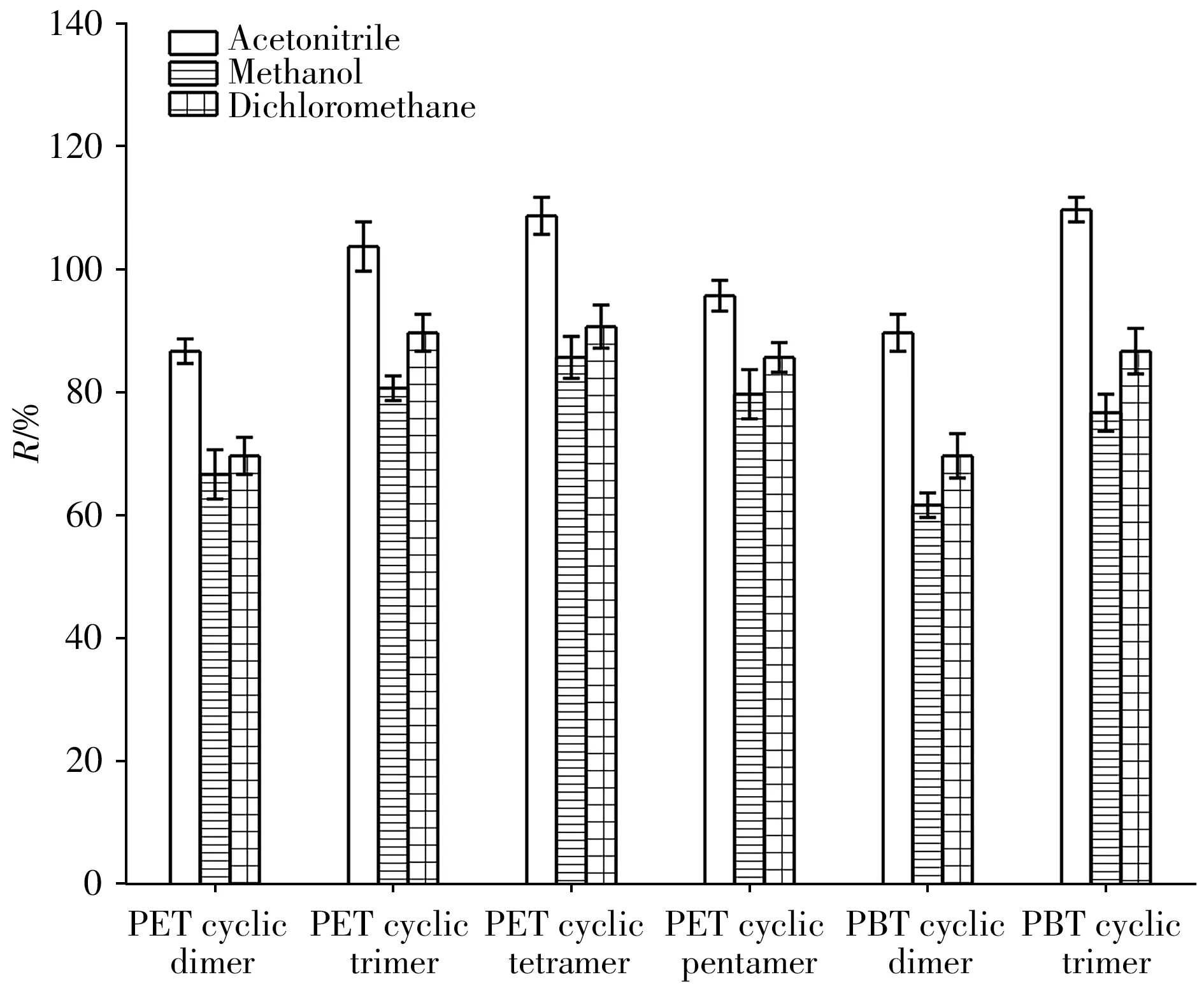
圖2 3種提取溶劑對目標物回收率的影響Fig. 2 The effect of three extraction solvents on the recovery of the target compounds
2.2.2 提取溶劑體積的優化提取溶劑體積也是影響目標物提取效率的一個重要因素, 本實驗對提取溶劑體積進行了優化。結果發現, 隨著提取溶劑體積的增加, 6種目標物的回收率均逐漸升高, 當提取溶劑體積大于6 mL時, 目標物的回收率趨于平緩。為了保證提取結果的穩定性, 本實驗選擇8 mL作為提取溶劑的體積。
實驗過程中發現渦旋后再對樣品進行超聲處理, 可以得到更好的提取效果。對于氮吹后使用的乙腈、甲醇和含0. 1%甲酸銨的乙腈溶液3種復溶溶劑進行考察, 結果表明, 當使用乙腈作為復溶溶劑時, 所得的溶解效果最好。因此, 本實驗選擇乙腈作為氮吹處理后的復溶溶劑。
2.3 線性范圍與檢出限
向3種食品中加入6種PET及PBT環狀低聚物的系列標準溶液, 在優化條件下進行測試, 以6種低聚物的質量濃度(X, μg/L)和峰面積(Y)繪制標準曲線。結果表明, 6種低聚物的線性范圍為10~1 000μg/L, 相關系數均大于0. 992, 表明本方法線性良好。
以未檢出低聚物的食品樣品為空白試樣進行提取試驗, 取不同濃度(低于限量0. 01μg/L)的溶液加標, 計算目標峰的信噪比(S/N)并進行驗證, 依據S/N≥3確定檢出限;S/N≥10確定定量下限。通過計算得到6種低聚物的檢出限為0. 11~44. 12μg/L, 定量下限為0. 36~147. 06μg/L。
2.4 相對標準偏差及回收率
按照本方法對水果罐頭、飲料和啤酒樣品進行50、100、200μg/L 3個水平的加標回收實驗, 平行測定6次, 計算回收率和相對標準偏差(RSD), 結果見表1。水果罐頭的平均加標回收率為80. 7%~103%, RSD為1. 3%~7. 2%;飲料樣品的平均加標回收率為80. 6%~119%, RSD為0. 40%~5. 5%;啤酒樣品的平均加標回收率為80. 8%~119%, RSD為0. 40%~9. 3%。結果表明方法的回收率和精密度良好, 滿足檢測要求, 可以準確測定覆膜鐵罐裝食品中PET及PBT環狀低聚物的遷移量。
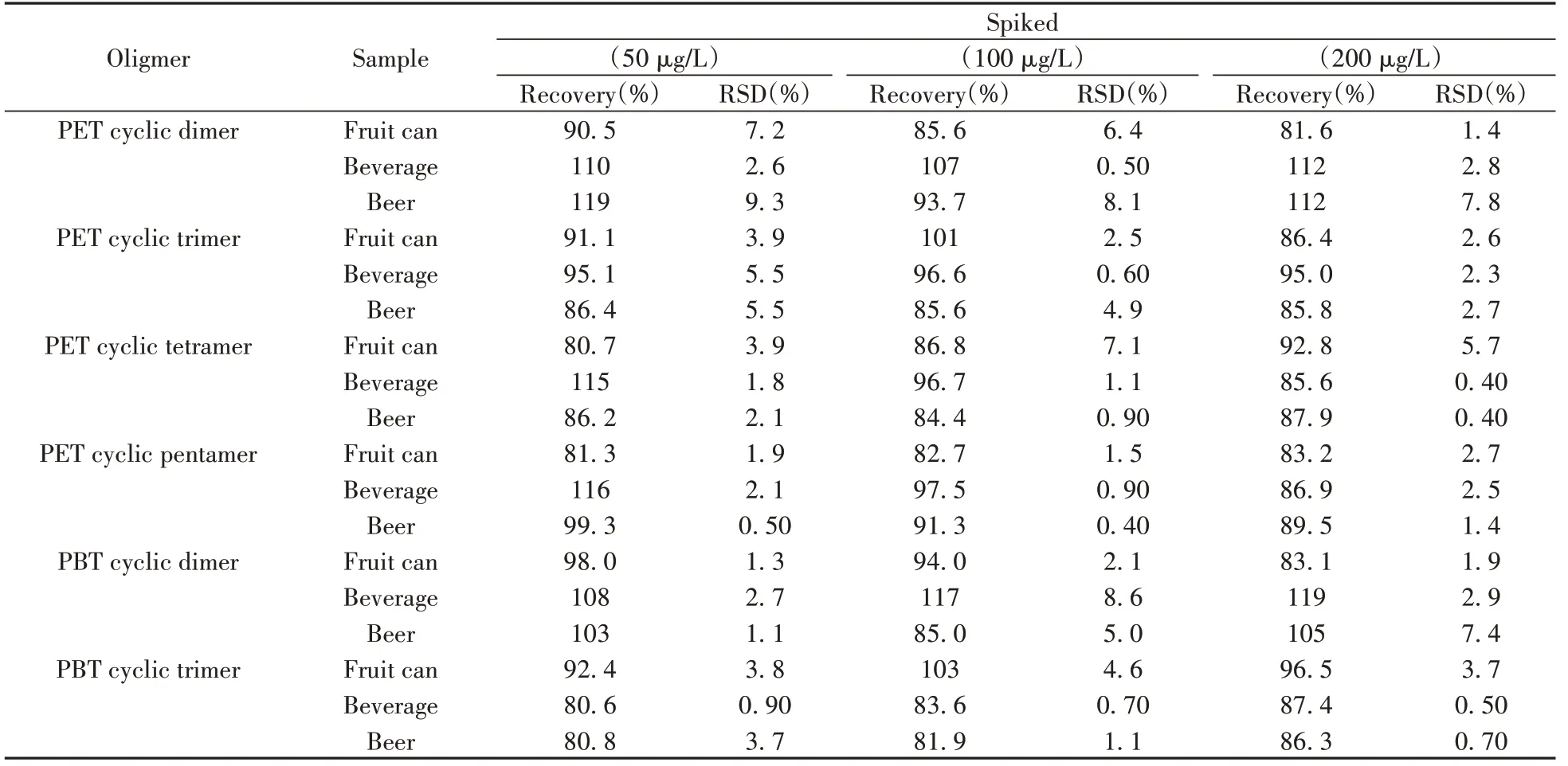
表1 水果罐頭、飲料和啤酒3種食品類型中目標物的平均加標回收率和相對標準偏差Table 1 The average recoveries and relative standard deviations of target substances in fruits cans, beverages and beer
2.5 實際樣品遷移測試
利用建立的方法對3類不同食品類別的覆膜金屬罐中可能遷移的PET和PBT環狀低聚物進行分析。由表2可知, 接觸飲料食品的覆膜金屬罐中PET和PBT環狀低聚物的遷移量明顯高于其他兩類食品, 其中PET環狀三聚體的平均遷移量高達35. 91μg/dm2, 其次為PBT環狀二聚體, 平均值為17. 34μg/dm2;接觸啤酒的覆膜金屬罐中PET環狀二聚體的遷移量整體偏低, 其平均值為0. 012~1. 61μg/dm2。通過對樣品測試可知, 飲料的pH值<水果罐頭的pH值<啤酒的pH值, 飲料的酸性最強。因此, 可能導致接觸飲料食品的覆膜金屬罐中PET和PBT環狀低聚物在酸性環境下的遷移量升高。
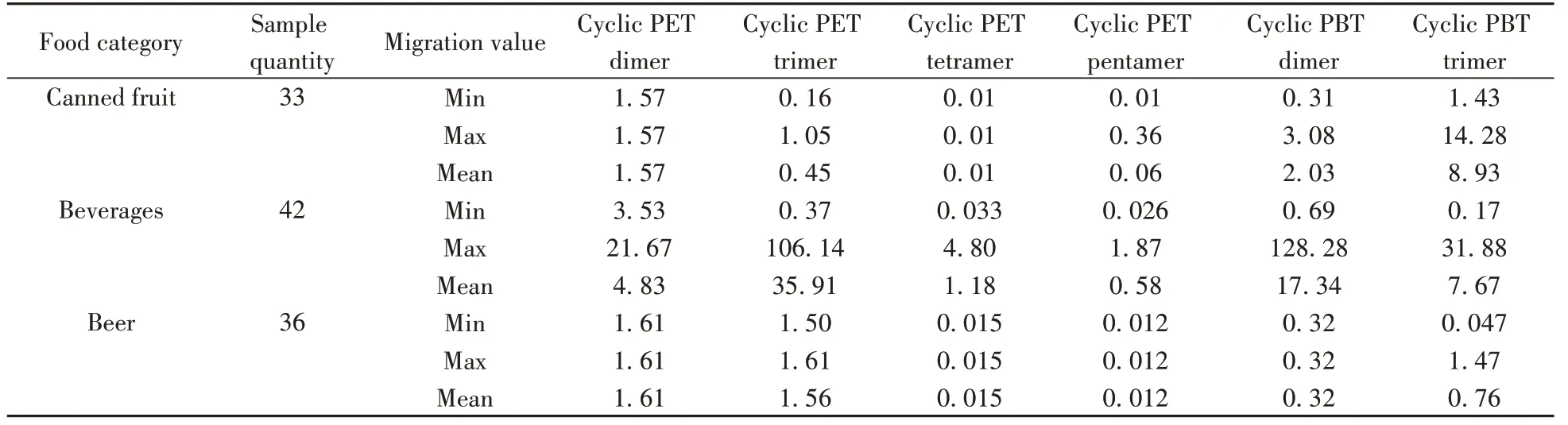
表2 不同食品類別的覆膜金屬罐中物質的遷移量Table 2 Migration results of substances in polymer-laminated metal cans of different food categories (μg/dm2)
2.6 TTC安全評估
由PBT和PET環狀低聚物的結構可知, 其不含具有水解、還原、增強毒性的功能基團, 而含有氧原子的芳香雜環。根據Toxtree評估結果, PBT和PET低聚物的結構均為CramerⅢ類, 可能會有毒性或活性功能基團, 閾值為1. 5μg/kg·BW/d。
根據食物平均攝入量(水果罐頭、飲料和啤酒分別為0. 006 5、0. 005 3、0. 014 kg·BW/d)、遷移量(表2)和平均S/V(表3)調查結果, 按“1. 4”中的公式計算與不同類別食品接觸的覆膜金屬罐中PBT和PET環狀低聚物的膳食暴露量(μg/kg·BW/d)。由表4可知, 接觸飲料食品的覆膜金屬罐中的PET環狀三聚體的膳食暴露量最大, 為1. 234μg/kg·BW/d;接觸水果罐頭食品的覆膜金屬罐中的PET環狀四聚體和接觸啤酒食品的覆膜金屬罐中的PET環狀五聚體的膳食暴露量最小, 為0. 001μg/kg·BW/d。3類食品接觸的覆膜金屬罐中PBT和PET環狀低聚物的膳食暴露量均低于TTC閾值。因此, 普通人群通過攝入覆膜金屬罐包裝的上述3類食品暴露于PBT和PET環狀低聚物所引起的健康風險較低, 不需要引起健康關注。
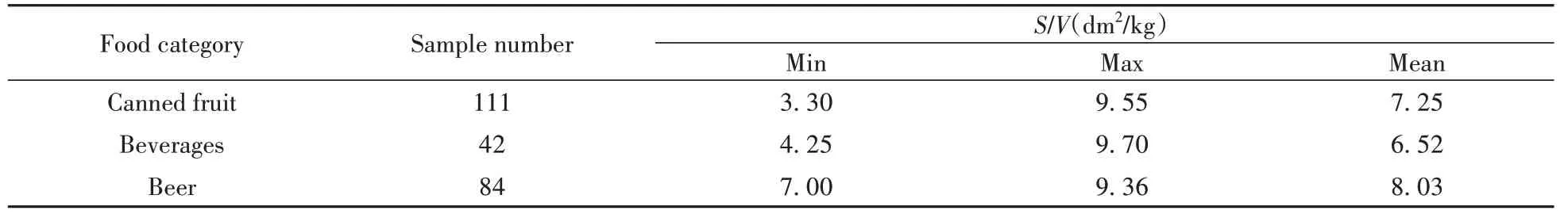
表3 不同類別食品接觸覆膜金屬罐材質時的S/VTable 3 S/V of different types of food contacted with polymer-laminated metal cans materials
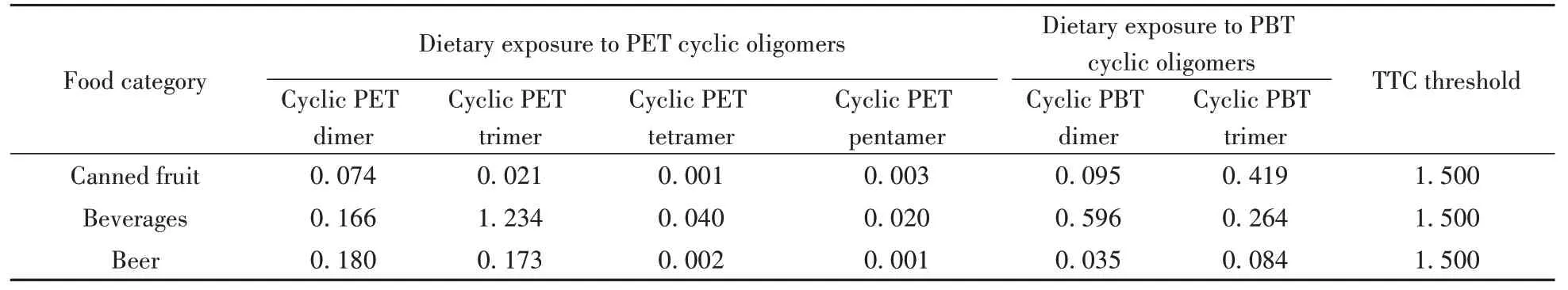
表4 普通人群對PBT和PET環狀低聚物的膳食暴露量Table 4 General population dietary exposure to PBT and PET cyclic oligomers (μg/kg·BW/d)
由于本研究膳食攝入量調查中的調查對象、調查區域未能覆蓋全國居民的食物消費情況;此外, 市場上覆膜金屬罐包裝的食品不斷變化, S/V調查未能涵蓋市場上所有類別的食品。因此, 本次評估所用的膳食攝入量數據和S/V數據可能會影響風險評估結果的準確性, 有待通過擴大調查范圍進一步改進。
3 結 論
本研究建立了一種UPLC-QTOF MS測定覆膜金屬罐包裝食品中PET和PBT環狀低聚物遷移量的方法, 基于我國食物消費量調查和S/V的調查, 采用TTC決策樹方法, 首次對水果罐頭、飲料和啤酒3類食品覆膜金屬罐中可能遷移出的PBT和PET環狀低聚物開展風險評估。評估結果表明, 我國普通人群通過攝入覆膜金屬罐包裝的上述3類食品暴露于PBT和PET環狀低聚物的風險處于可接受水平。該方法快速高效, 在食品接觸材料、食用香料等的風險評估方面擁有廣闊的應用前景。

