基于LncRNA表達的胃癌病人術后早期復發風險預測模型構建分析
彭啟旺 鄧浩 李威
胃癌起病隱匿,多數病人確診時已處于中晚期[1-2]。晚期胃癌常出現侵襲或轉移,即使行胃癌根治性切除術,也存在較高死亡風險[3]。早期識別胃癌術后早期復發的高風險病人并制定個性化治療方案,對延長病人的生存時間具重要意義。長鏈非編碼RNA(Long non-coding RNA,LncRNA)與胰腺癌、非小細胞肺癌等惡性腫瘤相關[4]。LncRNA通過調控染色體結構、基因轉錄、蛋白質翻譯、蛋白質活性等等過程參與腫瘤的進展[5]。有研究表明,胃癌LncRNA通過募集 WDR5/KAT2A 復合物作為胃癌“支架”刺激腫瘤發生和轉移[6],LncRNAs的異常表達可能間接反映胃癌的發生發展。基因通常不會單獨作用,因此有必要選擇合適的LncRNA并建立多LncRNA預測模型,為評估胃癌早期復發提供指導。本研究分析胃癌病人術后早期復發相關LncRNA,構建基于LncRNA表達的胃癌病人術后早期復發的預測模型。
對象與方法
一、對象
2016年6月~2019年1月我院行胃癌切除術的病人121例。納入標準:(1)病理檢查確診胃癌并行胃切除術和D2淋巴結清掃術[7];(2)病人未進行術前化療或放療;(3)腫瘤分化為中、高分化;(4)病人或其家屬知曉本研究并簽署知情同意書。排除標準:合并其他部位惡性腫瘤;合并嚴重基礎疾病,如心肺功能不全等;TNM分期≥Ⅲ期。剔除標準:術后半年內死亡;個人原因不能配合全程隨訪。本研究經過醫學倫理委員會審查。
二、方法
1.LncRNA 表達檢測:采用實時逆轉錄聚合酶鏈反應檢測。逆轉錄試劑盒購于美國Invit rogen公司,胎牛血清購于美國Gibco公司,TB Green Premix Ex TaqTM Ⅱ 及PrimeScriptTM RT Master Mix購于日本Takara公司,LipofectamineTM 2000 轉染試劑盒購于美國 Invitrogen 公司。
2.資料收集:收集病人一般資料,包括年齡、性別、淋巴結轉移情況,疾病分期、腫瘤最大徑、腫瘤位置,術后化療情況等。
3.隨訪:隨訪病人復發情況。通過組織病理學檢查確認病人是否復發。術后隨訪2年,共失訪21例,最終納入100例病人,其中31例病人出現復發為復發組,69例未復發的病人為未復發組。兩組病人年齡、性別、臨床特征等比較差異無統計學意義(P>0.05)。見表1。

表1 兩組病人臨床資料分析
三、統計分析和數據預處理
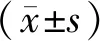
結果
1.異基因篩選及胃癌病人術后早期復發的風險因素分析:在胃癌術后病人中,edgeR 共篩選出992個DEL,其中772個上調,220個下調,單變量分析顯示,復發組與未復發組63 個 LncRNA 表達存在差異;Lasso-COX 回歸模型分析顯示,22個 LncRNA 是胃癌病人術后早期復發的風險因素;將22個 LncRNA 進一步納入多變量 COX 回歸分析中顯示,AC007991.4、AC079385.3和AL109615.2是胃癌病人術后早期復發的強風險因素,見圖1、2、3。

圖1 紅色表示上調的 LncRNA;綠色表示下調的 LncRNA
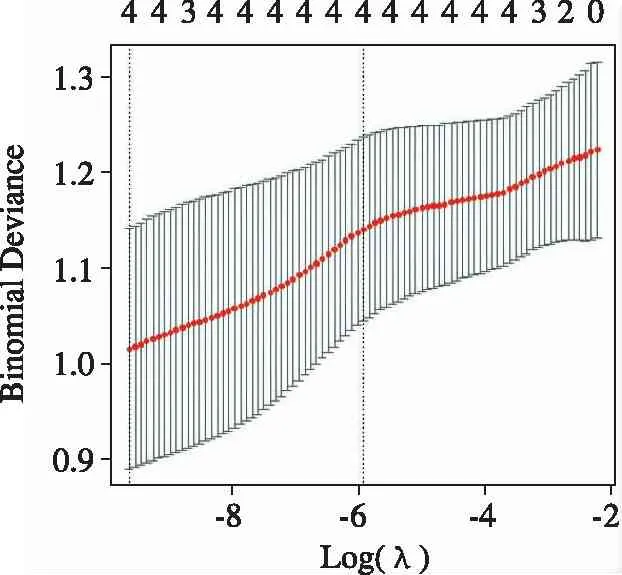
圖2 通過十倍交叉驗證法調節參數λ將模型中二項式偏差降到最小后篩選出的效能較好的特征集合

圖3 森林圖顯示AC007991.4、AC079385.3和AL109615.2是胃癌病人術后早期復發的風險因素
2.驗證集預測模型分析:繪制ROC曲線,AC007991.4、AC079385.3、AL109615.2及三者聯合預測胃癌病人術后早期復發的效能均較高,見圖4、表2。
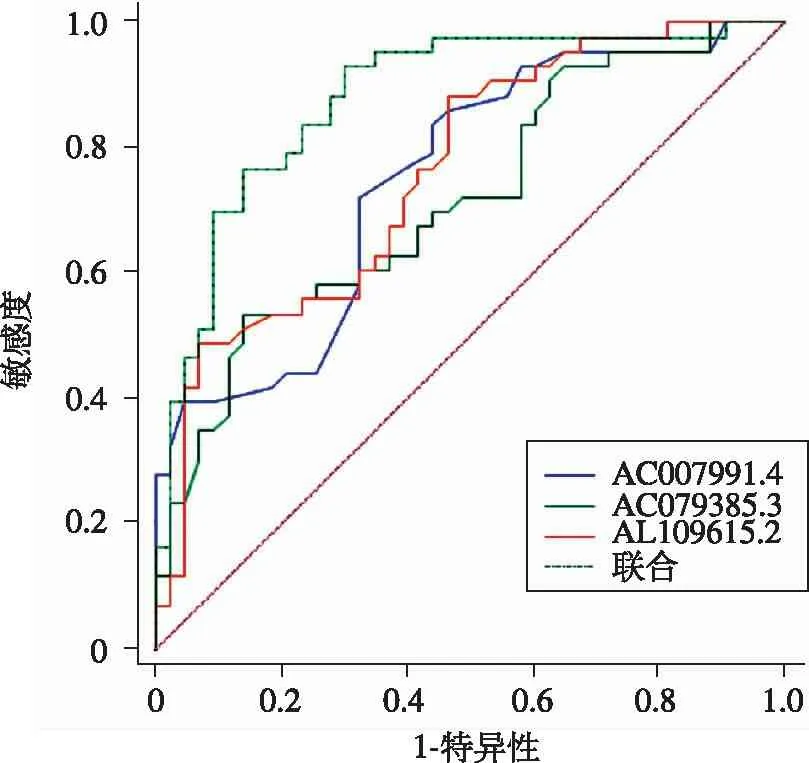
圖4 胃癌術后早期復發的ROC曲線

表2 預測模型ROC曲線參數
討論
胃癌早期癥狀不明顯,多數病人在確診時已是晚期,5年總體生存率低于25%[8]。開發一種可應用于臨床風險評估的預后分層系統,對于胃癌病人的治療和隨訪具有重要意義。LncRNA 是一類與基因表達調控功能相關的分子[9]。隨著LncRNA功能研究深入,越來越多的證據表明部分LncRNA在胃癌中異常表達并參與癌癥進展調控。Li等[10]研究發現,MAFG-AS1促進胃癌細胞增殖和侵襲,可能是一種有價值的預后生物標志物;Cai等[11]研究表明,LncRNA pcsk2-2可作為胃癌診斷的生物標志物。然而,這些研究僅討論了單一生物標志物的預測價值,但基因通常不會單獨作用。因此,需要選擇合適的LncRNA并建立多LncRNA預測模型。本研究納入121例病人,評估LncRNAs的表達與胃癌病人術后復發間的相關性。
本研究通過TCGA 獲得的RNA-seq數據顯示,在胃癌病人中共篩選出992個DEL,其中772個上調,220個下調;其中共63個LncRNA與胃癌病人術后早期復發的風險相關;Lasso-COX回歸及多變量COX進一步分析顯示,AC007991.4、AC079385.3和AL109615.2是胃癌病人術后早期復發的獨立風險因素,繪制ROC曲線顯示其預測效能較高,可用于臨床胃癌病人術后早期復發的早期預測。有研究認為,LncRNA在胃癌中異常表達,且其功能復雜。作為“支架”,可刺激蛋白質之間的相互作用[12];作為“向導”,LncRNA 能夠實現蛋白質和基因的混合[13];作為“增強子”,LncRNA 控制基因的轉錄,作為“誘餌”,LncRNA 與 microRNA 或蛋白質結合參與癌癥進展調控[14]。AC007991.4、AC079385.3和AL109615.2三種LncRNA在胃癌組織和細胞中的表達,AC007991.4在胃癌中弱表達,AC079385.3和AL109615.2都是潛在的onco-LncRNA。其中AC007991.4和AC079385.3都是反義LncRNA,位于8號染色體:39918076-39920890和12號染色體:106714924-106733066。目前關于AC007991.4和AC079385.3的分子功尚無完全明了。AL109615.2作為一種長基因間非編碼RNA,位于6號染色體:44058792-44089288,可競爭性結合miR-133b與血管內皮生長因子C誘導結直腸癌細胞轉移[15]。同時,在本研究中,為提高模型的預測準確性,以P<0.05和|logFC|≥1.5作為獲得DEL的截止點,應用Lasso和COX回歸分析來分析LncRNA的表達與胃癌病人術后復發的相關性。與以往研究相比,本研究有效地最小化了由單變量COX回歸引起的過擬合。與傳統模型相比,Lasso回歸評估過程包括與回歸嶺的關系、最佳子集選擇、套索系數估計之間的聯系和軟閾值,通過變量選擇和正則化提高了預測精度和可解釋性。
綜上所述,AC007991.4、AC079385.3和AL109615.2是影響胃癌術后病人早期復發的因素,構建風險預測模型,可以指導重點人群檢測,盡可能延長病人生存時間。本研究的不足之處在于納入的樣本量較少,且僅為我院胃癌病人,而基因表達常具人種差異,因此普遍性受限。隨訪時間為2年,隨訪時間較短,研究結果可能存在偏倚。后期需擴大樣本納入范圍,延長隨訪時間。

