慢性阻塞性肺疾病病人慢性支氣管炎和肺氣腫表型轉錄組學數據的生物信息學分析
高麗娟,秦江月,徐 丹,申永春,陳 梅,陳 磊,文富強
1.四川大學華西醫院 呼吸與危重癥醫學科/生物治療國家重點實驗室呼吸病學研究室(成都610041);2.成都市第五人民醫院 呼吸與危重癥醫學科(成都 611130)
慢性阻塞性肺疾病(簡稱慢阻肺)是一種以持續存在的呼吸系統癥狀以及不完全可逆的氣流受限為特征的常見慢性呼吸系統疾病,目前慢阻肺是全球排名前三位致死原因的疾病之一[1-2]。慢性支氣管炎(簡稱慢支炎)和肺氣腫是慢阻肺兩個經典臨床表型[3]。慢阻肺病人的慢支炎表型通常定義為每年慢性咳嗽、咳痰大于或等于3 個月,至少連續兩年。慢支炎病理特征包括持續氣道炎癥,氣道粘液高分泌[4],氣道重塑及狹窄[5-6]。慢阻肺病人的肺氣腫則是由于肺實質的破壞,隨后終末細支氣管遠端的氣道彈性下降,導致肺過度膨脹引起的[7-9]。慢支炎和肺氣腫病人的臨床癥狀和治療反應存在明顯差異。與慢支炎病人相比,肺氣腫病人肺功能更差,呼吸困難癥狀更嚴重[10-11]。并且以肺氣腫為主的慢阻肺病人對吸入性糖皮質激素和長效β受體激動劑的治療反應欠佳,對于肺功能和呼吸困難的改善有限[12]。以上研究提示,慢支炎和肺氣腫病人的發病機制可能并不完全相同。然而目前關于慢阻肺病人慢支炎表型和肺氣腫表型的發生發展機制尚未完全闡明。而深入探索慢阻肺病人不同臨床表型發病的分子機制,對于慢阻肺病人的精準治療具有重要的臨床意義。因此,本研究將通過分析數據庫GSE69818中慢阻肺病人的肺組織轉錄組信息,探究慢支炎表型和肺氣腫表型發生發展過程中可能的關鍵基因和信號通路。
1 資料與方法
1.1 資料來源
基因表達數據庫(Gene Expression Omnibus,GEO)http://www.ncbi.nlm.nih.gov/geo是目前最完善的公共基因表達數據儲存庫,我們從中下載轉錄組數據GSE69818,數據是基于Affymetrix Human Genome U219 Array所獲得的人轉錄組生物信息。GSE69818包含70個慢阻肺病人肺組織樣本,其中包括38例肺氣腫表型和32例慢支炎表型病人[13-16]。
1.2 獲取差異表達基因
利用R 語言的Rank Pord 軟件包分析慢支炎表型和肺氣腫表型的差異表達基因,認為P<0.05為表達差異具有統計學意義。
1.3 差異表達基因的基因本體及通路富集分析
對篩選出的差異表達基因,利用DAVID(http://david.abcc,ncifcrf.gov)在線分析軟件進行基因本體(gene oncology,GO)分析以及京都基因與基因組百科全書(kyoto encyclopedia of genes and genomes,KEGG)通路富集分析。P及錯誤發現率(false discovery rate,FDR)均小于0.05即視為具有統計學意義。
1.4 差異表達基因的蛋白相互作用網絡圖
STRING 數據庫(http://http://www.string-db.org/)是一個包含多種蛋白質互作關系的數據庫。對差異基因編碼的蛋白利用STRING進行蛋白-蛋白相互作用網絡分析。并將結果導入Cytoscape 軟件導出編碼蛋白互作用網絡圖(PPI)。
2 結果
2.1 差異表達基因分析
比較肺氣腫組和慢支炎組,篩選得到3 734個差異表達基因,其中肺氣腫組表達下調的基因2 073 個,表達上調的基因1 661個(見表1)。用差異基因繪制熱圖(見圖1),與慢支炎組相比,紅色表示上調基因,綠色表示下調基因。火山圖則直接反映出差異基因的表達情況,如圖1 所示,肺氣腫組的基因大部分下調,這與下調的基因數的結果相符。
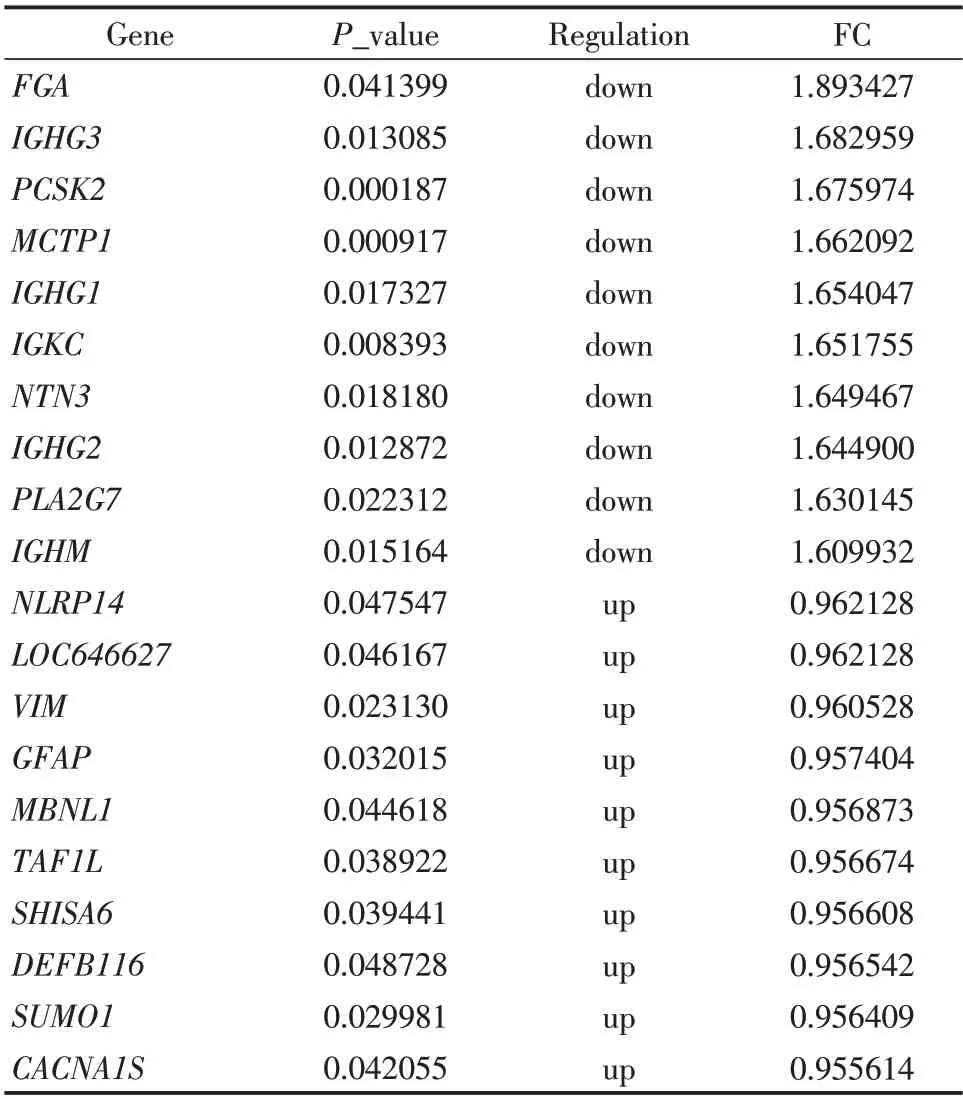
表1 前10名上調及下調差異表達基因Table1 The top 10 up-regulated and down-regulated mRNAs
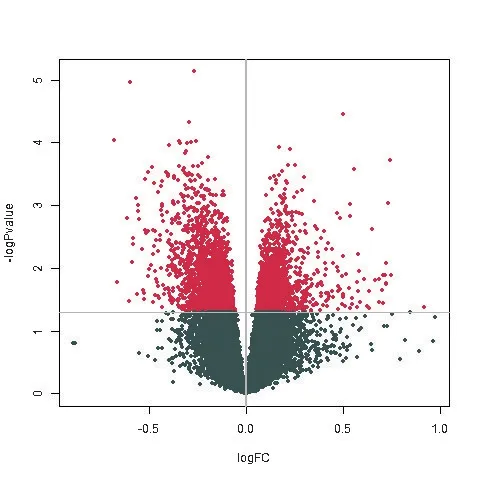
圖1 差異基因的火山圖Figure 1 The volcanic map of DEGs
2.2 差異表達基因的GO分析
將篩選出的差異表達基因利用DAVID 進行GO 分析。GO分析獲得了生物過程、分子功能、細胞組成3個部分的結果。其中在生物學過程中,差異基因主要涉及生物行為、生物黏附和生物相,分子功能中主要富集到抗氧化活性和催化活性,細胞組成主要包括細胞連接、細胞外區域和大分子絡合物(見圖2)。其中在生物學過程中,上調基因主要涉及表皮的發育、運動節律和嘌呤堿基轉運,分子功能主要涉及抗原結合、B細胞分化、和堿性磷酸酶活性,細胞組成主要包括T細胞受體復合體、高密度脂蛋白粒子和ABC 轉運體復合物。而對于下調的差異基因,在生物學過程中主要富集于無損側枝發芽、軸突中線選擇點識別和平滑內質網鈣離子穩態。分子功能主要涉及肽酶激活活動、膠原蛋白綁定和細胞骨架蛋白綁定。細胞組成主要包括基底膜、血小板α顆粒腔和頂體內膜。
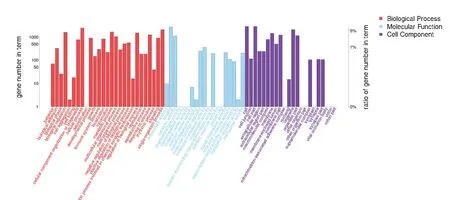
圖2 差異基因本體分析Figure 2 GO analysis
2.3 差異表達基因的KEGG分析
根據KEGG 分析結果,差異基因主要富集到流體剪切應力,動脈粥樣硬化,小細胞肺癌和ECM 受體連接(見圖3)。差異表達基因中上調部分主要富集于甘油磷脂代謝、原發性免疫缺陷、甘油酸代謝,而下調部分主要涉及細菌侵襲上皮細胞、細胞外基質(ECM)-受體相互作用和cGMP-PKG信號通路。
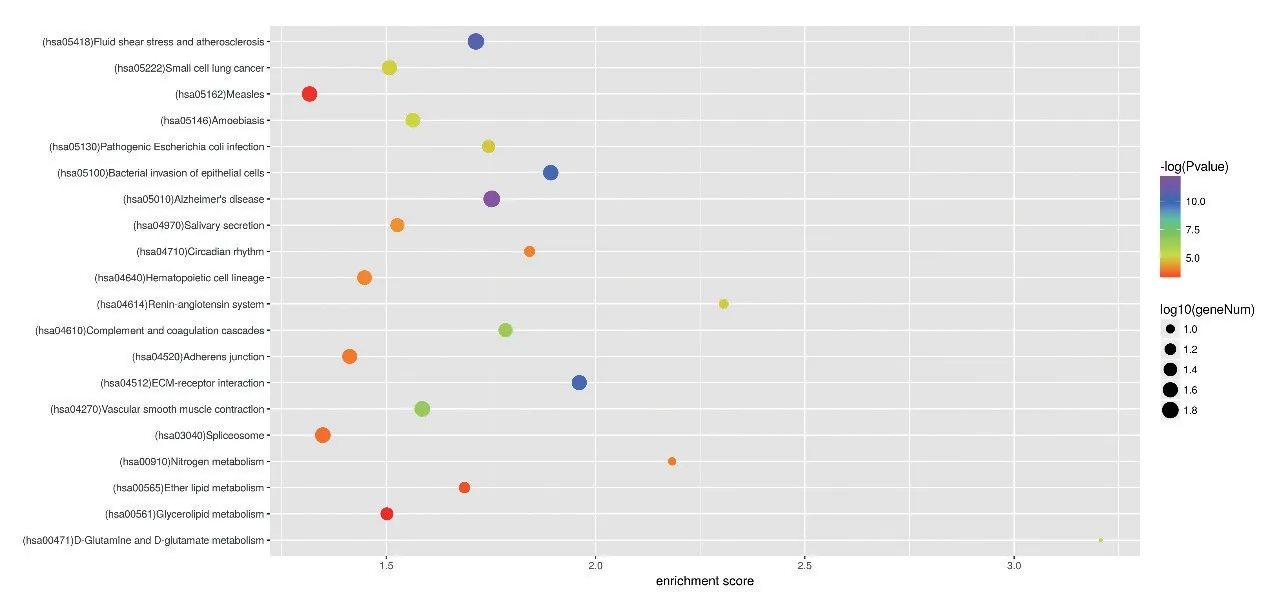
圖3 差異基因KEGG信號通路富集分析Figure 3 KEGG analysis
2.4 差異表達基因的蛋白相互作用網絡圖
選擇P小于0.01差異表達基因構建蛋白互作用網絡圖,其中包含738 個節點,通過Cyoscape 軟件篩選出排名前10的關鍵基因,包括ACTB、ITGB1、RHOA、FN1、SRSF1、CAV1、CTNNA1、VEGFA、HNRNPA1、APP(見圖4),其中有9 個下調基因(APP、ITGB1、FN1、RHOA、CAV1、CTNNA1、VEGFA、HNRNPA1、SRSF1),1 個上調基因(ACTB)。
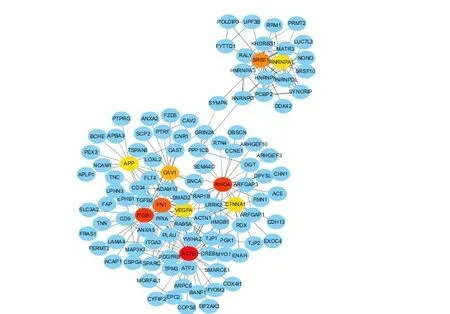
圖4 差異表達基因的蛋白互作網絡圖Figure 4 PPI analysis
3 討論
慢阻肺是一種慢性進行性疾病,而慢支炎和肺氣腫是其重要臨床表型,不同臨床表型的慢阻肺病人對治療反應以及臨床結局存在明顯差異。近年來,轉錄組學技術被廣泛應用于研究疾病的遺傳信息改變[17-18],進而了解疾病發生的分子機制。本研究表明,肺氣腫和慢支炎表型病人的肺組織在轉錄組水平上存在顯著差異。通過深入分析慢支炎和肺氣腫表型病人肺組織的轉錄組學數據,有助于探索不同表型慢阻肺的分子機制的異質性,為其精準治療提供新思路。
本研究通過Rank Pord軟件包對GSE69818轉錄組數據進行分析,獲得慢支炎表型和肺氣腫表型慢阻肺病人肺組織差異表達的3 734 個基因,其中1 661 個上調基因,2 073 個下調基因。根據PPI 結果,篩選出10個關鍵基因,包括ACTB、ITGB1、RHOA、FN1、SRSF1、CAV1、CTNNA1、VEGFA、HNRNPA1、APP(圖4)。大量研究表明FN1編碼的纖連蛋白作為肺基質結構的重要組成成分,在慢阻肺小氣道重塑中發揮著重要作用[19-20]。同時,篩選出的關鍵基因ITGB1可以編碼蛋白質整合素β1,而整合素β1在肺發育過程中參與調節分支形態形成和肺泡形成[21]。并且有研究報道ITGB1基因突變小鼠肺組織在老年階段表現出慢阻肺樣改變,包括肺氣腫改變、淋巴結增生和巨噬細胞浸潤增加[22],提示ITGB1可能與慢阻肺肺氣腫的發生發展密切相關,但具體機制尚不完全清楚。同時,本研究篩選出的關鍵基因CAV1的編碼蛋白是細胞質膜結構成分之一,有報道發現CAV1敲低后,香煙煙霧刺激誘導的肺上皮細胞的細胞凋亡明顯增加,此外,慢性香煙煙霧暴露后,CAV1基因敲除小鼠肺組織的細胞自噬和凋亡水平顯著增加,肺氣腫改變更明顯[23],提示CAV1可能參與調控香煙誘導的肺氣腫發生發展。但是,這些基因參與慢阻肺病人肺氣腫表型的具體致病機制仍需進一步研究。
通過GO富集分析,我們發現差異基因富集于B細胞分化等免疫反應、內質網鈣離子穩態等生物過程。有報道提出吸煙慢阻肺病人肺組織中記憶B細胞水平顯著增加,并可能與抗原特異性免疫反應相關[24]。同時ROCA 等[14]報道指出在慢阻肺合并肺氣腫病人肺組織中存在B 細胞相關基因的富集,而在慢支炎病人中卻并沒有相關基因富集。因此,B細胞相關免疫反應可能與慢阻肺肺氣腫表型的發展密切相關,但是其相關的分子機制仍需進一步研究。同時,有研究證實病毒刺激可以誘導支氣管細胞中內質網內鈣離子減少,從而擾亂細胞內鈣穩態,而細胞內鈣離子流量變化可以觸發NLRP3等炎癥小體激活以及炎癥因子IL-1β的分泌[25],IL-1β則在慢阻肺的氣道炎癥發展過程中起著重要作用,這提示本研究內質網鈣離子穩態可能參與慢阻肺慢支炎表型的發生發展,但暫無相關研究報道其中具體機制。因此,本研究篩選到的相關生物學過程可以為今后更進一步研究慢阻肺不同臨床表型的發病機制提供了新的可能和方向。
通過KEGG 路徑富集分析,本研究發現在慢支炎表型中上調的基因富集到了細胞外基質(ECM)-受體相互作用和cGMP-PKG 信號通路。以往的研究表明,異常的ECM 沉積可以驅動氣道炎癥、修復、細胞遷移和增殖,也是慢阻肺小氣道重塑的關鍵結構改變[26-28]。本研究發現FN1、COL4A1、COL4A2、COL6A3等基因均富集在了ECM 信號通路。其中COL4A1、COL4A2和FN1編碼蛋白都是ECM 的重要組成部分[29-30]。同時FRANCIS 等[31]研究發現COL6A3 參與細胞外基質(ECM)的錨定和重塑。而本研究篩選出的關鍵基因SRSF1則是富含精氨酸/絲氨酸的剪接因子蛋白家族的成員,它們與ECM 組裝有著密切的關系[32]。SUN 等[33]發現沉默SRSF1 可以抑制TGF-β1 誘導的人胎肺成纖維細胞增殖、分化和ECM沉積。以上參與調控ECM重塑的基因在慢支炎表型病人肺組織中上調,表明氣道和肺實質中ECM 異常沉積可能參與影響慢支炎表型病人的氣道重塑,但具體機制目前尚未完全闡述清楚。此外,有研究指出在肺部炎癥病人的支氣管上皮細胞中,cGMP-PKG通路顯著下調[35],提示cGMP-PKG通路可能影響肺部炎癥的發生,但其是否參與慢阻肺病人慢支炎的調控目前尚不清楚。因此,需要更多的研究探索慢阻肺病人慢支炎和肺氣腫表型的具體分子機制。
4 結論與啟示
本研究通過對GEO數據庫中慢阻肺病人慢支炎和肺氣腫表型肺組織的基因芯片數據進行深入挖掘與生物信息學分析,初步明確了調控慢阻肺病人慢支炎表型和肺氣腫表型的可能關鍵基因及相關通路,為慢阻肺的精準診治提供了潛在靶點,但后續還需要開展進一步的基礎與臨床研究,以探索慢阻肺病人的發病機制與臨床治療靶點。
(利益沖突:無)

