基于網絡藥理學、分子對接及大鼠實驗的黃芪-冬蟲夏草藥對治療IgA腎病作用機制研究
傅 奕,陳幫明,李 鑫,付 義,伍宏澤,劉永芳
1江西省中醫腎病臨床醫學研究中心九江市中醫院,九江 332000;2湖南中醫藥大學;3湖南中醫藥大學中醫診斷學湖南省重點實驗室;4湖南中醫藥大學中醫心肺病證辨證與藥膳食療湖南省重點研究室,長沙 410208
IgA腎病(IgA nephropathy,IgAN)是一種自身免疫性疾病,以免疫復合物IgA沉積在腎小球系膜區為特征,常伴內皮增生和足細胞損傷。在我國發病率高,約占原發性腎小球腎損害的32%~54%,約40%患者將在病程20年左右進入終末期腎病[1,2]。目前治療主要是控制血壓、降尿蛋白、激素及免疫抑制劑等,雖然可延緩疾病進展,但相關藥物不良反應也限制了療效[3]。因此,積極探索IgAN的理想治療藥物,保護腎臟功能,已成為亟待解決的臨床問題。
中醫藥治療IgAN歷史悠久,可提高療效、保護腎功能[4],但目前的研究角度尚單一,未能系統論證中醫藥治療IgAN的機制。陳幫明教授為江西省中醫腎病臨床醫學研究中心學科帶頭人,省級名中醫,集采眾家之長,認為正虛伏邪擾腎為本病病機[5]。針對正虛,擅用黃芪-冬蟲夏草藥對補益肺脾腎。黃芪甘溫,培補腎氣、健脾消腫,具有調節免疫、降低尿蛋白、保護腎功能等作用,可通過上調肝細胞生長因子(HGF)和下調轉化生長因子-β1(TGF-β1)而抑制腎纖維化,提高IgAN外周血B淋巴細胞和降低糖基化水平[6,7]。冬蟲夏草味甘性平,補益肺腎,可抑制VEGF及IgA系膜細胞增生,修復腎臟損傷[8,9];現代研究證實兩藥均有調節免疫、抑制系膜增生的功效,聯用可協同增效。故本文基于網絡方法的藥物作用機制發現策略,旨在從系統角度和分子水平發現研究付義主任黃芪-冬蟲夏草藥對的作用機制,與中醫學整體觀念和辨證論治原則具有異曲同工之妙,因此,運用網絡藥理學技術可預測黃芪-冬蟲夏草藥對治療IgAN的多成分-多靶點-多疾病的整合機制,同時為將來的實驗驗證提供方向。
1 材料與方法
1.1 實驗材料
黃芪-蟲草藥對由黃芪20g、冬蟲夏草10g組成,中藥飲片均購于江西中醫藥大學附屬九江市中醫院中藥房。本院制劑室根據人臨床等效劑量水煎濃縮為0.72 g/mL,置于無菌棕色瓶,4 ℃冰箱保存備用。牛血清白蛋白(BSA,美國Sigma-Aldrich公司,批號:20200823);脂多糖(LPS,美國Sigma-Aldrich公司,批號:20200815);四氯化碳(CCl4,上海阿拉丁生化科技股份供銷公司,批號:20200705);VEGFA(上海泛柯實業有限公司,批號20211205)。
選取SPF級雄性SD大鼠30只進行藥物血清制備,體質量180~220g,購于湖北省實驗動物研究中心,動物生產許可證號:SCXK(鄂)2020-0014。飼養于九江學院附屬醫院動物房,溫度21~25℃,相對濕度40%~70%,每日定時喂養,實驗動物倫理批號:LL20220304011。
1.2 黃芪-冬蟲夏草主要化學成分收集及篩選
應用TCMSP數據庫(http://lsp.nwu.edu.IgAN/tcmsp.php)及BATMAN-TCM數據庫(http://bionet.ncpsb.org/batman-tcm/)檢索所有活性成分。以口服生物利用度(oral bioavailability,OB)≥30%、類藥性(drug-likeness,DL)≥0.18為限制條件進行篩選,得到黃芪-冬蟲夏草生物活性成分。另外對未入選數據庫,但文獻報道有生物活性的化學成分也納入候選,建立藥物-化學成分數據集。
1.3 成分潛在靶點收集
應用TCMSP及BATMAN-TCM數據庫檢索黃芪-冬蟲夏草活性成分的靶基因,通過Cytoscape 3.7.2(https://cytoscape.org/)構建活性成分-靶點互作網絡。
1.4 IgAN疾病靶點篩選
設置檢索詞為“IgAN”,通過GeneCards數據庫(https://www.genecards.org/)及OMIM數據庫(https://www.omim.org/)進行檢索,篩選得到IgAN疾病靶點,并應用UniProt數據庫(https://www.uniprot.org/)篩選出人源靶點并進行標準化,獲得Swiss-Prot ID。
1.5 黃芪-冬蟲夏草活性成分與IgAN的共同靶點篩選及PPI網絡構建
明確IgAN相關靶點與黃芪-冬蟲夏草潛在靶點之間的相互作用,應用R語言(https://www.r-project.org/)軟件及Perl語言程序將疾病靶點與藥物靶點進行交集。應用STRING(https://string-db.org/)插件構建共同靶點互作網絡(protein-protein interaction,PPI)。應用count.R插件獲得共同蛋白靶點出現的頻次。
1.6 活性成分-IgAN-靶點互作網絡構建
應用Cytoscape 3.7.2軟件中merge功能構建活性成分-IgAN-靶點互作網絡。網絡圖中“node”代表活性成分和靶點,“edge”代表活性成分-IgAN-靶點之間的相互關系。查閱文獻,基于構建的網絡探討黃芪-冬蟲夏草治療IgAN的潛在機制。
1.7 GO生物功能分析和KEGG通路富集
應用R語言中Cluster Profiler GO.R插件及Perl語言對活性成分與IgAN共同靶點進行GO分析。應用Cluster Profiler KEGG.R插件進行KEGG通路分析。根據富集因子值分析核心通路富集程度,探究黃芪-冬蟲夏草治療IgAN的可能的生物功能及信號通路機制。
1.8 分子對接
采用AutoDock vina軟件對PPI網絡中度值最高的VEGFA與黃芪-冬蟲夏草5個主要成分進行分子對接。從RCSB PDB蛋白質結構數據庫和PubChem數據庫中分別獲得靶點蛋白的三維結構和主要成分的化學結構,采用AutoDock Tools對上述蛋白受體和配體進行常規處理,再用其插件Autogrid得到對接活性位點,進行分子對接,得到結合能(affinity)。
1.9 分組及給藥
實驗大鼠隨機分為空白組和模型組,模型組大鼠按改良的聯合免疫誘導法BSA+LPS+CCl4建立模型。具體方法:BSA,加蒸餾水配制成100 g/L濃度,按600 mg/kg隔日灌胃1次,持續12周;CCl4+蓖麻油,每只0.1 mL+0.3 mL,每周首日頸部皮下注射1次,持續12周;LPS按0.05 mg/只的量,于第6周和第8周首日尾靜脈各注射1次。空白組則采用同一時間、等體積的蒸餾水灌胃,蓖麻油(0.5 mL)皮下注射以及尾靜脈注射[10]。12周后,模型組大鼠腎臟病理免疫熒光提示腎小球IgA沉積[10]。造模成功大鼠隨機分為模型組和黃芪-冬蟲夏草藥對組,空白組、模型組按10 mL/kg給予蒸餾水灌胃;藥對組黃芪和蟲草配伍后用含0.1%羧甲基纖維素鈉的蒸餾水配制成生藥量為1.27 g/mL的溶液備用(根據黃芪與蟲草(2∶1)的劑量(黃芪20 g,蟲草10g),換算為動物給藥劑量配置)。每日1次,持續21日。
1.10 標本檢測
給藥第21天后分別收集大鼠24 h尿液,記錄尿量,并送醫院檢驗科檢測尿蛋白含量。治療結束后次日,安樂死大鼠,迅速暴露并分離出腎臟(在冰臺上操作),從腎門處剪下腎臟并快速剝離腎包膜,組織勻漿。送醫院檢驗科,采用酶聯免疫法按說明書測定腎組織VEGFA含量。
1.11 統計學處理
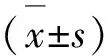
2 結果
2.1 黃芪-冬蟲夏草藥物有效成分挖掘
利用TCMSP數據庫對黃芪-冬蟲夏草藥對現有的成分進行挖掘,限定OB≥30%和DL≥0.18進行選取,去除重復成分后獲得27個有效成分(見表1)。
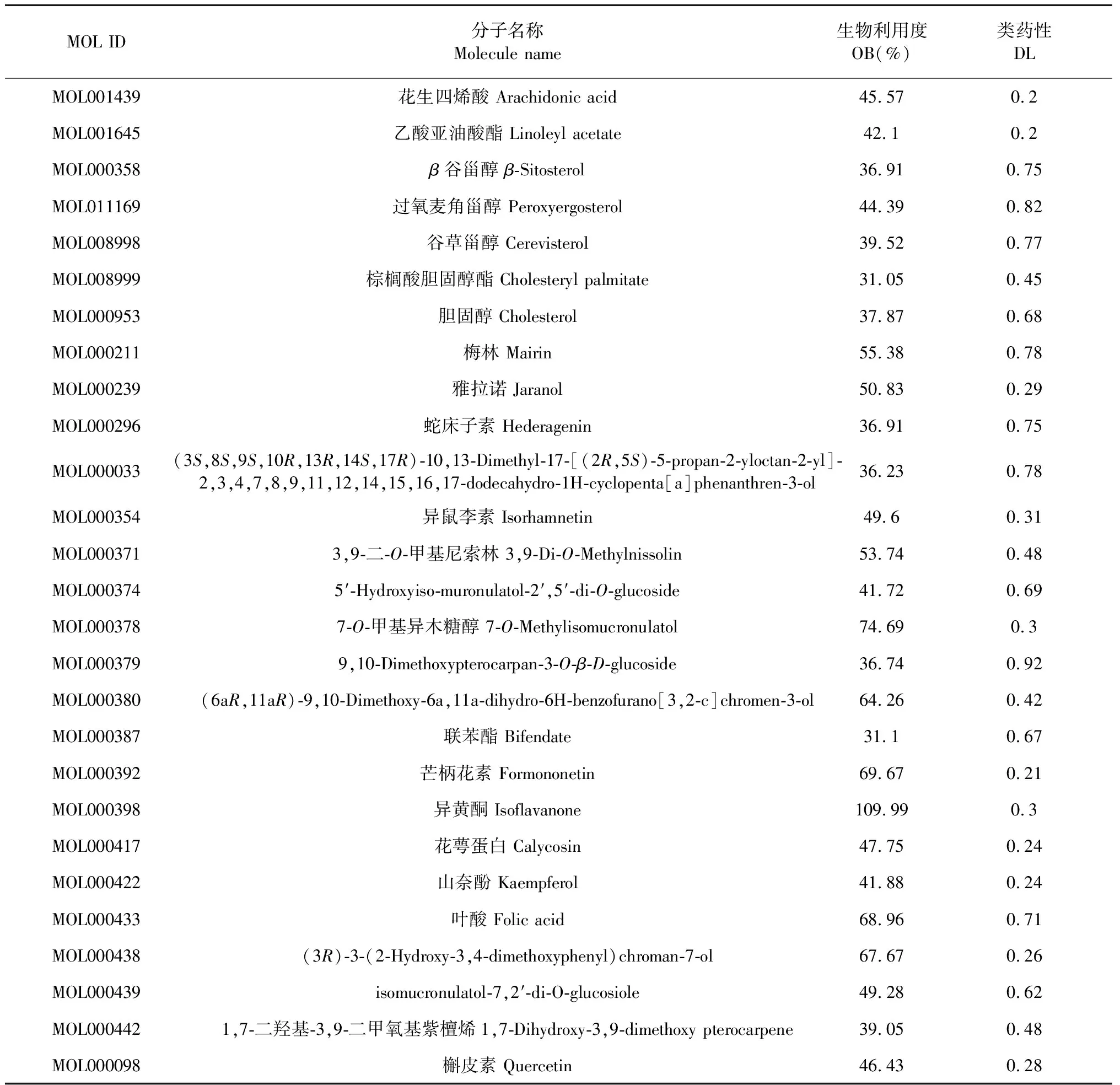
表1 黃芪-蟲草藥對活性成分
2.2 黃芪-冬蟲夏草的活性成分的收集和篩選
獲得27個生物活性成分,其作用靶點共109個(不含重復),其中排名靠前的主要成分有花生四烯酸、β-谷甾醇、槲皮素。對應成分與作用靶點,發現單個活性成分可作用多個靶點,多個活性成分也可共同作用單個靶點,證實黃芪-冬蟲夏草是以多靶點、多途徑來發揮整體作用。
2.3 IgAN的靶點篩選
利用GeneCards、OMIM數據庫挖掘得到IgAN的疾病治療靶點,設置Relevance score≥3.6并刪去重復靶點,共得到604個IgAN的疾病治療靶點。
2.4 共同靶點篩選及互作網絡構建
將604個IgAN治療靶點與藥物活性成分作用靶點應用R語言軟件及Perl語言程序篩選出共同靶點共37個;應用STRING數據平臺輸入37個共同靶點,在“high confidence:0.9”的模式下構建互作網絡(PPI)(見圖1)。應用count.R插件統計出現頻次前10的蛋白靶點,出現頻次較高的有VEGFA、HIF1A、NOS3、CASP3等(見表2),可作為黃芪-冬蟲夏草治療IgAN的潛在靶點。

圖1 共同靶點互作網絡(PPI)Fig.1 Common target interaction network (PPI)

表2 常見蛋白質靶點頻率
2.5 生物分子網絡構建
采用Cytoscape 3.7.2軟件在活性成分-靶點互作網絡圖中,共獲得42個節點(靶點37個,活性成分5個)(見圖2)。其中三角形代表黃芪-冬蟲夏草活性成分,橢圓形代表黃芪-冬蟲夏草活性成分與IgAN的共同靶點。
2.6 黃芪-冬蟲夏草治療IgAN的生物功能(GO)分析及核心通路篩選
并利用R語言軟件對以上共同靶點進行GO功能分析得到的柱狀圖(見圖3),其中的生物過程主要涉及類固醇結合、細胞凋亡過程的半胱氨酸型內肽酶活性、雌激素受體結合、膽固醇結合等。這體現了黃芪-冬蟲夏草可能通過調控多個復雜的生物過程來治療IgAN。圖4顯示了黃芪-冬蟲夏草作用靶點的KEGG通路富集分析結果。通過分析,37個共同靶點主要分布脂質與動脈粥樣硬化信號通路、AGE-RAGE信號通路、流體剪切應力與動脈粥樣硬化通路、PI3K-Akt信號通路等多條信號通路中,這些表明黃芪-冬蟲夏草通過作用于多條信號通路來協調治療IgAN。

圖2 活性成分-靶點互作網絡Fig.2 Interaction network of compounds-targets

圖3 GO功能分析直方圖Fig.3 Histogram of GO analysis
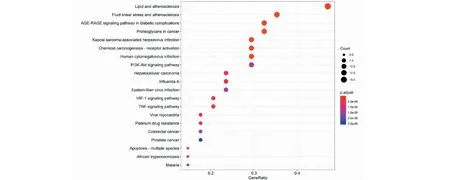
圖4 KEGG富集分析圖Fig.4 Results of KEGG pathway analysis
2.7 分子對接
采用AutoDock vina軟件將主要成分與關鍵靶點VEGFA進行分子對接后,得到結合能數值分別為β-谷甾醇-26.6 kJ/mol、異鼠李素-22.02 kJ/mol、山奈酚-19.34 kJ/mol、槲皮素-18.21 kJ/mol、花生四烯酸-12.89 kJ/mol,結合能越小對接越好。表中主要成分都能與靶點蛋白較好地結合。其中β-谷甾醇與VEGFA結合性最好(見圖5)。結果表明,這5種主要成分與蛋白靶點相互作用,結合后呈現穩定狀態。
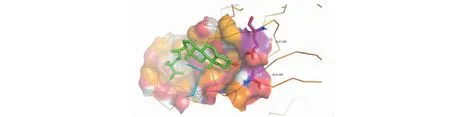
圖5 β-谷甾醇與VEGFA的分子對接圖Fig.5 Molecular docking diagram of β-sitosterol and VEGFA
2.8 黃芪-冬蟲夏草對IgAN大鼠對尿蛋白影響
模型組尿蛋白較空白組顯著增加(P<0.05),黃芪-冬蟲夏草組尿蛋白較模型組顯著降低(P<0.05),結果見表3。
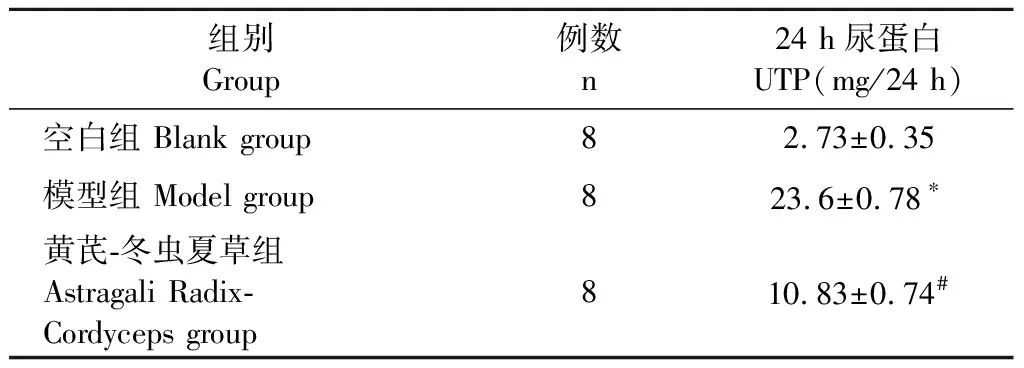
表3 尿蛋白定量
2.9 黃芪-冬蟲夏草對腎組織VEGFA含量的影響
與正常組比較,模型組VEGFA含量顯著升高(P<0.05),給予黃芪-冬蟲夏草治療后,VEGFA含量較模型組顯著下降(P<0.05),結果見表4。

表4 對腎組織VEGFA含量影響
3 討論與結論
依據其臨床特征,本病歸屬中醫學尿血、尿濁、慢腎風等范疇。中醫學認為本病多為脾腎虧虛為本,濕濁內蘊,日久成瘀為標;根據對文獻挖掘證據表明,中藥治療IgAN以補益肺脾腎為主,活血化瘀貫穿始終[11]。陳幫明主任認為IgAN免疫復合物沉積屬中醫“微干血”,“瘀、濁”為其核心病機,黃芪-冬蟲夏草藥對不僅可補益肺脾腎,且可抑制腎纖維化、祛除腎中頑瘀,延緩腎功能進展[5,12]。
本研究篩選出37個生物活性成分,從活性成分-靶點互作網絡構建結果中得知其關鍵活性成分是花生四烯酸、β-谷甾醇、異鼠李素、山奈酚、槲皮素。花生四烯酸是一種n-6必需脂肪酸,可調節人體免疫功能、抗血小板聚集、抗凝、抑制腎纖維化、保護足細胞[13,14];β-谷甾醇通過提高抗氧化酶的活性,如超氧化物歧化酶(SOD),谷胱甘肽(GSH)和過氧化氫酶(CAT)等,具有顯著抗氧化作用,且可以降低腫瘤壞死因子(TNF-α)、IL-6水平,抑制TLR受體信號轉導發揮抑炎作用[15]。異鼠李素通過作用TGF-β1/Smad3和TGF-β1/p38 MAPK通路抑制細胞外基質形成而抑制纖維化[16]。山奈酚可通過抑制ASK1/MAPK通路,顯著降低氧化應激和脂質過氧化[17];通過NF-κB信號通路抑制炎癥因子釋放[18]。槲皮素是一種黃酮類化合物,具有抗氧化、抑炎、降低代謝毒素、保護腎臟的作用[19]。綜上,黃芪-冬蟲夏草主要活性成分可能通過抗纖維化、抗氧化、調節免疫、抑制炎癥等從而發揮治療IgAN作用。
基于黃芪-冬蟲夏草活性成分-IgAN-靶點互作網絡,發現了VEGFA、HIF1A、NOS3、CASP3等關鍵靶點。研究表明,VEGFA是VEGF的亞型,可促進間質纖維化,在IgAN患者腎小球和腎小管上皮細胞中高表達,可破壞腎臟屏障,加重蛋白尿,可獨立預測IgAN患者臨床結局[20]。免疫復合物沉積系膜區,刺激內皮細胞分泌大量VEGF,與受體結合后誘導血管新生,同時通過刺激氧化應激、炎癥,進一步加重系膜增生,胞外基質增多,導致腎小球硬化[21]。HIF1A可以通過在轉錄和轉錄后激活Notch-1,從而促進腎纖維化[22]。NOS3可減少SOD水平,發揮抗氧化、抑炎作用[23]。Caspase-3是細胞凋亡過程中主要效應因子,介導腎臟炎癥反應、纖維化形成的相關凋亡[24]。
結合KEGG數據庫對信號通路注釋分析發現,黃芪-冬蟲夏草的生物有效成分可能通過作用于脂質與動脈粥樣硬化信號通路、AGE-RAGE信號通路、流體剪切應力與動脈粥樣硬化通路、PI3K-Akt信號通路等。脂質與動脈粥樣硬化是腎臟疾病合并心血管風險的主要因素[25]。流體剪切應力與動脈粥樣硬化通路是抑制炎癥、血管舒張、抗動脈粥樣硬化的主要途徑[26]。AGE/RAGE可促進炎性細胞因子釋放和細胞外基質生成,導致腎小球肥大和腎小球硬化,亦可與膠原蛋白發生交聯,而介導蛋白質沉積[27]。PI3K-Akt信號通路可介導腎臟炎癥和細胞凋亡[28]。
綜上,本研究顯示黃芪-冬蟲夏草通過作用于VEGFA、HIF1A、NOS3、CASP3關鍵靶點及脂質與動脈粥樣硬化信號通路、AGE-RAGE信號通路、流體剪切應力與動脈粥樣硬化通路、PI3K-Akt信號通路等多條信號通路而抑制纖維化、抗炎、氧化應激等多個病理環節,從而發揮多環節、多靶點的整合調節效應。分子對接也確證上述成分和靶點之間有較強的結合活性。同時結合了IgA大鼠模型對有強烈結合活性VEGFA靶點進行驗證,結果表明黃芪-冬蟲夏草藥對可以顯著降低模型組大鼠尿蛋白、VEGFA含量,證實黃芪-冬蟲夏草可通過多分子靶點、多途徑而延緩IgA腎病進程。

