2型糖尿病視網膜病相關危險因素研究
陳玉冰,孫 侃
(1.石河子大學醫學院,新疆 石河子 832000;2.石河子大學醫學院第一附屬醫院內分泌代謝科,新疆 石河子 832000)
根據國際糖尿病聯合會(IDF)的最新統計,預計2045年全球糖尿病患者在如今5億人的基礎上還將增加51%[1],在所有糖尿病的患者當中,2型糖尿病(T2DM)流行度最高,所占比例可達90%以上[2],當糖尿病到達一定程度時,可能會并發糖尿病視網膜病變(DR),這是當今社會造成嚴重視力影響甚至失明的主要原因[3],如何防治其發生發展便成為近年來大眾所關注的熱點問題。
DR發病率高且潛伏期長,早期一般沒有明顯癥狀,而當自覺視力受損時,已達到晚期病變,可供選擇的治療方法非常有限,需要接受反復治療,如激光光凝、玻璃體切割術等,但效果往往不理想,只能保存部分的視力功能[4],所以應盡早進行DR的防治及篩查。識別DR的危險因素有助于選擇適當的預防措施,故本次通過研究T2DM患者合并DR的患病率及相關獨立危險因素分析,從而為臨床防治DR的發生發展提供參考依據。
1 資料與方法
1.1一般資料:回顧性分析2020年8月1日~2021年7月31日在本院內分泌代謝科住院的T2DM患者共785例,其中男497例,女288例;年齡15~89歲,平均(57.15±12.974)歲。本次研究經過本院醫學倫理委員會同意。納入標準:①所有患者均符合1999年世界衛生組織(WHO)所制定的T2DM診斷標準;②所有患者均行眼底照相或造影檢查,若兩者都進行且結果存在差異,以眼底造影為準。排除標準:①排除1型糖尿病、高血壓等其他病變所致的眼底病變患者;②合并急性代謝性疾病及嚴重肝、腎、心功能不全者;③合并原發性腎臟損害者。
1.2研究方法:①資料:收集患者包括性別[男(%)][Sex,Men(%)]、年齡(Age)、病程(DUR)、收縮壓(SBP)、舒張壓(DBP)、空腹血糖(FPG)、糖化血紅蛋白(HbA1c)、空腹C肽(FCP)、三酰甘油(TG)、總膽固醇(TC)、低密度脂蛋白(LDL)、血肌酐(sCr)、尿酸(UA)、胱抑素C(CysC)、腎小球濾過率(eGFR)、尿微量白蛋白(MAU)共16項研究指標。②分組:對兩只眼睛進行分級,只選擇較差的眼睛進行分析,眼底病變按照2002年國際臨床分級標準,分為無DR組(NDR),輕、中、重非增殖期組(NPDR)、增殖期組(PDR)共5組。
1.3統計學方法:應用SPSS 26.0統計學軟件進行統計分析,組間差異性別用Fisher確切概率法分析,余連續數據用Kruskal-Wallis H檢驗分析,DR與各影響因素的關系用Spearman秩相關分析及多因素Logistic回歸分析。
2 結果
2.1T2DM患者中DR患病率:785例T2DM患者中共檢出DR患者175例,總患病率22.29%,其中輕度NPDR 110例(62.86%),中度NPDR 47例(26.86%),重度NPDR 6例(3.42%),PDR 12例(6.86%)。
2.2組間各影響因素差異性比較:DR不同分期組間各影響因素的差異性比較見表1。5組間的Age(歲)、DUR(年)、SBP(mmHg)、HbA1c(%)、FCP(nmol/L)、TC(mmol/L)、LDL(mmol/L)、sCr(mmol/L)、CysC(mg/L)、eGFR(ml·min/1.73 m2)、MAU(mg/L)差異有統計學意義(P<0.05),Sex[Men(%)]、DBP(mmHg)、FPG(mmol/L)、TG(mmol/L)、UA(μmol/L)差異無統計學意義(P>0.05)。

表1 DR不同分期組間各影響因素的差異性比較
2.3DR與各影響因素的Spearman相關性分析:DR與Age、DUR、SBP、HbA1c、TC、sCr、CysC、MAU的相關分析見表2。結果顯示DR與Age(r=0.184,P<0.05)、DUR(r=0.340,P<0.05)、SBP(r=0.126,P<0.05)、HbA1c(r=0.096,P<0.05)、TC(r=0.074,P<0.05)、sCr(r=0.134,P<0.05)、CysC(r=0.293,P<0.05)、MAU(r=0.236,P<0.05)呈正相關,表明年齡越大,病程越長,SBP越高,血清HbA1c、TC、sCr、CysC越高,MAU越高,DR越嚴重。

表2 DR與Age、DUR、SBP、HbA1c、TC、sCr、CysC、MAU的相關性分析
DR與FCP、eGFR、UA、 DBP 、 FPG 、TG、LDL的相關分析見表3。結果顯示DR與FCP(r=-0.147,P<0.05)、eGFR(r=-0.263,P<0.05)呈負相關,表明血清FCP、eGFR越低,DR越嚴重。

表3 DR與FCP、eGFR、UA、 DBP 、 FPG 、TG、LDL的相關性分析
2.4DR的多因素回歸分析:DR的多因素Logistic回歸分析見表4。結果顯示DUR(β=0.078,OR=1.082,P<0.05)、SBP(β=0.012,OR=1.012,P<0.05)、HbA1c(β=0.149,OR=1.160,P<0.05)、MAU(β=0.001,OR=1.001,P<0.05)為DR的獨立危險因素,表明DUR越長、SBP越高、血清HbA1c越高、MAU越高,DR發生率越高,FCP(β=-0.617,OR=0.540,P<0.05)為DR的保護因素,表明血清FCP越低,DR發生率越高。
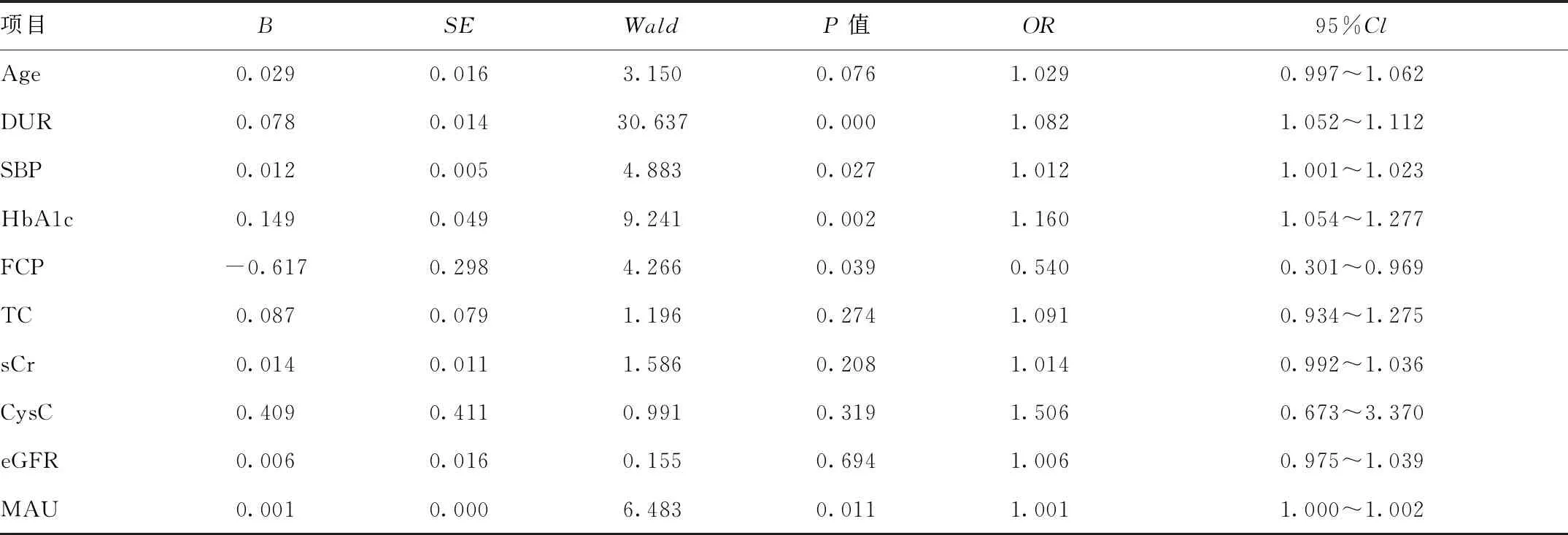
表4 DR的多因素Logistic回歸分析
3 討論
DR潛伏期長,病程不可逆,早期不累及黃斑則不會引起明顯的視力下降,所以患者就診時往往已經處于增殖期,此期視網膜新生血管形成、玻璃體積血,最后因玻璃體增殖膜的形成而導致視網膜脫離,造成失明,這也是DR成為致盲率較高眼底疾病的原因之一[5]。
眾所周知,雌激素對女性生殖健康非常重要,不僅于此,有研究表明,雌激素對血管內皮具有保護作用,可保護視網膜免受高血糖條件下的損害,甚至可選擇作為治療糖尿病視網膜病變的有效手段[6],故絕經前女性可能發生DR風險更低,本次研究結果表明,性別與DR無相關性,但收集數據中存在許多絕經后老年女性,DR與性別是否相關還須考慮多種因素影響,做具體研究。
年齡是否影響DR的發生說法不一,有學者認為,年齡越大,發生DR風險越高[7],但也有大型研究表示,年齡越輕,越容易發生DR[8]。本研究在排除病程等相關混雜因素之后,發現年齡與DR無明確相關性。糖尿病持續時間越長,發生DR的風險越高[9-10],在中國大陸一項13 473例T2DM患者合并DR相關危險因素的橫斷面研究中顯示,糖尿病持續時間每增加5年,DR的發生率顯著增加,但在糖尿病持續時間增加至20年后,DR的發生率將不再發生顯著變化[8]。
血壓(Bp)也是DR的一個重要危險因素。臨床試驗證據表明,在亞洲糖尿病合并高血壓的人群樣本中,治療但控制不良以及未經治療的高血壓與DR的發生顯著相關,其中較高的SBP水平與DR和可威脅視力的糖尿病視網膜病變(VTDR)相關,而DBP水平與DR和VTDR無關[11]。本次研究結果表明SBP越高,發生DR風險也越高,而DBP與DR不相關,這與Liu Lei[11]等研究結果一致。長期血糖控制不佳易導致DR的發生發展,HbA1c可以反映近2~3個月的血糖水平,不受瞬時血糖變化的影響,與DR風險密切相關[8,10-12]。有研究表明,HbA1c檢測是否存在DR比FPG更加敏感[13],這可能與FPG瞬時性大,受當前多種因素影響,不能代表長期血糖控制情況有關。FCP是胰島素產生和胰島素抵抗的生物標志物,可能對糖尿病微血管病變的發生、發展產生影響,且被認為與DR的發生呈負相關[14]。本次研究結果表明,FCP為DR的保護因素,即FCP越低,DR越嚴重,與Wang Y[14]等人結果一致。
DR與糖尿病腎病(DN)在糖尿病微血管病變中有近乎相同的發病機制,兩者關系密不可分[7,15],MAU對診斷早期DN有重要意義。本研究結果顯示,MAU升高是DR的獨立危險因素,與Ghamdi AHA[9]研究結果一致。sCr、eGFR、CysC經相關分析后顯示均與DR相關,但經多因素Logistic回歸分析后表明,sCr、eGFR、CysC不是DR的獨立危險因素,這與蔡鑫[16]、項杰等[17]人的研究不符。UA被認為是DR的獨立危險因素[17-18],原因可能與高尿酸可促進視網膜炎性反應和氧化應激有關[19],但本研究未發現UA與DR存在相關性,鑒于此,還需要更大樣本量的隨訪研究來證實。
血脂是否為DR獨立危險因素各研究結果并不一致。石家莊一項納入1 008例糖尿病患者的研究中,認為TC、TG與DR發生的危險程度相關[7],本研究結果則表明TC、TG、LDL并非與DR的獨立危險因素,這與譚慧玲等人[20]結果一致,造成這種差異性可能與地區、民族、生活習性等因素相關。
綜上所述,本研究結果表明DUR、SBP、HbA1c、MAU為DR的獨立危險因素,而FCP為DR的保護因素,這有助于對DR進行早期干預,如定期篩查,注意監測并控制血壓、血糖、尿微量白蛋白等,以減少DR的患病率,提高糖尿病患者的生活質量。然而,本課題研究的不足之處在于T2DM合并DR不同分期的樣本量較少,其代表性較局限,且未探討DR嚴重程度與各影響因素的回歸分析等,下一步研究還需改進。

