“氣生火”之謎
河北省邯鄲市第三十二中學 莘彬鋒
化學老師在元旦聯歡會上,表演了一個“魔術”:將包有過氧化鈉(化學式為NaO)粉末的脫脂棉置于蒸發皿中,用細長導管向脫脂棉上吹氣,稍后脫脂棉燃燒了起來。化學興趣小組的同學對此奇觀頗感興趣,決定對其探個究竟。
探究一:脫脂棉為什么會燃燒
根據物質燃燒的條件做出假設:①吹出的氣體與過氧化鈉反應生成了氧氣;②反應放出熱量,且溫度達到可燃物脫脂棉的著火點。
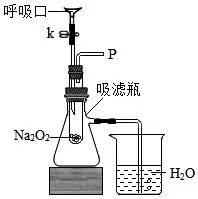
同學們設計了如下裝置進行實驗。向過氧化鈉粉末中不斷吹氣,觀察到過氧化鈉粉末由淡黃色逐漸變為白色。在導管口P 處放一根帶火星的木條,帶火星的木條復燃,說明試管內生成了氧氣。同時還觀察到燒杯中導管口出現氣泡,說明反應還放出了熱量。
通過實驗說明吹出的氣體與過氧化鈉反應生成了氧氣,且反應放出熱量,從而滿足了脫脂棉燃燒的條件,脫脂棉便燃燒起來。
探究二:吹出的哪些氣體與過氧化鈉發生了反應
同學們查閱資料:①過氧化鈉能與HO 反應,生成NaOH;過氧化鈉能與CO反應,生成NaCO。②過氧化鈉與氮氣不反應。通過探究反應后試管內殘留白色固體的成分,得出吹出的哪些氣體與過氧化鈉發生了反應。根據已有化學知識及資料做出如下猜想:
猜想①:白色固體成分是NaCO;
猜想②:白色固體成分是NaOH;
猜想③:白色固體成分是NaCO和NaOH。
小紅設計實驗方案并進行實驗:取少量試管內殘留的白色固體于干凈試管中,加入適量水,振蕩,固體全部溶解;滴入無色酚酞溶液,發現酚酞溶液變紅色,據此得出猜想②正確。但是小組其他同學認為此結論不正確,因為碳酸鈉溶液也顯堿性,也能使無色酚酞溶液變紅。
小萌又設計實驗方案進行實驗:取少量試管內殘留的白色固體于干凈試管中,加入適量水,振蕩,固體全部溶解;向溶液中滴入幾滴稀鹽酸,無明顯現象,據此得出猜想②正確。小臻否定了這個結論,他認為滴加稀鹽酸的量過少,可能鹽酸先與氫氧化鈉反應,還未來得及與碳酸鈉反應,因此即便白色固體中有碳酸鈉也看不到有氣泡產生。
小臻同學設計如下實驗方案進行實驗:①取少量試管內殘留的白色固體溶于水,向其中加入過量的氯化鋇溶液,振蕩,靜置,觀察到有白色沉淀產生,說明白色固體中含有碳酸鈉;②取適量步驟①的上層清液,滴加兩滴酚酞溶液,溶液變紅色,說明白色固體中含有氫氧化鈉。由此可知,猜想③正確。
小臻同學解釋:加入過量的氯化鋇溶液既能驗證碳酸鈉是否存在,又能將碳酸鈉全部除去,防止其對驗證氫氧化鈉產生干擾。
通過探究可知,吹出的氣體中CO、HO 都與NaO發生了反應。因此,過氧化鈉應該密封保存。化工廠存有過氧化鈉時,一旦失火,注意既不能選用二氧化碳滅火器滅火,也不能選用水基型滅火器滅火。

